Sélénium
| Sélénium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
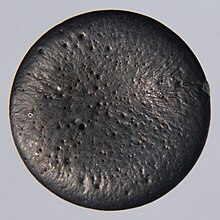
 Surfaces de semi-métal Se gris cristal apparaissant en plaques grises et argentées plus claires sur Se noir amorphe | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Position dans le tableau périodique | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbole | Se | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom | Sélénium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numéro atomique | 34 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe | 16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Période | 4e période | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bloc | Bloc p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Famille d'éléments | Non-métal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration électronique | [Ar] 3d10 4s2 4p4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électrons par niveau d’énergie | 2, 8, 18, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés atomiques de l'élément | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse atomique | 78,971 ± 0,008 u[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique (calc) | 115 pm (103 pm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de covalence | 120 ± 4 pm[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de van der Waals | 190 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État d’oxydation | ±2, 4, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électronégativité (Pauling) | 2,48 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxyde | acide fort | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergies d’ionisation[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1re : 9,752 39 eV | 2e : 21,19 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3e : 30,820 4 eV | 4e : 42,945 0 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5e : 68,3 eV | 6e : 81,7 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7e : 155,4 eV | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopes les plus stables | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques du corps simple | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État ordinaire | solide | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Allotrope à l'état standard | Sélénium gris (hexagonal) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Autres allotropes | Sélénium rouge α, β et γ (monoclinique), sélénium noir (vitreux) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse volumique | 4,79 g·cm-3 (gris), 4,28 g·cm-3 (vitreux)[1] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Système cristallin | Hexagonal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureté (Mohs) | 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Couleur | gris métallique | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point de fusion | 221 °C (gris)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point d’ébullition | 685 °C (gris)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de fusion | 6,694 kJ·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de vaporisation | 95,48 kJ·mol-1 (1 atm, 685 °C)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molaire | 16,42×10-6 m3·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pression de vapeur | 0,000 13 mbar (170 °C)[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitesse du son | 3 350 m·s-1 à 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur massique | 320 J·kg-1·K-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité électrique | 1,0×10-4 S·m-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité thermique | 2,04 W·m-1·K-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Divers | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CAS | [4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No ECHA | 100.029.052 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CE | 231-957-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Précautions | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| H301, H331, H373, H413, P273, P304+P340 et P308+P310 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SIMDUT[5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Produit non contrôlé |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unités du SI & CNTP, sauf indication contraire. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| modifier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Le sélénium est l'élément chimique de numéro atomique 34, de symbole Se. Ce troisième élément du groupe VI A (groupe des chalcogènes) est un non-métal. La chimie du corps simple et de ses principaux composés présente une grande analogie avec celle du soufre, mais aussi avec celle du tellure.
Généralité sur l'élément et histoire[modifier | modifier le code]
Le sélénium est un oligoélément et un bioélément, mais à très faible dose. Il est toxique (voire très toxique sous certaines formes) à des concentrations à peine plus élevées que celles qui en font un oligoélément indispensable au régime animal. Il n'a pas d'effet majeur sur les maladies, mis à part les graves intoxications aux métaux lourds[6]. Le soufre et le sélénium sont très souvent interchangeables, mais aucunement dans le rôle nutritif sélectif du sélénium. Les territoires du globe terrestre pouvaient être caractérisés par le taux moyen de Se dans le sang humain dans les années 1990, il existait des zones riches et pauvres selon ce critère, le Venezuela figurant en tête avec 0,8 µg/L et l'Égypte en queue de peloton avec 0,07 µg/L[citation nécessaire].
Le sélénium a été découvert par les chimistes Jöns Jacob Berzelius et Johan Gottlieb Gahn en 1817 dans la matière boueuse subsistant dans la "chambre de plomb" d'une usine proche de Grispholm, proche lors de la préparation industrielle ancienne d'acide sulfurique. Les éléments sélénium et tellure, qui étaient associés dans ce milieu réactionnel, résultat du grillage des pyrites, ont été découverts respectivement au début du XIXe siècle et à la fin du XVIIIe siècle.
Le tellure a reçu le premier son nom, du mot latin tellus signifiant la terre, le globe terrestre. Comme le sélénium lui ressemble, a des propriétés chimiques analogues et lui est toujours associé dans les minerais, comme le sont la Terre et la Lune, on lui a donné un nom dérivé de Σελήνη (Selếnê) ou σελήνη (selênê), terme grec désignant la Lune, satellite de la Terre, et Séléné, déesse de la Lune.
Le degré d'oxydation de l'ion Se peut être -II, II (le plus commun), IV et VI. Il caractérise les combinaisons du Se.
Isotopes[modifier | modifier le code]
Le sélénium possède 29 isotopes connus, de nombre de masse variant de 65 à 94, ainsi que neuf isomères nucléaires. Parmi ces isotopes, cinq sont stables : 74Se, 76Se, 77Se, 78Se et 80Se, et sont naturellement présents avec un radioisotope le 82Se à demi-vie extrêmement longue, de 108 milliards de milliards d'années (environ 8 milliards de fois l'âge de l'Univers).
La masse atomique standard du sélénium est de 78,96(3) u.
Occurrences naturelles et principaux gisements et installations productives[modifier | modifier le code]
Le clarke du sélénium est de 0,1 ppm (0,1 g/t). Il est 50 fois plus commun que le tellure, mais environ 4 000 fois moins que le soufre.
Le sélénium natif est un minéral, métalloïde natif rare. L'essentiel du Se semble substituer, en tout ou partie, au soufre dans ces combinaisons minérales. Il est présent dans un grand nombre de minéraux sulfures, tels que les pyrites sélénifères.
Les séléniures de Pb, Fe, Cu, Zn ... comme la clausthalite PbSe et l'umangite Cu3Se2, voire la crookesite CuThSe, existent dans la nature, même s'ils sont des minéraux rares.

Le sélénium se concentre dans certaines plantes, céréales ou herbes, ou levures. Les concentrations peuvent être parfois trop élevées et toxiques, mais le plus souvent les très faibles concentrations des céréales ne sont pas toujours assimilables par la présence conjointes de bio-complexants[Quoi ?], ce qui entraîne des déficiences drastiques nuisibles au bien-être et à la santé, dans certaines régions du globe.
La production de sélénium provient essentiellement du retraitement des boues résiduelles du raffinage par électrolyse du plomb, du nickel ou du cobalt, et surtout du cuivre. Les boues anodiques, dans le cas de l'affinage électrolytique du cuivre, peuvent contenir jusqu'à 10 pour cent de sélénium. Elles sont grillées pour obtenir le dioxyde de sélénium SeO2, corps solide. Cette opération rappelle le grillage de minerais sulfurés ou les anciens procédés de fabrication d'acides sulfuriques. Il suffit de réduire l'oxyde ou anhydride sélénieux par l'anhydride sulfureux SO2 soit :
- SeO2solide + 2 SO2gaz → Serouge amorphe, en flocons + 2 SO3gaz
Le sélénium Se8 amorphe est purifié par plusieurs distillations sous vide. La production mondiale annuelle de sélénium est de l'ordre de quelques milliers de tonnes. Avant les années 2000, les principaux producteurs étaient les États-Unis, le Canada, la Suède et le Japon.
Propriétés du corps simple et des corps composés[modifier | modifier le code]
Propriétés physiques et chimique du corps simple[modifier | modifier le code]

Le corps simple est polymorphe, généralement sous la forme de solides gris de structure complexe. On distingue principalement :
- quatre formes amorphes, Se8 noir, la plus compacte, Se8 rouge et poudreux, et les Se noirs, respectivement amorphe (poudreux, pulvérulent) et vitreux (solide compact), mélanges de cycles Se8 et de longues chaînes Sen, produits par la trempe de Se liquide.
- trois formes cristallines, deux monocliniques Se8 métastables et rouges, dites Seα et Seβ, et la principale trigonale, assemblage en spirale de macromolécules Sen par liaison covalente. Cette dernière forme, grise à éclat métallique, est à la fois la plus dense et la plus stable.

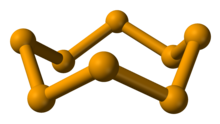
Les formes amorphes sont plus ou moins métastables ou instables, elles donnent à température ambiante ou avec une légère activation thermique le Segris semi-métal.
Le sélénium gris, semi-métal proche du Te gris, à reflet métallique est un semi-conducteur thermosensible (sa faible conductivité électrique augmente lorsque la température s'accroît), photosensible (sa résistance électrique diminue avec son exposition aux photons de la lumière par illumination croissante) et à propriétés photovoltaïques (conversion de la lumière en courant électrique) ce qui est utile pour des photocopieurs ou des cellules photoélectriques[7].
Le sélénium rouge, assemblage de cycle Se8, isolant, soluble dans le sulfure de carbone, qui proviennent de sélénium en solution ou s'y forme facilement, peut ainsi être amorphe (désordonné) ou cristallisé. Le Se rouge amorphe est léger et floconneux de faible densité avoisinant 4,29 à 4,3. Seα et Seβ cristallisent dans deux réseaux monocliniques différents, respectivement de densité intermédiaire 4,39 et de densité anormalement faible entre 4 et 3,97.

La présence de Sen a apparemment un effet noircissant ou grisonnant sur la matière. Le sélénium noir amorphe est analogue au Sμ. Le sélénium noir vitreux, analogue au Sλ est élastique au-dessus de 60 °C, puis plastique vers 100 °C.
Le sélénium gris, de densité proche de 4,8 à 20 °C, fond au-delà de 220 °C, le liquide pur ou Se liquide est noir et très visqueux. L'ébullition n'apparaît qu'à une température très légèrement inférieure à 685 °C, la vapeur de sélénium monoatomique dégagée est jaune, ce qui rappelle la couleur du soufre solide. Notons que dans les soufrières ou émanation de soufre, le sélénium se distingue du soufre par la couleur rouge de son dépôt de sublimation.
Chimie du sélénium[modifier | modifier le code]
Le sélénium peut réagir ou s'associer avec de nombreux corps simples, comme les halogènes, l'oxygène, l'hydrogène et les métaux, et donne des composés de propriétés assez voisines des composés soufrés, c'est-à-dire incluant du soufre.
L'association ou combinaisons avec les métaux forme des corps chimiques, nommé séléniures.
Le corps simple sélénium décompose l'iodure d'hydrogène en séléniure d'hydrogène (ou gaz hydrogène sélénié) et en iode corps simple.
- Se corps simple + 2 HIgaz fumant ou liquéfié sous pression → SeH2 gaz + I2 solide parfois sublimé en gaz
L'attaque par un acide oxydant, tel que l'acide nitrique concentré, donne l'anhydride sélénieux ou dioxyde de sélénium. Ce dernier corps se présente sous forme de longue chaînes, c'est un corps solide volatile (par dépolymérisation), très soluble dans l'eau ; sa structure diffère radicalement du gaz dioxyde de soufre SO2.
- 3 Se corps simple + 4 HNO3 acide oxydant (liquide fumant à chaud) → 3 H2SeO3acide sélénieux + 4 NO gaz + 8 H2O
avec SeO2 n )anhydride sélénieux polymérisé formé à partir l'acide sélénieux (par perte d'eau).
Notez que la réaction analogue avec le corps simple soufre donne l'acide sulfurique. Pour obtenir l'anhydride sélénique SeO3 (liquide très acide, avide d'eau) ou l'acide sélénique H2SeO4, il faut imposer la calcination du corps simple sélénium par le nitrate de potassium à sec, puis traiter le séléniate de potassium par des sels de plomb et laver avec l'acide sulfhydrique. L'anhydride sélénique peut être concentré jusqu'à sa température d'ébullition 290 °C, mais il se décompose vers 350 °C en deux gaz oxygène et dioxyde de sélénium. L'acide sélénique est pratiquement aussi fort que l'acide sulfurique, mais il est aussi plus oxydant que ce dernier. Il justifie l'existence des ions séléniates SeO42−.
Le dioxyde de sélénium est décomposé en solution par les métaux zinc et fer en poudre ou limaille, par l'acide sulfureux ou l'hydrogène sulfuré, et laisse du sélénium amorphe rouge très léger ou fleur de sélénium. L'acide sélénieux H2SeO3 existe en solution et explique la présence d'ions sélénites SeO32−.
Combinaisons du sélénium[modifier | modifier le code]
Le dioxyde de sélénium ou anhydride sélénieux SeO2 est un solide macromoléculaire à liaisons covalentes, ce qui le différencie radicalement du gaz anhydride sulfureux à température ambiante.

L'anhydride sélénique SeO3
L'acide sélénique H2SeO4 se présente sous forme de cristaux, incolores et hygroscopiques, qui fondent à une température inférieure à 60 °C. En milieu aqueux, il donne une solution aqueuse, beaucoup plus oxydante que l'acide sulfurique, qui dissout l'or natif ou le platine natif.
Le séléniure d'hydrogène H2Se est un gaz toxique, incolore à odeur désagréable.
Détection et quantification analytique[modifier | modifier le code]
La matière séléniée, c'est-à-dire à base de sélénium, peut être identifiée au laboratoire par une attaque à l'acide sulfurique concentré, souvent à chaud. L'acide sélénieux H2SeO3 solubilisé est ensuite réduit par le gaz SO2 ou un corps réducteur en Se rouge.
Dans les sédiments et dans les tissus musculaires, le dosage se fait avec un spectrophotomètre[8],[9]. Toutefois, un traitement préalable doit se faire sur chacun des échantillons.
Pour les sédiments, une minéralisation acide de l’échantillon transforme préalablement le sélénium en sa forme hydrure via du borohydrure de sodium (NaBH4) en milieu acide. Puis le sélénium chauffé dans une cellule est réduit en sélénium élémentaire. Finalement, un étalonnage est fait par spectrophotométrie d’absorption atomique[8].
Pour les tissus musculaires, l’échantillon est traité par digestion acide des tissus biologiques en milieu très oxydant. Le nitrate de magnésium permet l’oxydation complète de la matière organique et stabilise le Sélénium. Ensuite, pour passer du Se(6) à Se(4) il faut rajouter de l'acide chlorhydrique HCl(aq). Le sélénium est ensuite transformé sous sa forme hydrure (H2Se) avec du borohydrure de sodium (NaBH4) en milieu acide. À ce point, l’hydrure est chauffé en sélénium élémentaire. Finalement, l’étalonnage est fait par spectrophotométrie d’absorption atomique[9].
Pour l’analyse du sélénium dans l’eau, la méthode se fait par spectrométrie d’émission au plasma d’argon et la détection est faite par spectrométrie de masse (ICP-MS)[10].

Utilisations industrielles du sélénium[modifier | modifier le code]
Le sélénium est utilisé dans différents capteurs ou connecteurs électroniques, en chimie (vulcanisation), dans la fabrication du verre et dans l'élaboration de pigments, en métallurgie et en agriculture.
Corps simple ou semi-conducteur quasi-pur[modifier | modifier le code]
Il peut être comme semi-conducteur sous forme de Se gris métal, mais aussi à l'état amorphe en xérographie.
- Photocopieur, imprimante laser et autres appareils xérographiques.
Le sélénium est utilisé pour recouvrir le « tambour » (cylindre brillant). Il est chargé électriquement, puis un rayon laser décharge plus ou moins (en rendant le sélénium conducteur) les parties blanches ou claires de l'image.
- cellules photoélectriques
Il a été utilisé précocement pour redresser le courant alternatif en courant continu.
Il sert à améliorer les qualités de l'acier inoxydable et du cuivre. la métallurgie électrolytique du manganèse réclame du sélénium dans un rapport un pour mille. Cette dépendance explique l'envolée des prix du sélénium, d'abord lentement de 4 à 6 dollars la livre de métalloïde en 2003, jusqu'à 12 ou 14 dollars en . Elle a été causée par les aciéristes chinois, qui souhaitaient remplacer le nickel (devenu trop cher par l'effet de leur propre demande) par le manganèse dans la production d'acier inoxydable[11].
Le sélénium sert à masquer la couleur verte lors de la production du verre. C'est un savon des verriers.
En agriculture, c'est un complément à doses très faibles des sols agricoles pauvres et/ou dans le régime alimentaire des animaux.
Semi-conducteur industriel[modifier | modifier le code]
La découverte des propriétés photosensibles est due à Willoughby Smith (en) et à son assistant J. May, qui travaillaient dans une société de télégraphie, en 1873[12].
C'est à l'aide d'une cellule de Smith que Alexander Graham Bell met au point son photophone en 1880, un système de téléphone sans fil utilisant un signal lumineux[13],[14].
De nombreuses recherches ont été menées pour utiliser ces propriétés photosensibles, en particulier pour la transmission d'images, sans grand succès[15]. Elles aboutiront seulement à produire des générateurs photovoltaïques, peu performants par rapport à ceux disponibles aujourd'hui.

Toute une génération de photographes, dans les années 1950 et 1960 lui doit néanmoins les premiers appareils à posemètre. Reconnaissables à des plaquettes placées à l'avant du boîtier, ces posemètres au sélénium convenaient seulement pour des mesures en lumière du jour. Un simple dispositif à galvanomètre recueillait le faible courant généré par la cellule. S'il a été remplacé dans les années 1960 par le sulfure de cadmium, certains appareils comme le FED-5 soviétique l'ont utilisé jusqu'en 1990. Il a le grand avantage de fonctionner sans piles.

De même, il était utilisé pour les premiers dispositifs de redressement « solide » affublés de multiples ailettes.
Le sélénium est en effet un semi-conducteur de type « P ». Du sélénium cristallisé est déposé sur une plaque d'aluminium, puis on forme une couche de jonction par différents procédés (par exemple une forte tension inverse).
Son temps de réponse est moyen, sa tension inverse de l'ordre de 30 V maximum nécessite souvent de monter des éléments en série.
Il a été utilisé pour le redressement du courant alternatif, jusqu'à l'apparition des redresseurs au silicium (vers 1970), plus performants et surtout plus fiables. De nombreux redresseurs au sélénium ont en effet fini dans une épouvantable fumée âcre !
Son usage comme semi-conducteur est devenu marginal, à l'exception de dispositifs limiteurs de tension où il reste en compétition avec les MoV (Metal-Oxyde Varistor).
Il semble retrouver une seconde jeunesse :
- dans des capteurs d'image pour rayons « X » car il permet la conversion directe rayonnement→flux d'électrons ;
- dans la fabrication de cellules photovoltaïques dites « couches minces » de grande dimension au rendement honorable (15 %) et au coût réduit, à base de CuInSe2 ;
- dans certains semi-conducteurs composites, notamment pour la formation de points quantiques.
Quelques usages techniques des corps composés[modifier | modifier le code]
- L'acide sélénieux appliqué à la surface de l'acier permet de changer son aspect et de le protéger. Cette opération couramment appelée brunissage est souvent utilisée sur de petites pièces d'armes à feu.
- Pigment : les rouges de cadmium (clair, moyen, foncé du type rubis) sont des sélénio-sulfures ou sulfo-séléniures de cadmium.
- Colorant pour le verre et matières plastiques : le beau rouge profond est obtenu avec du sulfoséléniure de cadmium (rouge de cadmium).
Pharmacologie et nutrition[modifier | modifier le code]
- Le sélénium est un oligo-élément constituant des sélénoprotéines dont fait partie le principal antioxydant intracellulaire, la glutathion péroxydase[16]. On en trouve dans les œufs (16 à 48 % du besoin quotidien moyen selon qu'il s'agisse d'un œuf de canard, poule, oie ou dinde et selon le système d'élevage)[17], les rognons de porc ou de bœuf, l’ail, le poisson et les mollusques. La nutrition occidentale satisfait largement les besoins quotidiens en cet élément[18] mais il est impossible de prédire les concentrations corporelles de sélénium à partir de l'apport nutritionnel parce que son utilisation et sa rétention sont dépendantes de la présence d'acide folique, de vitamine B12 et négativement affectées par la présence d'homocystéine[19].
- Le sulfure de sélénium est employé comme traitement en dermatologie, en raison de son action fongicide, ou par exemple dans le traitement des pellicules grasses.
- Le sélenium a une efficacité prouvée[20]dans les orbithopathie dysthyroïdiennes d'importance moyenne. Il améliore la qualité de vie et diminue les conséquences oculaires.
- La consommation quotidienne de sélénium (200 µg) pourrait diminuer le risque de survenue de plusieurs cancers[21] (dont ceux de la prostate et du côlon). Cela n'a cependant pas été confirmé[22]. Par contre, un taux sanguin de sélénium trop important pourrait augmenter le risque de cancer[23]. L'addition de sélénium au régime diminue la cancérogenèse induite chimiquement chez les rongeurs[24]. Dans ces études, les composés organiques du sélénium sont plus efficaces et moins toxiques que les sels de sélénium. Les composés organiques testés sont les sélénocyanates, la sélénométhionine, la noix du Brésil (riche en sélénium), l'ail et le brocoli cultivés sur sol riche en sélénium.
- Il existerait également une diminution de la fréquence des maladies cardio-vasculaires[réf. nécessaire]. Il diminuerait le taux de cholestérol sanguin, en augmentant légèrement la fraction HDL[25]. Le sélénium participerait au maintien des défenses immunitaires (il diminuerait en particulier la charge virale chez les patients porteurs du VIH[26]), à la fonction thyroïdienne.
- L'effet favorable d'une supplémentation alimentaire sur le plan cardio-vasculaire et métabolique ne serait observé que chez les individus présentant un faible stock de sélénium, tandis que la supplémentation serait au contraire toxique chez les sujets non carencés en sélénium[27].
Pour résumer, à chaque fois qu'une pathologie est susceptible d'entraîner une production accrue de radicaux libres provoquant des lésions des cellules et une augmentation de médiateurs inflammatoires tels que les cytokines, le sélénium est susceptible de jouer un rôle protecteur. Cet effet serait dû à des enzymes, les glutathion-peroxydases dont certaines sont des séléno-protéines, c'est-à-dire dont le site actif comprend l'acide aminé sélénocystéine[28]. Par contre, aucun effet sur la mortalité n'a été démontré[29].
Effets secondaires[modifier | modifier le code]
Le sélénium est toxique à trop forte dose. Il peut entraîner des nausées, des diarrhées, une fragilisation des ongles, la perte des cheveux ou de la fatigue. Les recommandations américaines indiquent une dose quotidienne maximale à 400 µg/jour, or la supplémentation atteint facilement 200 µg/jour, en plus de l'apport nutritionnel, ce qui expose à un risque de surdosage[18].
Les études sur les animaux semblent montrer que des personnes qui prennent de fortes doses de suppléments de sélénium, sur une longue période, voient leur risque de diabète de type 2 se majorer un peu[30].
Toxicologie, écotoxicologie[modifier | modifier le code]
Le sélénium métallique est un élément trace essentiel (qui semble notamment limiter les risques de cancer de la prostate[31]) mais nombre de ses composés sont extrêmement toxiques[32] et sa dose toxique pour l'Homme est très facilement atteignable (400 µg/jour)[33]. Il n'est donc pas recommandé d’en prendre sous forme de supplément alimentaire, mais de consommer des aliments en contenant naturellement (champignons, foie, crustacés, etc.).
Il est plus toxique sous forme d'oxyanions séléniate (plus rare) et plus encore sous forme de sélénite (forme soluble, hautement toxique et bio-assimilable du sélénium, qui est la forme du sélénium la plus courante dans l’environnement).
Effets environnementaux[modifier | modifier le code]
Il est présent dans l'environnement et la biomasse sous plusieurs formes chimiques ; sous divers degrés d’oxydation ou même sous des formes complexées dans l’environnement. La forme sélénite, la plus toxique, est aussi la plus fréquente.
Certaines matières résiduelles d’origines industrielles ou agricoles (engrais chimiques) en contiennent des doses suffisantes pour polluer l'environnement où le sélénium peut être bioaccumulé par la chaîne alimentaire. De plus son temps de demi-vie d’élimination dans l’organisme (dépuration) est long (19 à 42 jours).
Une pollution par le sélénium peut ainsi faire diminuer la biomasse jusqu’à 72 % chez certaines espèces de poissons[34].
Il est impératif de maîtriser les techniques d’analyse du sélénium pour en identifier toutes ses formes lors d’analyse de l’eau[8], des sols[9] et de chair (tissus musculaires en général)[35] pour la santé publique et conjointement celle de l’environnement.

Seuil de toxicité[modifier | modifier le code]
Le seuil de toxicité dans l'environnement varie selon le contexte et l'espèce. Un seuil est actuellement établi à environ 3-4 µg/g pour les sédiments, le sol et l'eau[34]. Ce seuil est cependant controversé parce que la toxicité du sélénium varie beaucoup selon sa forme, selon des synergies avec d'autres molécules (thiols ou mercure[36] organique ou inorganique, par exemple), et parce qu'il semble inadapté à la variabilité des espèces et des contextes (un lac, milieu statique, n'est par exemple pas comparable à des eaux à fort débit (fleuve, rivière, etc.), de plus la sensibilité variable des espèces testées en laboratoire devrait affecter la détermination des seuils). Chez les poissons, pour les tissus musculaires, le seuil varie selon la tolérance de l'espèce observée. Des bases permettent de comparer les seuils de toxicités pour quelques poissons et oiseaux étudiés[34]. Pour l’instant la recherche n'a pas été orientée vers la détermination de seuils plus précis, mais des arguments plaident pour des études approfondies[réf. nécessaire].
Importance du contexte : Les cellules de la levure Saccharomyces cerevisiae tolèrent normalement quelques millimoles de sélénite. mais en présence de thiols dans leur milieu de croissance elles meurent en présence d'une dose mille fois plus faible (de l'ordre de la micromole). Le glutathion et le sélénite réagissent spontanément en produisant plusieurs composés contenant du sélénium (sélénodiglutathione, glutathiosélénol), du séléniure d'hydrogène) et du sélénium élémentaire, ainsi que des espèces réactives de l'oxygène. Des chercheurs ont étudié la toxicité des composés issus de la réaction entre glutathion et sélénite de sodium. Ils ont conclu que le sélénodiglutathione, le sélénium élémentaire, ou les espèces réactives de l'oxygène n'étaient pas en cause. Par contre, la formation extracellulaire de séléniure d'hydrogène peut expliquer l'aggravation de la toxicité du sélénite en présence de thiols ; la production directe de séléniure d'hydrogène avec la D-cystéine désulfhydrase induit en effet une mortalité élevée de S. cerevisiae. L'absorption de sélénium par la levure est considérablement renforcée en présence de thiol externe, très probablement parce qu'il favorise l'internalisation du séléniure d'hydrogène. La toxicité du sélénium, dans ce modèle fongique, semble pouvoir être expliquée par la consommation de glutathion réduit intracellulaire, ce qui conduit à la mort des cellules via de graves stress oxydatifs[37].
Cycle et toxicité du sélénium : Certains micro-organismes extrêmophiles contribuant à son cycle biogéochimique lui résistent cependant.
C'est par exemple le cas de la bactérie tellurique Cupriavidus metallidurans CH34 (anciennement Ralstonia metallidurans, fréquemment trouvée dans les sols ou sédiments contaminés par des métaux.
Elle se détoxique (et détoxique le sol) en réduisant le sélénite en précipité de sélénium élémentaire insoluble et bien moins toxique).
Des radiotoxicologues ont mis en évidence deux voies de réduction du sélénium chez cette bactérie :
- transformation du sélénite et/ou du séléniate en sélénium organique sous forme de sélénométhionine incluse dans des protéines bactériennes ;
- précipitation du sélénite en nanoparticules de sélénium élémentaire (procédé observé pour le sélénite, mais non pour le séléniate).
Du sélénodiglutathion est trouvé chez des bactéries exposées au séléniate en milieu limité en sulfate.
Le séléniate semble moins bioassimilable : les bactéries qui y sont exposées en accumulent vingt-cinq fois moins que de sélénium lorsqu’elles sont exposées à du sélénite.
Des bactéries mutantes (résistantes au sélénite) ont été étudiées par le CEA qui a observé qu'elles n’exprimaient pas une protéine membranaire (DedA) ; ce qui leur permet de moins accumuler de sélénium après exposition au sélénite (comparativement à la même bactérie non mutée). Le séléniate pourrait quant à lui être dégradé par la sulfate perméase de C. metallidurans CH34[38].
Notes et références[modifier | modifier le code]
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-420-09084-0)
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », Dalton Transactions, , p. 2832 - 2838 (DOI 10.1039/b801115j)
- Entrée « Selenium » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 21 août 2018 (JavaScript nécessaire)
- Base de données Chemical Abstracts interrogée via SciFinder Web le 15 décembre 2009 (résultats de la recherche)
- « Sélénium cristallin » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Le sélénium réduit la toxicité du méthylmercure et d'une manière générale, celle des dérivés d'alkylmercure.
- « SÉLÉNIUM 3. Sources et utilisations. Toxicité », sur universalis.fr.
- Centre d’Expertise en Analyse Environnementale du Québec, Détermination du sélénium dans les sédiments : méthode par spectrophotométrie d’absorption atomique après minéralisation et génération d’hydrure, 2003, 1-17
- Centre d’Expertise en Analyse Environnementale du Québec, Détermination du sélénium dans les tissus animaux : méthode par spectrophotométrie d’absorption atomique après minéralisation et génération d’hydrure, 2003, 1-18
- Centre d’Expertise en Analyse Environnementale du Québec, Détermination des métaux à l’état de trace en conditions propres dans l’eau : méthode par spectrométrie d’émission au plasma d’argon et détection par spectrométrie de masse, 2003, 1-29
- Daniel Krajka, Envol du prix du sélénium, Usine Nouvelle, 3 mars 2004.
- « Willoughby SMITH, Letter to Latimer Clark, 4 février 1873. "Effect of Light on Selenium during the passage of an Electric Current", Nature, 20 February 1873, p.303. », sur Histoire de la télévision (consulté le ).
- (en) http://www.princeton.edu/~achaney/tmve/wiki100k/docs/Photophone.html
- (en) J. Clarke, « An introduction to communications with optical carriers », sur ieeexplore.ieee.org, Students' Quarterly Journal, (consulté le ).
- « L'âge du sélénium », sur Histoire de la télévision (consulté le ).
- Carence alimentaire en sélénium
- Bogumila Pilarczyk & al. (2019) Eggs as a source of selenium in the human diet| Journal of Food Composition and Analysis ; Volume 78, May 2019, Pages 19-23| https://doi.org/10.1016/j.jfca.2019.01.014 (résumé)
- Bleys J, Navas-Acien A, Guallar E, Selenium and diabetes: more bad news for supplements, Ann Intern Med, 2007;147:271-272
- (en) Combs GF, Watts JC, Jackson MI, Johnson LK, Zeng H, Scheett AJ et al., « Determinants of Selenium Status in Healthy Adults », Nutr. J., vol. 10, no 1, , p. 75 (PMID 21767397, DOI 10.1186/1475-2891-10-75, lire en ligne)
- Claudio Marcocci, George J. Kahaly, Gerasimos E. Krassas et Luigi Bartalena, « Selenium and the Course of Mild Graves' Orbitopathy », New England Journal of Medicine, vol. 364, no 20, , p. 1920–1931 (ISSN 0028-4793, PMID 21591944, DOI 10.1056/NEJMoa1012985, lire en ligne, consulté le )
- Effects of selenium supplementation for cancer prevention in patients with carcinoma of the skin, L. C. Clark, G. F. Combs Jr, B. W. Turnbull, E. H. Slate, D. K. Chalker, J. Chow, L. S. Davis, R. A. Glover, G. F. Graham, E. G. Gross, A. Krongrad, J. L. Lesher Jr, H. K. Park, B. B. Sanders Jr., C. L. Smith, J. R. Taylor, JAMA. 1996;276:1957-1963
- Lippman SE, Klein EA, Goodman PJ et al., Effect of selenium and vitamin E on risk of prostate cancer and other cancers, The Selenium and Vitamin E Cancer Prevention Trial (SELECT),JAMA. 2009;301:39-51
- Bleys J, Navas-Acien A, Guallar E, Serum selenium levels and all-cause, cancer, and cardiovascular mortality among US adults, Arch Intern Med, 2008;168:404-410
- Chimioprévention
- Rayman MP, Stranges S, Griffin BA, Pastor-Barriuso R, Guallar E, Effect of supplementation with high-selenium yeast on plasma lipids: A randomized trial, Ann Intern Med, 2011;154:656-665
- (en) Suppression of human immunodeficiency virus type 1 viral load with selenium supplementation, Barry E. Hurwitz, Johanna R. Klaus, Maria M. Llabre, Alex Gonzalez, Peter J. Lawrence, Kevin J. Maher, Jeffrey M. Greeson, Marianna K. Baum, Gail Shor-Posner, Jay S. Skyler, Neil Schneiderman, Arch Intern Med. 2007;167:148-154
- Rayman M.P., Selenium and human health, The Lancet 2012;379:1256-1268
- Rotruck JT, Pope AL, Ganther HE et al., Selenium: biochemical role as a component of glutathione peroxidase, Science, 1973;179:588-90
- (en) Goran Bjelakovic, Dimitrinka Nikolova, Lise Lotte Gluud, Rosa G. Simonetti, Christian Gluud, Mortality in randomized trials of antioxidant supplements for primary and secondary prevention, JAMA. 2007;297:842-857
- Stranges S, Marshall JR, Natarajan R,Effects of Long-Term Selenium Supplementation on the Incidence of Type 2 Diabetes, Annals of Internal Medicine, 2007;147:217-223
- Conclusions et recommandations des études faites durant 5 ans par le WCR
- Fiche toxicologique du sélénium(INRS)
- Bleys Joachim, DIABETES CARE, APRIL 2007, 30 (4)
- S.J. Hamilton, Science of the Total Environment, 2004, 326, 1-31
- Centre d’Éxpertise en Analyse Environnementale du Québec, Détermination des métaux à l’état de trace en conditions propres dans l’eau : méthode par spectrométrie d’émission au plasma d’argon et détection par spectrométrie de masse, 2003, 1-29
- Emilien Pelletier ; Modification de la bioaccumulation du sélénium chez Mytilus edulis en présence du mercure organique et inorganique ; Can. J. Fish. Aquat. Sci. 43(1): 203–210 (1986); doi:10.1139/f86-023 ; 1986 CNRC Canada (Résumés anglais et français).
- Tarze A., Dauplais M., Grigoras I., Lazard M., Ha Duong N.T., Barbier F., Blanquet S., Plateau P. Extracellular production of hydrogen selenide accounts for thio-assisted toxicity of selenite against saccharomyces cerevisiae. THE JOURNAL OF BIOLOGICAL CHEMISTRY 282 (2007)12, 8759-8767
- Laure AVOSCAN (thèse de Doctorat à l'Université de Grenoble « Étude de la résistance de Cupriavidus metallidurans CH34 aux oxyanions sélénite et séléniate : accumulation, localisation et transformation du sélénium », 2007, CEA de Saclay
Bibliographie[modifier | modifier le code]
- Pierre Blazy et El-Aïd Jdid, Métallurgie de sélénium et du tellure, Fiche M 2370, Edition Techniques de l'Ingénieur, 15 pages.
- Alain Foucault, Jean-François Raoult, Fabrizio Cecca, Bernard Platevoet, Dictionnaire de Géologie - 5e édition, édition Dunod, 2014, 416 pages. Avec la simple entrée "Sélénium" p. 317.
- Bruce Herbert Mahan, Chimie, InterEdition, Paris, 1977, 832 p. (Traduction de University Chemistry, 2e éd., Addison-Wesley Publishing Company, Massachusetts, 1969 (ISBN 978-2-7296-0065-5)), en particulier p. 630 et p. 640-641.
- Paul Pascal, Nouveau traité de chimie minérale, Paris, Masson, (réimpr. 1966), 32 vol.
« 13.1 & 13.2 Oxygène, azote, oxydes, eau oxygénée, la combustion, soufre, sélénium, tellure, polonium »
- Thomas Thomson, Système de chimie, tome 4, Paris, 1818, traduit de la cinquième édition 1817 de l'anglais par Jean Riffault, p. 822 en particulier sur ce nouveau élément Se pp 740-748.
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
- Acide sélénique
- Anhydride sélénieux ou sélénite des anciens chimistes
- Acide sélénophosphorique
- Benzènesélénol
- Bessamatic
- Carence alimentaire en sélénium
- Cellules photovoltaïques au sélénium ou Cellule CIGS
- Chalcocite
- Chalcogénure
- Chalcophile
- Complément minéral A12CE
- Composé organosélénié
- Diséléniure
- Diséléniure de diphényle
- Disulfure de sélénium
- Éléments du bloc p
- Glutathion peroxydase
- Groupe fonctionnel du sélénium et de l'oxygène (ou de l'azote) en chimie organique
- Guilleminite
- Intoxication au sélénium (maladie professionnelle)
- Isotopes du sélénium
- Maladie de Keshan
- Métabolisme du sélénium
- Méthylsélénol
- Photophone (téléphonie)
- Réactif de Woollins
- Redresseur au sélénium
- Sélénite (sel)
- Sélénite de sodium
- Séléniate
- Séléniate de zinc
- Sélénium natif
- Séléniure
- Séléniure d'argent
- Séléniure de bismuth ou minéral guanajuatite
- Séléniure de cadmium et Rouge de cadmium
- Séléniure d'hydrogène
- Séléniure de plomb ou minéral clausthalite
- Séléniure de zinc
- Séléno- comme préfixe
- Sélénol
- Sélénocystéine et Sélénocystéine synthase
- Sélénométhionine
- Sélénoprotéine Sélénoprotéine P
- Sélénourée
- Sélone
- soufre sélénifère, variante du soufre natif
- Sulfoséléniure de bismuth ou minéral paraguanajuatite
- Thioséléniure
- Verre de chalcogénure
- Virage (photographie)
Liens externes[modifier | modifier le code]
- BRGM Panorama 2010 du marché du sélénium, août 2011
- (en) « Technical data for Selenium » (consulté le ), avec en sous-pages les données connues pour chaque isotope
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
| Métaux alcalins | Métaux alcalino-terreux | Lanthanides | Métaux de transition | Métaux pauvres | Métalloïdes | Non-métaux | Halogènes | Gaz nobles | Éléments non classés |
| Actinides | |||||||||
| Superactinides |



