Lipide


Les lipides constituent la matière grasse des êtres vivants. Ce sont des molécules hydrophobes ou amphiphiles — molécules hydrophobes possédant un domaine hydrophile — très diversifiées, comprenant entre autres les graisses, les cires, les stérols, les vitamines liposolubles, les mono-, di- et triglycérides, ou encore les phospholipides.
Les lipides peuvent se présenter à l'état solide, comme les cires, ou bien liquide, comme les huiles. Leur nature amphiphile conduit les molécules de certains lipides à s'organiser en vésicules, liposomes et micelles lorsqu'elles se trouvent en milieu aqueux. Cette propriété est à la base des mécanismes du vivant, permettant la formation de structures biologiques — cellules, organites — délimitées par des membranes constituées principalement de lipides. Les lipides assurent par ailleurs diverses autres fonctions biologiques[1],[2], notamment de signalisation cellulaire (signalisation lipidique) et de stockage de l'énergie métabolique par lipogenèse, énergie ensuite libérée notamment par β-oxydation.
Les lipides biologiques dérivent essentiellement de deux types de composés jouant le rôle de briques élémentaires, les groupes cétoacyle d'une part et les unités isoprène d'autre part. De ce point de vue, ils peuvent être classés en huit catégories différentes : les acides gras, les acylglycérols, les phosphoglycérides, les sphingolipides, les glycolipides et les polycétides, qui résultent de la condensation de groupes cétoacyle, auxquels s'ajoutent les stérols et les prénols, qui sont produits à partir d'unités isoprène[1].
Bien que le terme lipide soit souvent utilisé comme synonyme de graisse, ces deux termes ne sont pas équivalents car tous les lipides ne sont pas des graisses, lesquelles correspondent stricto sensu aux seuls triglycérides. Les lipides englobent à la fois les acides gras et leurs dérivés — y compris les mono-, di- et triglycérides ainsi que les phospholipides — mais aussi les métabolites comprenant des stérols, comme le cholestérol.
Classification[modifier | modifier le code]
La classification des lipides est un sujet complexe qui se heurte à la difficulté de définir des critères objectifs permettant de distinguer les lipides des autres classes de molécules organiques. L'IUPAC, par exemple, a publié en 1994[3] une classification des lipides excluant le cholestérol, classé comme terpénoïde[4], bien que le cholestérol soit indiscutablement de nature lipidique pour une très large majorité de biochimistes[5]. La classification des lipides actuellement généralement acceptée[1] établit huit classes, fondées en partie sur les définitions de l'IUPAC.
Acides gras[modifier | modifier le code]




Les acides gras sont des acides carboxyliques à chaîne aliphatique. Les acides gras naturels possèdent une chaîne carbonée de 4 à 36 atomes de carbone (rarement au-delà de 28) et typiquement en nombre pair. C'est cette chaîne carbonée qui confère aux acides gras leur caractère hydrophobe. Cette classe de molécules biologiques est présente en abondance chez les eucaryotes et les bactéries mais pas chez les archées, ce qui distingue ces dernières des bactéries parmi les procaryotes. La biosynthèse des acides gras est catalysée essentiellement par l'acide gras synthase et repose sur des condensations de Claisen successives d'unités malonyl-CoA ou méthylmalonyl-CoA sur une amorce d'acétyl-CoA.
Divers groupes fonctionnels contenant de l'oxygène, de l'azote, des halogènes ou du soufre peuvent être ajoutés à la chaîne hydrocarbonée des acides gras, qui peut être saturée ou insaturée et présenter dans ce cas une isomérie cis/trans affectant sensiblement la conformation générale des molécules. Les acides gras insaturés naturels adoptent généralement une configuration cis qui tend à courber la chaîne hydrocarbonée et ainsi à fluidifier les bicouches lipidiques en abaissant leur température de fusion ; il existe cependant des acides gras trans naturels, bien qu'ils résultent souvent d'un processus d'hydrogénation industrielle[6].
Certains acides gras ne peuvent être synthétisés en quantité suffisante par l'organisme et doivent alors être apportés entièrement ou partiellement par le régime alimentaire. C'est le cas notamment des acides gras dits « oméga-3 » et « oméga-6 », qui sont dits « essentiels ». Plus précisément, les mammifères sont incapables de synthétiser l'acide α-linolénique (ω-3) et l'acide linoléique (ω-6), mais peuvent en revanche convertir par exemple l'acide α-linolénique en acide docosahexaénoïque (DHA), un ω-3. Ces acides gras agissent de manière complexe dans l'organisme : les métabolites issus des oméga-6 sont pro-inflammatoires, prothrombotiques et hypertenseurs tandis que ceux issus des oméga-3 ont globalement un effet inverse.
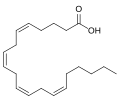
Les eicosanoïdes sont un autre exemple d'acides gras qui jouent un rôle physiologique important, cette fois comme vecteurs de signalisation cellulaire (on parle dans ce cas de signalisation lipidique). Issus principalement de l'acide arachidonique et de l'acide eicosapentaénoïque, ils regroupent les prostaglandines, les leucotriènes, la prostacycline et les thromboxanes.
-
Acide palmitique, saturé
-
Acide oléique, insaturé
-
Acide arachidonique, un des précurseurs d'eicosanoïdes
Acylglycérols ou glycérides[modifier | modifier le code]
Les glycérides sont constitués d'un résidu de glycérol estérifié par un, deux ou trois acides gras, ce qu'on appelle respectivement monoglycérides, diglycérides et triglycérides[7]. Les acides gras d'une même molécule de glycéride sont généralement différents les uns des autres. Ces lipides servent avant tout à stocker de l'énergie métabolique et constituent l'essentiel de la graisse animale. L'hydrolyse des liaisons ester pour libérer le glycérol et les acides gras constitue la première étape de la lipolyse, poursuivie notamment par la β-oxydation.
Certains glycolipides, organisés autour d'un résidu de glycérol lié par une liaison osidique à un ou plusieurs oses, sont considérés comme des glycérides, notamment les digalactosyldiacylglycérols membranaires des plantes[8], qu'on trouve également dans les séminolipides des spermatozoïdes chez les mammifères[9].
Phosphoacylglycérols ou phosphoglycérides[modifier | modifier le code]

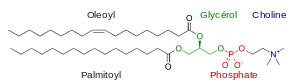
Les phosphoglycérides représentent, avec les sphingolipides, les principaux phospholipides, qui sont les principaux constituants des membranes biologiques — hormis chez les archées — et participent au métabolisme et à la signalisation cellulaire[10]. Les tissus nerveux et le cerveau en contiennent de grandes quantités, et des changements dans leur composition ont été impliqués dans divers troubles neurologiques[11].
Les phosphoglycérides bactériens diffèrent des phosphoglycérides d'eucaryotes par la position stéréochimique du groupe polaire sur le résidu de glycérol, les premiers étant sn-1 tandis que les seconds sont sn-3[12].
Parmi les phosphoglycérides des membranes biologiques se trouvent les phosphatidylcholines (lécithine), les phosphatidyléthanolamines et les phosphatidylsérines. Chez les eucaryotes, les phosphatidylinositols et les acides phosphatidiques jouent un rôle de messager secondaire (ou peuvent être précurseurs de messagers secondaires) en plus de leur rôle structurel dans les membranes. Des étherlipides dérivant structurellement de ces phosphoglycérides jouent également un rôle en signalisation cellulaire chez les eucaryotes, tels que les plasmalogènes, et sont les constituants essentiels des membranes plasmiques chez les archées[13].
Sphingolipides[modifier | modifier le code]


Les sphingolipides forment un ensemble complexe de composés[14] constitués d'un alcool aliphatique aminé, produit de novo à partir de la sérine et d'une acyl-CoA à longue chaîne, et convertie en céramides, phosphosphingolipides, glycosphingolipides et d'autres composés. Le principal alcool aminé des mammifères est la sphingosine. Les céramides — N-acylsphingoïdes — forment un sous-ensemble important des dérivés sphingoïdes, avec un acide gras lié par une liaison amide. Ces acides gras sont généralement saturés ou mono-insaturés avec une chaîne hydrocarbonée de 16 à 26 atomes de carbone.
Les sphingolipides les plus importants sont les sphingomyélines, des phosphosphingolipides constitués d'un céramide lié à un phosphocholine chez les mammifères[15] ou à une phosphoéthanolamine chez les insectes[16], tandis que les mycètes ont des phytocéramides liés à des groupes inositol phosphate et contenant du mannose[17]. Les glycosphingolipides forment une famille de molécules diversifiée constituées d'un ou plusieurs résidus osidiques liés à la base sphingoïde par une liaison osidique, comme les cérébrosides et les gangliosides.

Saccharolipides ou glycolipides[modifier | modifier le code]

Les glycolipides résultent de l'estérification d'oses ou de l'amidification d'osamines par des acides gras, formant des structures moléculaires compatibles avec les bicouches lipidiques des membranes biologiques. Dans ces composés, un ose joue le rôle du glycérol pour les glycérides et les phosphoglycérides. Les glycolipides les plus courants sont les acyles de glucosamine précurseurs du lipide A du lipopolysaccharide des bactéries à Gram négatif. Les molécules de lipide A sont généralement des disaccharides de glucosamine, qui peuvent porter jusqu'à sept résidus d'acides gras. Le lipopolysaccharide minimal requis pour le développement d'E. coli est le Kdo2-lipide A, un disaccharide hexa-acétylé de glucosamine glycosylé avec deux molécules d'acide céto-3-désoxy-D-manno-octulosonique (KDO)[18].
Polycétides[modifier | modifier le code]

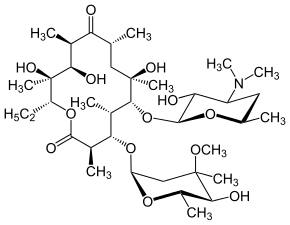
Les polycétides sont une famille de molécules naturelles très diversifiées et pourvues de diverses activités biologiques et propriétés pharmacologiques produites par les animaux, les plantes, les bactéries, et les mycètes[19],[20]. Ils comprennent des macrolides, des ansamycines, des polyènes, des polyéthers, des tétracyclines, des acétogénines, ainsi que divers composés tels que l'acide usnique, le discodermolide ou le radicicol. On distingue les polycétides :
- de type I, souvent produits par des mégasynthases multimodulaires, c'est-à-dire de grosses enzymes pourvues de plusieurs sites actifs assurant des réactions différentes et complémentaires ;
- de type II, de nature souvent aromatique et produits par un processus itératif réalisé par un ensemble d'enzymes dissociées ;
- de type III, souvent de petites molécules aromatiques produites par des espèces fongiques.
Ils sont généralement produits par condensation de Claisen d'acétyl-CoA, de propionyl-CoA et d'unités moléculaires dérivées de la malonyl-CoA, selon un processus semblable à celui de la biosynthèse des acides gras[21]. De nombreux polycétides sont des molécules cycliques dont la structure est modifiée par glycosylation, méthylation, hydroxylation, oxydation, voire d'autres réactions. De nombreux composés couramment utilisés comme antimicrobiens, antiparasitaires et anticancéreux sont des polycétides ou leurs dérivés, tels que l'érythromycine, les tétracyclines, les avermectines et les épothilones[22].
Stérols[modifier | modifier le code]

Les stérols, comme le cholestérol et ses dérivés, sont des constituants importants des membranes biologiques[23], à côté des phosphoglycérides et des sphingomyélines. Les stéroïdes, qui partagent tous le même noyau stérane à quatre cycles fusionnés, sont susceptibles d'agir biologiquement comme hormones et comme vecteurs de signalisation cellulaire (signalisation lipidique). Les stéroïdes à 18 atomes de carbone (C18) comprennent les œstrogènes tandis que les stéroïdes en C19 comprennent les androgènes tels que la testostérone et l'androstérone. Les stéroïdes en C21 comprennent les progestatifs ainsi que les glucocorticoïdes et les minéralocorticoïdes. Les sécostéroïdes, qui comprennent diverses formes de vitamine D (ergocalciférol et cholécalciférol notamment), sont caractérisés par le clivage du cycle B du noyau cyclopentanophénanthrène (stérane)[24]. Les acides biliaires et leurs conjugués sont d'autres exemples de stérols[25] ; chez les mammifères, ce sont des dérivés oxydés du cholestérol produits dans le foie. Chez les plantes, on trouve des phytostérols tels que le β-sitostérol, le stigmastérol, le brassicastérol, ce dernier étant également utilisé comme biomarqueur pour la croissance des algues[26]. L'ergostérol est le principal stérol membranaire chez les mycètes.
-
Nomenclature du stérane
Prénols[modifier | modifier le code]




Les prénols sont synthétisés à partir de précurseurs à cinq atomes de carbone, l'isopentényl-pyrophosphate (IPP) et le diméthylallyl-pyrophosphate (DMAPP), issus de la voie du mévalonate[27] chez tous les eucaryotes supérieurs et la plupart des bactéries ; chez les plantes, certains protozoaires et la plupart des bactéries (dans ce cas, parallèlement à la voie du mévalonate), ces précurseurs sont issus de la voie du méthylérythritol phosphate.
Les isoprénoïdes simples sont formés par l'addition successive d'unités en C5 et sont classés selon le nombre de ces unités terpène. Les composés contenant plus de 40 atomes de carbone sont appelés polyterpènes.
Les caroténoïdes sont des isoprénoïdes simples importants qui agissent comme des antioxydants et comme précurseurs de la vitamine A[28].
Les quinones et les hydroquinones sont une autre classe de molécules, qui contiennent une chaîne latérale isoprénique attachée à un noyau quinonoïde d'origine non isoprénique[29]. La vitamine E et les vitamines K, ainsi que les ubiquinones, sont des exemples de cette classe.
Les bactéries produisent des polyprénols appelés bactoprénols dans lesquels l'unité isoprénique terminale liée à l'hydroxyle reste insaturée, tandis que les animaux produisent des dolichols dans lequel l'unité isoprénique terminale est réduite[30].
Fonctions biologiques[modifier | modifier le code]
Membranes biologiques[modifier | modifier le code]
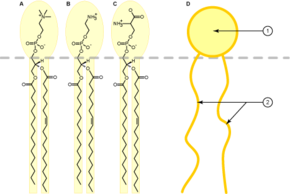
Les cellules d'eucaryotes sont compartimentées en organites délimités par des membranes et qui réalisent différentes fonctions biologiques. Les principaux constituants de ces membranes sont les phosphoglycérides : c'est le cas par exemple dans les membranes plasmiques et le système endomembranaire. Ce sont des molécules amphiphiles, c'est-à-dire qu'elles possèdent à la fois une région hydrophile — un résidu de glycérol-3-phosphate souvent appelé « tête hydrophile » — et une région hydrophobe souvent appelée « queue hydrophobe » constituée d'acides gras. Les membranes contiennent également des lipides autres que les phosphoglycérides, notamment des sphingomyélines et des stérols, ces derniers étant surtout représentés chez les animaux par le cholestérol.
Les membranes biologiques s'organisent autour d'une bicouche lipidique, constituée de deux feuillets parallèles dans lesquels les phosphoglycérides s'orientent pour présenter leur tête hydrophile au contact de l'eau et leurs queues hydrophobes au contact de l'autre feuillet. La formation d'une telle bicouche est thermodynamiquement favorable lorsque des phosphoglycérides se trouvent en milieu aqueux : c'est l'effet hydrophobe[31] ; l'orientation et la distribution spatiale des molécules d'eau autour d'une telle bicouche est étroitement conditionnée par la configuration des molécules amphiphiles qui la composent, de sorte que ces molécules d'eau forment comme des « clathrates » autour des lipides solvatés[32]. De telles bicouches tendent également à se refermer sur elles-mêmes, formant des vésicules. Selon la concentration en lipides, leur interaction biophysique peut conduire à la formation de micelles, de liposomes ou de surfaces membranaires. D'autres modes d'agrégation sont également observés et relèvent du polymorphisme des molécules amphiphiles. Le comportement des phases lipidiques est un domaine d'étude en biophysique et fait l'objet de recherches académiques[33],[34]. Selon certaines théories, la formation de protocellules délimitées par une membrane lipidique aurait été une étape de l'abiogenèse[35].
Chez les plantes, les membranes de thylakoïdes sont particulièrement riches en monogalactosyl diglycérides (MGDG), qui ne forment pas spontanément de bicouche lipidique mais entrent néanmoins dans de telles structures lorsqu'ils interagissent avec les caroténoïdes et les chlorophylles des membranes de thylakoïdes[36], de sorte que les membranes des thylakoïdes s'organisent en bicouche lipidique dynamique[37] ; elles contiennent en revanche peu de phospholipides.
Stockage d'énergie métabolique[modifier | modifier le code]
Les triglycérides stockés dans le tissu adipeux est la principale forme de stockage de l'énergie chez les animaux et les plantes. Les adipocytes sont les cellules chargées de la synthèse et de la dégradation des triglycérides chez les animaux ; chez ces derniers, la dégradation des triglycérides est essentiellement contrôlée par la lipase hormonosensible[38]. L'oxydation complète des acides gras, essentiellement par β-oxydation, fournit davantage d'énergie — sous forme d'ATP — que celle des glucides et des protéines : environ 37 kJ·g-1 contre 17 kJ·g-1 respectivement[39]. Les triglycérides sont par exemple le carburant utilisé par les oiseaux migrateurs pour assurer leurs vols à longue distance.
Signalisation cellulaire[modifier | modifier le code]
Ce n'est qu'assez récemment qu'a été établi le rôle déterminant de la signalisation lipidique comme composante de la signalisation cellulaire[40],[41]. La signalisation lipidique peut faire intervenir des récepteurs couplés aux protéines G ou des récepteurs nucléaires, et différents types de lipides ont été identifiés comme molécules de signalisation cellulaire et comme messagers secondaires[42]. On compte parmi eux la sphingosine-1-phosphate, un sphingolipide issu d'un céramide et agissant comme un puissant messager intervenant dans la régulation de la mobilisation du calcium[43], dans la croissance des cellules et dans l'apoptose[44] ; les diglycérides et les phosphatidylinositol phosphates (PIP), qui interviennent dans l'activation de la protéine kinase C[45] ; les prostaglandines, qui sont des eicosanoïdes impliqués dans les processus inflammatoires et immunitaires[46] ; les hormones stéroïdiennes telles que l'œstrogène, la testostérone et le cortisol, qui régulent les diverses fonctions du métabolisme, la reproduction et la pression artérielle ; les oxystérols tels que le 25-hydroxycholestérol, qui sont des agonistes des récepteurs nucléaires des oxystérols[47].
Les lipides de type phosphatidylsérine sont connus pour intervenir dans la signalisation de la phagocytose des cellules apoptotiques. Ils assurent cette fonction en se retrouvant dans le feuillet externe de la membrane plasmique après inactivation des flippases, qui les placent exclusivement dans le feuillet cytosolique, et activation des scramblases, qui les font passer d'un feuillet à l'autre : la présence de phosphatidylsérines dans le feuillet externe de la membrane plasmique est reconnue par certaines cellules, qui les phagocytent, de même qu'elles phagocytent d'éventuels fragment cellulaires exposant le feuillet interne de la membrane plasmique[48].
Autres fonctions[modifier | modifier le code]
Les vitamines liposolubles — vitamine A, vitamines D, vitamine E et vitamines K — sont des terpénoïdes emmagasinés dans le foie et les tissus adipeux. Ce sont des substances essentielles assurant diverses fonctions biologiques. Les acylcarnitines interviennent dans le métabolisme des acides gras et leur transport dans et hors des mitochondries, à l'intérieur desquelles ils sont dégradés par β-oxydation[49]. Les polyprénols et leurs dérivés phosphorylés jouent quant à eux un rôle important dans le transport des oligosaccharides à travers les membranes. Les dérivés osidiques à polyprénol phosphate et polyprénol diphosphate interviennent dans les réactions de glycosylation extra-cytoplasmiques, dans la biosynthèse extracellulaire de polysaccharides (par exemple dans la polymérisation du peptidoglycane chez les bactéries) et dans la N-glycosylation des protéines chez les eucaryotes[50],[51]. Les cardiolipines sont une sous-classe de phosphoglycérides contenant quatre résidus acyle et trois résidus de glycérol ; elles sont particulièrement abondantes dans la membrane mitochondriale interne[52],[53]. On pense qu'elles activent les enzymes qui interviennent dans la phosphorylation oxydative[54].
Métabolisme[modifier | modifier le code]
Les triglycérides, les stérols et les phospholipides membranaires des plantes et des animaux constituent l'essentiel des lipides de l'alimentation humaine et de celle des autres animaux. Le métabolisme lipidique est l'ensemble des processus par lesquels chaque tissu synthétise et dégrade ses lipides structurels et fonctionnels.
Digestion[modifier | modifier le code]

La digestion de certains lipides commence au niveau de la bouche avec l'action de la lipase linguale, une enzyme qui clive certains triglycérides à chaînes courtes en diglycérides et acides gras, tandis que les mucines de la salive des mammifères contribuent, par leur viscosité et leur action mécanique, à dissocier le bol alimentaire et à libérer les lipides.
Cependant, les lipides sont digérés essentiellement dans l'intestin grêle. La présence de graisses à ce niveau favorise la sécrétion d'hormones qui stimulent la libération, par le pancréas de la lipase pancréatique, enzyme active à pH acide, et de bile, cette dernière conduisant à une émulsion permettant l'absorption des lipides. La digestion complète des triglycérides conduit à un mélange d'acides gras, de monoglycérides, de diglycérides et de triglycérides non digérés, mais pas de glycérol libre.
Les triglycérides ne peuvent être absorbés par l'intestin grêle. En revanche, les entérocytes de la paroi intestinale absorbent le contenu des micelles en suspension dans la bile et reforment des triglycérides conditionnés avec des lipoprotéines dans de grandes micelles appelées chylomicrons. Ces derniers sont sécrétés dans les chylifères du système lymphatique, qui les déverse ensuite dans le sang depuis le conduit thoracique. Ainsi, contrairement aux autres nutriments, les triglycérides absorbés par l'alimentation passent dans le sang en court-circuitant le foie.
Biosynthèse[modifier | modifier le code]
Chez les animaux, des lipides peuvent être produits en réponse à l'absorption d'un excès de glucides (sucres). Ceci fait intervenir la biosynthèse des acides gras à partir d'acétyl-CoA, puis l'estérification d'une molécule de glycérol par les acides gras produits pour former une molécule de triglycéride. Ce processus est appelé lipogenèse.
Les acides gras sont produits par l'acide gras synthase, une enzyme qui polymérise les monomères acétyl-CoA, puis réduit le polymère résultant. La chaîne acyle de l'acide gras est allongée de manière itérative par un cycle de réactions qui ajoutent un groupe acétyle, le réduit en alcool, le déshydrate en alcène, et enfin le réduit à nouveau pour former un groupe alcane.
Les enzymes de la biosynthèse des acides gras sont classées en deux groupes distincts : chez les animaux et les champignons, toutes ces réactions sont réalisées par une protéine unique se comportant comme une enzyme multifonctionnelle[55], tandis que, chez les plastes des plantes et les bactéries, ces réactions sont réalisées chacune par une protéine dédiée, chacune se comportant comme une enzyme monofonctionnelle réalisant une étape particulière de cette voie métabolique[56],[57]. Ces acides gras peuvent être par la suite convertis en triglycérides qui sont conditionnés dans des lipoprotéines sécrétées par le foie.
La biosynthèse des acides gras insaturés fait intervenir des réactions de désaturation par lesquelles une double liaison est introduite dans la chaîne de l'acide gras. Ainsi, chez l'homme, la désaturation de l'acide stéarique par la stéaryl-CoA 9-désaturase conduit à l'acide oléique. L'acide linoléique, doublement insaturé, ainsi que l'acide α-linolénique, triplement insaturé, ne peuvent pas être produits par les tissus des mammifères, de sorte qu'ils doivent nécessairement être apportés par l'alimentation : ce sont des acides gras essentiels.
La biosynthèse des triglycérides intervient dans le réticulum endoplasmique à travers des voies métaboliques qui transfèrent les résidus acyle d'unités acyl-CoA aux groupes hydroxyle d'un résidu de glycérol.
Les terpènes et terpénoïdes, dont font partie les caroténoïdes, sont formés par assemblage et modification d'unités isoprène fournis par l'isopentényl-pyrophosphate et le diméthylallyl-pyrophosphate[27]. Ces précurseurs peuvent être obtenus de différentes manières. Chez les animaux et chez les archées, la voie du mévalonate produit ces molécules à partir de l'acétyl-CoA[58], tandis que les plantes et les bactéries les produisent à partir de pyruvate et de glycéraldéhyde-3-phosphate à travers la voie du méthylérythritol phosphate[27],[59]. La biosynthèse des stéroïdes est l'une des utilisations de tels isoprénoïdes activés les plus importantes, par l'intermédiaire du squalène et du lanostérol. Ce dernier peut ensuite être converti en cholestérol et en ergostérol[59],[60].
Dégradation[modifier | modifier le code]
La β-oxydation est la voie métabolique par laquelle les acides gras sont dégradés en acétyl-CoA dans les mitochondries ou dans les peroxysomes. L'oxydation des acides gras est, pour une large part, semblable, en sens inverse, à la biosynthèse des acides gras : des unités de deux atomes de carbone sont retirées séquentiellement à partir de l'extrémité de la chaîne hydrocarbonée de l'acide gras à l'issue de réactions de déshydrogénation, d'hydratation et d'oxydation pour former un β-cétoacide, clivé par thiolyse. L'acétyl-CoA est enfin converti en ATP, CO2 et H2O à travers le cycle de Krebs et la chaîne respiratoire. L'oxydation complète d'une molécule de palmitate produit ainsi 108 molécules d'ATP. La dégradation des acides gras insaturés ou à nombre impair d'atomes de carbone nécessitent des enzymes supplémentaires.
Diététique[modifier | modifier le code]
L'essentiel des lipides absorbés par l'alimentation est présent sous forme de triglycérides, de cholestérol et de phospholipides. Ils facilitent l'absorption des vitamines liposolubles — vitamine A, vitamine D, vitamine E et vitamine K — et des caroténoïdes. Chez les mammifères, certains acides gras, appelés acides gras essentiels, doivent être apportés par l'alimentation car ils ne peuvent être produits par l'organisme à partir d'autres précurseurs. C'est par exemple le cas de l'acide linoléique, un acide gras oméga-6, et de l'acide α-linolénique, un acide gras oméga-3. Ces deux acides gras essentiels sont des acides gras polyinsaturés à 18 atomes de carbone qui ne diffèrent que par le nombre et la position des doubles liaisons. La plupart des huiles végétales sont riches en acide linoléique, comme l'huile de carthame, l'huile de tournesol et l'huile de maïs. L'acide α-linolénique est présent dans les feuilles vertes et dans un ensemble de graines, de fruits à écale et de gousses, notamment l'huile de lin, l'huile de colza, l'huile de noix et l'huile de soja[61]. Les huiles de poisson sont particulièrement riches en acides gras ω-3 à longue chaîne tels que l'acide eicosapentaénoïque (EPA) et l'acide docosahexaénoïque (DHA). De nombreuses études ont démontré les effets bénéfiques pour la santé d'un régime alimentaire riche en acides gras ω-3 du point de vue du développement des enfants, de la prévention de cancers, de maladies cardiovasculaires et de divers troubles psychiques tels que la dépression, le trouble du déficit de l'attention et la démence[62],[63]. A contrario, il est établi que la consommation d'acides gras trans tels que ceux présents dans les huiles végétales hydrogénées sont des facteurs de risque accru pour les maladies cardiovasculaires[64],[65],[66].
Si la nature des lipides absorbés par l'alimentation est déterminante pour la santé, leur quantité totale importe finalement assez peu. Quelques études ont lié la quantité totale de lipides absorbés à un risque accru d'obésité[67],[68] et de diabète[69], mais de nombreuses études, dont certaines réalisées sur un grand nombre de personnes pendant plusieurs années[70], n'ont pas établi de tels liens[71],[72]. Ces études ne permettent pas non plus d'établir un lien entre le pourcentage de calories apportées par les lipides et un risque accru de cancer, de maladie cardiovasculaire ou d'obésité ; ainsi, contrairement aux idées véhiculées au siècle dernier, les régimes à faible apport en graisses ne sont pas nécessairement bénéfiques pour la santé[73], car les plats dits allégés issus de l'industrie agroalimentaire sont souvent enrichis en sucres cachés[74],[75],[76].
Notes et références[modifier | modifier le code]
- (en) Eoin Fahy, Shankar Subramaniam, Robert C. Murphy, Masahiro Nishijima, Christian R. H. Raetz, Takao Shimizu, Friedrich Spener, Gerrit van Meer, Michael J. O. Wakelam et Edward A. Dennis, « Update of the LIPID MAPS comprehensive classification system for lipids », Journal of Lipid Research, vol. 50, , S9-S14 (PMID 19098281, DOI 10.1194/jlr.R800095-JLR200, lire en ligne)
- (en) Shankar Subramaniam, Eoin Fahy, Shakti Gupta, Manish Sud, Robert W. Byrnes, Dawn Cotter, Ashok Reddy Dinasarapu et Mano Ram Maurya, « Bioinformatics and Systems Biology of the Lipidome », Chemical Reviews, vol. 111, no 10, , p. 6452-6490 (DOI 10.1021/cr200295k, lire en ligne)
- (en) Glossary of names of organic comounds and reactive intermediates based on structure, International Union of Pure and Applied Chemistry, Orgnanic Division - Commission on Nomenclature of Organic Chemistry, and Commission on Physical Organic Chemistry, 1994
- (en) Voir l'entrée des terpènoïdes sur le site de l'IUPAC
- (en) Konrad Bloch, « discours du 11 décembre 1964 » en recevant le prix Nobel de physiologie ou médecine.
- (en) J. Edward Hunter, « Dietary trans fatty acids: Review of recent human studies and food industry responses », Lipids, vol. 41, no 11, , p. 967-992 (PMID 17263298, DOI 10.1007/s11745-006-5049-y, lire en ligne)
- (en) Rosalind A. Coleman et Douglas P. Lee, « Enzymes of triacylglycerol synthesis and their regulation », Progress in Lipid Research, vol. 43, no 2, , p. 134-176 (PMID 14654091, DOI 10.1016/S0163-7827(03)00051-1, lire en ligne) DOI
- (en) Georg Hölzl, « Structure and function of glycoglycerolipids in plants and bacteria », Progress in Lipid Research, vol. 46, no 5, , p. 225-243 (PMID 17599463, DOI 10.1016/j.plipres.2007.05.001, lire en ligne)
- (en) Koichi Honke, Yanglong Zhang, Xinyao Cheng, Norihiro Kotani et Naoyuki Taniguchi, « Biological roles of sulfoglycolipids and pathophysiology of their deficiency », Glycoconjugate Journal, vol. 21, nos 1-2, , p. 59-62 (PMID 15467400, DOI 10.1023/B:GLYC.0000043749.06556.3d, lire en ligne)
- (en) Michael J. Berridge et Robin F. Irvine, « Inositol phosphates and cell signalling », Nature, vol. 341, , p. 197-205 (DOI 10.1038/341197a0, lire en ligne)
- (en) Akhlaq A Farooqui, Lloyd A Horrocks et Tahira Farooqui, « Glycerophospholipids in brain: their metabolism, incorporation into membranes, functions, and involvement in neurological disorders », Chemistry and Physics of Lipids, vol. 106, no 1, , p. 1-29 (DOI 10.1016/S0009-3084(00)00128-6, lire en ligne)
- (en) Pavlina T. Ivanova, Stephen B. Milne, Mark O. Byrne, Yun Xiang et H. Alex Brown, « Glycerophospholipid Identification and Quantitation by Electrospray Ionization Mass Spectrometry », Methods in Enzymology, vol. 432, , p. 21–57 (DOI 10.1016/S0076-6879(07)32002-8, lire en ligne)
- (en) Fritz Paltauf, « Ether lipids in biomembranes », Chemistry and Physics of Lipids, vol. 74, no 2, , p. 101-139 (DOI 10.1016/0009-3084(94)90054-X, lire en ligne)
- (en) Alfred H. Merrill Jr. et Konrad Sandhoff, « Chapter 14 Sphingolipids: metabolism and cell signaling », New Comprehensive Biochemistry, Biochemistry of Lipids, Lipoproteins and Membranes, 4e édition, vol. 36, , p. 373–407 (DOI 10.1016/S0167-7306(02)36016-2, lire en ligne)
- (en) Taro Hori et Mutsumi Sugita, « Sphingolipids in lower animals », Progress in Lipid Research, vol. 32, no 1, , p. 25-45 (PMID 8415797, DOI 10.1016/0163-7827(93)90003-F, lire en ligne)
- (en) Herbert Wiegandt, « Insect glycolipids », Biochimica et Biophysica Acta (BBA) - Lipids and Lipid Metabolism, vol. 1123, no 2, , p. 117-126 (PMID 1739742, DOI 10.1016/0005-2760(92)90101-Z, lire en ligne)
- (en) Xueli Guan, Markus R. Wenk, « Biochemistry of inositol lipids », Frontiers in Bioscience, vol. 13, , p. 3239-3251 (PMID 18508430, DOI 10.2741/2923, lire en ligne)
- (en) Christian R. H. Raetz, Teresa A. Garrett, C. Michael Reynolds, Walter A. Shaw, Jeff D. Moore, Dale C. Smith Jr., Anthony A. Ribeiro, Robert C. Murphy, Richard J. Ulevitch, Colleen Fearns, Donna Reichart, Christopher K. Glass, Chris Benner, Shankar Subramaniam, Richard Harkewicz, Rebecca C. Bowers-Gentry, Matthew W. Buczynski, Jennifer A. Cooper, Raymond A. Deems et Edward A. Dennis, « Kdo2-Lipid A of Escherichia coli, a defined endotoxin that activates macrophages via TLR-4 », Journal of Lipid Research, vol. 47, , p. 1097-1111 (PMID 16479018, DOI 10.1194/jlr.M600027-JLR200, lire en ligne)
- (en) Christopher T. Walsh, « Polyketide and Nonribosomal Peptide Antibiotics: Modularity and Versatility », Science, vol. 303, no 5665, , p. 1805-1810 (PMID 15031493, DOI 10.1126/science.1094318, lire en ligne)
- (en) Patrick Caffrey, Jesus F. Aparicio, Francisco Malpartida et Sergey B. Zotchev, « Biosynthetic Engineering of Polyene Macrolides Towards Generation of Improved Antifungal and Antiparasitic Agents », Current Topics in Medicinal Chemistry, vol. 8, no 8, , p. 639-653 (PMID 18473889, DOI 10.2174/156802608784221479, lire en ligne)
- (en) John A. Robinson, « Polyketide Synthase Complexes: Their Structure and Function in Antibiotic Biosynthesis », Philosophical Transactions of the Royal Society Biological Sciences, vol. 332, no 1263, , p. 107-114 (PMID 1678529, DOI 10.1098/rstb.1991.0038, lire en ligne)
- (en) Robert E. Minto et Brenda J. Blacklock, « Biosynthesis and function of polyacetylenes and allied natural products », Progress in Lipid Research, vol. 47, no 4, , p. 233-306 (PMID 18387369, DOI 10.1016/j.plipres.2008.02.002, lire en ligne)
- (en) Diana Bach et Ellen Wachtel, « Phospholipid/cholesterol model membranes: formation of cholesterol crystallites », Biochimica et Biophysica Acta (BBA) - Biomembranes, vol. 1610, no 2, , p. 187-197 (PMID 12648773, DOI 10.1016/S0005-2736(03)00017-8, lire en ligne)
- (en) Roger Bouillon, Annemieke Verstuyf, Chantal Mathieu, Sophie Van Cromphaut, Ritsuko Masuyama, Petra Dehaes et Geert Carmeliet, « Vitamin D resistance », Best Practice & Research Clinical Endocrinology & Metabolism, vol. 20, no 4, , p. 627-645 (PMID 17161336, DOI 10.1016/j.beem.2006.09.008, lire en ligne)
- (en) David W. Russell, « THE ENZYMES, REGULATION, AND GENETICS OF BILE ACID SYNTHESIS », Annual Review of Biochemistry, vol. 72, , p. 137-174 (PMID 12543708, DOI 10.1146/annurev.biochem.72.121801.161712, lire en ligne)
- (en) Jennifer C. Villinski, John M. Hayes, Simon C. Brassella, Virginia L. Riggert et Robert B. Dunbar, « Sedimentary sterols as biogeochemical indicators in the Southern Ocean », Organic Geochemistry, vol. 39, no 5, , p. 567–588 (DOI 10.1016/j.orggeochem.2008.01.009, lire en ligne)
- (en) Tomohisa Kuzuyama et Haruo Seto, « Diversity of the biosynthesis of the isoprene units », Natural Product Reports, vol. 20, no 2, , p. 171-183 (PMID 12735695, DOI 10.1039/B109860H, lire en ligne)
- (en) A.V. Rao et L.G. Rao, « Carotenoids and human health », Pharmacological Research, vol. 55, no 3, , p. 207-216 (PMID 17349800, DOI 10.1016/j.phrs.2007.01.012, lire en ligne)
- (en) Anders Brunmark et Enrique Cadenas, « Redox and addition chemistry of quinoid compounds and its biological implications », Free Radical Biology and Medicine, vol. 7, no 4, , p. 435-477 (PMID 2691341, DOI 10.1016/0891-5849(89)90126-3, lire en ligne)
- (en) Ewa Swiezewska et Witold Danikiewicz, « Polyisoprenoids: Structure, biosynthesis and function », Progress in Lipid Research, vol. 44, no 4, , p. 235-258 (DOI 10.1016/j.plipres.2005.05.002, lire en ligne)
- (en) P. M. Wiggins, « Role of water in some biological processes », Microbiology and Molecular Biology Reviews, vol. 54, no 4, , p. 432-449 (PMID 2087221, PMCID 372788, lire en ligne)
- (en) « Nonpolar solutes enhance water structure within hydration shells while reducing interactions between them », Proceedings of the National Academy of Sciences of the United States of America, vol. 102, no 19, , p. 6777-6782 (PMID 15867152, PMCID 1100774, DOI 10.1073/pnas.0500225102, lire en ligne)
- (en) Gerrit van Meer, Dennis R. Voelker et Gerald W. Feigenson, « Membrane lipids: where they are and how they behave », Nature Reviews Molecular Cell Biology, vol. 9, no 2, , p. 112-124 (PMID 18216768, PMCID 2642958, DOI 10.1038/nrm2330, lire en ligne)
- (en) Gerald W. Feigenson, « Phase behavior of lipid mixtures », Nature Chemical Biology, vol. 2, no 11, , p. 560-563 (PMID 17051225, PMCID 2685072, DOI 10.1038/nchembio1106-560, lire en ligne)
- (en) Daniel Segré, Dafna Ben-Eli, David W. Deamer et Doron Lancet, « The Lipid World », Origins of life and evolution of the biosphere, vol. 31, no 1, , p. 119-145 (PMID 11296516, DOI 10.1023/A:1006746807104, lire en ligne)
- (en) R. C. Yashroy, « Lamellar dispersion and phase separation of chloroplast membrane lipids by negative staining electron microscopy », Journal of Biosciences, vol. 15, no 2, , p. 93-98 (DOI 10.1007/BF02703373, lire en ligne)
- (en) R. C. Yashroy, « Magnetic resonance studies of dynamic organisation of lipids in chloroplast membranes », Journal of Biosciences, vol. 15, no 1990, , p. 281-288 (DOI 10.1007/BF02702669, lire en ligne)
- (en) Dawn L. Brasaemle, « Thematic review series: Adipocyte Biology. The perilipin family of structural lipid droplet proteins: stabilization of lipid droplets and control of lipolysis », Journal of Lipid Research, vol. 48, no 12, , p. 2547-2559 (PMID 17878492, DOI 10.1194/jlr.R700014-JLR200, lire en ligne)
- « snv.jussieu.fr/vie/dossiers/gl… »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?).
- (en) Xuemin Wang, « Lipid signaling », Current Opinion in Plant Biology, vol. 7, no 3, , p. 329-336 (PMID 15134755, DOI 10.1016/j.pbi.2004.03.012, lire en ligne)
- (en) Ashok Reddy Dinasarapu, Brian Saunders, Iley Ozerlat3 Kenan Azam et Shankar Subramaniam, « Signaling gateway molecule pages—a data model perspective », Bioinformatics, vol. 27, no 12, , p. 1736-1738 (PMID 21505029, PMCID 3106186, DOI 10.1093/bioinformatics/btr190, lire en ligne)
- (en) Kathleen M. Eyster, « The membrane and lipids as integral participants in signal transduction: lipid signal transduction for the non-lipid biochemist », Advances in Physiology Education, vol. 31, no 1, , p. 5-16 (PMID 17327576, DOI 10.1152/advan.00088.2006, lire en ligne)
- (en) V. Hinkovska-Galcheva, S. M. VanWay, T. P. Shanley et R. G. Kunkel, « The role of sphingosine-1-phosphate and ceramide-1-phosphate in calcium homeostasis », Current Opinion in Investigational Drugs, vol. 9, no 11, , p. 1192-1205 (PMID 18951299)
- (en) Sahar A. Saddoughi, Pengfei Song et Besim Ogretmen, « Roles of Bioactive Sphingolipids in Cancer Biology and Therapeutics », Lipids in Health and Disease, vol. 49, , p. 413-440 (PMID 18751921, PMCID 2636716, DOI 10.1007/978-1-4020-8831-5_16)
- (en) Christian Klein et Anant N. Malviya, « Mechanism of nuclear calcium signaling by inositol 1,4,5-trisphosphate produced in the nucleus, nuclear located protein kinase C and cyclic AMP-dependent protein kinase », Frontiers in Bioscience, vol. 13, , p. 1206-1226 (PMID 17981624, DOI 10.2741/2756, lire en ligne)
- (en) Joshua A. Boyce, « Eicosanoids in asthma, allergic inflammation, and host defense », Current Molecular Medicine, vol. 8, no 5, , p. 335-349 (PMID 18691060, DOI 10.2174/156652408785160989, lire en ligne)
- (en) Jerzy Bełtowski, « Liver X Receptors (LXR) as Therapeutic Targets in Dyslipidemia », Cardiovascular Therapeutics, vol. 26, no 4, , p. 297-316 (PMID 19035881, DOI 10.1111/j.1755-5922.2008.00062.x, lire en ligne)
- (en) Mona Biermann, Christian Maueröder, Jan M Brauner, Ricardo Chaurio, Christina Janko, Martin Herrmann et Luis E Muñoz, « Surface code—biophysical signals for apoptotic cell clearance », Physical Biology, vol. 10, no 6, , p. 065007 (PMID 24305041, DOI 10.1088/1478-3975/10/6/065007, lire en ligne)
- (en) C. Indiveri, A. Tonazzi et F. Palmieri, « Characterization of the unidirectional transport of carnitine catalyzed by the reconstituted carnitine carrier from rat liver mitochondria », Biochimica et Biophysica Acta (BBA) - Biomembranes, vol. 1069, no 1, , p. 110-116 (PMID 1932043, DOI 10.1016/0005-2736(91)90110-T, lire en ligne)
- (en) Armando J. Parodi et Luis F. Leloir, « The role of lipid intermediates in the glycosylation of proteins in the eucaryotic cell », Biochimica et Biophysica Acta (BBA) - Reviews on Biomembranes, vol. 559, no 1, , p. 1-37 (PMID 375981, DOI 10.1016/0304-4157(79)90006-6, lire en ligne)
- (en) Ari Helenius et Markus Aebi, « Intracellular Functions of N-Linked Glycans », Science, vol. 291, no 5512, , p. 2364-2369 (PMID 11269317, DOI 10.1126/science.291.5512.2364, lire en ligne)
- (en) Marcin Nowicki, Franck Müller et Margrit Frentzen, « Cardiolipin synthase of Arabidopsis thaliana », FEBS Letters, vol. 579, no 10, , p. 2161-2165 (PMID 15811335, DOI 10.1016/j.febslet.2005.03.007, lire en ligne)
- (en) Vishal M. Gohil et Miriam L. Greenberg, « Mitochondrial membrane biogenesis: phospholipids and proteins go hand in hand », Journal of Cell Biology, vol. 184, no 4, , p. 469-472 (PMID 19237595, PMCID 2654137, DOI 10.1083/jcb.200901127, lire en ligne)
- (en) Frederic L. Hoch, « Cardiolipins and biomembrane function », Biochimica et Biophysica Acta (BBA) - Reviews on Biomembranes, vol. 1113, no 1, , p. 71-133 (PMID 10206472, DOI 10.1016/0304-4157(92)90035-9, lire en ligne)
- (en) Subrahmanyam S. Chirala et Salih J. Wakil, « Structure and function of animal fatty acid synthase », Lipids, vol. 39, no 11, , p. 1045-1053 (PMID 15726818, DOI 10.1007/s11745-004-1329-9, lire en ligne)
- (en) Stephen W. White, Jie Zheng, Yong-Mei Zhang et Charles O. Rock, « The structural biology of type II fatty acid biosynthesis », Annual Review of Biochemistry, vol. 74, , p. 791-831 (PMID 15952903, DOI 10.1146/annurev.biochem.74.082803.133524, lire en ligne)
- (en) John B. Ohlrogge et Jan G. Jaworski, « Regulation of Fatty Acid Synthesis », Annual Review of Plant Physiology and Plant Molecular Biology, vol. 48, , p. 109-136 (PMID 15012259, DOI 10.1146/annurev.arplant.48.1.109, lire en ligne)
- (en) Laura L. Grochowski, Huimin Xu et Robert H. White, « Methanocaldococcus jannaschii Uses a Modified Mevalonate Pathway for Biosynthesis of Isopentenyl Diphosphate », Journal of Bacteriology, vol. 188, no 9, , p. 3192-3198 (PMID 16621811, PMCID 1447442, DOI 10.1128/JB.188.9.3192-3198.2006, lire en ligne)
- (en) Hartmut K. Lichtenthaler, « The 1-deoxy-D-Xylulose-5-Phosphate Pathway of Isoprenoid Biosynthesis in Plants », Annual Review of Plant Physiology and Plant Molecular Biology, vol. 50, , p. 47-65 (PMID 15012203, DOI 10.1146/annurev.arplant.50.1.47, lire en ligne)
- (en) N. D. Lees, B. Skaggs, D. R. Kirsch et M. Bard, « Cloning of the late genes in the ergosterol biosynthetic pathway of Saccharomyces cerevisiae — A review », Lipids, vol. 30, no 3, , p. 221-226 (PMID 7791529, DOI 10.1007/BF02537824, lire en ligne)
- (en) Gian Luigi Russo, « Dietary n − 6 and n − 3 polyunsaturated fatty acids: From biochemistry to clinical implications in cardiovascular prevention », Biochemical Pharmacology, vol. 77, no 6, , p. 937-946 (PMID 19022225, DOI 10.1016/j.bcp.2008.10.020, lire en ligne)
- (en) Natalie D. Riediger, Rgia A. Othman, Miyoung Suh et Mohammed H. Moghadasian, « A Systemic Review of the Roles of n-3 Fatty Acids in Health and Disease », Journal of the Academy of Nutrition and Dietetics, vol. 109, no 4, , p. 668-679 (PMID 19328262, DOI 10.1016/j.jada.2008.12.022, lire en ligne)
- (en) Claudio Galli et Patrizia Risé, « Fish Consumption, Omega 3 Fatty Acids and Cardiovascular Disease. The Science and the Clinical Trials », Nutrition and Health, vol. 20, no 1, , p. 11-20 (PMID 19326716, DOI 10.1177/026010600902000102, lire en ligne)
- (en) R. Micha et D. Mozaffarian, « Trans fatty acids: Effects on cardiometabolic health and implications for policy », Prostaglandins, Leukotrienes and Essential Fatty Acids, vol. 79, nos 3-5, , p. 147-152 (PMID 18996687, PMCID 2639783, DOI 10.1016/j.plefa.2008.09.008, lire en ligne)
- (en) I. Dalainas et H. P. Ioannou, « The role of trans fatty acids in atherosclerosis, cardiovascular disease and infant development », International Angiology : a Journal of the International Union of Angiology, vol. 27, no 2, , p. 146-156 (PMID 18427401, lire en ligne)
- (en) Dariush Mozaffarian et Walter C. Willett, « Trans fatty acids and cardiovascular risk: A unique cardiometabolic imprint? », Current Atherosclerosis Reports, vol. 9, no 6, , p. 486-493 (PMID 18377789, DOI 10.1007/s11883-007-0065-9, lire en ligne)
- (en) Arne Astrup, Jørn Dyerberg, Matthew Selleck et Steen Stender, « Nutrition transition and its relationship to the development of obesity and related chronic diseases », Obesity Reviews, vol. 9, no s1, , p. 48-52 (PMID 18307699, DOI 10.1111/j.1467-789X.2007.00438.x, lire en ligne)
- (en) Arne Astrup, « The Role of Dietary Fat in Obesity », Seminars in Vascular Medicine, vol. 5, no 1, , p. 40-47 (PMID 15968579, DOI 10.1055/s-2005-871740, lire en ligne)
- (en) Arne Astrup, « Dietary Management of Obesity », Journal of Parenteral & Enteral Nutrition, vol. 32, no 5, , p. 575-577 (PMID 18753397, DOI 10.1177/0148607108321707, lire en ligne)
- notamment une étude portant sur 49 000 femmes pendant huit ans baptisée Women's Health Initiative Dietary Modification Trial, mais aussi la Nurses' Health Study et la Health Professionals Follow-up Study
- (en) Shirley A. A. Beresford, Karen C. Johnson, Cheryl Ritenbaugh, Norman L. Lasser, Linda G. Snetselaar, Henry R. Black, Garnet L. Anderson, Annlouise R. Assaf, Tamsen Bassford, Deborah Bowen, Robert L. Brunner, Robert G. Brzyski, Bette Caan, Rowan T. Chlebowski, Margery Gass, Rosanne C. Harrigan, Jennifer Hays, David Heber, Gerardo Heiss, Susan L. Hendrix, Barbara V. Howard, Judith Hsia, F. Allan Hubbell, Rebecca D. Jackson, Jane Morley Kotchen, Lewis H. Kuller, Andrea Z. LaCroix, Dorothy S. Lane, Robert D. Langer, Cora E. Lewis, JoAnn E. Manson, Karen L. Margolis, Yasmin Mossavar-Rahmani, Judith K. Ockene, Linda M. Parker, Michael G. Perri, Lawrence Phillips, Ross L. Prentice, John Robbins, Jacques E. Rossouw, Gloria E. Sarto, Marcia L. Stefanick, Linda Van Horn, Mara Z. Vitolins, Jean Wactawski-Wende, Robert B. Wallace et Evelyn Whitlock, « Low-Fat Dietary Pattern and Risk of Colorectal Cancer – The Women's Health Initiative Randomized Controlled Dietary Modification Trial », Journal of the American Medical Association, vol. 295, no 6, , p. 643-654 (PMID 16467233, DOI 10.1001/jama.295.6.643, lire en ligne)
- (en) Barbara V. Howard, JoAnn E. Manson, Marcia L. Stefanick, Shirley A. Beresford, Gail Frank, Bobette Jones, Rebecca J. Rodabough, Linda Snetselaar, Cynthia Thomson, Lesley Tinker, Mara Vitolins et Ross Prentice, « Low-Fat Dietary Pattern and Weight Change Over 7 Years – The Women's Health Initiative Dietary Modification Trial », Journal of the American Medical Association, vol. 295, no 1, , p. 39-49 (PMID 16391215, DOI 10.1001/jama.295.1.39, lire en ligne)
- (en) « Fats and Cholesterol », The Nutrition Source, sur Harvard School of Public Health (consulté le )
- (en) Patty W. Siri-Tarino, Qi Sun, Frank B. Hu et Ronald M. Krauss, « Saturated Fatty Acids and Risk of Coronary Heart Disease: Modulation by Replacement Nutrients », Current Atherosclerosis Reports, vol. 12, no 6, , p. 384-390 (PMID 20711693, PMCID 2943062, DOI 10.1007/s11883-010-0131-6, lire en ligne)
- (en) Frank B. Hu, « Are refined carbohydrates worse than saturated fat? », The American Journal of Clinical Nutrition, vol. 91, no 6, , p. 1541-1542 (PMID 20410095, PMCID 2869506, DOI 10.3945/ajcn.2010.29622, lire en ligne)
- (en) Marianne U. Jakobsen, Claus Dethlefsen, Albert M. Joensen, Jakob Stegger, Anne Tjønneland, Erik B. Schmidt et Kim Overvad, « Intake of carbohydrates compared with intake of saturated fatty acids and risk of myocardial infarction: importance of the glycemic index », The American Journal of Clinical Nutrition, vol. 91, no 6, , p. 1764-1768 (PMID 20375186, DOI 10.3945/ajcn.2009.29099, lire en ligne)
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
- Lipogenèse
- Biosynthèse des acides gras
- β-oxydation
- Classification des lipides
- Indice chimique
- Test d'émulsion