Peptide
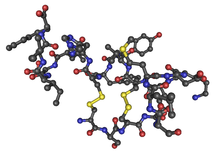


Un peptide est un polymère d’acides aminés reliés entre eux par des liaisons peptidiques.
Il existe une énorme variété de peptides différents. Par exemple, sachant qu'il existe 20 acides aminés distincts chez les mammifères, le nombre de peptides différents formés de seulement dix résidus d'acides aminés vaut un peu moins de 1,668 × 1013, soit près de 16 680 milliards.
Les peptides constitués d’un faible nombre d’acides aminés (de deux à quelques dizaines) sont nommés oligopeptides. Ils ne sont généralement pas issus de la traduction d’ARNm, mais d’une synthèse enzymatique. Ces oligopeptides peuvent aussi être classés selon le nombre d’acides aminés : ceux comportant deux acides aminés (comme l'aspartame ou l'alitame) sont nommés dipeptides, et ceux comportant trois acides aminés sont nommés tripeptides. Généralement, lorsqu’ils sont plus longs, on parle simplement de peptides (c'est-à-dire qu’on ne précise plus le nombre d’acides aminés).
Les polymères comprenant un plus grand nombre d’acides aminés sont nommés polypeptides. Ceux-ci sont généralement issus d’une traduction d’ARNm.
Les protéines, enfin, sont des assemblages d’un ou plusieurs polypeptides ayant subi des modifications post-traductionnelles et un repliement protéinique.
Les neuropeptides sont des peptides sécrétés par un neurone, qui se singularisent alors par leur fonction (neurotransmetteur).
Description[modifier | modifier le code]
Après la constitution de la chaine peptidique, une extrémité est porteuse d'un groupement amine libre — l'extrémité N — ou amino-terminale, et l'autre d'un groupement carboxylique — extrémité C — ou carboxyl-terminale. Dans certains cas ces groupements, tout comme les chaines latérales des acides aminés, peuvent être modifiés. Par convention, et également à cause de la direction de leur synthèse, les séquences peptidiques sont toujours considérées dans le sens N vers C. Pour les acides aminés dicarboxyliques ou diaminés, on précise le carboxyle ou l'amine engagé dans la liaison peptidique.

Différentes classes de peptides[modifier | modifier le code]
Les peptides ribosomiques sont synthétisés par traduction de l'ARNm et sont utilisés comme molécule signal ou comme hormone peptidique.
Les peptides non ribosomiques représentent une famille très diverse de produits naturels avec de très nombreuses activités biologiques et de propriétés pharmacologiques.
Les peptides en cosmétique[modifier | modifier le code]
La peau est, par sa taille, l’un des organes les plus importants du corps humain. Elle est composée de différentes couches de cellules où de nombreux peptides ont pu être identifiés et utilisés en cosmétique.
L’élastine est une protéine structurale sécrétée par les fibroblastes impliquée dans les propriétés d’élasticité de la peau. La séquence VGVAPG a été identifiée plusieurs fois dans cette protéine[1]. Le palmitoyle oligopeptide Pal-VGVAPG-OH stimule la prolifération des fibroblastes permettant de rendre à la peau plus d’élasticité. On peut donc le retrouver dans des produits cosmétiques revendiquant une amélioration de la fermeté du buste par exemple ou du visage avec une action contre les rides[réf. nécessaire].
Le collagène est une protéine présente dans la matrice extracellulaire qui confère aux tissus une résistance mécanique à l’étirement. Le GHK[2] a été identifié comme un fragment issu de la dégradation du collagène. Le palmitoyle oligopeptide Pal-GHK-OH stimule la production de collagène permettant le remplacement de celui dégradé. Il peut être utilisé dans des produits cosmétiques ayant des revendications variées par exemple ceux ayant pour finalité de lutter contre les rides ou contre les vergetures. On le retrouve également dans des produits proposant une augmentation du volume des lèvres.
On retrouve également des peptides dans des immunoglobulines qui sont des glycoprotéines douées d’une fonction anticorps[3]. Ainsi le Palmitoyl tétrapeptide-7 (Pal-GQPR-OH) inhibe la production d’interleukine 6 (agent pro-inflammatoire) ce qui a pour effet de protéger la peau des agressions externes retardant ainsi son vieillissement (il stimule également la production de collagène). Là encore les applications sont diverses, mais on peut considérer par exemple qu’en renforçant la structure de la peau fragile du contour de l’œil, cette séquence peptidique permet d’éviter la perméabilité capillaire et donc l’apparition de cernes.
Les peptides sont aussi présents dans des mécanismes décontractant par le biais des enképhalines comme la kyotorphine (YR)[4] identifiée en 1979. Il a pour effet de décontracter les muscles et a donc naturellement été utilisé dans l’industrie cosmétique pour diminuer les rides d’expression.
Enfin les cheveux sont également concernés par les peptides[5]. Ainsi le biotinyl tripeptide-1 (Biot-GHK-OH) agit à la fois sur l’enracinement mais également sur la croissance du cheveu. Il permet donc des revendications cosmétiques contre la chute de cheveux.
Les peptides bioactifs[modifier | modifier le code]
Définition[modifier | modifier le code]
Les peptides bioactifs sont des séquences protéiques de 2 et 20 acides aminés, dérivés de produits alimentaires comme le lait ou les protéagineuses. Ce sont de courtes séquences d’acides aminés à activité biologique, capables d’exercer différentes actions physiologiques dans l’organisme[6].
Obtention de peptides bioactifs[modifier | modifier le code]
Les peptides peuvent être générés en laboratoire, par hydrolyse enzymatique de protéines préexistantes, ou bien lors de la digestion des protéines. Une fois assimilés par l’organisme, ils deviennent métaboliquement actifs.
Au préalable, les protéines dont on souhaite extraire les peptides sont purifiés par diverses méthodes (extraction à l’éthanol, CO2 supercritique, etc.) afin de retirer les éventuels contaminants. Elles sont ensuite dégradées en plus petits fragments par hydrolyse enzymatique, ou par fermentation[7]. Pour modifier ou améliorer les peptides, l’hydrolyse enzymatique est la meilleure façon de faire à condition que cela se fasse dans les conditions spécifiques (pH, température, solubilité, etc.) propres à l’enzyme.
Les biopeptides peuvent se trouver dans différentes macrostructures biologiques : ils peuvent être incorporés, dispersés ou en suspension dans des émulsions, liposomes ou des biopolymères afin d’atteindre leur activité métabolique optimale. Ce sont des stratégies de protection contre les possibles hydrolyses lors de la digestion, afin de ne pas dégrader les biopeptides et, par extension, leur activité métabolique[8].
À la suite de la réaction enzymatique, l’hydrolysat obtenu est centrifugé. Le surnageant, riche en peptides de faible poids moléculaires, est récupéré et les peptides sont isolés (par chromatographie, ultrafiltration, etc.) pour sélectionner les peptides d’intérêt.
Effets potentiels sur la santé[modifier | modifier le code]
L’usage des peptides bioactifs en alimentaire a fait l’objet d’un grand intérêt ces dernières années. D’un point de vue nutritionnel, des études ont montré que ces molécules possèdent des propriétés antimicrobiennes, antihypertensives, antioxydantes ou immunitaires intéressantes[7].
Différentes formulations alimentaires incluant les peptides sont en cours de recherche. Ils pourraient être utilisés comme ingrédients principaux afin de mieux réguler les fonctions métaboliques du corps humain. Par exemple, les biopeptides issus des produits laitiers s’avèrent avoir des rôles physiologiques tels que l’amélioration de la défense immunitaire ou encore la diminution du risque d’obésité[9]. À cet effet, certaines marques se sont lancées dans la production de produits laitiers fermentés pour lutter contre certaines pathologies.
De plus, des peptides capables d’inhiber l’activité de l’ACE, réduisant ainsi la pression artérielle, ont été identifiés chez diverses espèces animales et végétales[10].
Ils peuvent également avoir des propriétés antidiabétiques : certains peptides issus du haricot noir (AKSPLF, ATNPLF, FEELN, and LSVSVL) se sont montrés efficaces pour inhiber certains transporteurs de glucose comme GLUT2 ou SGLT1, faisant baisser le taux de glycémie. Cependant, ces résultats restent encore à étudier in vivo[11].
De même, des études se penchent sur les effets hypocholestérolémiants des peptides comme chez le soja (LPYP, IAVPGEVA and IAVPTGVA) pourrait avoir des multiples effets sur la voie d’absorption des LDL, contribuant à un meilleur contrôle de la cholestérolémie[11].
Ces effets pourraient se combiner pour un même peptide, rendant leur étude plus complexe.
Ainsi, les peptides bioactifs seraient une piste intéressante pour augmenter la valeur nutritionnelle de certains aliments. Pour l'heure, leurs effets bénéfiques sur la santé nécessitent des études complémentaires. À cet effet, l’utilisation de ces peptides en tant qu’aliments fonctionnels ou nutricaments est encore soumise à contrôle, notamment pour augmenter leur stabilité et évaluer les risques de toxicité et d’allergie chez l’Homme[10].
Notes et références[modifier | modifier le code]
- R. M. Senior, G. L. Griffin, R. P. Mecham et D. S. Wrenn, « Val-Gly-Val-Ala-Pro-Gly, a repeating peptide in elastin, is chemotactic for fibroblasts and monocytes », The Journal of Cell Biology, vol. 99, no 3, , p. 870–874 (ISSN 0021-9525, PMID 6547961, PMCID PMC2113419, lire en ligne, consulté le )
- F. X. Maquart, L. Pickart, M. Laurent et P. Gillery, « Stimulation of collagen synthesis in fibroblast cultures by the tripeptide-copper complex glycyl-L-histidyl-L-lysine-Cu2+ », FEBS letters, vol. 238, no 2, , p. 343–346 (ISSN 0014-5793, PMID 3169264, lire en ligne, consulté le )
- N. I. Veretennikova, G. I. Chipens, G. V. Nikiforovich et Y. R. Betinsh, « Rigin, another phagocytosis-stimulating tetrapeptide isolated from human IgG. Confirmations of a hypothesis », International Journal of Peptide and Protein Research, vol. 17, no 4, , p. 430–435 (ISSN 0367-8377, PMID 7309346, lire en ligne, consulté le )
- H. Takagi, H. Shiomi, H. Ueda et H. Amano, « Morphine-like analgesia by a new dipeptide, L-tyrosyl-L-arginine (Kyotorphin) and its analogue », European Journal of Pharmacology, vol. 55, no 1, , p. 109–111 (ISSN 0014-2999, PMID 436940, lire en ligne, consulté le )
- H. Uno et S. Kurata, « Chemical agents and peptides affect hair growth », The Journal of Investigative Dermatology, vol. 101, no 1 Suppl, , p. 143S–147S (ISSN 0022-202X, PMID 8326148, lire en ligne, consulté le )
- Karine Pierre, « Les peptides bioactifs du lait : un atout pour la santé humaine ? », sur CERIN (consulté le )
- (en) Eric Daliri, Deog Oh et Byong Lee, « Bioactive Peptides », Foods, vol. 6, no 5, , p. 32 (ISSN 2304-8158, DOI 10.3390/foods6050032, lire en ligne, consulté le )
- Sami Saadi, Nazamid Saari, Farooq Anwar et Azizah Abdul Hamid, « Recent advances in food biopeptides: Production, biological functionalities and therapeutic applications », Biotechnology Advances, vol. 33, no 1, , p. 80–116 (ISSN 0734-9750, DOI 10.1016/j.biotechadv.2014.12.003, lire en ligne, consulté le )
- Jolanta Artym et Michał Zimecki, « Milk-derived proteins and peptides in clinical trials », Postępy Higieny i Medycyny Doświadczalnej, vol. 67, , p. 800–816 (ISSN 1732-2693, DOI 10.5604/17322693.1061635, lire en ligne, consulté le )
- (en) Barbara Walther et Robert Sieber, « Bioactive Proteins and Peptides in Foods », International Journal for Vitamin and Nutrition Research, vol. 81, no 23, , p. 181–192 (ISSN 0300-9831 et 1664-2821, DOI 10.1024/0300-9831/a000054, lire en ligne, consulté le )
- (en) Eric Daliri, Deog Oh et Byong Lee, « Bioactive Peptides », Foods, vol. 6, no 5, , p. 32 (ISSN 2304-8158, PMID 28445415, PMCID PMC5447908, DOI 10.3390/foods6050032, lire en ligne, consulté le )

