Fièvre Q
| Causes | Coxiella burnetii |
|---|---|
| Transmission | Transmission vectorielle (d), transmission aéroportée (d), transmission par contact (d) et contamination féco-orale |
| Incubation min | 3 j |
| Incubation max | 32 j |
| Symptômes | Fièvre, céphalée, nausée, frissonnement (en), vomissement, diarrhée, douleur abdominale, douleur thoracique, douleur musculo-squelettique secondaire chronique (d), toux, anorexie, exanthème, hépatomégalie, splénomégalie, hypotension artérielle et bradycardie |
| Médicament | Doxycycline, DL-ofloxacine, azithromycine, péfloxacine et hydroxychloroquine |
|---|---|
| Spécialité | Infectiologie |
| CIM-10 | A78 |
|---|---|
| CIM-9 | 083.0 |
| DiseasesDB | 11093 |
| MedlinePlus | 001337 |
| eMedicine |
227156 ped/1973 |
| MeSH | D011778 |
| Patient UK | Q-fever-pro |
La fièvre Q ou coxiellose est une maladie causée par la bactérie Coxiella burnetii. Ce microorganisme est répandu dans le monde entier, les réservoirs de l’agent pathogène sont nombreux chez les mammifères sauvages et domestiques : on peut le détecter chez les bovins, les moutons, les chèvres et autres mammifères domestiques, ainsi que les chats et les chiens. La transmission de l'infection se fait par voie aérienne par l’inhalation de particules contaminées en suspension dans l’air et le contact cutané ou muqueux avec les selles, l'urine, les sécrétions vaginales, le sperme, le lait, le placenta des animaux infectés[1],[2]. La période d'incubation est de 9 à 40 jours. Il s’agit probablement de la zoonose la plus contagieuse qui existe, car une seule bactérie suffit à infecter un homme[3].
Histoire[modifier | modifier le code]
Pour comprendre l’origine de la fièvre Q, il faut remonter à 1935 dans la ville de Brisbane, au Queensland en Australie où durant cette période on constate l’apparition d’épisodes fébriles chez des employés d’abattoirs[4]. Celle-ci interpelle le biologiste australien Edward Holbrook Derrick (en), alors directeur du laboratoire de microbiologie et d’anatomopathologie du ministère de la santé du Queensland[5].
Faute de trouver l’agent infectieux responsable de ce qu’il décide d’appeler « the Query fever »[4] et suspectant une origine virale de la maladie, il décide d’envoyer des échantillons de sang de patients à son collègue virologue, l’australien Frank Macfarlane Burnet. À cette époque, ce dernier est directeur de l’institut médical Walter et Eliza Hall (en), et il recevra en 1960 le prix Nobel de médecine pour ses recherches sur la tolérance immuno acquise chez les patients greffés. Avec son collaborateur Mavis Freeman, Macfarlane parvient à reproduire en 1937 la maladie sur différents animaux. Ils parviennent ainsi à isoler sur des coupes de rate de souris l’agent infectieux qui, au premier abord, ressemble à s’y méprendre à des bactéries de type Rickettsies. Derrick et ses associés finiront par la nommer à tort Rickettsia burnetii en hommage à son ami virologue. L’étude épidémiologique de ce qui s’appelle aujourd’hui la fièvre Q amène Derrick et son équipe aux conclusions suivantes : d’une part, les animaux sauvages constituent le réservoir naturel de la maladie et les animaux domestiques un réservoir secondaire ; d’autre part, les vecteurs de transmissions sont de la famille des arthropodes, plus particulièrement des tiques.
Durant la même période, de l’autre côté du Pacifique, le bactériologiste Américain Gordon Davis étudie dans le Montana la fièvre pourprée des montagnes rocheuses. Son étude porte sur des tiques prélevées près de la crique du bassin du Nine Mile, qui induisent après morsure une maladie fébrile chez certains cochons d’Inde. Cependant, même si les deux agents pathogènes semblent proches, les symptômes cliniques et les données biologiques semblent ne pas correspondre à la fièvre pourprée. C’est en 1936, avec l’arrivée d’un autre bactériologiste américain dans l’équipe de Davis au laboratoire des Rocky Mountain, Herald Rea Cox, qu’il est démontré que l’agent étiologique possède à la fois des propriétés de virus et de Ricketssies. Cox réussit à propager l’agent infectieux dans des œufs embryonnés et il décide de le nommer Rickettsia diaporica (ou agent Nine Mile), dérivé du mot grec pour sa capacité à passer à travers les pores d’un filtre. Mais c’est un événement fortuit qui établira le lien entre les travaux de Derrick/Burnet en Australie et ceux de Cox aux États-Unis. En effet, en 1938, Rolla Eugene Dyer (en), directeur de l’institut national de santé américaine (NIH), se contamine accidentellement avec un échantillon présent dans le laboratoire des Rocky Moutain (en) à Hamilton où il se rendait pour vérifier la possibilité de cultiver Rickettsia diaporica dans des œufs. Il développe alors une fièvre passagère qu’il réussit à reproduire sur des cobayes en leurs inoculant son propre sang. De plus, il retrouve dans les coupes de rates de ces mêmes animaux l’agent infectieux Rickettsia diaporica. Cet événement interpelle Dyer qui avait déjà eu vent des travaux australiens sur Rickettsies Burnetii. Guidé par son intuition, il demande alors à son collègue australien Macfarlane Burnett de lui faire parvenir des échantillons de rates provenant d’animaux infectés par l’agent de la fièvre Q. L’immunité croisée alors retrouvée entre les agents isolés de son sang, les cobayes infectés par son sang, et ceux infectés par l’agent de la fièvre Q confirme son hypothèse. Rickettsia burnetii et Rickettsia diaporica sont en réalité le même agent, responsable de la fièvre Q. Ce n’est finalement qu’en 1948, après que la distinction entre cette espèce de bactéries et les autres Rickettsia soit significative, que l’entomologiste américain Cornelius Becker Philip, membre du laboratoire de Rocky Moutain, décide de créer un nouveau genre de bactéries : les Coxiella. En hommage à Macfarlane Burnet et à Herald Cox, il décide d’appeler l’agent infectieux de la fièvre Q Coxiella Burnetii.
Écoépidémiologie[modifier | modifier le code]
Il existe probablement un ou plusieurs réservoirs-animaux, dont peut-être les rats (Rattus norvegicus et Rattus rattus)[6].
Incidence et aspects épidémiologiques[modifier | modifier le code]
L'agent pathogène peut être retrouvé partout dans le monde à l’exception de l’Antarctique et de la Nouvelle-Zélande.
En Europe, l'infection se manifeste plutôt sous la forme d’une hépatite que d’une pneumonie comme aux États-Unis. La bactérie est extrêmement résistante et infectieuse : un organisme unique est capable de provoquer une infection. La voie de contamination la plus courante de l'infection est l’inhalation de poussière contaminée[4], le contact du lait[réf. nécessaire], de la viande, de la laine contaminée et, plus particulièrement les produits de la mise bas[4].
À l'inverse, toutes les études[réf. nécessaire] ont montré qu'il n'y avait pas de contamination par voie orale, c'est-à-dire en consommant des aliments (lait, fromage, viande) issus d'animaux infectés.
Les tiques peuvent transmettre l'agent pathogène à d'autres animaux. La transmission d’humain à humain semble extrêmement rare et jusqu'ici n’a été décrite que dans très peu de cas.
Les hommes sont un peu plus souvent affectés que les femmes, ce qui peut très probablement être attribué à des taux d'emploi différents dans des professions spécifiques ainsi que la sécrétion d’œstrogènes chez la femme ayant un rôle protecteur[réf. nécessaire].
Parmi les métiers « à risque » on peut citer, (mais la liste n’est pas limitative) :
- le personnel vétérinaire,
- les ouvriers des parcs à bétail,
- les fermiers,
- les tondeurs,
- les transporteurs d’animaux,
- les techniciens de laboratoire manipulant des échantillons vétérinaires potentiellement infectés ou visitant les abattoirs,
- les équarrisseurs qui traitent les carcasses des kangourous.
Physiopathologie[modifier | modifier le code]
L’entrée de C.burnetii dans les cellules (monocytes et macrophages) s’opère de façon passive par phagocytose. Immédiatement, l’environnement acide du phagosome (pH à 4,5) permet sa multiplication où elle survit par :
- la production d’enzymes à haut point isoélectrique ;
- l’inhibition de la production de radicaux libres ;
- la sécrétion de superoxyde dismutase ;
- l’inhibition de l’étape finale de maturation du phagosome (fusion avec la cathepsine D).
La bactérie a une infectiosité majeure puisqu’une seule bactérie est suffisante pour provoquer une infection. Chez l’animal, la voie respiratoire est associée à une pneumopathie et la voie intrapéritonéale est associée à une hépatite.
L’inhibition de l’apoptose est un facteur important de la virulence de C.burnetii. La survie et la multiplication dans la vacuole acide protège la bactérie des antibiotiques et font de Coxiella burnetii une espèce bactérienne unique en son genre.
Initialement, cette vacuole contenant la bactérie a été faussement identifiée comme étant un « gros phagolysome ». Mais un nombre croissant de preuves indique désormais que cette vacuole est en réalité un compartiment spécialisé, activement modifié par C.burnetii. Nous parlons de « vacuole parasitophore » ou (PV). Certaines expériences de cultures cellulaires montrent que ces vacuoles sont dépourvues de protéines p62 et GM130, marqueurs du noyau et de l’appareil de Golgi ; ce qui indique une séparation efficace de la vacuole des autres compartiments de la cellule hôte.
C. burnetii présente un cycle de développement comportant une forme intracellulaire et une forme extracellulaire plus petite, produite par pseudosporulation[4]. Ces pseudospores métaboliquement inactifs sont extrêmement résistants dans le milieu extérieur (agents chimiques désinfectants, pH, température, dessiccation, pression osmotique). C. burnetii peut survivre 40 mois dans du lait conservé à température ambiante, deux ans à −20 °C et huit mois dans de la laine conservée à +20 °C.
Le contrôle immunitaire de C. burnetii est assuré par les lymphocytes T mais ne permet pas toujours l’éradication définitive de la bactérie. Chez les vertébrés, l’infection aiguë conduit à la formation de granulomes, témoins d’une réponse immunitaire locale efficace. C’est pourquoi C. burnetii est indétectable par PCR ou immunohistochimie dans ces lésions. Dans la fièvre Q chronique, la réponse immunitaire étant inefficace, voire délétère, C.burnetii se multiplie dans les macrophages et est à l’origine d’une bactériémie prolongée malgré la forte concentration des trois classes d’anticorps (IgG, M et A de phase I et de phase II). Il existe une inversion du ratio CD4/CD8. À ce stade, les biopsies de foie, de valve cardiaque ou d’anévrisme ne présentent pas de granulome mais des cellules avec une grande vacuole contenant C. burnetii. L’interleukine 10, cytokine à propriété anti-inflammatoire, est fortement sécrétée dans le contexte de fièvre Q chronique, notamment par les monocytes des patients « en rechute ». Dans ce contexte, elle est également corrélée à un mauvais contrôle de la réplication bactérienne. Son inhibition expérimentale par des anticorps restaure les propriétés bactéricides des macrophages.
Il existe de nombreux facteurs susceptibles d’avoir une influence sur l’infection à C.burnetii, notamment son passage vers la chronicité. De nombreux travaux expérimentaux chez l’animal ont permis de mettre en évidence ces différents facteurs.
Le rôle protecteur des hormones féminines (17β-œstradiol) a été démontré et pourrait expliquer pourquoi le sex-ratio est déséquilibré en faveur des hommes seulement après la puberté. A contrario, les femelles animales gestantes ont plus de fièvre Q chronique et d’endocardites car C. burnetii persiste dans l’utérus, les glandes mammaires et peut être réactivée par d’autres gestations.
L’immunodépression est corrélée avec la gravité de l’infection au cours de la fièvre Q aiguë et elle favorise la fièvre Q chronique. Une immunodépression expérimentale (par injection de cortisone) est responsable d’une réactivation chez des animaux apparemment guéris. Le rôle des lymphocytes T est souligné par le fait que les souris athymiques développent toujours une infection chronique, ce qui n’est pas le cas pour les souris euthymiques.
Une persistance antigénique non infectieuse au sein des macrophages pourrait être responsable d’un syndrome de fatigue chronique post fièvre Q par une stimulation non contrôlée du système immunitaire. On parle d’IMC (complexe immunomodulateur) pour définir ces fragments de bactéries qui peuvent persister dans les macrophages longtemps après une infection.
Clinique[modifier | modifier le code]
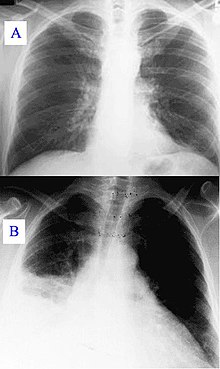
La manifestation la plus répandue est un syndrome grippal avec un début brusque[1], fièvre, malaise, maux de tête violents, myalgies (douleurs des muscles), perte d'appétit, toux sèche, douleur pleurétique, frissons, confusion et symptômes gastro-intestinaux à type de nausées, vomissements et diarrhée. La fièvre dure approximativement 7 à 14 jours.
Pendant sa progression, la maladie peut évoluer vers une pneumonie atypique, qui peut mettre en cause le pronostic vital en raison d’un syndrome de détresse respiratoire aiguë (ARDS), de tels symptômes se produisent habituellement pendant les 4 à 5 premiers jours de la maladie.
Plus rarement la fièvre Q provoque une hépatite[1] (granulomateuse[7]) qui se manifeste par un malaise général, de la fièvre, une augmentation de volume du foie (hépatomégalie), une douleur dans le quadrant supérieur droit de l'abdomen et parfois un ictère (jaunisse).
La forme chronique de la fièvre Q se manifeste principalement par l’inflammation de la paroi interne du cœur (endocardite[1]) chez un patient présentant une valvulopathie préexistante connue ou méconnue et qui peut survenir des mois ou des années après l’infection initiale. En l’absence de traitement, la maladie est habituellement mortelle. Cependant avec un traitement approprié la létalité atteint 10 %.
Formes cliniques en médecine humaine[modifier | modifier le code]
- Fausses couches et accouchement prématurés[8]
- Pneumonie atypique
- Hépatites[1]
- Forme typhoïde
- Endocardite infectieuse subaiguë[9],[10], voire chronique[1]
- Myocardite
- Péricardite
- Méningite, encéphalite[11]
- Neuropathie périphérique[11]
Formes cliniques en médecine vétérinaire[modifier | modifier le code]
Carnivores domestiques[modifier | modifier le code]
Les chiens et les chats peuvent être infectés par la fièvre Q et sont donc une source reconnue d’infections animales et humaines même si, en Europe, leur rôle potentiel reste peu étudié. Les animaux infectés restent le plus souvent asymptomatiques tout en étant contagieux mais des cas d’avortements ont été décrits à plusieurs reprises.
Petits ruminants[modifier | modifier le code]
Chez les petits ruminants, les avortements, souvent tardifs, sont la manifestation clinique la plus fréquente et la plus visible[4]. Ils peuvent apparaître isolément ou massivement (jusque 90 % des animaux gestants). Des cas de pneumonies, de kératoconjonctivites, de jeunes mort nés ou faibles sont également connus.
L’infection chronique avec excrétion de la bactérie par voie vaginale ou mammaire sur de longues périodes est plus fréquente chez la chèvre. Chez le mouton, le rôle de C. burnetii dans certains cas de mammites est toujours discuté.
Bovins[modifier | modifier le code]
La prévalence sérologique de C. burnetii est remarquablement homogène en Europe : environ 60 % des troupeaux montrent la trace sérologique d’une infection. L’expression clinique est moins fréquente. On estime qu’environ 3 à 10 % de ces troupeaux montrent ou ont montré des troubles associés en tout ou en partie à la présence de fièvre Q. Chez le bovin, si le signe le plus facile à mettre en évidence par l’éleveur reste l’avortement[4], ce n’est pas le plus fréquent. L’infertilité, les métrites (essentiellement tardives après l'insémination artificielle)), le repeat breeding, la rétention placentaire, la naissance de veaux faibles sont des signes d’appels souvent méconnus mais qui constituent la part majeure des pertes économiques liées à la fièvre Q. En cas d’avortement, le fœtus est macroscopiquement normal hormis certains cas de bronchopneumonie. Les placentas peuvent montrer des lésions intercotylédonnaires fibrineuses, la présence d’exsudat, mais ces lésions ne sont ni systématiques ni pathognomoniques. Par ailleurs, des cas de bronchopneumonie et de myocardites ont été décrits après inoculation expérimentale. Le rôle potentiel dans des atteintes mammaires est fréquemment évoqué mais reste discuté.
Autres espèces[modifier | modifier le code]
L’infection par C. burnetii a été mise en évidence dans de nombreuses espèces animales, depuis l’amibe jusqu’au chameau. Les ongulés sauvages, les porcs, les oiseaux, les chevaux, les rongeurs peuvent être infectés sans que la clinique exacte qui en résulte soit réellement connue.
Diagnostic[modifier | modifier le code]
Signes cliniques[modifier | modifier le code]
- Syndrome infectieux avec fièvre élevée
- Altération de l'état général avec myalgies, asthénie
- Signes respiratoires
- Atteinte hépatique
Signes biologiques[modifier | modifier le code]
- Syndrome inflammatoire
- Cytolyse hépatique
l'hépatite de la fièvre Q se manifeste par une élévation des transaminases ALAT et transaminases ASAT, mais le diagnostic de certitude n’est possible que sur la biopsie du foie. - Séroconversion de la sérologie de Coxiella burnetii
Le diagnostic repose habituellement sur la sérologie (recherche des anticorps, c'est-à-dire de la réponse de l’organisme à l’infection) plutôt que sur la recherche du germe infectant lui-même. La sérologie permet de détecter une infection chronique alors que des niveaux élevés d'anticorps sont retrouvés dans l’infection aigüe contre la forme virulente de la bactérie. La détection moléculaire de l'ADN bactérien est de plus en plus utilisée. La culture est techniquement difficile et n’est pas disponible en routine dans la plupart des laboratoires de microbiologie.
Signes radiologiques[modifier | modifier le code]
Pneumopathie atypique
Échocardiographie[modifier | modifier le code]

La fièvre Q peut provoquer une endocardite (infection des valves du cœur) chez les patients présentant une valvulopathie. Le diagnostic est fait par échocardiographie.
Signes histologiques[modifier | modifier le code]
Ponction biopsie hépatique : permet de découvrir des granulomes en beignets avec un anneau de fibrine[7].
Traitement[modifier | modifier le code]

Le traitement de la fièvre Q à sa phase aiguë avec un antibiotique est très efficace et devrait être prescrit avec l’avis d’un infectiologue. On utilise généralement les cyclines, la doxycycline, la tétracycline, le chloramphénicol, la ciprofloxacine, l’ofloxacine avec l’hydroxychloroquine. La forme chronique est plus difficile à traiter et peut nécessiter jusqu'à quatre ans de traitement avec la doxycycline et les quinolones ou la doxycycline avec l’hydroxychloroquine.
Il est particulièrement difficile de traiter la fièvre Q pendant la grossesse parce que la doxycycline et la ciprofloxacine sont contrindiquées pendant la grossesse. Le traitement à privilégier est le cotrimoxazole pendant cinq semaines[12].
Prévention en médecine humaine[modifier | modifier le code]
Il existe un moyen de prévention efficace de la fièvre Q, par la vaccination intradermique utilisant un vaccin composé d'organismes tués de Coxiella burnetii[13]. En 2011, l'EFSA (de l'anglais : European Food Safety Authority) a estimé que la vaccination était la protection la plus efficace à long terme[14].
Un test cutané et une analyse de sang préalables à la vaccination doivent être réalisés afin de rechercher s'il n'y a pas d'immunité préexistante, car la vaccination des sujets immunisés peut avoir comme conséquence une réaction locale sévère. Après injection d'une dose unique de vaccin, l'immunité protectrice dure pendant de nombreuses années et la revaccination n'est généralement pas exigée. Un contrôle sérologique annuel est en principe recommandé.
En 2001, l’Australie a lancé un programme national de vaccination contre la fièvre Q pour les personnes travaillant dans des métiers « à risque ».
Prévention en médecine vétérinaire[modifier | modifier le code]
Prévention non médicale de la fièvre Q[modifier | modifier le code]
La prévention non médicale de la fièvre Q passe par les mesures classiques prises lors de pathologies infectieuses abortives. Leur efficacité ne doit pas être sous estimée dans le cadre d’une gestion globale de la fièvre Q. L’isolement des femelles ayant avorté[4], le ramassage et la destruction des produits de mises bas[4], la minimisation de la formation d’aérosol lors des manipulations d’effluents d’élevage sont les mesures minimales qui diminuent le risque de contamination animale et humaine.
Utilisation raisonnée d’antibiotique[modifier | modifier le code]
L’efficacité des antibiotiques, et en particulier des tétracyclines, dans la prévention et le traitement de la fièvre Q a été et reste discutée. Un consensus existe pour estimer que les antibiotiques ne peuvent éliminer les C. burnetii chez un animal infecté ni empêcher ou prévenir les signes cliniques sur le long terme. Néanmoins, leur utilisation à des moments précis (tarissement, animaux gestants, post-vêlage) semble donner de bons résultats transitoires, en attendant une vaccination, dans certaines exploitations. Le protocole le plus couramment employé reste l’utilisation de tétracyclines longue action, à 20 mg/kg, cette injection étant éventuellement renouvelée 2 semaines plus tard.[réf. nécessaire] Des résultats futurs devraient préciser l’intérêt de cette utilisation.
Vaccin Phase 1[modifier | modifier le code]
Du même type que le vaccin utilisé en médecine humaine dans certains pays, un vaccin basé sur C. burnetii phase 1, cultivés sur œufs SPF, jouit à présent d’une autorisation de Mise sur le marché européenne. Ce vaccin est basé sur les lipopolysaccharides pariétaux (LPS) complets, ultra-purifiés. L'ensemble des animaux de plus de trois mois, non gestants de l'exploitation devront être vaccinés.
Divers[modifier | modifier le code]
En raison de son mode de transmission, cette bactérie peut être utilisée comme agent vecteur dans la guerre biologique. Voir également bioterrorisme.
Notes et références[modifier | modifier le code]
- (en) NR Parker, JH Barralet, AM Bell, « Q fever », Lancet, no 367, , p. 679–688 (PMID 16503466, lire en ligne, consulté le ).
- Guy Czaplicki, Jean-Yves Houtain, Cédric Mullender et Sarah Rebecca Porter, « Apparent prevalence of antibodies to Coxiella burnetii (Q fever) in bulk tank milk from dairy herds in southern Belgium », Veterinary Journal (London, England: 1997), vol. 192, no 3, , p. 529–531 (ISSN 1532-2971, PMID 21962829, DOI 10.1016/j.tvjl.2011.08.033, lire en ligne, consulté le )
- Matteo Bonazzi, « Développement d’un crible multi-phénotypique pour l’étude des interactions hôte/pathogène », sur cnrs.fr, (consulté le ).
- Gwenaël Vourc'h et al., Les zoonoses : Ces maladies qui nous lient aux animaux, Éditions Quæ, coll. « EnjeuxScience », (ISBN 978-2-7592-3270-3, lire en ligne), Quelques exemples de maladies zoonotiques, « La fièvre Q », p. 77-78, accès libre.
- Dr MBOUSSOU Yoan Michel, Complications périnatales associées à une exposition à la fièvre Q : étude épidémiologique à l’île de la Réunion, Île de la Réunion, Université de Bordeaux 2, (lire en ligne), p. 9-16.
- (en)Coxiella burnetii (Q fever) in Rattus norvegicus and Rattus rattus at livestock farms and urban locations in the Netherlands; could Rattus spp. represent reservoirs for (re)introduction?, Preventive Veterinary Medicine, In Press, Corrected Proof, Available online 2 June 2011 a Netherlands Centre for Infectious Disease Control, Institut national de la santé publique et de l'environnement (RIVM), P.O. Box 1, 3720 BA Bilthoven.
- (en) van de Veerdonk FL, Schneeberger PM., « Patient with fever and diarrhea », Clin Infect Dis, vol. 42, , p. 1051–1052 (PMID 16514741, lire en ligne).
- (en) Carcopino X, Raoult D, Bretelle F, Boubli L, Stein A. « Q Fever during pregnancy: a cause of poor fetal and maternal outcome » Ann N Y Acad Sci. 2009;1166:79-89. DOI 10.1111/j.1749-6632.2009.04519.x.
- De laco AC, Praz G. « Fièvre qui dure : que faire ? [Various causes of fever of unknown origin »] Rev Med Suisse 2008;4(174):2139-40, 2142-4. .
- (en) Griffin AT, Espinosa M, Nakamatsu R. « Q fever endocarditis: an unusual presentation » Am J Med Sci. 2012;344(6):480-4. DOI 10.1097/MAJ.0b013e3182684979.
- (en) Bernit E, Pouget J, Janbon F, Dutronc H, Martinez P, Brouqui P, Raoult D. « Neurological involvement in acute Q fever: a report of 29 cases and review of the literature » Arch Intern Med. 2002;162(6):693-700. .
- (en) Carcopino X, Raoult D, Bretelle F, Boubli L, Stein A, « Managing Q fever during pregnancy: The benefits of long-term Cotrimoxazole therapy », Clin Infect Dis, vol. 45, , p. 548–555 (lire en ligne).
- (en)Leone M. « Effect of sex on Coxiella burnetii » J Infect Dis. 1996;173:484-87.
- Depêche vétérinaire, « Fièvre Q : la vaccination est l’option la plus efficace à long terme » estime l’EFSA[PDF], 4 juin 2010.

