Inhibiteur sélectif de la recapture de la sérotonine
Les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS ; SSRI (Selective Serotonin Reuptake Inhibitor) en anglais) sont une classe médicamenteuse de psychotropes, de type antidépresseurs. Ils opèrent dans le cerveau, notamment en augmentant le taux d'un neurotransmetteur appelé sérotonine (5-hydroxytryptamine ou 5-HT). Ils agissent en inhibant la recapture de la sérotonine au niveau de la synapse[1].
Les ISRS sont fréquemment prescrits, outre leur indication principale qu'est la dépression, dans les cas d'anxiété et de trouble obsessionnel compulsif et dans les douleurs neuropathiques réfractaires (duloxétine), en réduisant la charge émotionnelle, en augmentant le tonus (effet booster) et en créant une désinhibition potentiellement dangereuse (virage maniaque, bipolarité iatrogène[2] au niveau du gyrus cingulaire). Ils ont aussi un effet négatif sur la libido (diminution ou absence de désir sexuel) ; cet effet indésirable permet de retarder l'orgasme chez les hommes souffrant d'éjaculation précoce avec un succès estimé de 60 % en l'absence d'études sérieuses.
Ce sont les antidépresseurs les plus prescrits dans de nombreux pays[3].
Indications[modifier | modifier le code]
La principale indication des ISRS réside dans le traitement de la dépression associé à une psychothérapie. Les ISRS sont souvent prescrits pour les troubles anxieux (comme la phobie sociale et les troubles paniques), les troubles obsessionnels compulsifs et le syndrome de stress post-traumatique. Ils sont aussi très souvent prescrits pour lutter contre l’impulsivité et l’irritabilité ainsi que les symptômes anxieux et dépressifs du trouble de la personnalité borderline malgré le manque de preuves solides[4],[5]. Ils sont aussi utilisés pour traiter les troubles de dépersonnalisation malgré de faibles résultats[6]. La plupart des essais cliniques ont donné des résultats négatifs concernant l'utilisation des antidépresseurs de type ISRS dans le traitement de l'anorexie mentale[7].
Liste d'ISRS[modifier | modifier le code]
Les médicaments de cette classe comprennent diverses molécules. Ils ont un nom reconnu internationalement : la dénomination commune internationale. Les génériques reprennent souvent cette DCI. Les noms commerciaux entre parenthèses sont ceux que l'on trouve en France, il existe de nombreuses autres appellations en fonction des pays.
- la fluoxétine (Prozac) ;
- la paroxétine (Deroxat, Divarius, Paxil) ;
- la sertraline (Zoloft) ;
- le citalopram (Seropram, Celexa) ;
- l'oxalate d'escitalopram (Seroplex, Cipralex) ;
- l'indalpine (en) ;
- la zimelidine ;
- la dapoxétine (Priligy) ;
- le maléate de fluvoxamine (Floxyfral) ;
Agents proches[modifier | modifier le code]
Il existe des inhibiteurs de la recapture de la sérotonine non sélectifs :
- les IRSNa : les inhibiteurs de la recapture de la sérotonine et de la noradrénaline : duloxétine (Cymbalta), venlafaxine (Effexor) ;
- les inhibiteurs de la recapture de la sérotonine de la noradrénaline et de la dopamine ;
- les promoteurs sélectifs de la recapture de la sérotonine : tianeptine (Stablon) ;
Autres types d'antidépresseurs[modifier | modifier le code]
Les ISRS ne sont pas la seule famille d'antidépresseurs existant. D'autres sont des antagonistes de la sérotonine, ou inhibent d'autres récepteurs ou enzymes :
- les antidépresseurs tricycliques ;
- les inhibiteurs de monoamine oxydase ;
- un antidépresseur mélatoninergique, l'agomélatine ;
- les agonistes dopaminergiques (recherche) (pramipexole, aripiprazole) ;
- la plante appelée millepertuis perforé.
Suppléments de 5-HTP au lieu d'ISRS[modifier | modifier le code]
Une alternative controversée à la prescription d'ISRS est la supplémentation en 5-HTP, dont le mécanisme d'action est différent : au lieu d'interrompre la recapture de la sérotonine, le 5-HTP, étant un précurseur de la sérotonine, permet d'en augmenter la concentration[8], alors que l'ajout de sérotonine directement - selon les études effectuées - serait inutile[9], voir dangereux en raison du risque d'apparition d'un syndrome serotoninergique.
Mécanismes d'actions[modifier | modifier le code]
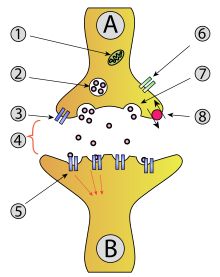
Augmentation de la sérotonine dans la fente synaptique[modifier | modifier le code]
Dans le cerveau, l'information passe d'un neurone à l'autre par l'intermédiaire de la synapse, un espace entre deux neurones où le neurone qui envoie l'information libère des neurotransmetteurs. Ces neurotransmetteurs sont ensuite capturés par les récepteurs du neurone récepteur de l'information. Le neurone récepteur s'active et propage l'intervention jusqu’à une autre synapse grâce à un potentiel d'action. L'activation est transmise à chaque synapse par le même processus. Dans ce processus, environ 10 % des neurotransmetteurs libérés sont fonctionnellement perdus par recapture par le neurone émetteur, et donc sont émis mais pas reçus par le neurone post-synaptique.
Les ISRS ont un degré d'activité variable pour les autres transporteurs monoaminergiques. Les ISRS purs ont seulement une faible affinité pour les transporteurs de la noradrénaline et de la dopamine.
Un des mécanismes impliqués dans la dépression serait liée à un déficit en sérotonine. Les ISRS agissent en empêchant la recapture de la sérotonine par le neurone pré-synaptique. De fait, ce neurotransmetteur va rester plus longtemps dans l'espace synaptique, augmentant sa probabilité d'être reconnu par le neurone récepteur et majorant ainsi la stimulation de ce neurone[10].
Les ISRS sont décrits comme sélectifs parce qu'ils agissent uniquement sur les pompes de recapture spécialisées dans la sérotonine, par opposition à d'autres antidépresseurs qui agissent aussi sur d'autres neurotransmetteurs.
Recherche chez l'animal nouveau-né[modifier | modifier le code]
On peut créer des modèles animaux de dépression en donnant de la clomipramine (antidépresseur tricyclique) à des animaux nouveau-nés entre 8 et 21 jours de vie[11],[12]. En 1997 Lundbeck a trouvé que le traitement avec l'ISRS LU-10-134-C, qui diffère seulement de son produit citalopram par deux atomes, pourrait donner des résultats similaires au clomipramine[13]. L'exposition néonatale au citalopram (ISRS) et à l'escitalopram opèrent des changements persistants de la transmission sérotonergique du cerveau, ce qui entraine des changements comportementaux[14],[15]. Ces anomalies comportementales, dues à l'exposition néonatale d'antidépresseurs, présentes chez les animaux adultes sont renversés par un traitement antidépresseur[16].
En traitant des souris normales et des souris knock-out qui manquent du transporteur sérotonine avec la fluoxétine, des scientifiques ont montré que les réactions émotionnelles normales chez l'adulte, comme une courte latence pour éviter des chocs de pieds et la tendance à explorer de nouveaux environnements, dépendaient du processus de déblocage des transporteurs de sérotonine pendant la période néonatale[17],[18]. Mais, quand de jeunes souris ont été traitées avec la SNRI desimipramine, elles se sont développées comme des adultes normaux, ce qui suggère que la sérotonine et la noradrénaline ont des effets différents sur le développement du cerveau[19].
Effets à long terme[modifier | modifier le code]
Certains effets secondaires peuvent perdurer indéfiniment après l'arrêt du traitement, parfois de manière atténuée ; aucune étude solide sur l'homme n'a évalué la prévalence de ce syndrome, qui a été reconnu par l'agence européenne des médicaments (EMA) en juin 2019, avec une demande aux laboratoires concernés d'ajouter une alerte à destination des patients[20].
Un traitement avec de la fluoxétine a mis en évidence une désensibilisation du récepteur de la sérotonine 5HT1A après son arrêt chez des rats[21]. Ces changements à long terme des récepteurs 5HT, tout comme d’autres plus complexes, peuvent être dus à des modifications en termes d’expression des différents gènes[22],[23],[24],[25],[26].
Certaines de ces modifications d’expression des gènes sont le résultat d’une modification de l’ADN causée par un remodelage de la chromatine[27],[28] et plus particulièrement un phénomène épigénétique de modification des histones[29] par méthylation de l’ADN à la suite de l’augmentation de l’expression des protéines MeCP2 et MBD1[30]. Ces mêmes mécanismes peuvent d’ailleurs aussi entrer en ligne de compte dans le mode d’action des thérapies électroconvulsives[31],[32].
La dysfonction sexuelle post ISRS pourrait être causée par les changements épigénétiques observés après la prise d'ISRS [33]. Cette dysfonction sexuelle pourrait persister indéfiniment chez certains individus[34]. Chez les animaux, les ISRS donnés à de jeunes rats pourraient entraîner une dysfonction érectile permanente, mais pas chez les rats adultes[35].
Comme ces changements sont très complexes, et peuvent donner lieu à des modifications permanentes de la structure de la chromatine, il a été suggéré que les ISRS pouvaient altérer de manière définitive l’expression des gènes au sein du cerveau[36], donnant lieu à diverses perturbations au niveau des neurotransmetteurs[36] et entraîner des perturbations endocriniennes[36]. Cependant, sans recherche plus approfondies[37], les causes sous-jacentes de ces phénomènes resteront inconnues.
Critiques des ISRS dans la dépression[modifier | modifier le code]
L'efficacité des ISRS dans le traitement de la dépression légère à modérée est discutée. Deux méta-analyses d'essais cliniques trouvent que, en cas de dépression légère ou de dépression modérée, qui correspondent à la grande majorité des cas de dépression, l'effet des ISRS est petit ou nul comparé au placebo. Cependant, dans les cas de dépression sévère, l'effet des ISRS est cliniquement significatif[38],[39]. L'(in)efficacité des antidépresseurs de seconde génération est similaire[40].
Une méta-analyse largement rapportée analysa 35 essais cliniques fournis à la Food and Drug Administration (FDA) avant l'autorisation de mise sur le marché (AMM) pour quatre nouveaux antidépresseurs (incluant les ISRS paroxétine et fluoxétine et les non ISRS nefazodone et l'IRSNa venlafaxine). Les auteurs ont conclu que, bien que l'efficacité supérieure des ISRS à un placebo soit significative, elle n'excédait pas les critères NICE d'un effet cliniquement significatif. En particulier, ils trouvèrent que la taille de l'effet (en anglais : effect size) était très petite pour les dépressions modérées mais augmentait lorsque la dépression était sévère[39]. Certains chercheurs ont discuté l'analyse statistique de cette étude, suggérant qu'elle sous-estimait l'effect size des antidépresseurs mais même quand ils réanalysaient les données, ils trouvaient que l'efficacité était toujours inférieure au seuil NICE de différence cliniquement significative quand tous les résultats sont combinés (même si, séparément, la venlafaxine et la paroxetine dépassaient ce seuil)[41],[42]. Une revue de 2010 arrive à la même conclusion[38],[43].
Effets indésirables[modifier | modifier le code]
- Alcoolisme : le professeur David Healy soutient que cette classe de médicament induit l'alcoolisme[44] confirmant ainsi une étude de l'université Yale parue en [45] ;
- Libido et sexualité
Les ISRS peuvent causer différentes dysfonctions sexuelles comme une anorgasmie, une diminution de la libido, des troubles de l'érection et un retard à l'éjaculation (c'est pourquoi ils sont étudiés dans le traitement de l'éjaculation précoce[46]). Les premières études montraient qu'il n'y avait pas de différence significative, du point de vue des effets indésirables, avec un placebo. Cependant, la question n'avait pas été clairement posée aux sujets. Les études plus récentes, tenant compte de cet aspect, font apparaître que 17 à 41 % de patients en souffrent[47],[48] bien que le manque de groupe placebo dans ces études tende à surestimer cette mesure. On pense que cela est causé par la libération de concentration extracellulaire de sérotonine dans le cerveau qui diminue la dopamine et la noradrénaline. Des essais cliniques sont menés afin de démontrer l'intérêt de l'agoniste de la dopamine Requip (ropinirole) pour contrer ces effets secondaires (durant le traitement par ISRS et également dans le cas de PSSD)[49] et également de l'amantadine[50],[51],[52]. Certains médicaments antidépresseurs ne sont pas associés avec des effets indésirables sexuels (comme le bupropione, le trazodone, l'agomélatine, la tianeptine, le nefazodone, le moclobémide, la mirtazapine[53],[54]). On a décrit un Post SSRI Sexual Dysfunction (PSSD) qui est un dysfonctionnement sexuel causé par un traitement par les médicaments antidépresseurs ISRS. Le PSSD persiste après la fin du traitement par l'ISRS et peut devenir chronique et irréversible[55],[56]. Des changements s'opèrent au niveau de la fonction de l'axe hypothalamo-hypophyso-testiculaire[57] : diminution des taux de testostérone[58], diminution du nombre de spermatozoïdes (qui réaugmente après de l'arrêt du traitement)[59] et entraîne une diminution de la qualité du sperme avec des dégâts sur son ADN (ceux-ci étant réversibles après l'arrêt du traitement)[60].
Dans le cas où il existe des dysfonctions sexuelles (désir sexuel hypoactif, anorgasmie, trouble de l'excitation…) avant l'apparition d'un état dépressif, une utilisation d'un ISRS sera déconseillée car cela pourrait avoir un effet contre-productif[61],[62]. - Malformations
Chez la femme enceinte, la paroxétine est associée à certaines malformations cardiaques. Il existe un risque possible de troubles comportementaux chez l'enfant de la mère exposée[63], dont des comportements de types autistiques[64]. Ce risque, non confirmé, serait toutefois faible[65],[66]. - Virage maniaque (manie ou hypomanie)
Des utilisateurs avec des troubles bipolaires sont à plus grand risque[67]. - Dépendance
Cela est particulièrement important avec la paroxétine[68],[69]. Les ISRS ont un potentiel d'abus faible[réf. souhaitée].
Lors de l'arrêt d'un antidépresseur, remplacer un traitement antidépresseur avec une demi-vie courte par un antidépresseur avec une demi-vie plus longue (ex : fluoxétine ou citalopram) peut diminuer la sévérité et la probabilité de souffrir de syndrome d'arrêt des antidépresseurs[70],[71].
- Levée d'inhibition
(idées suicidaires et passages à l'acte surtout chez l'enfant et l'adolescent)[72],[73],[74],[75].
Par exemple une analyse de la FDA reprenant des essais cliniques sur des enfants avec un état dépressif majeur trouva une augmentation statistiquement significative des risques de « idées suicidaires et comportement suicidaire » d'environ 80 % et d'agitation et d'hostilité de 130 %[76].
En 2004, la MHRA (Medicines and Healthcare products Regulatory Agency) du Royaume-Uni jugea la fluoxétine comme le seul antidépresseur qui offrait un rapport bénéfice-risque favorable dans la dépression bien qu'il soit associé à une petite augmentation du risque d'auto-agressivité et d'idées suicidaires[77]. Cependant, la fluoxétine n'a pas d'AMM anglais pour cette utilisation. - Perte ou gain de poids (gain de poids plus important avec la paroxétine[78])
- Tremblements[79]
- Akathisie[80],[81],[82],[83]
- Augmentation des saignements, en particulier digestif[84], surtout s'ils sont associés aux anti-inflammatoire nonstéroïdiens[85]. Augmentation des hémorragies intra-cérébrales (RR=1,48)[86].
- Photosensibilité[87]
- Risque augmenté de fracture[88]
- Anhédonie [89]
Effets indésirables à sourcer [réf. nécessaire]
- Troubles du système nerveux autonome comme une hypotension orthostatique ou augmentation ou diminution de la transpiration
- Troubles digestifs à types de nausées vomissements ;
- Syndrome de sécrétion inappropriée de l'hormone anti-diurétique (SIADH) ;
- Modification des rêves qui deviennent plus vivants ou bizarres[réf. nécessaire] ;
- Apathie[réf. nécessaire] ;
- Céphalées (effet à court terme fréquent)[réf. nécessaire] ;
- Bruxisme[réf. nécessaire] ;
- Acouphènes[réf. nécessaire] ;
- Étourdissement[réf. nécessaire] ;
- Fatigue[réf. nécessaire] ;
- Mydriase (dilatation de la pupille)[réf. nécessaire] ;
- Rétention urinaire[réf. nécessaire] ;
- Insuffisance rénale[réf. nécessaire] ;
- Paresthésies[réf. nécessaire] ;
- Syndromes dissociatifs et troubles cognitifs[réf. nécessaire]
La plupart des effets secondaires disparaissent après une phase d'adaptation à l'exception notable des troubles d'ordre sexuels. Ainsi souvent l'instauration d'un IRS se fait de manière progressive.
Syndrome de discontinuation associé aux antidépresseurs[modifier | modifier le code]
L'arrêt ou la réduction marquée de la dose d'un traitement ISRS peut provoquer un syndrome de discontinuation associé aux antidépresseurs.
Notes et références[modifier | modifier le code]
- (en) F. Artigas, D. Nutt, R. Shelton, « Mechanism of action of antidepressants », Psychopharmacology bulletin, vol. 36, supp. 2, , p. 123-132 (lire en ligne, consulté le ).
- (en) Wand BM, Parkitny L, O'Connell NE, Luomajoki H, McAuley JH, Thacker M, Moseley GL. « Cortical changes in chronic low back pain: Current state of the art and implications for clinical practice » Man Ther. 2011;16(1):15-20. DOI 10.1016/j.math.2010.06.008
- (en) SH Preskorn, R Ross, CY Stanga, Sheldon H. Preskorn (éditeur), Hohn P. Feighner (éditeur), Christina Y. Stanga (éditeur) et Ruth Ross (éditeur), Antidepressants : Past, Present and Future, Berlin, Springer, , 615 p. (ISBN 978-3-540-43054-4, lire en ligne), « Selective Serotonin Reuptake Inhibitors », p. 241–62
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3811092/
- https://emedicine.medscape.com/article/913575-medication?form=fpf#2
- (en) Nick Medford, « Understanding and treating depersonalization disorder », Advances in Psychiatric Treatment (2005) (consulté le )
- Flament MF, Bissada H, Spettigue W, « Evidence-based pharmacotherapy of eating disorders », The International Journal of Neuropsychopharmacology / Official Scientific Journal of the Collegium Internationale Neuropsychopharmacologicum (CINP), vol. 15, no 2, , p. 189–207 (PMID 21414249, DOI 10.1017/S1461145711000381)
- (en) Hinz M, Stein A, Uncini T. « 5-HTP efficacy and contraindications » Neuropsychiatr Dis Treat. 2012;8:323-8. DOI 10.2147/NDT.S33259
- (en) Alan Frazer, « Amine Precursors and Depression », Archives of General Psychiatry, vol. 32, no 1, , p. 22–30 (ISSN 0003-990X, DOI 10.1001/archpsyc.1975.01760190024002, lire en ligne, consulté le ).
- « Inhibiteurs de recapture sérotonine (IRS) », sur pharmacomedicale.org (consulté le )
- (en) Vogel G, Neill D, Hagler M, Kors D, « A new animal model of endogenous depression: a summary of present findings », Neurosci Biobehav Rev, vol. 14, no 1, , p. 85–91 (PMID 2183099, lire en ligne)
- (en) Velazquez-Moctezuma J, Aguilar-Garcia A, Diaz-Ruiz O, « Behavioral effects of neonatal treatment with clomipramine, scopolamine, and idazoxan in male rats », Pharmacol Biochem Behav, vol. 46, no 1, , p. 215–7 (PMID 7902983, lire en ligne)
- (en) Hansen HH, Sánchez C, Meier E, « Neonatal administration of the selective serotonin reuptake inhibitor Lu 10-134-C increases forced swimming-induced immobility in adult rats: a putative animal model of depression? », J. Pharmacol Exp Ther, vol. 283, no 3, , p. 1333–41 (PMID 9400008, lire en ligne)
- (en) Popa D, Léna C, Alexandre C, Adrien J, « Lasting syndrome of depression produced by reduction in serotonin uptake during postnatal development: evidence from sleep, stress, and behavior », J Neurosci, vol. 14, no 2, , p. 3546–3554 (PMID 18385313, lire en ligne)
- (en) Maciag D, Simpson KL, Coppinger D. et al., « Neonatal antidepressant exposure has lasting effects on behavior and serotonin circuitry », Neuropsychopharmacology, vol. 31, no 1, , p. 47–57 (PMID 16012532, DOI 10.1038/sj.npp.1300823)
- (en) Maciag D, Williams L, Coppinger D, Paul IA, « Neonatal citalopram exposure produces lasting changes in behavior which are reversed by adult imipramine treatment », Eur J Pharmacol, vol. 532, no 3, , p. 265–9 (PMID 16483567, DOI 10.1016/j.ejphar.2005.12.081)
- (en)NEUROSCIENCE: Prozac Treatment of Newborn Mice Raises Anxiety - Holden 306 (5697): 792 - Science
- (en) Early-Life Blockade of the 5-HT Transporter Alters Emotional Behavior in Adult Mice - Ansorge et al. 306 (5697): 879 - Science
- (en) Inhibition of Serotonin But Not Norepinephrine Transport during Development Produces Delayed, Persistent Perturbations of Emotional Behaviors in Mice - Ansorge et al. 28 (1): …
- (en) EMA, Pharmacovigilance Risk Assessment Committee (PRAC), « PRAC recommendations on signals »
- (en) Raap DK, Garcia F, Muma NA, Wolf WA, Battaglia G, van de Kar LD, « Sustained desensitization of hypothalamic 5-Hydroxytryptamine1A receptors after discontinuation of fluoxetine: inhibited neuroendocrine responses to 8-hydroxy-2-(Dipropylamino)Tetralin in the absence of changes in Gi/o/z proteins », J Pharmacol Exp Ther, vol. 288, no 2, , p. 561–7 (PMID 9918559, lire en ligne)
- (en) Faure C, Mnie-Filali O, Haddjeri N, « Long-term adaptive changes induced by serotonergic antidepressant drugs », Expert Rev Neurother, vol. 6, no 2, , p. 235–45 (PMID 16466303, DOI 10.1586/14737175.6.2.235, lire en ligne)
- (en) Palotás M, Palotás A, Puskás LG et al., « Gene expression profile analysis of the rat cortex following treatment with imipramine and citalopram », Int J Neuropsychopharmacol, vol. 7, no 4, , p. 401–13 (PMID 15315716, DOI 10.1017/S1461145704004493, lire en ligne)
- (en) Kálmán J, Palotás A, Juhász A et al., « Impact of venlafaxine on gene expression profile in lymphocytes of the elderly with major depression--evolution of antidepressants and the role of the "neuro-immune" system », Neurochem Res, vol. 30, no 11, , p. 1429–38 (PMID 16341940, DOI 10.1007/s11064-005-8513-9)
- (en) Yamada M, Yamada M, Higuchi T, « Antidepressant-elicited changes in gene expression: remodeling of neuronal circuits as a new hypothesis for drug efficacy », Prog. Neuropsychopharmacol Biol Psychiatry, vol. 29, no 6, , p. 999–1009 (PMID 15975701, DOI 10.1016/j.pnpbp.2005.03.022, lire en ligne)
- (en) Boehm C, Newrzella D, Herberger S, Schramm N, Eisenhardt G, Schenk V, Sonntag-Buck V, Sorgenfrei O, « Effects of antidepressant treatment on gene expression profile in mouse brain: cell type-specific transcription profiling using laser microdissection and microarray analysis », J Neurochem, vol. 97, no Suppl 1, , p. 44–9 (PMID 16635249, DOI 10.1111/j.1471-4159.2006.03750.x)
- (en) Hyman SE, « Even chromatin gets the blues », Nat Neurosci, vol. 9, no 4, , p. 465–6 (PMID 16568101, DOI 10.1038/nn0406-465)
- (en) Newton SS, Duman RS, « Chromatin remodeling: a novel mechanism of psychotropic drug action », Mol Pharmacol, vol. 70, no 2, , p. 440–3 (PMID 16728645, DOI 10.1124/mol.106.027078, lire en ligne)
- (en) Tsankova NM, Berton O, Renthal W, Kumar A, Neve RL, Nestler EJ, « Sustained hippocampal chromatin regulation in a mouse model of depression and antidepressant action », Nat Neurosci, vol. 9, no 4, , p. 519–25 (PMID 16501568, DOI 10.1038/nn1659)
- (en) Cassel S, Carouge D, Gensburger C et al., « Fluoxetine and cocaine induce the epigenetic factors MeCP2 and MBD1 in adult rat brain », Mol Pharmacol, vol. 70, no 2, , p. 487–92 (PMID 16670375, DOI 10.1124/mol.106.022301, lire en ligne)
- (en) Altar CA, Laeng P, Jurata LW et al., « Electroconvulsive seizures regulate gene expression of distinct neurotrophic signaling pathways », J Neurosci, vol. 24, no 11, , p. 2667–77 (PMID 15028759, DOI 10.1523/JNEUROSCI.5377-03.2004, lire en ligne)
- (en) Tsankova NM, Kumar A, Nestler EJ, « Histone modifications at gene promoter regions in rat hippocampus after acute and chronic electroconvulsive seizures », J Neurosci, vol. 24, no 24, , p. 5603–10 (PMID 15201333, DOI 10.1523/JNEUROSCI.0589-04.2004, lire en ligne)
- (en) Areeg Bala, Hoang Minh Tue Nguyen et Wayne J. G. Hellstrom, « Post-SSRI Sexual Dysfunction: A Literature Review », Sexual Medicine Reviews, vol. 6, no 1, , p. 29–34 (ISSN 2050-0521 et 2050-0513, PMID 28778697, DOI 10.1016/j.sxmr.2017.07.002, lire en ligne, consulté le ) :
« Long-term usage of SSRIs is hypothesized to cause persistent downregulation of 5HT1A (even after discontinuation of SSRIs) by epigenetic changes in the form of increased expression of methyl binding proteins MeCP2 and MBD1. This leads to more production of HDAC2 mRNA and lowers the production of histone H3 deacetylase.These epigenetic changes were observed in three areas of the brain: the frontal cortex, the dentate gyrus of the hippocampus, and the caudate-putamen. (...) this downregulation and desensitization of 5HT1A are involved in the regulation of sexual motivation, and thus proposed this as a theory for PSSD. »
- « Sexual Side Effects of Antidepressant Medications: An Informed Consent Accountability Gap »
- Enis Rauf Coskuner, Mehmet Gokhan Culha, Burak Ozkan et Elcin Orhan Kaleagasi, « Post-SSRI Sexual Dysfunction: Preclinical to Clinical. Is It Fact or Fiction? », Sexual Medicine Reviews, vol. 6, no 2, , p. 217–223 (ISSN 2050-0521, PMID 29463440, DOI 10.1016/j.sxmr.2017.11.004, lire en ligne, consulté le ) :
« animal studies suggest that SSRIs might cause permanent sexual dysfunction after ending SSRI exposure at a young age but not in adulthood in rats »
- (en) Csoka AB, Szyf M., « Epigenetic side-effects of common pharmaceuticals: a potential new field in medicine and pharmacology. », Med Hypotheses. 2009 Nov;73(5):770-80. doi: 10.1016/j.mehy.2008.10.039. Epub 2009 Jun 5, no 73(5):770-80, (lire en ligne)« SSRI antidepressants have been shown to cause long-term alterations in gene expression, presumably resulting from chronic elevation of serotonin (5-HT) neurotransmission in the brain. Some of these gene expression changes are a result of altered DNA structure caused by chromatin remodeling. It has been suggested that chronic antidepressant use can result in persistently altered cerebral gene expression leading to compromised catecholaminergic neurotransmission and neuroendocrine disturbances, such as decreased testosterone levels[115],reduced fertility[116], and persistent, sexual dysfunction[117–120] »
- (en) Szyf M, « Toward a Discipline of Pharmacoepigenomics », Current Pharmacogenomics, vol. 2, no 4, , p. 357–377 (DOI 10.2174/1570160043377358, lire en ligne)
- (en) Jay C. Fournier, Robert J. DeRubeis, Steven D. Hollon, Sona Dimidjian, Jay D. Amsterdam, Richard C. Shelton, Jan Fawcett, « Antidepressant Drug Effects and Depression Severity », The Journal of the American Medical Association, vol. 303, no 1, , p. 47–53 (PMID 20051569, DOI 10.1001/jama.2009.1943, lire en ligne)
- (en) Kirsch I, Deacon BJ, Huedo-Medina TB, Scoboria A, Moore TJ, Johnson BT, « Initial Severity and Antidepressant Benefits: A Meta-Analysis of Data Submitted to the Food and Drug Administration », PLoS Medicine, vol. 5, no 2, , e45 (PMID 18303940, PMCID 2253608, DOI 10.1371/journal.pmed.0050045)
- (en) Gartlehner G, Hansen RA, Morgan LC, Thaler K, Lux L, Van Noord M, Mager U, Thieda P, Gaynes BN, Wilkins T, Strobelberger M, Lloyd S, Reichenpfader U, Lohr KN, « Comparative benefits and harms of second-generation antidepressants for treating major depressive disorder: an updated meta-analysis », Ann Intern Med, vol. 155, no 11, , p. 772-85. (PMID 22147715, DOI 10.7326/0003-4819-155-11-201112060-00009, lire en ligne [html])
- (en) Horder J, Matthews P, Waldmann R, « Placebo, Prozac and PLoS: significant lessons for psychopharmacology », Journal of Psychopharmacology, vol. 25, no 10, , p. 1277–88 (PMID 20571143, DOI 10.1177/0269881110372544)
- (en) Fountoulakis KN, Moller H-J, « Efficacy of antidepressants: a re-analysis and re-interpretation of the Kirsch data », International Journal of Neuropsychopharmacology, vol. 14, no 3, , p. 1–8 (PMID 20800012, DOI 10.1017/S1461145710000957)
- (en) John Kelley, « Antidepressants: Do They "Work" or Don't They? », Scientific American, (lire en ligne)
- (en) By Jerome Burne for MailOnline, « Could your medicine give you a drink problem? The disturbing side-effects even the manufacturers don't know about », Daily Mail, (lire en ligne, consulté le ).
- http://wp.rxisk.org/driven-to-drink-antidepressants-and-cravings-for-alcohol/
- (en) Waldinger MD, Olivier B, « Utility of selective serotonin reuptake inhibitors in premature ejaculation », Current Opinion in Investigational Drugs, vol. 5, no 7, , p. 743–7 (PMID 15298071)
- (en) Hu XH, Bull SA, Hunkeler EM et al., « Incidence and duration of side effects and those rated as bothersome with selective serotonin reuptake inhibitor treatment for depression: patient report versus physician estimate », The Journal of Clinical Psychiatry, vol. 65, no 7, , p. 959–65 (PMID 15291685, DOI 10.4088/JCP.v65n0712, lire en ligne)
- (en) Landén M, Högberg P, Thase ME, « Incidence of sexual side effects in refractory depression during treatment with citalopram or paroxetine », The Journal of Clinical Psychiatry, vol. 66, no 1, , p. 100–6 (PMID 15669895, DOI 10.4088/JCP.v66n0114)
- (en) « Treating Sexual Dysfunction From SSRI Medication: a Study Comparing Requip CR to Placebo » sur le site américain clinicaltrials.gov
- (en) Shrivastava RK, Shrivastava S, Overweg N, Schmitt M, « Amantadine in the treatment of sexual dysfunction associated with selective serotonin reuptake inhibitors », Journal of clinical psychopharmacology, vol. 15, no 1, , p. 83–4 (PMID 7714234, DOI 10.1097/00004714-199502000-00014)
- (en) Balogh S, Hendricks SE, Kang J, « Treatment of fluoxetine-induced anorgasmia with amantadine », The Journal of clinical psychiatry, vol. 53, no 6, , p. 212–3 (PMID 1607353)
- (en) Keller Ashton A, Hamer R, Rosen RC, « Serotonin reuptake inhibitor-induced sexual dysfunction and its treatment: a large-scale retrospective study of 596 psychiatric outpatients », Journal of sex & marital therapy, vol. 23, no 3, , p. 165–75 (PMID 9292832, DOI 10.1080/00926239708403922)
- (en) Clayton AH, « Antidepressant-Associated Sexual Dysfunction: A Potentially Avoidable Therapeutic Challenge », Primary Psychiatry, vol. 10, no 1, , p. 55–61
- (en) Kanaly KA, Berman JR, « Sexual side effects of SSRI medications: potential treatment strategies for SSRI-induced female sexual dysfunction », Current Women's Health Reports, vol. 2, no 6, , p. 409–16 (PMID 12429073)
- (en) Bahrick AS. « Post SSRI Sexual Dysfunction » American Society for the Advancement of Pharmacotherapy Tablet 2006;7:2-10.
- (en) Csoka AB, Bahrick AS, Mehtonen O-P, « Persistent Sexual Dysfunction after Discontinuation of Selective Serotonin Reuptake Inhibitors (SSRIs) », J Sex Med, vol. 5, no 1, , p. 227–33 (PMID 18173768, DOI 10.1111/j.1743-6109.2007.00630.x, lire en ligne)
- (en) Safarinejad MR, « Evaluation of endocrine profile and hypothalamic-pituitary-testis axis in selective serotonin reuptake inhibitor-induced male sexual dysfunction », J Clin Psychopharmacol, vol. 28, no 4, , p. 418–23 (PMID 18626269, DOI 10.1097/JCP.0b013e31817e6f80, lire en ligne)
- (en) Alan Jay Cohen, « Antidepressant-Induced Sexual Dysfunction Associated with Low Serum Free Testosterone », sur Psychiatry Online,
- (en) Tanrikut C, Schlegel PN, « Antidepressant-associated changes in semen parameters », Urology, vol. 69, no 1, , p. 185.e5–7 (PMID 17270655, DOI 10.1016/j.urology.2006.10.034, lire en ligne)
- (en) Safarinejad MR, « Sperm DNA damage and semen quality impairment after treatment with selective serotonin reuptake inhibitors detected using semen analysis and sperm chromatin structure assay », J Urol, vol. 180, no 5, , p. 2124–8 (PMID 18804223, DOI 10.1016/j.juro.2008.07.034, lire en ligne)
- (en) Sutherland JE, Sutherland SJ, Hoehns JD, « Achieving the best outcome in treatment of depression », Journal of Family Practice, vol. 52, no 3, , p. 201–09 (PMID 12620174, lire en ligne)
- (en) Timothy R. Berigan, « Assessing Sexual Function of Patients Before Initiating SSRI Therapy », Prim Care Companion J Clin Psychiatry, vol. 4, no 3, , p. 181 (PMID 181186, PMCID PMC181186, lire en ligne)
- (en) Tuccori M, Testi A, Antonioli L. et al. « Safety concerns associated with the use of serotonin reuptake inhibitors and other serotonergic/noradrenergic antidepressants during pregnancy: a review » Clin Ther. 2009;31:1426-1453
- (en) Croen LA, Grether JK, Yoshida CK, Odouli R, Hendrick V, « Antidepressant use during pregnancy and childhood autism spectrum disorders » Arch Gen Psychiatry 2011;68:1104-1112
- (en) Hviid A, Melbye M, Pasternak B, « Use of selective serotonin reuptake inhibitors during pregnancy and risk of autism » N Engl J Med. 2013;369:2406-2415
- « Antidépresseurs et malformations congénitales » Rev Prescrire 2006;26(273):430-431
- (en) Joseph MF, Youngstrom EA, Soares JC, « Antidepressant-coincident mania in children and adolescents treated with selective serotonin reuptake inhibitors », Future Neurol, vol. 4, no 1, , p. 87-102. (PMID 19884978, PMCID PMC2655139, lire en ligne [html])
- (en) Haddad PM, Anderson IM, « Recognising and managing antidepressant discontinuation symptoms », Advances in Psychiatric Treatment, vol. 13, no 6, , p. 447–457 (DOI 10.1192/apt.bp.105.001966, lire en ligne)
- http://www.benzo.org.uk/healy.htm
- (en) P.M. Haddad et I.M. Anderson, « Recognising and managing antidepressant discontinuation symptoms », Advances in Psychiatric Treatment, vol. 13, no 6, , p. 447 (DOI 10.1192/apt.bp.105.001966)
- (en) Warner CH, Bobo W, Warner C, Reid S, Rachal J., « Antidepressant discontinuation syndrome. », Am Fam Physician, nos 1;74(3):449-56., , p. 449-56. (lire en ligne)
- Voir article du Science et Avenir d'octobre 2010, sur la corrélation potentielle entre la prise d'ISRS et le passage au suicide voire à un massacre suivi du suicide, à défaut du lien vers le magazine lien vers un article basé sur des études scientifiques récentes : http://www.psychomedia.qc.ca/depression/2010-07-22/depression-la-theorie-sous-jacente-aux-antidepresseurs-remise-en-question
- (en) Stone MB, Jones ML, « Clinical review: relationship between antidepressant drugs and suicidal behavior in adults » [PDF], Overview for December 13 Meeting of Psychopharmacologic Drugs Advisory Committee (PDAC), FDA, (consulté le ), p. 11–74
- (en) Levenson M, Holland C, « Statistical Evaluation of Suicidality in Adults Treated with Antidepressants » [PDF], Overview for December 13 Meeting of Psychopharmacologic Drugs Advisory Committee (PDAC), FDA, (consulté le ), p. 75–140
- (en) Olfson M, Marcus SC, Shaffer D, « Antidepressant drug therapy and suicide in severely depressed children and adults: A case-control study », Archives of General Psychiatry, vol. 63, no 8, , p. 865–72 (PMID 16894062, DOI 10.1001/archpsyc.63.8.865)
- (en) Hammad TA, « Review and evaluation of clinical data. Relationship between psychiatric drugs and pediatric suicidal behavior » [PDF], FDA, (consulté le ), p. 42; 115
- (en) « Report of the CSM expert working group on the safety of selective serotonin reuptake inhibitor antidepressants » [PDF], MHRA, (consulté le )
- (en) Hasnain M, W Victor RV, Hollett B. « Weight gain and glucose dysregulation with second-generation antipsychotics and antidepressants: a review for primary care physicians » Postgrad Med. 2012;124(4):154-67. DOI 10.3810/pgm.2012.07.2577
- (en) Schechter DS, Nunes EV, « A case of reversible parkinsonism in a 90-year-old man on sertraline », Journal of Clinical Psychiatry, vol. 58, no 6, , p. 275 (PMID 9228898, DOI 10.4088/JCP.v58n0607f)
- (en) Stahl SM, Lonnen AJ. « The Mechanism of Drug-induced Akathsia » CNS Spectr. 2011. pii: Stahl.
- (en) Lane RM. « SSRI-induced extrapyramidal side-effects and akathisia: implications for treatment » J Psychopharmacol. 1998;12(2):192-214
- (en) Koliscak LP, Makela EH. « Selective serotonin reuptake inhibitor-induced akathisia » J Am Pharm Assoc. (2003). 2009 Mar-Apr;49(2):e28-36; quiz e37-8
- (en) Leo RJ. « Movement disorders associated with the serotonin selective reuptake inhibitors » J Clin Psychiatry. 1996 Oct;57(10):449-54.
- (en) Andrade C, Sandarsh S, Chethan KB, Nagesh KS, « Serotonin reuptake inhibitor antidepressants and abnormal bleeding: a review for clinicians and a reconsideration of mechanisms » J Clin Psychiatry, 2004;71:1565-75
- (en) Loke YK, Trivedi AN, Singh S. « Meta-analysis: gastrointestinal bleeding due to interaction between selective serotonin uptake inhibitors and non-steroidal anti-inflammatory drugs » Aliment Pharmacol Ther. 2008;27:31-40
- (en) Hackam DG, Mrkobrada M, « Selective serotonin reuptake inhibitors and brain hemorrhage: a meta-analysis », Neurology, vol. 79, no 18, , p. 1862-5 (PMID 23077009, DOI 10.1212/WNL.0b013e318271f848)
- (en) SSRIs and Depression
- Bérengère Aubry-Rozier, « [Drugs induced osteopathies] », Revue Medicale Suisse, vol. 13, no 553, , p. 549–553 (ISSN 1660-9379, PMID 28718587, lire en ligne, consulté le )
- (en) « Dysrégulation du système dopaminergique dans les troubles dépressifs majeurs »,
- (en) Cet article est partiellement ou en totalité issu des articles intitulés en anglais « Selective serotonin reuptake inhibitor » (voir la liste des auteurs) et « Antidepressant discontinuation syndrome » (voir la liste des auteurs).
Voir aussi[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- Atlas of psychiatric pharmacotherapy, Roni Shiloh [et al.], 2e éd., Londres, Informa Health Care, 2006.
- (en) Samuel H. Barondes, Better than Prozac: creating the next generation of psychiatric drugs, Oxford, Oxford University Press, 2003.
- Charles-Henri Beau, Sandrine Thauby, Synopsis 2007 des médicaments en psychiatrie, Callian, Éd. Santé, prévention, communication, 2007.
- David Cohen, Suzanne Cailloux-Cohen et l'AGIDS-SMQ, Guide critique des médicaments de l'âme, Montréal, Éd. de l'Homme, 1995.
- Philippe Dorosz, Philippe, Guide pratique des médicaments en neuro-psychiatrie, Paris, Maloine, 2005.
- David Healy, Le Temps des antidépresseurs, Paris, Les Empêcheurs de penser en rond, 2002 [trad. de The antidepressant era, Cambridge (Mass.), Harvard University Press, 1997].
- (en) David Healy, The creation of psychopharmacology, Cambridge (Mass.), Harvard University Press, 2002, réédition 2004.
- David Healy, Les Médicaments psychiatriques démystifiés, Issy-les-Moulineaux, Elsevier-Masson, 2009 [trad. et adaptation par Monique Debauche de Psychiatric drugs explained, 5e éd., Edinburgh, Churchill Livingstone, 2009].
- Guy Hugnet, Antidépresseurs : la grande intoxication : ce que 5 millions de patients ne savent pas encore, Paris, Le Cherche midi, 2004.
- (en) Medication management in mental health, ed. by Neil Harris, John Baker, and Richard Gray, Oxford, Wiley-Blackwell, 2009.
- (en) Metabolic effects of psychotropic drugs, ed. by Jogin Thakore and Brian E. Leonard, Basel-Paris, Karger, 2009.
- Antoine Pelissolo, Bien se soigner avec les médicaments psy : antidépresseurs, tranquillisants, somnifères, Paris, Éd. Odile Jacob, 2005.
- Antoine Pelissolo, Des troubles anxieux à la dépression, Paris, éd. Phase 5, 2006.
- Philippe Pignarre, Comment la dépression est devenue une épidémie, Paris, La Découverte, 2001.
- Philippe Pignarre, Les Malheurs des psys : psychotropes et médicalisation du social, Paris, La Découverte, 2006.
- (en) Principles and practice of psychopharmacotherapy, by Philip G. Janicak [et al.], 4th ed., Philadelphia, Lippincott Williams & Wilkins, 2006.
- Denis Richard, Jean-Louis Senon, Nicolas Tournier, Médicaments en psychiatrie, Rueil-Malmaison, Lamarre, 2006.
- (en) Alan F. Schatzberg, Jonathan O. Cole, Charles DeBattista, Manual of clinical psychopharmacology, 5th ed., American Psychiatric Publ., 2005.
- Stephen M. Stahl, Psychopharmacologie essentielle. Le guide du prescripteur, Paris, Médecine-sciences Flammarion, 2007 [trad. de Essential psychopharmacology. The prescriber's guide, Cambridge, Cambridge University Press, 2005].
- (en) Padraig Wrigh, Core psychopharmacology, Edinburgh, Saunders Elsevier, 2006.
- (en) L. Tamam, N. Ozpoyraz, « Selective serotonin reuptake inhibitor discontinuation syndrome : a review » Adv Ther. 2002;19::17-26. .
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- (fr) antidepresseur : Les dangers des antidepresseurs ISRS.et des solutions.
- MEDLINEplus drug information database
- The FDA Ban of L-Tryptophan
- FDA "black box" warning for SSRIs
- FDA list of SSRIs reciving the "black box" warning
- FDA advisory regarding Suicidality in Adults Being Treated with Antidepressant Medications

