« SARS-CoV-2 » : différence entre les versions
→Incubation : ajout d'une référence |
→Taux de létalité : Référence |
||
| Ligne 65 : | Ligne 65 : | ||
* le taux de létalité des cas confirmés à l'échelle mondiale, communiqué par l'OMS le {{date-|3 mars 2020-}}, est de 3,4 %<ref>{{Lien web |titre=WHO Director-General's opening remarks at the media briefing on COVID-19 - 3 March 2020 |url=https://www.who.int/dg/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19---3-march-2020 |site=who.int |éditeur=[[Organisation mondiale de la santé]] |date=3 mars 2020}}</ref> |
* le taux de létalité des cas confirmés à l'échelle mondiale, communiqué par l'OMS le {{date-|3 mars 2020-}}, est de 3,4 %<ref>{{Lien web |titre=WHO Director-General's opening remarks at the media briefing on COVID-19 - 3 March 2020 |url=https://www.who.int/dg/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19---3-march-2020 |site=who.int |éditeur=[[Organisation mondiale de la santé]] |date=3 mars 2020}}</ref> |
||
Le taux de létalité est toutefois un chiffre qu'il faut interpréter avec beaucoup de précaution<ref>{{Article |langue=en |auteur1=Mike Famulare |titre=2019-nCoV: preliminary estimates of the confirmed-case-fatality-ratio and infection-fatality-ratio, and initial pandemic risk assessment |éditeur=Institute for |
Le taux de létalité est toutefois un chiffre qu'il faut interpréter avec beaucoup de précaution<ref>{{Article |langue=en |auteur1=Mike Famulare |titre=2019-nCoV: preliminary estimates of the confirmed-case-fatality-ratio and infection-fatality-ratio, and initial pandemic risk assessment |périodique=Github |éditeur=Institute for disease modeling |date=19/02/2020 |issn= |lire en ligne=https://institutefordiseasemodeling.github.io/nCoV-public/analyses/first_adjusted_mortality_estimates_and_risk_assessment/2019-nCoV-preliminary_age_and_time_adjusted_mortality_rates_and_pandemic_risk_assessment.html |consulté le=12/03/2020 |pages= }}.</ref>, dans la mesure où beaucoup de pays ont des taux de tests de dépistage par habitant très différents ({{ex}} le taux chinois est 45 fois plus élevé que le taux français). La proportion de contaminés asymptomatiques (et donc non décelés) est probablement supérieure à 40%, ce qui diminue beaucoup la létalité réelle par rapport à celle qui est constatée à partir du chiffre des contaminés. |
||
== Taxonomie et phylogénie (origine du virus) == |
== Taxonomie et phylogénie (origine du virus) == |
||
| Ligne 115 : | Ligne 115 : | ||
Dans une étude publiée avec relecture par les pairs le 10 mars<ref>{{Article |langue=en |prénom1=Stephen A. |nom1=Lauer |prénom2=Kyra H. |nom2=Grantz |prénom3=Qifang |nom3=Bi |prénom4=Forrest K. |nom4=Jones |titre=The Incubation Period of Coronavirus Disease 2019 (COVID-19) From Publicly Reported Confirmed Cases: Estimation and Application |périodique=Annals of Internal Medicine |date=2020-03-10 |issn=0003-4819 |doi=10.7326/M20-0504 |lire en ligne=https://annals.org/aim/fullarticle/2762808/incubation-period-coronavirus-disease-2019-covid-19-from-publicly-reported |consulté le=2020-03-16 }}</ref>, portant sur 181 cas documentés (avec une sur-représentation possible des cas les plus sévères selon les auteurs), la période d'incubation [[Médiane (statistiques)|médiane]] est estimée à 5,1 jours, tandis que 97,5% de ceux qui développeront des symptômes le font en moins de 11,5 jours; cette étude suggère que sur {{Nombre|10000|}} cas, 101 développent des symptômes plus tard que 14 jours de suivi actif et de quarantaine. |
Dans une étude publiée avec relecture par les pairs le 10 mars<ref>{{Article |langue=en |prénom1=Stephen A. |nom1=Lauer |prénom2=Kyra H. |nom2=Grantz |prénom3=Qifang |nom3=Bi |prénom4=Forrest K. |nom4=Jones |titre=The Incubation Period of Coronavirus Disease 2019 (COVID-19) From Publicly Reported Confirmed Cases: Estimation and Application |périodique=Annals of Internal Medicine |date=2020-03-10 |issn=0003-4819 |doi=10.7326/M20-0504 |lire en ligne=https://annals.org/aim/fullarticle/2762808/incubation-period-coronavirus-disease-2019-covid-19-from-publicly-reported |consulté le=2020-03-16 }}</ref>, portant sur 181 cas documentés (avec une sur-représentation possible des cas les plus sévères selon les auteurs), la période d'incubation [[Médiane (statistiques)|médiane]] est estimée à 5,1 jours, tandis que 97,5% de ceux qui développeront des symptômes le font en moins de 11,5 jours; cette étude suggère que sur {{Nombre|10000|}} cas, 101 développent des symptômes plus tard que 14 jours de suivi actif et de quarantaine. |
||
Plus de la moitié des contaminations seraient le fait de porteurs ne montrant pas encore de symptômes<ref>{{Article |langue=en |auteur1= |prénom1=Tapiwa |nom1=Ganyani |prénom2=Cecile |nom2=Kremer |prénom3=Dongxuan |nom3=Chen |prénom4=Andrea |nom4=Torneri |titre=Estimating the generation interval for COVID-19 based on symptom onset data |périodique=bioRxiv |éditeur=Infectious Diseases (except HIV/AIDS) |date=2020-03-08 |issn= |doi=10.1101/2020.03.05.20031815 |lire en ligne=http://medrxiv.org/lookup/doi/10.1101/2020.03.05.20031815 |consulté le=2020-03-16 |pages= }}</ref>. |
|||
=== Durée de survie du virus hors de l'organisme === |
=== Durée de survie du virus hors de l'organisme === |
||
Version du 16 mars 2020 à 20:19
2019-nCoV
| Domaine | Riboviria |
|---|---|
| Ordre | Nidovirales |
| Sous-ordre | Cornidovirineae |
| Famille | Coronaviridae |
| Sous-famille | Orthocoronavirinae |
| Genre | Betacoronavirus |
| Sous-genre | Sarbecovirus |
Modèle:Arbre début
- Modèle:Arbre/Branche finale Espèce : Coronavirus associé au SRAS
- Coronavirus du SRAS (SARS-CoV)
- Modèle:Arbre/Branche finale Coronavirus du SRAS 2 (SARS-CoV-2, proposition ICTV[2] en prépublication)
Le coronavirus du syndrome respiratoire aigu sévère 2 (SARS-CoV-2 en abrégé), découvert et décrit en 2019 dans la ville de Wuhan (province de Hubei, en Chine), est le coronavirus source d'une maladie émergente : la pandémie de maladie à coronavirus de 2019-2020.



Cette pneumonie atypique, dite maladie à coronavirus 2019 (COVID-19), a été déclarée urgence de santé publique de portée internationale par l'Organisation mondiale de la santé (OMS) le [3]. Une quarantaine de jours plus tard, le 11 mars, l'OMS déclare qu'il s'agit d'une pandémie.
Apparenté au coronavirus du SRAS, d'un diamètre de 125 nanomètres (« légèrement plus grand que les virus de la grippe, du SRAS et du MERS »)[4], le SARS-CoV-2 appartient au sous-genre Sarbecovirus du genre Betacoronavirus[5]. L'origine du virus est probablement chez les pangolins ou les chauves-souris.
Il ne faut pas confondre le SARS-CoV-2 (nom du virus) et la COVID-19 (nom, féminin, de la maladie due au virus).
Ressources scientifiques
Les archives de prépublications, notamment bioRxiv et medRxiv, et divers forums de chercheurs, permettent une diffusion rapide – mais non formellement validée par les pairs – de l'information scientifique concernant SARS-CoV-2[6]. BioRxiv a publié le premier preprint sur SARS-CoV-2 (alors nommé 2019-nCoV) le 19 janvier[7] et medRxiv le 24 janvier[8].
Les premières publications scientifiques validées par les pairs datent du 24 janvier 2020[9],[10]. Plusieurs grandes revues et grands éditeurs scientifiques, devant l'urgence de la situation, ont décidé de rendre disponibles hors abonnement un certain nombre de publications scientifiques sur le nouveau coronavirus et la pneumonie associée: c'est notamment le cas de Elsevier[11], The Lancet[12], The New England Journal of Medicine[13], Science[14], Springer-Nature[15] ou encore Wiley[16] .
Nom du virus et de la maladie
Au début de l'épidémie, le virus a souvent été nommé « le coronavirus », « le nouveau coronavirus », « le coronavirus de Wuhan », ou encore « le coronavirus du marché aux fruits de mer de Wuhan ». L'Organisation mondiale de la santé (OMS) avait recommandé dans un premier temps l'appellation « 2019-nCoV » (sous-titre du présent article) tant qu'un nom définitif n'avait pas été fixé par l'International Committee on Taxonomy of Viruses (ICTV) conformément à ses recommandations générales en cas d'émergence épidémiologique[17].
Le , le groupe d'étude Nidovirales de l'ICTV a proposé le nom SARS-CoV-2 au terme d'une analyse taxonomique poussée[2]. Ce travail montre notamment que le nouveau coronavirus appartient à la même espèce biologique que SARS-CoV qui avait causé l'épidémie de SRAS en 2003, même si le syndrome observé en 2019 diffère de celui-ci. L'OMS donne à la pneumonie de Wuhan le nom officiel de COVID-19[18], pour "coronavirus disease 2019" (acronyme à utiliser au féminin pour "la" maladie: "la COVID-19"). La pathologie pulmonaire est également citée dans certaines grandes revues sous la dénomination "Fièvre des rizières" compte tenu de son émergence initiale sur le territoire chinois[19].
Même si nommer différemment la maladie et l'agent qui la cause est habituel (ex. HIV cause le sida), et si la définition des espèces biologiques dépend d'autres éléments que ceux purement conjoncturels (ex. Botrytis cinerea cause la pourriture grise mais aussi la pourriture noble recherchée pour la vinification des sauternes), l'apparition des deux noms le même jour a d'abord suscité quelques incompréhensions tant chez un public peu averti mais sensibilisé par une situation de crise[20], que dans la communauté scientifique[21],[22].
Symptômes chez l'humain

Les maladies que provoquent les coronavirus peuvent aller du rhume (ils en sont la seconde cause aux États-Unis[23]) à des maladies plus graves telles que le syndrome respiratoire aigu sévère (SRAS, épidémie en 2003) et le syndrome respiratoire du Moyen-Orient (MERS-CoV, épidémie en 2012).
La première description scientifique de la pathologie et de l'épidémiologie de SARS-CoV-2 date du 24 janvier 2020, faite par un consortium de médecins de Wuhan et de Pékin, et basée sur la petite cohorte des 41 premiers cas étudiés à Wuhan en décembre 2019[10]. L'âge médian des patients était de 49 ans ; aucun n'avait moins de 18 ans. Le délai médian entre l'infection et l'hospitalisation était de 7 jours (4-8 jours) ; la dyspnée s'est déclarée à 8 jours (5-13 jours) pour 51 % d'entre eux, et s'est aggravée à 9 jours (8-14 jours) pour 27 % d'entre eux ; l'admission en unité de soins intensifs est devenue nécessaire à 10,5 jours (8-17 jours) pour 39 % d'entre eux. Quelques semaines plus tard, 28 (68 %) des 41 patients étaient sortis de l'hôpital tandis que 6 (15 %) étaient décédés.
Les symptômes rapportés évoquent grossièrement ceux de la grippe saisonnière : fièvre, fatigue, toux sèche, manque de souffle, difficultés à respirer[24],[25], pneumonie, insuffisance rénale se concluant par la mort dans les cas sévères[26],[27].
75% des premiers hospitalisés présentent une lymphopénie (manque de lymphocytes) mais des signes vitaux stables à leur admission[24]. 25% des diagnostiqués ont des symptômes sévères. Parmi les 41 premiers patients hospitalisés et diagnostiqués positifs au coronavirus 2019, la majorité étaient en bonne santé avant leur infection, un tiers étant concerné par des problèmes de santé préalables. Les trois quarts des patients toussaient, un peu plus de la moitié ressentait une gêne respiratoire, et un tiers avait des difficultés respiratoires sévères nécessitant des soins intensifs[28],[10]. Le 23 janvier 2020, l'OMS déclare que la plupart des patients décédés avaient un système immunitaire affaibli par des problèmes de santé tels que l'hypertension, le diabète ou une maladie cardiovasculaire[29].
Taux de létalité
Il reste incertain car estimer le nombre réel de cas et le nombre de décès attribuables à SARS-CoV-2 est difficile[30],[31],[32]. En outre, il peut évoluer avec des mutations du virus.
La première évaluation de létalité a été communiquée le 14 février par le Centre chinois de contrôle et de prévention des maladies (CDC chinois) d'après les 44 672 premiers cas confirmés[33] :
- il était alors estimé à 2,3 % ; la COVID-19 étant doux pour 81 % des patients et souvent plus dur pour les personnes âgées ou porteurs d'une autre maladie (seuls 2,2 % des cas déclarés avaient moins de 20 ans)[4], mais d'autres cas étaient symptomatiques ou non identifiés ; puisque 1,2 % des cas confirmés étaient asymptomatiques[33] ;
- l'OMS, se basant sur les chiffres fournis par les pays (infections avérées, décès...) a confirmé un taux de létalité d'environ 2 % (426 décès sur 20 588 infections)[34], taux semblant faible comparé à celui d'autres coronavirus comme le SARS-CoV ou le MERS-COV (9,8 % et 34 % respectivement[35]), mais bien plus élevée par exemple que pour la plupart des virus grippaux chez l'humain ;
- mais fin février, le CDC chinois a réévalué à la hausse ce taux de mortalité (passé de 2,3 % à 3,46 %)[36].
- le taux de mortalité est différent en fonction du pays et fonction de la possibilité d'accès aux services hôspitaliers. Au 11 mars 2020, la létalité était de 6,6 % en Italie (827 décès pour 12 462 infectés[37]) contre 0,8 % en Corée du Sud (66 décès pour 7 869 infectés[38]).
- le taux de létalité des cas confirmés à l'échelle mondiale, communiqué par l'OMS le , est de 3,4 %[39]
Le taux de létalité est toutefois un chiffre qu'il faut interpréter avec beaucoup de précaution[40], dans la mesure où beaucoup de pays ont des taux de tests de dépistage par habitant très différents (ex. : le taux chinois est 45 fois plus élevé que le taux français). La proportion de contaminés asymptomatiques (et donc non décelés) est probablement supérieure à 40%, ce qui diminue beaucoup la létalité réelle par rapport à celle qui est constatée à partir du chiffre des contaminés.
Taxonomie et phylogénie (origine du virus)

Le virus SARS-CoV-2 appartient à l'espèce SARS-CoV, dans le genre Betacoronavirus et la famille Coronaviridae[2]. La morphologie des virions est typique de celle des coronavirus[25], avec notamment le halo de protubérances protéiques ("Spike") qui leur a donné leur nom ("virus à couronne").
Le nombre de génomes isolés et séquencés croît rapidement ainsi que leurs origines géographiques : ils sont 529 au [41] (les premiers génomes séquencés, originaires de Wuhan, l'ont été par le CDC chinois, l'Institut de biologie des agents pathogènes et l'hôpital Wuhan Jinyintan[42],[43]). Ceci a permis de rapidement montrer que SARS-CoV-2 a des similitudes avec les Betacoronavirus trouvés chez les chauves-souris[44],[45]. Il forme une souche virale génétiquement distincte des autres coronavirus humains MERS[44] ou à d'autres espèces plus bénignes, mais appartenant à la même espèce biologique que le SARS-CoV[2], dans le sous-genre Sarbecovirus[46],[47],[48].
Le marché de gros de fruits de mer de Huanan, à Wuhan, a été désigné comme source initiale de l'épidémie par les autorités locales le 31 décembre 2019[49]. Il a été fermé au lendemain même, le 1er janvier 2020. Les premiers symptômes attribuables a posteriori à SARS-CoV-2 seraient toutefois apparus dès le 1er décembre 2019 chez un patient n'ayant pas fréquenté ce marché[10], de même qu'un tiers des 41 cas signalés à Wuhan en décembre 2019 ; des experts en ont déduit que l'origine de l'épidémie pourrait être antérieure à décembre 2019, et ne pas se trouver sur le marché de Wuhan[50],[51]. Le pangolin est fortement suspecté, mais n'étant pas très commun, il est possible qu'un autre mammifère soit aussi impliqué [4].
Une analyse phylogénétique et génomique précoce excluait quasiment une descendance directe de SARS-CoV-2 à partir des souches classiques de SARS-CoV[52]. Selon ses auteurs un événement de recombinaison homologue pourrait avoir "mélangé" un Betacoronavirus de « clade A » (virus de type Bat SARS CoVZC45 et CoVZXC21) avec un bétacoronavirus encore inconnu. Cette étude suggère par ailleurs, en examinant la fréquence d'usage des codons, qu'un serpent de la région de Wuhan serait le "réservoir sauvage le plus probable" pour SARS-CoV-2 (bien qu'aucun coronavirus ne soit déjà connu chez les animaux à sang froid), hypothèse largement reprise par la presse[53] puis remise en cause puis formellement écartée[54],[55] de même, quelques jours après, que l'hypothèse d'une recombinaison récente[56].
En outre, même si ce marché vendait une grande diversité de faune sauvage[57], les chauves-souris ne semblent pas en faire partie, et leur consommation n'est pas traditionnelle dans la région, malgré des affirmations de vidéos devenues virales sur Internet[58],[59], contribuant à une forme de xénophobie anti-asiatique développée à cette occasion. Si SARS-CoV-2 semble bien issu d'un virus de chauve-souris, il peut être passé à l'homme via un hôte intermédiaire de la même façon que le SARS-CoV (hôte intermédiaire: la civette) ou le MERS-CoV (hôte intermédiaire: le dromadaire). Certains experts[60],[61] avancent l'hypothèse du Pangolin, un mammifère en danger qui fait l'objet d'une consommation illégale en Chine et qui était en vente sur le marché de Wuhan: en effet, on trouve chez le pangolin des coronavirus quasiment identiques au SARS-CoV-2[62],[63].
Sur la base des séquences complètes disponibles, l'initiative GISAID commence dès fin janvier 2020 à distinguer une histoire évolutive de SARS-CoV-2[64] : des mutations groupées dans le temps et dans l'espace de l'épidémie, ainsi que le long du génome.
Bruno Canard, directeur de recherche CNRS, relève que « les coronavirus responsables des épidémies de SRAS (syndrome respiratoire aigu sévère), du MERS (Middle East Respiratory Syndrom) et du SARS-CoV-2 proviennent de virus issus du monde animal qui ont franchi la barrière inter-espèces ». Il estime ainsi que « l’anthropisation globale du monde favorise l’émergence de virus qui étaient jusqu’à présent cachés chez les animaux et étaient maintenus dans leurs habitats naturels par une biodiversité importante ». Il souligne que « plusieurs études ont d’ailleurs démontré que la biodiversité est le meilleur rempart contre les émergences virales »[65]. Selon le chercheur Serge Morand, « la Chine du Sud et l’Asie du Sud-Est présentent toutes [les] caractéristiques de biodiversité, d’intensification agronomique et d’élevage (qui entraîne une crise de la biodiversité) et d’intégration dans le marché international et touristique », favorables à « l’émergence d’une nouvelle maladie infectieuse à potentiel pandémique »[66].
Génome
Son génome, d'abord réputé stable[67] est constitué d'un ARN simple-brin de 29 903 nucléotides. Il a été séquencé le à l'université Fudan de Shanghai en Chine[68],[69],[70],[71].
Le SARS-CoV-2 a rapidement produit au moins trois souches[72]. Les génomes complets de ces trois souches et d'autres génomes disponibles de Betacoronavirus ont été alignés et comparés entre eux[72].
En termes d'homologie, le SARS-CoV-2 est :
- à 50 % semblable à celui du MERS-CoV[73] ;
- à 79,5 % semblable à celui du SARS-CoV[74] ;
- à 96 % semblable à celui d'un coronavirus d'une chauves-souris chinoise du genre Rhinolophe : Rhinolophus affinis[44],[75] ;
- à 99 % homologue à un coronavirus présent chez les pangolins[76],[77],[78].
Cela laisse supposer que l'origine du virus est chez les pangolins ou les chauves-souris[45],[55],[4],[75].
Biologie moléculaire (fonctionnement du virus)
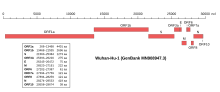

Le premier génome entièrement séquencé est celui de la souche Wuhan-Hu-1, diffusé le 23 janvier 2020, deux semaines après la découverte de la maladie [68]. L'organisation de l'ARN génomique, qui comprend 29903 nucléotides, est typique de celle d'un Betacoronavirus. Un segment de la protéine spike (la protéine des protubérances qui forment la « couronne ») semble caractéristique de SARS-CoV-2, ainsi que peut-être un court gène supplémentaire, dont la réalité biologique et le rôle éventuel restent toutefois à démontrer[79]. Cette protéine, qui sert au virus à s'attacher à la cellule, probablement activée par la furine de l'hôte, est apparemment beaucoup plus efficace que celle du SARS-CoV et expliquerait pourquoi le COVID-19 se répand beaucoup plus vite que le SRAS[80]. La publication du génome a conduit à plusieurs expériences de modélisation de la protéine Spike (S), présumée jouer un rôle dans la liaison du virus au récepteur cellulaire.
Au 23 janvier 2020, deux groupes chinois pensent que cette protéine S conserve une affinité suffisante avec le récepteur du SARS-CoV (enzyme de conversion de l'angiotensine 2, ACE2) pour l'utiliser comme mécanisme d'entrée cellulaire[81]. L'identification de ACE2 comme récepteur cellulaire est également décrite indépendamment par trois autres groupes de chercheurs[44],[82],[83]. Le récepteur cellulaire de MERS-CoV, DPP4, ne semble pas reconnaître la protéine Spike de SARS-CoV-2[83], en accord avec la plus grande proximité moléculaire de SARS-CoV-2 avec SARS-CoV qu'avec MERS-CoV.
Le 14 mars 2020, les travaux d'un autre groupe chinois suggèrent toutefois qu'une voie d'entrée cellulaire supplémentaire pourrait être utilisée par SARS-CoV-2: l'immunoglobuline transmembranaire CD147 (en)[84].
Suite à l'entrée du virus dans la cellule, la protéine Spike est maturée par la protéase cellulaire à sérine TMPRSS2, là encore comme c'est le cas pour SARS-CoV: cette découverte donne des pistes pour l'élaboration de traitements antiviraux[83].
Le virus provoquerait en particulier :
- une réponse inflammatoire excessive du système immunitaire inné[85].
- des effets neurologiques, dont les principaux signes sont les maux de tête, des nausées et vomissements[86] ; Un nombre croissant de preuves indique que les coronavirus ne colonisent pas que les voies respiratoires, mais aussi le système nerveux central en y faisant des dégâts neurologiques. Ainsi le SARS-CoV a déjà été associé a des atteintes cérébrales et notamment du tronc cérébral chez des humains, comme dans le modèle animal en laboratoire. Et d'autres coronavirus peuvent se propager par des voies synaptiques vers le centre cardiorespiratoire situé dans le tronc cérébral, à partir de mécanorécepteurs et de chimiorécepteurs présent dans les poumons et reliés au cerveau et à la moelle épinière[86].
Épidémiologie
Incubation
La période d'incubation de SARS-CoV-2 est estimée entre 2 et 14 jours[87], parfois plus longue (jusqu'à 24 jours)[88].
Dans une étude publiée avec relecture par les pairs le 10 mars[89], portant sur 181 cas documentés (avec une sur-représentation possible des cas les plus sévères selon les auteurs), la période d'incubation médiane est estimée à 5,1 jours, tandis que 97,5% de ceux qui développeront des symptômes le font en moins de 11,5 jours; cette étude suggère que sur 10 000 cas, 101 développent des symptômes plus tard que 14 jours de suivi actif et de quarantaine.
Plus de la moitié des contaminations seraient le fait de porteurs ne montrant pas encore de symptômes[90].
Durée de survie du virus hors de l'organisme
Un coronavirus - hors organisme - reste infectieux environ 2 à 3 heures dans l'air (en milieu sec)[91] et peut-être jusqu'à 3 jours en milieu humide, ce qui exclut tout risque de contamination par colis voyageant entre continents autrement que directement en avion: dans les cas les plus rapides par mer, ils parcourent la distance Chine–États-Unis en 4 jours[92],[93].
Sur des surfaces lisses non poreuses (acier inoxydable, plastique, céramiques, verre...) des travaux antérieurs on montré que SARS-CoV, très proche, peut rester infectieux jusqu'à 9 jours[94], sauf s'il s'agit de cuivre, laiton, bronze qui sont naturellement biocides pour de nombreux organismes et microbes.
Pour SARS-CoV-2, la durée de demie-vie (temps nécessaire pour que la moitié des virus soient inactivés) est dans un environnement moyen d'environ 13 heures sur de l'inox et 16 heures sur du polypropylène[91].
Le papier/carton (non plastifié) ou la plupart des textiles de vêtements non-imperméables ne sont pas considéré comme « lisses », et de manière générale les virus de ce type y survivent bien moins longtemps que sur une surface lisse de métal ou plastique[91].
Au 12 mars 2020, selon les CDC américains rien n'indique que le virus se propage par l'eau potable, les piscines ou les bains à remous[95].
Vulnérabilité du virus au savon et aux désinfectants
À la différence des norovirus ou d'autres virus courants protégés par une enveloppe protéique plus ou moins solide, tous les coronavirus (dont le SARS-CoV-2) sont très vulnérables au savon, aux solutions hydro-alcooliques et aux désinfectants ménagers courants, ainsi qu'aux désinfectants industriels et hospitaliers adaptés ; les coronavirus déposés (via des gouttelettes ou des aérosols) sur les surfaces intérieures sont immédiatement détruits car leur enveloppe protectrice n'est qu'une simple couche de lipides[95].
Pour le SRAS, un temps de contact d'une minute avec de l'eau de Javel diluée à 0,1 % ou avec une solution à 62–71 % d’éthanol réduisait aussi significativement l'infectivité des virus déposés sur des surfaces lisses ; mi-, on espère qu'il en va de même pour le SARS-CoV-2[94].
Historique (dispersion du virus)
Dans les premières semaines de l'épidémie de 2019-2020, le virus s'est propagé via des voyageurs vers différents pays d'Asie[96],[97],[98], le 21 janvier en Amérique du Nord[99], le 24 janvier, en Australie[100], en Europe[101],[102], le 16 février en Afrique[103] et le 26 février en Amérique du Sud[104].
À la date du 16 mars 2020 on compte 6 513 décès et 77 257 guérisons pour 169 387 cas confirmés[105] (le cap des 100 000 cas est franchi le 6 mars), le tout principalement dans la province du Hubei. Ces chiffres constituent probablement une large sous-estimation de l'ampleur de l'épidémie[106],[107], la maladie restant souvent discrète notamment chez les sujets jeunes et les tests de dépistage n'étant pas appliqués systématiquement à tous les cas suspects.
Le , la transmission interhumaine a été confirmée dans le Guangdong, en Chine, selon Zhong Nanshan, chef de l'équipe de la commission de la santé enquêtant sur l'épidémie[108]. La première description scientifiquement détaillée d'une transmission interhumaine au sein d'une famille a été publiée par une équipe de médecins de Hong Kong et de Shenzhen le 24 janvier 2020[9]. Le taux de reproduction (Ro) préliminaire de SARS-CoV-2, c’est-à-dire le nombre moyen de personnes infectées par un patient, a été estimé entre 1,4 et 2,5 par l'OMS le 23 janvier 2020[109]. Il serait comparable à celui de SARS-CoV et de la grippe de 1918, compris entre 1,4 et 3,8[110].
Situation épidémique
En décembre 2019 et janvier 2020, l'épidémie est encore principalement concentrée sur la Chine et touche surtout la province du Hubei. Le premier cas exporté hors de la Chine continentale est découvert le 13 janvier en Thaïlande[111]. La situation évoluant rapidement au niveau mondial, elle est déclarée urgence de santé publique de portée internationale par l'OMS le 30 janvier 2020[3]. C'est la sixième fois seulement que l'OMS déclenchait ce niveau d'alerte dans son histoire.
Mi-février 2020, le plus important foyer hors de Chine était le paquebot de croisière Diamond Princess, en quarantaine dans le port de Yokohama[112]. Dans la troisième semaine de février toutefois, des foyers secondaires d'importance ont émergé en Corée du Sud, en Italie et en Iran[113], faisant craindre une installation durable de l'épidémie au niveau mondial[114]. Cette crainte se confirme début mars: le 11 mars, le directeur général de l'OMS déclare que "la COVID-19 peut être qualifiée de pandémie"[115] et le 15 mars, le nombre de cas hors de Chine dépasse celui dénombré en Chine continentale[105].
Un premier décès hors de Chine est déclaré le 1er février aux Philippines : c'est un touriste venu de Wuhan où il a probablement été contaminé[116]. Le premier décès hors d'Asie survenu en France le 15 février[117] est également un cas importé de Chine. Le 6 mars, l'Italie devenait le second pays en nombre de décès après la Chine[105].
Traitement et vaccins
L'essentiel de la lutte contre la COVID-19 repose sur des mesures épidémiologiques: diagnostic fiable et rapide de la maladie en période d'incubation, mesures de confinement (qui peuvent aussi être un facteur de diffusion intragroupe[118]).
Traitements antiviraux
Le SARS-CoV-2 étant de nature virale, les antibiotiques et les bactériophagiques sont inadaptés, étant donné qu'ils ne traitent que les pathologies bactériennes. Toutefois, les bactéries étant plus susceptibles d'adhérer aux cellules infectées par un virus tel le coronavirus[119], on observe une surinfection bactérienne, en particulier par le Streptococcus pneumoniae dans 10 % des cas d'infection virale[25]. Dans cette situation, la prescription d'un antibiotique adapté à la sensibilité de la bactérie se justifie donc.
Aucun traitement antiviral spécifique n'est actuellement disponible[120], mais des antiviraux existants pourraient être repositionnés[121], y compris des inhibiteurs de protéase comme l'indinavir, le saquinavir et le lopinavir/ritonavir[122], ou encore le nelfinavir[123]. L'efficacité de l'inhibiteur de polymérase sofosbuvir, utilisé contre l'hépatite C, est également en cours d'évaluation en janvier 2020[124]. Le 2 février, des médecins thaïlandais ont annoncé avoir traité un patient avec succès en utilisant une combinaison des anti-HIV lopinavir et ritonavir ainsi que l'anti-grippal oseltamivir[125],[126]. Un analogue de nucléoside comme le remdésivir fait également l'objet de recherches à la suite d'un résultat positif[127]. Les traitements reçus par les patients concernent donc essentiellement l'atténuation des symptômes de fièvre, toux et dyspnée, afin de favoriser leur guérison spontanée[24],[105],[128]. Le Centre chinois de contrôle et de prévention des maladies a démarré dès janvier l'évaluation de l'efficacité de traitements existants contre les pneumonies[129], l'efficacité ayant été montrée in vitro[130]. Les médicaments présentant des essais thérapeutiques en phase IV (la plus avancée) sont l'umifénovir (Arbidol) et le lopinavir[131]. Le mésylate de camostat aurait une action inhibitrice de l'entrée du virus [132]. En effet, une enzyme nécessaire à la réplication virale, la protéase à sérine TMPRSS2, est inactivée par l'utilisation d'une thérapie contre l'inflammation chronique du pancréas[133].
Un repositionnement constituant une première piste est celui d'une molécule initialement antipaludique, la chloroquine, dont l'effet anticoronaviral avait déjà été démontré sur le SRAS[134]. Le 19 février, une lettre parue dans la revue BioScience Trends indique que des études cliniques chinoises ont montré une efficacité apparente du phosphate de chloroquine dans le traitement du virus[135]. Ces données sont cependant encore limitées notamment en raison de la petite taille de l'échantillon statistique (100 patients)[136]. Un consensus d'experts chinois recommande le 20 février d'inclure le phosphate de chloroquine dans les recommandations de prise en charge des patients sans contre-indication à la chloroquine, à raison de 500 mg deux fois par jour pendant 10 jours pour les patients diagnostiqués comme des cas légers, modérés et sévères de maladie[136],[137]. Il est cependant à noter que la prise de chloroquine à haute dose peut provoquer des effets secondaires potentiellement sérieux, en particulier celui d'une intoxication aiguë susceptible de déclencher des problèmes cardiaques ou respiratoires, et que la dose recommandée par les chercheurs chinois se rapproche de cette zone de risque[136]. Le 25 février, le professeur Didier Raoult recommande l'utilisation de la chloroquine pour les patients porteurs du virus[138], prédisant même une « fin de partie » pour le virus[139]. Sa déclaration est vivement critiquée par des médecins et scientifiques français sur les réseaux sociaux pour son manque de pondération[136] vis-à-vis de la limitation des données cliniques et des risques liés à la prise de chloroquine. L'Inserm tempère également et rappelle qu'aucune prise de médicament quel qu'il soit n'est anodine, et qu'il ne faut pas se faire prescrire la molécule pour l’utiliser en automédication[140],[141].
L'injection d'ACE2, point d'attache du virus aux cellules eucaryotes[142],[143] , ralentirait la pénétration du virus et protégerait les poumons. Assez paradoxalement cependant, des études mettent en avant le risque accru d'infection par Sars-Cov2 des patients souffrant d'hypertension ou de diabète traités par les inhibiteurs de l'enzyme de conversion ou par les Antagoniste des récepteurs de l'angiotensine II[144], qui présentent un nombre accrus de récepteurs de l'enzyme ACE2. Les effets induits d'une modification des traitements, par exemple pour ceux qui ont des pathologies cardiaques [145],même s'ils ne seraient pas négligeables, pourraient être limités s'ils restent temporaires.
Des approches thérapeutiques basées sur l'antigène CD147, s'il est confirmé qu'il est l'autre point d'entrée du virus, pourraient présenter des effets indésirables moindres[84].
Vaccins à l'étude
À plus long terme, plusieurs équipes internationales travaillent à la mise au point ou à l'adaptation d'un vaccin[146],[147]. Même si l'épidémie de SRAS a finalement été maîtrisée sans vaccin[148], la proximité moléculaire de SARS-CoV-2 avec SARS-CoV est un atout puisqu'au-delà d'indéniables différences entre ces deux virus[149], elle permet de capitaliser sur les connaissances acquises alors[150] (faisant au passage regretter que les recherches sur la mise au point d'un vaccin anti-SARS-CoV aient été interrompues lorsque ce premier virus a été considéré éradiqué).
Début février 2020, une équipe de recherche de l'Imperial College de Londres a fait une percée significative en réduisant une partie du temps de développement normal du vaccin « de deux à trois ans à seulement quatorze jours »[151],[152]. L'équipe de l'Imperial College est désormais au stade de test du vaccin sur les animaux[151]. En , un vaccin est en cours d'élaboration en Russie[153],[154], et un autre est préparé par la firme pharmaceutique Johnson & Johnson, mais ne serait pas disponible avant un an[155].
À la même période, en France, dans le cadre d'une recherche vaccinale concernant le MERS-CoV en cours depuis 2012, l'institut Pasteur pourrait utiliser et adapter ces vaccins pour SARS-CoV-2. Plusieurs équipes de l'Institut Pasteur travaillent sur son adaptation et seraient en mesure de produire ce vaccin en cas d'épidémie[156].
L'institut Robert-Koch préconise la vaccination contre le pneumocoque des personnes âgées, en particulier autour des foyers d'infection[157].
Le développement d'anticorps monoclonaux spécifiques est une autre piste[158],[159] de traitement qui a par ailleurs déjà montré son efficacité dans le cas du MERS-CoV[160],[161]. Ceci, d'autant que les anticorps produits naturellement n’empêcheraient pas les infections récidivantes chez certains patients[162],[163]. Un essai est déjà en cours en Chine avec le Tocilizumab [164]. Un traitement conçu à partir du plasma des patients immunisés diminuerait la mortalité par deux[165]. Il doit être possible comme cela a été tenté pour le virus HIV[166],[167],[168], de produire des lymphocytes B modifiés par Cirspr-Cas9 contre le virus Sars-Cov2.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Severe acute respiratory syndrome coronavirus 2 » (voir la liste des auteurs).
- (en) « Virus Taxonomy: 2018b Release », ICTV, (consulté le ).
- (en) Alexander E. Gorbalenya, Susan C. Baker, Ralph S. Baric, Raoul J. de Groot, Christian Drosten, Anastasia A. Gulyaeva, Bart L. Haagmans, Chris Lauber, Andrey M Leontovich, Benjamin W. Neuman, Dmitry Penzar, Stanley Perlman, Leo L.M. Poon, Dmitry Samborskiy, Igor A. Sidorov, Isabel Sola et John Ziebuhr, « Severe acute respiratory syndrome-related coronavirus – The species and its viruses, a statement of the Coronavirus Study Group », bioRxiv, (DOI 10.1101/2020.02.07.937862, lire en ligne, consulté le )
- « Déclaration sur la deuxième réunion du Comité d’urgence du Règlement sanitaire international (2005) concernant la flambée de nouveau coronavirus 2019 (2019-nCoV) tenue le 30 janvier 2020 », sur www.who.int (consulté le )
- (en) Fisher D. et Heymann D., « Q&A: The novel coronavirus outbreak causing COVID-19 », BMC Med, (lire en ligne)
- (en) « Phylogeny of SARS-like betacoronaviruses including novel coronavirus from Wuhan using data generated by the Shanghai Public Health Clinical Center & School of Public Health, the National Institute for Viral Disease Control and Prevention, the Institute of Pathogen Biology, and the Wuhan Institute of Virology shared via GISAID », sur https://nextstrain.org/, (consulté le ).
- (en) « 2019-nCoV in bioRxiv », sur bioRxiv (consulté le )
- (en) Tianmu Chen, Jia Rui, Qiupeng Wang et Zeyu Zhao, « A mathematical model for simulating the transmission of Wuhan novel Coronavirus », bioRxiv, Systems Biology, (DOI 10.1101/2020.01.19.911669, lire en ligne, consulté le )
- (en) Jonathan M Read, Jessica RE Bridgen, Derek AT Cummings et Antonia Ho, « Novel coronavirus 2019-nCoV: early estimation of epidemiological parameters and epidemic predictions », medRxiv, Infectious Diseases (except HIV/AIDS), (DOI 10.1101/2020.01.23.20018549, lire en ligne, consulté le )
- (en) Jasper Fuk-Woo Chan, Shuofeng Yuan, Kin-Hang Kok et Kelvin Kai-Wang To, « A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster », The Lancet, , S0140673620301549 (DOI 10.1016/S0140-6736(20)30154-9, lire en ligne, consulté le )
- (en) Chaolin Huang, Yeming Wang, Xingwang Li et Lili Ren, « Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China », The Lancet, , S0140673620301835 (DOI 10.1016/S0140-6736(20)30183-5, lire en ligne, consulté le ).
- (en) Elsevier, « Novel Coronavirus Information Center », sur Elsevier Connect (consulté le )
- (en) « COVID-19 Resource Centre », sur www.thelancet.com (consulté le )
- (en) « Coronavirus (Covid-19) — NEJM », sur New England Journal of Medicine (consulté le )
- (en) « Coronavirus », sur Science | AAAS (consulté le )
- « Coronavirus | Springer Nature | For Researchers | Springer Nature », sur www.springernature.com (consulté le )
- (en) « Novel Coronavirus - Wiley Online Library », sur Novel Coronavirus (consulté le )
- « WHO | WHO best practices for naming of new human infectious diseases », sur WHO (consulté le )
- (en) « Novel Coronavirus (2019-nCoV) Situation Report – 22 » [PDF], sur who.int, Organisation mondiale de la santé, (consulté le ) : « Following WHO best practices for naming of new human infectious diseases, which were developed in consultation and collaboration with the World Organisation for Animal Health (OIE) and the Food and Agriculture Organization of the United Nations (FAO), WHO has named the disease COVID-19, short for “coronavirus disease 2019.” », p. 1.
- (en) Quentin Remy, P.Hamber Mossan, Peter Robin et Mathew Martin et al., "SARS-Cov-2, a new type of virus", Clinical Epidemiology, , Vol. 56, p.30-43
- « Epidémie de Covid-19 : la difficulté de bien nommer le virus et la maladie », Le Monde.fr, (lire en ligne, consulté le ).
- (en) Shibo Jiang, Zhengli Shi, Yuelong Shu et Jingdong Song, « A distinct name is needed for the new coronavirus », The Lancet, , S0140673620304190 (DOI 10.1016/S0140-6736(20)30419-0, lire en ligne, consulté le )
- (en) Yuntao Wu, Wenzhe Ho, Yaowei Huang et Dong-Yan Jin, « SARS-CoV-2 is an appropriate name for the new coronavirus », The Lancet, , S0140673620305572 (DOI 10.1016/S0140-6736(20)30557-2, lire en ligne, consulté le ).
- (en) Marie E. Killerby, Holly M. Biggs, Amber Haynes et Rebecca M. Dahl, « Human coronavirus circulation in the United States 2014–2017 », Journal of Clinical Virology, vol. 101, , p. 52–56 (DOI 10.1016/j.jcv.2018.01.019, lire en ligne, consulté le ).
- (en) Hui DS, I Azhar E, Madani TA, Ntoumi F, Kock R,, Dar O, Ippolito G, Mchugh TD, Mchugh TD, Memish ZA et al., « The continuing 2019-nCoV epidemic threat of novel coronaviruses to global health – The latest 2019 novel coronavirus outbreak in Wuhan, China », International Journal of Infectious Diseases, vol. 91, , p. 264-266 (PMID 31953166, DOI 10.1016/j.ijid.2020.01.009, lire en ligne, consulté le )
 .
.
- (en) Na Zhu, Dingyu Zhang, Wenling Wang et Xingwang Li, « A Novel Coronavirus from Patients with Pneumonia in China, 2019 », New England Journal of Medicine, , NEJMoa2001017 (ISSN 0028-4793 et 1533-4406, DOI 10.1056/NEJMoa2001017, lire en ligne, consulté le )
- (en-CA) « Wuhan Novel Coronavirus (2019-nCoV) », sur Ontario.ca, (consulté le ).
- « Experts explain the latest bulletin of unknown cause of viral pneumonia » [archive du ], sur Wuhan Municipal Health Commission, (consulté le ).
- « Coronavirus : ce que l'on sait des premiers patients touchés par l'épidémie », sur Franceinfo, (consulté le ).
- « Déclaration du Directeur général de l’OMS sur les recommandations du Comité d’urgence du RSI sur le nouveau coronavirus », sur www.who.int, (consulté le ).
- (en) Anna Fifield, « As families tell of pneumonia-like deaths in Wuhan, some wonder if China virus count is too low », The Washington Post, (lire en ligne)
- (en-GB) Lily Kuo et Lillian Yang, « Coronavirus: Chinese hospitals not testing patients, say relatives », The Guardian, (ISSN 0261-3077, lire en ligne, consulté le )
- (en-US) Wenxin Fan, « Relatives Wonder Why Pneumonia Deaths Not in Coronavirus Tally », Wall Street Journal, (ISSN 0099-9660, lire en ligne, consulté le )
- The Novel Coronavirus Pneumonia Emergency Response Epidemiology Team. The Epidemiological Characteristics of an Outbreak of 2019 Novel Coronavirus Diseases (COVID-19) — China, 2020. China CDC Weekly, 2020, 2(8): 113–122 (résumé).
- (en) « Novel Coronavirus (2019-nCoV) situation reports », sur www.who.int (consulté le )
- « Coronavirus (SRAS-CoV et MERS-CoV) », sur Inserm - La science pour la santé (consulté le )
- Wang Y, Wang Y, Chen Y & Qin Q (2020) Unique epidemiological and clinical features of the emerging 2019 novel coronavirus pneumonia (COVID-19) implicate special control measures ; J Med Virol. 5 mars 2020 ; Epub 2020 Mar 5 (résumé)
- (it) « Covid-19 Bollettino 11/03/2020 » [PDF], sur Ministère de la Santé (Italie) (consulté le ).
- (kr) « 코로나바이러스감염증-19(COVID-19) » (consulté le ).
- « WHO Director-General's opening remarks at the media briefing on COVID-19 - 3 March 2020 », sur who.int, Organisation mondiale de la santé,
- (en) Mike Famulare, « 2019-nCoV: preliminary estimates of the confirmed-case-fatality-ratio and infection-fatality-ratio, and initial pandemic risk assessment », Github, Institute for disease modeling, (lire en ligne, consulté le ).
- Trevor Bedford and Richard Neher, « Genomic epidemiology of novel coronavirus (nCoV) using data generated by Fudan University, China CDC, Chinese Academy of Medical Sciences, Chinese Academy of Sciences, Zhejiang Provincial Center for Disease Control and Prevention and the Thai National Institute of Health shared via GISAID », nextstrain.org (consulté le )
- « Initial genome release of novel coronavirus », Virological, (consulté le )
- (en) Wu, F. et al., « Wuhan seafood market pneumonia virus isolate Wuhan-Hu-1, complete genome », sur GenBank, (consulté le )
- (en) Shi, ZL et al., « Discovery of a novel coronavirus associated with the recent pneumonia outbreak in humans and its potential bat origin », bioRxiv, (lire en ligne)
- (en) Benvenuto D. et al., « The 2019-new Coronavirus epidemic: evidence for virus evolution », bioRxiv.org, (lire en ligne)
- « Phylogeny of SARS-like betacoronaviruses », nextstrain (consulté le )
- Hui DS, I Azhar E, Madani TA, Ntoumi F, Kock R, Dar O, Ippolito G, Mchugh TD, Memish ZA, Drosten C, Zumla A, Petersen E. The continuing 2019-nCoV epidemic threat of novel coronaviruses to global health – The latest 2019 novel coronavirus outbreak in Wuhan, China. Int J Infect Dis. 2020 Jan 14;91:264–266. DOI 10.1016/j.ijid.2020.01.009

- Antonio C. P. Wong, Xin Li, Susanna K. P. Lau, Patrick C. Y. Woo: Global Epidemiology of Bat Coronaviruses, in: Viruses. 2019 Feb; 11(2): 174, doi:10.3390/v11020174
- (zh) « Notice d'information de la Commission municipale de la santé de Wuhan sur la situation actuelle de l'épidémie de pneumonie dans notre ville [en chinois] », sur http://wjw.wuhan.gov.cn/, (consulté le )
- (en-US) Antigone Barton, « UPDATE Wuhan coronavirus – 2019-nCoV Q&A #6: An evidence-based hypothesis », sur Science Speaks: Global ID News, (consulté le )
- (en) Jon CohenJan. 26 et 2020, « Wuhan seafood market may not be source of novel virus spreading globally », sur Science | AAAS, (consulté le )
- Ji, Wang, Zhao et Zai, « Homologous recombination within the spike glycoprotein of the newly identified coronavirus may boost cross‐species transmission from snake to human », Journal of Medical Virology, (DOI 10.1002/jmv.25682)
- Conversation, « Snakes could be the source of the Wuhan coronavirus outbreak », sur CNN (consulté le )
- (en-US) Robertson D.L., « nCoV's relationship to bat coronaviruses & recombination signals (no snakes) », sur Virological, (consulté le )
- (en) Callaway E. et Cyranoski D., « Why snakes probably aren’t spreading the new China virus », Nature, (ISSN 0028-0836 et 1476-4687, DOI 10.1038/d41586-020-00180-8, lire en ligne, consulté le )
- (en) Dimitrios Paraskevis, Evangelia Georgia Kostaki, Gkikas Magiorkinis et Georgios Panayiotakopoulos, « Full-genome evolutionary analysis of the novel corona virus (2019-nCoV) rejects the hypothesis of emergence as a result of a recent recombination event », bioRxiv, Microbiology, (DOI 10.1101/2020.01.26.920249, lire en ligne, consulté le )
- « Wuhan virus: a visual explainer », sur South China Morning Post (consulté le ).
- « #VraiOuFake Coronavirus : la consommation d'une soupe de chauve-souris à Wuhan est-elle à l'origine de l'épidémie ? », sur Franceinfo, (consulté le )
- (en-US) James Palmer, « Don’t Blame Bat Soup for the Wuhan Virus », sur Foreign Policy (consulté le )
- (en) David Cyranoski, « Did pangolins spread the China coronavirus to people? », Nature, , d41586–020–00364-2 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/d41586-020-00364-2, lire en ligne, consulté le )
- « Coronavirus : le pangolin a-t-il pu servir d’hôte intermédiaire ? », Le Monde.fr, (lire en ligne, consulté le ).
- (en) Ping Liu, Wu Chen et Jin-Ping Chen, « Viral Metagenomics Revealed Sendai Virus and Coronavirus Infection of Malayan Pangolins (Manis javanica) », Viruses, vol. 11, no 11, , p. 979 (ISSN 1999-4915, PMID 31652964, PMCID PMC6893680, DOI 10.3390/v11110979, lire en ligne, consulté le ).
- (en) Matthew C. Wong, Sara J. Javornik Cregeen, Nadim J. Ajami et Joseph F. Petrosino, « Evidence of recombination in coronaviruses implicating pangolin origins of nCoV-2019 », bioRxiv, Microbiology, (DOI 10.1101/2020.02.07.939207, lire en ligne, consulté le ).
- « GISAID - Next betaCoV App », sur www.gisaid.org (consulté le )
- Anaïs Culot, « La science fondamentale est notre meilleure assurance contre les épidémies », sur lejournal.cnrs.fr, (consulté le ).
- « La crise de la biodiversité favorise les maladies infectieuses émergentes », sur Charlie Hebdo.fr, (consulté le ).
- « Coronavirus chinois : les raisons pour lesquelles il ne faut pas paniquer », sur LExpress.fr, (consulté le )
- (en) « Wuhan seafood market pneumonia virus », sur NCBI (consulté le ).
- « New-type coronavirus causes pneumonia in Wuhan: expert – Xinhua | English.news.cn » (consulté le ).
- « CoV2020 », platform.gisaid.org (consulté le ).
- (en) Wu, F. et al., « Wuhan seafood market pneumonia virus isolate Wuhan-Hu-1, complete genome », sur GenBank, (consulté le ).
- SARS-CoV, B. S. (2020). Mutation and Recombination.
- Lu R, Zhao X, Li J, et al. (2020) Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding. The Lancet; 395: 565–74.
- Lee E.Y, Ng M.Y & Khong P.L (2020) COVID-19 pneumonia: what has CT taught us?. The Lancet Infectious Diseases.
- (en) Peng Zhou, Xing-Lou Yang, Xian-Guang Wang et Ben Hu, « A pneumonia outbreak associated with a new coronavirus of probable bat origin », Nature, (ISSN 0028-0836 et 1476-4687, DOI 10.1038/s41586-020-2012-7, lire en ligne, consulté le )
- Hervé Morin, Coronavirus : le pangolin a-t-il pu servir d’hôte intermédiaire ?, Le Monde, 7 février 2020. L’université d’agriculture de Chine du Sud a annoncé qu'un séquencage du virus trouvés chez des pangolins montrait qu'il était homologue à 99 % à celui du SARS-CoV-2. Le pangolin aurait pu servir d'espèce réservoir ou hôte entre la chauve-souris et l'homme, une hypothèse discutée par plusieurs spécialistes
- Expert reaction to statement from South China Agricultural University that research has identified the pangolin as a possible coronavirus host, Science Media Center, 7/02/2020.
- nCoV-2019 - Spike Protein Receptor Binding Domain Shares High Amino Acid Identity With a Coronavirus Recovered from a Pangolin Viral Metagenomic Dataset, Novel 2019 coronavirus, nCoV-2019 Evolutionary History, Virological.org, 30 janvier 2020.
- (en) Sandeep Chakraborty, « Ubiquitous genomic fragment in human 2019-nCoV viruses in the spike-protein, also encoding a novel 87 aa protein, completely missing in all other coronaviruses », OSF preprints, Open Science Framework, (DOI 10.31219/osf.io/6vd54, lire en ligne, consulté le )
- (en) Smriti Mallapaty, « Why does the coronavirus spread so easily between people? », Nature, vol. 579, no 7798, , p. 183 (DOI 10.1038/d41586-020-00660-x).
- (en) Xu, X. et al., « Evolution of the novel coronavirus from the ongoing Wuhan outbreak and modeling of its spike protein for risk of human transmission », SCIENCE CHINA Life Sciences, (lire en ligne)
- (en) Michael C. Letko et Vincent Munster, « Functional assessment of cell entry and receptor usage for lineage B β-coronaviruses, including 2019-nCoV », bioRxiv, (DOI 10.1101/2020.01.22.915660, lire en ligne, consulté le )
- (en) Markus Hoffmann, Hannah Kleine-Weber, Nadine Krueger et Marcel A Mueller, « The novel coronavirus 2019 (2019-nCoV) uses the SARS-coronavirus receptor ACE2 and the cellular protease TMPRSS2 for entry into target cells », bioRxiv, Molecular Biology, (DOI 10.1101/2020.01.31.929042, lire en ligne, consulté le )
- (en) Ke Wang, Wei Chen, Yu-Sen Zhou et Jian-Qi Lian, « SARS-CoV-2 invades host cells via a novel route: CD147-spike protein », bioRxiv, Microbiology, (DOI 10.1101/2020.03.14.988345, lire en ligne, consulté le )
- Christopher M. Coleman, Krystal L. Matthews, Lindsay Goicochea et Matthew B. Frieman, « Wild-type and innate immune-deficient mice are not susceptible to the Middle East respiratory syndrome coronavirus », The Journal of General Virology, vol. 95, no Pt 2, , p. 408–412 (ISSN 0022-1317, PMID 24197535, PMCID 3917065, DOI 10.1099/vir.0.060640-0, lire en ligne, consulté le ).
- Li YC, Bai WZ, Hashikawa T. (2020) The neuroinvasive potential of SARS-CoV2 may be at least partially responsible for the respiratory failure of COVID-19 patients.J Med Virol. 2020 Feb 27; . Epub 2020 Feb 27 (résumé)
- (en-US) Roni Caryn Rabin, « What Is the Coronavirus? Symptoms, Treatment and Risks », The New York Times, (ISSN 0362-4331, lire en ligne, consulté le )
- Clinical characteristics of 2019 novel coronavirus infection in China (sur medrxiv, plate-forme de préimpression)
- (en) Stephen A. Lauer, Kyra H. Grantz, Qifang Bi et Forrest K. Jones, « The Incubation Period of Coronavirus Disease 2019 (COVID-19) From Publicly Reported Confirmed Cases: Estimation and Application », Annals of Internal Medicine, (ISSN 0003-4819, DOI 10.7326/M20-0504, lire en ligne, consulté le )
- (en) Tapiwa Ganyani, Cecile Kremer, Dongxuan Chen et Andrea Torneri, « Estimating the generation interval for COVID-19 based on symptom onset data », bioRxiv, Infectious Diseases (except HIV/AIDS), (DOI 10.1101/2020.03.05.20031815, lire en ligne, consulté le )
- van Doremalen, N., Bushmaker, T., Morris, D., Holbrook, M., Gamble, A., Williamson, B., ... & Lloyd-Smith J (2020) Aerosol and surface stability of HCoV-19 (SARS-CoV-2) compared to SARS-CoV-1. medRxiv.
- « VERIFY: Can you get Coronavirus from packages shipped from China? », sur wbir.com (consulté le )
- « #VraiOuFake Un colis en provenance de Chine peut-il transmettre le coronavirus ? », sur Franceinfo, (consulté le )
- Kampf G, Todt D, Pfaender S & Steinmann E (2020) Persistence of coronaviruses on inanimate surfaces and its inactivation with biocidal agents. Journal of Hospital Infection ; Mars 2020 , Vol.104, no 3, Pages 246–251
- Robert F. Service (2020) Does disinfecting surfaces really prevent the spread of coronavirus? ; 12 mars 2020 Science News/HealthCoronavirus | doi:10.1126/science.abb7058
- (en) « China coronavirus: Hong Kong scraps major Lunar New Year events », sur South China Morning Post, (consulté le )
- (en) hermesauto, « Wuhan virus: Vietnam confirms 2 cases of Sars-like coronavirus », The Straits Times, (consulté le )
- (en) hermesauto, « Singapore confirms first case of Wuhan virus », The Straits Times, (consulté le )
- « New Virus Spreads to U.S., Sparking Rush to Contain Outbreak », sur www.bloomberg.com, (consulté le )
- (en) Scott Morrison, « Update on Coronavirus pic.twitter.com/Ol8DRQtVQJ », sur @ScottMorrisonMP, (consulté le )
- « Coronavirus : un troisième cas d’infection confirmé en France », Le Monde.fr, (lire en ligne, consulté le ).
- « Coronavirus : 5 nouveaux cas "sans gravité" en France dont un enfant de 9 ans scolarisé dans 2 écoles », sur lci.fr, (consulté le )
- APANEWS, « Coronavirus : l’Egypte enregistre le premier cas en Afrique », sur apanews.net (consulté le )
- (en) « Brazil confirms first coronavirus case in Latin America: source », Reuters, (lire en ligne, consulté le ).
- (en-US) « Wuhan Coronavirus (2019-nCoV) global cases (by JHU CSSE) », sur Johns Hopkins University Center for Systems Science and Engineering (consulté le )
- (en) « Two thirds of COVID-19 cases exported from mainland China may be undetected | Imperial News | Imperial College London », sur Imperial News (consulté le )
- « L’épidémie de coronavirus très sous-estimée dans le monde », La Croix, (ISSN 0242-6056, lire en ligne, consulté le )
- (en) Associated Press, « China confirms human-to-human transmission of new coronavirus », sur CBC.ca, (consulté le )
- (en) « Statement on the meeting of the International Health Regulations (2005) Emergency Committee regarding the outbreak of novel coronavirus 2019 (n-CoV) on 23 January 2020 », sur www.who.int (consulté le )
- (en) Julien Riou et Christian L. Althaus, « Pattern of early human-to-human transmission of Wuhan 2019-nCoV », bioRxiv, , p. 2020.01.23.917351 (DOI 10.1101/2020.01.23.917351, lire en ligne, consulté le )
- « Déclaration de l’OMS sur le nouveau coronavirus en Thaïlande », sur www.who.int (consulté le )
- (en) Princess Cruises, « Princess Cruises: Diamond Princess Coronavirus & Quarantine Updates - Notices & Advisories », sur www.princess.com, mon feb 17 15:21:24 pst 2020 (consulté le )
- « Coronavirus: l'Italie, la Corée du Sud et l'Iran tentent d'endiguer l'épidémie », sur RFI, (consulté le )
- « Coronavirus : la contamination s’accélère à travers la planète », Le Monde.fr, (lire en ligne, consulté le )
- « Allocution liminaire du Directeur général de l’OMS lors du point presse sur la COVID-19 - 11 mars 2020 », sur www.who.int (consulté le )
- « Coronavirus : les Philippines enregistrent le premier décès hors de Chine », sur France 24, (consulté le )
- « Coronavirus : un premier décès sur le territoire français », sur Franceinfo, (consulté le )
- « Coronavirus : des passagers du paquebot en quarantaine ont échappé aux contrôles », sur Europe 1 (consulté le ).
- Anna Golda, Natalia Malek, Bartosz Dudek, Slawomir Zeglen, Jacek Wojarski, Marek Ochman, Ewa Kucewicz, Marian Zembala, Jan Potempa et Krzysztof Pyrc, « Infection with human coronavirus NL63 enhances streptococcal adherence to epithelial cells », The Journal of General Virology, no Pt 6, , p. 1358–1368 (PMID 21325482, PMCID 3168281, DOI 10.1099/vir.0.028381-0, lire en ligne, consulté le )
- Lu H. Drug treatment options for the 2019-new coronavirus (2019-nCoV). Biosci Trends. 28 janvier 2020. DOI 10.5582/bst.2020.01020
- (en) « WHO says new China coronavirus could spread, warns hospitals worldwide », Reuters, (lire en ligne, consulté le )
- « China Testing HIV Drug as Treatment for New Coronavirus, AbbVie Says », The New York Times, (lire en ligne)
- (en) Zhijian Xu, Cheng Peng, Yulong Shi et Zhengdan Zhu, « Nelfinavir was predicted to be a potential inhibitor of 2019 nCov main protease by an integrative approach combining homology modelling, molecular docking and binding free energy calculation », bioRxiv, Pharmacology and Toxicology, (DOI 10.1101/2020.01.27.921627, lire en ligne, consulté le ).
- Abdo Elfiky, « Sofosbuvir Can Inhibit the Newly Emerged Coronavirus (2019-nCoV) in Wuhan, China », (Preprints with the Lancet, Powered by SSRN),
- « Thai doctors have been using a cocktail of flu and HIV drugs to treat coronavirus cases », Business Insider, (lire en ligne, consulté le )
- « Coronavirus: Thailand has apparent treatment success with antiviral drug cocktail », South China Morning Post, (lire en ligne, consulté le )
- (en) Michelle L. Holshue, Chas DeBolt, Scott Lindquist, Kathy H. Lofy, John Wiesman, Hollianne Bruce, Christopher Spitters, Keith Ericson, Sara Wilkerson, Ahmet Tural, George Diaz, Amanda Cohn, LeAnne Fox, Anita Patel, Susan I. Gerber, Lindsay Kim, Suxiang Tong, Xiaoyan Lu, Steve Lindstrom, Mark A. Pallansch, William C. Weldon, Holly M. Biggs, Timothy M. Uyeki, et Satish K. Pillai, « First Case of 2019 Novel Coronavirus in the United States », The New England Journal of Medicine, (PMID 32004427, DOI 10.1056/NEJMoa2001191, lire en ligne, consulté le )
- (en) « Q&A on coronaviruses » [archive du ], sur World Health Organization (WHO) (consulté le )
- (en) « China CDC developing novel coronavirus vaccine » [archive du ], sur Xinhua, (consulté le )
- "Nature, 4/02/20: Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro".
- « DrugVirus.info », sur drugvirus.info (consulté le )
- (en) "Cell, 5/3/20:SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor"
- (en) "5/3/20, cell:SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor "
- (en) Martin J Vincent, Eric Bergeron, Suzanne Benjannet et Bobbie R Erickson, « Chloroquine is a potent inhibitor of SARS coronavirus infection and spread », Virology Journal, vol. 2, no 1, , p. 69 (DOI 10.1186/1743-422X-2-69, lire en ligne, consulté le )
- (en) Jianjun Gao, Zhenxue Tian et Xu Yang, « Breakthrough: Chloroquine phosphate has shown apparent efficacy in treatment of COVID-19 associated pneumonia in clinical studies », BioScience Trends, vol. advpub, (DOI 10.5582/bst.2020.01047, lire en ligne, consulté le )
- « La chloroquine est-elle un bon traitement contre le coronavirus ? », sur Sciences et Avenir (consulté le )
- (en) Philippe Colson, Jean-Marc Rolain et Didier Raoult, « Chloroquine for the 2019 novel coronavirus SARS-CoV-2 », International Journal of Antimicrobial Agents, , p. 105923 (DOI 10.1016/j.ijantimicag.2020.105923, lire en ligne, consulté le )
- « Coronavirus : le professeur Raoult, spécialiste des maladies infectieuses, valide un traitement contre le Covid-19 », sur France 3 Provence-Alpes-Côte d'Azur (consulté le )
- « ”Fake news” et désinformation autour du coronavirus SARS-CoV2 », sur Salle de presse | Inserm, (consulté le )
- Pauline Moullot, « La chloroquine, un médicament contre le paludisme, est-elle efficace contre le Covid-19 ? », sur Libération.fr, (consulté le ).
- (en) Haibo Zhang et all, « Angiotensin-converting enzyme 2 (ACE2) as a SARS-CoV-2 receptor: molecular mechanisms and potential therapeutic target », SpringerLink, (lire en ligne)
- (en) « ESR Connect with Josef Penninger: ACE2 – a rational frontline therapy for COVID-19 », Youtube, (lire en ligne)
- (en) « Are patients with hypertension and diabetes mellitus at increased risk for COVID-19 infection? », Lancet, (lire en ligne)
- (en) « The Role of Angiotensin II in the Process of Atherosclerosis », Youtube, (lire en ligne)
- « DIRECT. Le gouvernement américain tente de développer un vaccin contre le coronavirus 2019-nCoV », sur Franceinfo, (consulté le ).
- « Coronavirus : « La France travaille à un vaccin » », La Croix, (ISSN 0242-6056, lire en ligne, consulté le )
- Pierre Sautreuil, « Coronavirus : mais au fait, c'était quoi le Sras ? », sur Le Figaro.fr, (consulté le )
- « COVID-19 : S’inspirer du SRAS pour développer le vaccin », sur santé log, (consulté le )
- (en) Xiaolong Tian, Cheng Li, Ailing Huang et Shuai Xia, « Potent binding of 2019 novel coronavirus spike protein by a SARS coronavirus-specific human monoclonal antibody », bioRxiv, Microbiology, (DOI 10.1101/2020.01.28.923011, lire en ligne, consulté le )
- (en) « Coronavirus: 'Significant breakthrough' in race for vaccine made by UK scientists », sur Sky News (consulté le )
- (en) « Imperial researchers in race to develop a coronavirus vaccine | Imperial News | Imperial College London », sur Imperial News (consulté le )
- Le Figaro avec Reuters, « Coronavirus: un vaccin en cours d'élaboration en Russie », sur Le Figaro.fr, (consulté le ).
- (en) « Coronavirus 'may become global emergency' as 18 deaths confirmed », sur Sky News (consulté le ).
- (en-GB) Haroon Siddique (now), Ben Quinn, Stephanie Convery (earlier) et Libby Brooks, « China coronavirus: 14 test negative in UK as military doctors sent to Wuhan – as it happened », The Guardian, (ISSN 0261-3077, lire en ligne, consulté le ).
- « Coronavirus : « La France travaille à un vaccin » », La Croix, (ISSN 0242-6056, lire en ligne, consulté le ).
- (de) « Gesundheitssenatorin begrüßt Ausweitung des Risikogebiets durch Robert-Koch-Institut », sur www.berlin.de, (consulté le )
- (en) Lin Li, Ting Sun, Yufei He et Wendong Li, « Epitope-based peptide vaccine design and target site characterization against novel coronavirus disease caused by SARS-CoV-2 », bioRxiv, , p. 2020.02.25.965434 (DOI 10.1101/2020.02.25.965434, lire en ligne, consulté le )
- (en-GB) « Vir Biotechnology discovers two antibodies against new coronavirus » (consulté le )
- (en) Anurodh Shankar Agrawal, Tianlei Ying, Xinrong Tao et Tania Garron, « Passive Transfer of A Germline-like Neutralizing Human Monoclonal Antibody Protects Transgenic Mice Against Lethal Middle East Respiratory Syndrome Coronavirus Infection », Scientific Reports, vol. 6, no 1, , p. 1–8 (ISSN 2045-2322, DOI 10.1038/srep31629, lire en ligne, consulté le )
- (en) Jia Liu, Xin Zheng, Qiaoxia Tong et Wei Li, « Overlapping and discrete aspects of the pathology and pathogenesis of the emerging human pathogenic coronaviruses SARS-CoV, MERS-CoV, and 2019-nCoV », Journal of Medical Virology, (ISSN 1096-9071, DOI 10.1002/jmv.25709, lire en ligne, consulté le )
- (en) « People can get the coronavirus more than once, experts warn — recovering does not necessarily make you immune », sur Business Insider France (consulté le )
- (en) Lan Lan, Dan Xu, Guangming Ye et Chen Xia, « Positive RT-PCR Test Results in Patients Recovered From COVID-19 », JAMA, (DOI 10.1001/jama.2020.2783, lire en ligne, consulté le )
- (en) « A multicenter, randomized controlled trial for the efficacy and safety of tocilizumab in the treatment of new coronavirus pneumonia (COVID-19) », Chinese Clinical Trial Registry, (lire en ligne)
- « Treating coronavirus: How blood plasma from recovered patients may help », sur statnews.com, (consulté le )
- Hugo Mouquet, « Ingénierie de lymphocytes B humains produisant des anticorps neutralisant le virus VIH-1 par édition génique CRISPR-Cas9 », huffingtonpost, (lire en ligne)
- (en) « Antigen-specific humoral immune responses by CRISPR/Cas9-edited B cells », biorxiv, (lire en ligne)
- (en) « CRISPR/Cas9-Based Antiviral Strategy: Current Status and the Potential Challenge », Nbci, (lire en ligne)
Voir aussi
Bibliographie
- Wang Y, Wang Y, Chen Y & Qin Q (2020) Unique epidemiological and clinical features of the emerging 2019 novel coronavirus pneumonia (COVID-19) implicate special control measures ; J Med Virol. 5 mars 2020 ; Epub 2020 Mar 5 (résumé).
Articles connexes
- Pandémie de maladie à coronavirus de 2019-2020
- Maladie à coronavirus 2019
- Syndrome respiratoire aigu sévère lié au coronavirus
- Coronavirus du syndrome respiratoire du Moyen-Orient
- Enzyme de conversion de l'angiotensine 2 (ACE2), porte d'entrée du virus
Liens externes
- CDC chinois (Chinese Center for Disease Control and Prevention)
- Institut de Biologie des Agents pathogènes (Institute of Pathogen Biology)
- Carte de l'épidémie actualisée en temps réel par le Center for Systems Science and Engineering de la Johns Hopkins University de Baltimore
- (en-US) Gardner L., « Mapping the Wuhan Coronavirus (2019-nCoV) », sur systems.jhu.edu, (consulté le )
- Questions fréquentes sur les nouveaux coronavirus et Rapports quotidiens de situation sur le nouveau Coronavirus (2019-nCoV) [en anglais] par l'Organisation Mondiale de la Santé
- Fiche-maladie régulièrement actualisée par l'Institut Pasteur
- « Coronavirus 2019-nCoV : le point sur la situation en France et dans le monde », sur le site du Dictionnaire Vidal (consulté le ).
- "Analyses bioinformatiques du coronavirus 2019-nCoV : pourquoi et comment ?", article rédigé par deux bioinformaticiens sur bioinfo-fr.net, 05 février 2020