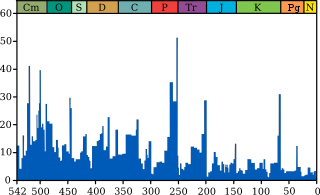
Extinction Crétacé-Paléogène
Le graphique bleu indique le pourcentage apparent (pas en nombre absolu) de genres d'animaux marins ayant disparu au cours d'un intervalle de temps. Il ne représente pas toutes les espèces marines, mais seulement les espèces marines fossiles. Les 5 plus grandes extinctions sont liées, voir les extinctions massives pour plus de détails.


L'extinction Crétacé-Paléogène ou extinction K-Pg[a], antérieurement dénommée extinction Crétacé-Tertiaire[b] ou extinction K-T[c], est une extinction massive et à grande échelle d'espèces animales et végétales qui s'est produite sur une courte période de temps (à l'échelle géologique) il y a 66 millions d'années[d],[2]. Notamment, cette extinction inclut la disparition des dinosaures non aviens.
Le remplacement abrupt des faunes et des flores, que l'on retrouve dans toutes les régions du monde, a historiquement servi à délimiter l'Ère secondaire (aujourd'hui dénommée Mésozoïque) de l'Ère tertiaire (aujourd'hui regroupée avec l'ancienne Ère quaternaire au sein du Cénozoïque[e]). Sur le terrain, la frontière entre les deux ensembles est appelée « limite Crétacé-Paléogène ou limite K-Pg » (antérieurement « limite Crétacé-Tertiaire » ou « limite K-T »), le Crétacé étant la dernière période du Mésozoïque et le Paléogène la première du Cénozoïque. La limite K-Pg est fréquemment marquée par une mince couche d'argile présentant un taux anormalement élevé d'iridium, que l'on retrouve dans diverses régions du monde. L'hypothèse principale est que la chute de l'astéroïde à l'origine du cratère de Chicxulub a été l'événement déclencheur de l'extinction K-Pg.
Premières hypothèses[modifier | modifier le code]
Dinosaures et mammifères[modifier | modifier le code]
La majorité des paléontologues admettent que les oiseaux appartiennent au groupe des dinosaures ; les autres dinosaures sont dits non aviens[3].
Les fossiles de dinosaures non aviens se trouvant presque uniquement au-dessous de la limite K-Pg, les paléontologues estiment majoritairement que ces dinosaures se sont éteints juste avant, ou pendant l'événement. Dans cette interprétation, le fait que quelques fossiles de dinosaures non aviens aient été découverts au-dessus de la limite K-Pg est entièrement dû à des remaniements des sédiments, c'est-à-dire que l'érosion les a ramenés à la surface avant qu'ils ne soient recouverts par un dépôt de sédiments plus récents[4],[5],[6]. Cette théorie pourra être vérifiée, puisque des systèmes de datation, utilisés depuis le début des années 2010, permettent de dater directement les ossements, contrairement aux méthodes antérieures qui ne dataient que les sédiments qui les entourent[7].
Les mosasaures, les plésiosaures, les ptérosaures et de nombreuses espèces de plantes et d'invertébrés se sont également éteints.
Les clades de mammifères et d'oiseaux ont survécu avec peu d'extinctions, et une radiation évolutive des taxons du Maastrichtien s'est produite bien après la limite. Le taux d'extinction et de radiation varie d'un clade à l'autre[8].
L'Australie, l'Amérique du Sud et Madagascar, isolées des autres continents à l'époque de l'événement, ont développé au Cénozoïque des faunes de mammifères distinctes.
Entre impact cosmique et volcanisme[modifier | modifier le code]
Les théories scientifiques expliquent les extinctions K-Pg par un ou plusieurs événements catastrophiques, tels que des impacts massifs d'astéroïdes, ou une activité volcanique accrue, l'activité volcanique semblant cependant être antérieure. La datation de plusieurs cratères d'impact (comme l'impact de Chicxulub) et celle des roches issues d'une activité volcanique massive dans les trapps du Deccan coïncident avec la période approximative de l'événement d'extinction. Ces événements géologiques auraient réduit la quantité de lumière solaire arrivant au sol, limitant ainsi la photosynthèse et menant à un changement massif de l'écologie terrestre.
D'autres chercheurs avancent que l'extinction a été plus progressive, résultant de changements plus lents du niveau de la mer ou du climat[8].
Toutefois, les paléobotanistes, notamment les palynologues étudiant le pollen, semblent avoir montré au niveau de la limite K-Pg, et plus particulièrement sur les sites nord-américains, que l'extinction a été rapide et cohérente avec l'hypothèse d'un impact : disparition quasi instantanée du pollen d'angiospermes dominant au Maastrichien, fern spike (« pic des fougères »)[9] coïncidant avec le pic d'iridium, végétation opportuniste (fougères le plus souvent) puis réapparition progressive de gymnospermes puis d'angiospermes, et reconstitution progressive de la biodiversité[10],[11],[12].
En mars 2010, un groupe de 41 scientifiques s'est accordé, dans la revue Science, sur le fait que la chute de l'astéroïde à l'origine du cratère de Chicxulub a été l'événement déclencheur de l'extinction K-Pg[13].
Mais, quatre ans plus tard, la même revue relance le débat en publiant une nouvelle étude géochronologique, laquelle permet une datation plus précise de l'événement du plateau du Deccan, remettant en question l'idée que les gigantesques effusions de lave du Deccan auraient eu lieu trop tôt pour avoir joué un rôle dans les extinctions. L'étude montre que ce phénomène chevauche bien la période géologique d'extinctions majeures et redonne de la crédibilité à l'hypothèse soutenue par Gerta Keller (paléontologue de l'Université de Princeton) attribuant l'extinction au volcanisme du Deccan[f],[14],[15]. Lors de cet épisode volcanique, parmi les plus destructeurs de toute l'histoire de la Terre, les volcans auraient pu éjecter dans l'atmosphère assez de dioxyde de carbone et de soufre pour brutalement réchauffer la Terre et acidifier ses océans, en tuant les trois quarts des formes terrestres de vie, dont tous les dinosaures non aviens.
Coïncidence entre météorite et volcanisme[modifier | modifier le code]
En octobre 2015, une datation encore plus précise des coulées de lave des trapps du Deccan, basée sur le rapport isotopique 40Ar/39Ar de l'argon, est obtenue par l'équipe de Paul R. Renne[16] de l'université de Californie à Berkeley. Les épisodes les plus importants et les plus continus d'émissions de laves du Deccan, représentant 70 % du total, sont datés de moins de 50 000 ans après la chute de la météorite de Chicxulub.
Cette coïncidence convainc les auteurs que l'épisode paroxysmal des trapps serait une conséquence de l'impact de la météorite de Chicxulub[16]. Le choc de la météorite aurait induit une onde sismique énorme, équivalent d'un tremblement de terre de magnitude 11, qui aurait fragilisé la croûte terrestre de l'autre côté du globe, aux « antipodes » en longitude, mais pas en latitude.
Ainsi, après l'extinction massive due à l'impact de la météorite de Chicxulub, les éruptions volcaniques du Deccan, avec leurs quantités énormes de gaz létaux expulsées — dont le sulfure d'hydrogène (H2S) —, auraient prolongé les effets du nuage soulevé par l'impact météoritique[16],[17].
En avril 2019, une découverte majeure de fossiles dans le Dakota du Nord, datant du moment même de l'impact météoritique, permet de préciser les scénarios d'extinction correspondants[18].
Schémas d'extinction[modifier | modifier le code]
Bien que l'événement de la limite K-Pg ait été de grande ampleur, il y a eu une variabilité significative du taux d'extinction entre les différents groupes d'espèces. On suppose que des particules atmosphériques ont bloqué la lumière du Soleil, réduisant la quantité d'énergie solaire pouvant atteindre la Terre. Les effectifs des espèces dépendant de la photosynthèse ont donc diminué, certaines espèces se sont même éteintes.
Vers la fin du Crétacé, les organismes qui photosynthétisent, dont le phytoplancton et les plantes terrestres, étaient comme de nos jours à la base de la chaîne alimentaire. L'extinction d'espèces végétales alors dominantes a causé un remaniement important de ce groupe d'organismes[19]. L'observation suggère que les animaux herbivores se sont éteints quand les plantes dont ils dépendaient pour se nourrir sont devenues rares. En conséquence, les prédateurs supérieurs comme le Tyrannosaure ont également péri.
Les coccolithophorides (des algues unicellulaires microscopiques) et les mollusques, incluant les ammonites, les rudistes, les escargots d'eau douce et les moules, ainsi que les organismes dont la chaîne alimentaire inclut ces animaux à coquilles, se sont éteints ou ont connu de lourdes pertes.
Par exemple, on pense que les ammonites étaient la nourriture principale des mosasaures, un groupe de reptiles marins géants qui se sont éteints précisément à cette période[20].
Les omnivores, les insectivores et les charognards ont survécu à l'extinction, peut-être en raison de la plus grande disponibilité de leurs sources de nourriture. À la fin du Crétacé, il ne semble y avoir eu aucun mammifère purement herbivore ou purement carnivore. Les mammifères et les oiseaux qui ont survécu à l'extinction se sont nourris d'insectes, de vers et d'escargots, qui eux-mêmes se nourrissaient de matière morte végétale ou animale. Les scientifiques pensent que ces organismes ont survécu à l'effondrement des chaînes alimentaires basées sur les plantes parce qu'ils se sont nourris de détritus ou d'autres matériaux organiques non vivants[8],[21],[22].
Dans les cours d'eau, peu de groupes d'animaux se sont éteints, parce que ces organismes dépendent moins directement des plantes vivantes pour leur nourriture, et plus des détritus qui ruissellent de la terre, ce qui les a protégés de l'extinction[23]. Des mécanismes semblables mais plus complexes ont été observés dans les océans.
Les extinctions ont été plus nombreuses parmi des animaux vivant dans la zone pélagique que parmi ceux des fonds sous-marins. Les animaux de la zone pélagique dépendent presque entièrement de la production primaire du phytoplancton vivant, alors que des animaux vivant dans les fonds marins s'alimentent de détritus au moins en partie voire entièrement[8].
Les plus grands survivants aérobies de l'événement, les crocodiliens et les champsosaures, étaient semi-aquatiques et ont eu accès aux détritus. Les crocodiliens modernes peuvent vivre comme charognards et survivre pendant des mois sans nourriture. En outre, dans leur jeunesse, ils se développent lentement et se nourrissent pendant leurs premières années en grande partie d'invertébrés et d'organismes morts ou de fragments d'organismes. Ces caractéristiques ont permis la survie de ces espèces à la fin du Crétacé[21].
Après l'événement K-Pg, la biodiversité a eu besoin d'un temps substantiel pour récupérer, en dépit de l'existence de nombreuses niches écologiques[8].
Microbiota[modifier | modifier le code]
La limite K-Pg est associée à un taux de disparition et d'apparition d'espèces particulièrement élevé. Ce phénomène a notamment touché les nanoplanctons à l'origine des dépôts calcaires du Crétacé. De nombreuses espèces disparues ont été remplacées par de nouvelles[24],[25]. L'analyse statistique des disparitions des espèces marines suggère que la diminution de la diversité a davantage été provoquée par une forte hausse des extinctions, plutôt que par une diminution de l'apparition de nouvelles espèces par spéciation[26].
Les données concernant les phytoplanctons appelés dinophytes ne sont pas aussi bien expliquées durant cette période de transition du Crétacé au Paléogène[1], principalement parce que seuls les kystes fournissent de bonnes traces fossiles dans ce groupe, or les espèces de dinophytes ne passent pas toutes par le stade de kyste, ce qui est probablement à l'origine d'une sous-estimation de leur diversité[8]. Les études récentes tendent à indiquer qu'il n'y aurait pas eu de variations significatives des dinophytes au niveau des couches de dépôts fossiles qui constituent la limite entre Crétacé et Tertiaire[27].
Des traces géologiques de radiolaires existent depuis la période cambrienne[28], et leurs squelettes siliceux fossiles peuvent être facilement repérés et suivis au cours de la limite K-Pg. Il n'y a aucune preuve d'extinction de masse de ces organismes, et en raison du refroidissement des températures au début du Paléocène, on note une productivité élevée pour ces espèces au niveau des latitudes élevées de l'hémisphère sud[8]. En ce qui concerne les diatomées, environ 46 % des espèces ont survécu à la transition Crétacé-Paléocène, ce qui suggère un taux de renouvellement significatif des espèces, mais pas une extinction catastrophique au passage de la limite K-Pg[8],[29].
La présence des foraminifères planctoniques au passage de la limite K-Pg a été étudiée dès les années 1930[30],[31]. Ces recherches, stimulées par la possibilité d'un impact cosmique, produisirent de nombreuses publications détaillant leur extinction au cours de cette période de transition[8]. Cependant, des discussions sont en cours entre ceux qui croient que les données fossiles indiquent une extinction substantielle[32] et ceux qui pensent que les données fossiles montrent de multiples extinctions et apparitions d'espèces au passage de cette limite[33],[34]. Parmi ces espèces, les espèces benthiques, c'est-à-dire celles des fonds marins, semblent toutes s'éteindre.
Les chercheurs pensent que la biomasse des océans a diminué après les extinctions qui ont eu lieu sur les côtes et que ces foraminifères dépendaient des débris organiques pour leur alimentation. Lorsque plus tard le nombre d'espèces de micro-organismes marins a réaugmenté, on observe une augmentation concomitante du nombre d'espèces de foraminifères benthiques, vraisemblablement en raison de l'augmentation des ressources alimentaires[8]. Autrement dit, le rétablissement des populations de phytoplancton, au début du Paléocène, a fourni la source de nourriture nécessaire pour alimenter de nouveau de grandes populations de foraminifères benthiques, qui se nourrissent toujours principalement de détritus.
Au début du Paléocène, le rétablissement final de ces populations benthiques s'est réalisé en plusieurs étapes, qui ont duré plusieurs centaines de milliers d'années[35],[36].
Invertébrés marins[modifier | modifier le code]

Il y a une grande variabilité en ce qui concerne les taux d'extinction des invertébrés marins au passage de la limite K-Pg. Le nombre de fossiles et de sites fossilifères connus est faible, de ce fait les taux d'extinction calculés à partir des données récoltées peuvent ne pas correspondre à la réalité, les surestimant[8].
Les ostracodes, une classe de petits crustacés qui étaient très communs lors du Maastrichtien supérieur, ont laissé des traces fossiles dans un grand nombre d'endroits. Un examen de ces fossiles prouve que la diversité des ostracodes est plus faible au cours du Paléocène qu'à n'importe quelle autre période du Tertiaire. Cependant, dans l'état actuel de la recherche, on ne peut pas déterminer si ces extinctions se sont produites avant ou pendant l'intervalle de la limite[37],[38].
Chez les coraux du Crétacé tardif, environ 60 % des genres appartenant à l'ordre des Scleractinia (coraux durs) n'ont pas réussi à passer la limite K-Pg et à atteindre le Paléocène. L'analyse approfondie des extinctions de coraux de cette époque montre qu'environ 98 % des espèces coloniales qui habitaient les eaux tropicales chaudes et peu profondes se sont éteintes. Les coraux solitaires, qui ne forment généralement pas de récifs et habitent des régions plus froides et plus profondes de l'océan (au-dessous de la zone photique) ont moins été affectés par la limite K-Pg. Les espèces des colonies coralliennes dépendent d'une symbiose avec des algues photosynthétiques, dont les populations se sont effondrées en raison des événements entourant la limite K-Pg[39],[40],[41]. Cependant, l'explication de l'extinction K-Pg et du rétablissement au Paléocène par l'utilisation des données des fossiles de coraux doit être relativisée en raison des changements qui se sont produits dans les écosystèmes de coraux au passage de la limite K-Pg[8].
Les nombres de genres de céphalopodes, d'échinodermes et de bivalves ont diminué significativement après la limite K-Pg[8]. La plupart des espèces de brachiopodes, un petit phylum d'invertébrés marins, ont survécu à l'événement K-Pg et se sont diversifiés au début du Paléocène.

Mis à part la sous-classe des Nautiloidea, représentée aujourd'hui par les espèces des nautiles et un groupe issu d'une évolution de ceux-ci, à savoir les Coleoidea qui regroupe entre autres les octopodes, les calmars et les seiches, toutes les autres espèces de mollusques de la classe des céphalopodes se sont éteintes à la limite K-Pg. Parmi celles-ci, il y avait les espèces du super-ordre des Belemnoidea et les ammonites, une sous-classe de céphalopodes à coquille univalve, très diversifiés, dont les spécimens étaient nombreux, et à la répartition large. Des études scientifiques réalisées sur le sujet ont précisé que la stratégie reproductrice des nautiloïdes survivants, qui s'appuyait sur des œufs moins nombreux et plus gros, a joué un rôle dans leur conservation par rapport aux ammonites au cours de l'extinction. Les ammonites, elles, utilisaient d'une stratégie planctonique, c'est-à-dire que les œufs et larves étaient aussi nombreux que petits, ce qui aurait été très défavorable. Des chercheurs ont montré qu'à la suite de la disparition des ammonites, les nautiloïdes ont connu une radiation évolutive avec des formes et des complexités de coquille qui n'avaient été auparavant observées que chez les ammonites[42],[43].
Environ 35 % des genres d'échinodermes se sont éteints à la limite K-Pg, ce qui est peu car ce sont les taxons qui prospéraient à la fin du Crétacé dans les eaux peu profondes, à faible latitude, qui ont eu le taux d'extinction le plus élevé. Au niveau des latitudes moyennes, les échinodermes d'eaux profondes ont été beaucoup moins affectés par l'extinction. Ce serait une perte d'habitat qui serait responsable de ces extinctions, spécifiquement la submersion des récifs d'eau peu profonde existant à ce moment-là, lors d'un épisode transgressif survenu à une période proche de celle de l'extinction[44].
D'autres groupes invertébrés marins, notamment des bivalves comme les rudistes et les inocérames, se sont également éteints à la limite K-Pg[45],[46].
Vertébrés marins[modifier | modifier le code]
Un nombre substantiel de fossiles de poissons ont été découverts. Cela fournit de bonnes bases pour comprendre les modèles d'extinction de ces classes de vertébrés marins. Parmi les Chondrichthyes, approximativement 80 % des familles de requins, de raies et autres poissons cartilagineux ont survécu à l'événement d'extinction[8]. Par ailleurs, moins de 10 % des familles de poissons osseux, c'est-à-dire les téléostéens, se sont éteintes[47]. Toutefois, sur l'île Seymour, située au large de la péninsule Antarctique, un site fossile daté de la période précédant immédiatement l'événement présente des preuves d'une mort massive chez des poissons osseux. On spécule que les poissons ont subi un stress environnemental avant l'événement de la limite K-Pg et que ce dernier a dû précipiter l'extinction de masse[48]. Cependant, il semble que les environnements marins et d'eau douce ont atténué l'effet de l'extinction sur les poissons[49].
Invertébrés terrestres[modifier | modifier le code]
Les dommages causés par les insectes sur les feuilles fossilisées de plantes à fleurs de quatorze emplacements en Amérique du Nord ont été employés comme indicateur de la diversité des insectes à travers la limite K-Pg et analysés pour déterminer le taux d'extinction. Les chercheurs ont constaté que les sites du Crétacé, avant l'événement d'extinction, avaient une grande richesse en plantes et diverses formes d'alimentation par les insectes. Cependant, au début du Paléocène, la flore était relativement diverse avec peu de prédation des insectes, même 1,7 million d'années après le phénomène d'extinction[50],[51].
Plantes terrestres[modifier | modifier le code]
Il existe des preuves dominantes d'une rupture globale des groupes de plantes à la limite K-Pg[52]. Cependant, il y a eu d'importantes disparités selon les régions observées dans la succession des plantes. En Amérique du Nord, les données suggèrent une dévastation massive des plantes dans les sections de limite K-Pg, bien qu'il y ait aussi eu des changements mégafloraux substantiels avant la limite[53].
Dans les latitudes élevées de l'hémisphère sud, comme la Nouvelle-Zélande et l'Antarctique, la décroissance de masse de la flore n'a causé aucun renouvellement significatif dans les espèces, mais des changements dramatiques à court terme dans l'abondance relative des groupes de plantes[50],[54]. En Amérique du Nord, approximativement 57 % des plantes se sont éteintes. Le redressement des plantes au Paléocène a commencé par des recolonisations dominées par les fougères qui présentent alors un net pic d'abondance d'espèces illustré par les données géologiques ; on a d'ailleurs observé ce même type de recolonisation de fougères après l'éruption du mont Saint Helens en 1980[55].
En raison de la destruction en masse des plantes à la limite K-Pg, il y a eu prolifération des organismes détritivores comme les mycètes qui n'ont pas besoin de photosynthèse et utilisent les nutriments de la végétation en décomposition. La domination des espèces fongiques (« pic fongique[g] ») a duré seulement quelques années tandis que l'atmosphère se dégageait et qu'il y avait abondance de matière organique. Une fois l'atmosphère dégagée, les organismes photosynthétiques comme les fougères et d'autres plantes sont revenues[56]. La polyploïdie semble avoir augmenté la capacité des plantes à fleur à survivre à l'extinction, probablement parce que les copies additionnelles du génome que ces plantes possédaient leur ont permis de s'adapter plus facilement aux conditions environnementales en pleine mutation qui ont suivi l'impact[57].
Il n'y a aucune trace d'extinctions de masse d'amphibiens à la limite K-Pg, et il y a une preuve irréfutable que la plupart des amphibiens ont survécu à l'événement relativement indemnes[8]. Plusieurs études approfondies des genres de salamandres dans les lits fossiles du Montana montrent que sur sept genres, six étaient inchangés après l'événement[58].
Les espèces de grenouilles semblent avoir survécu jusqu'au Paléocène avec peu d'extinction d'espèces. Cependant, les fossiles pour des familles et des genres de grenouille sont irréguliers[8]. Une étude approfondie de trois genres de grenouilles du Montana montrent qu'elles n'étaient pas changées par l'événement K-Pg et qu'elles ont survécu apparemment sans changement[58]. Les données montrent peu ou pas de preuve d'extinction de familles amphibies qui encadrent l'événement K-Pg. La survie amphibie a résulté de la capacité du clade à se réfugier dans l'eau ou à construire des terriers en sédiments, sol, bois, ou sous des roches[49].
Reptiles non archosauriens[modifier | modifier le code]

Les deux taxa de reptiles non archosauriens vivants, les testudines (tortues) et lépidosauriens (serpents, lézards et lézards verts), ainsi que les choristodères (des archosauromorphes semi-aquatiques qui se sont éteints au début du Miocène) ont survécu au passage de la limite K-Pg[8]. Plus de 80 % des espèces de tortues du Crétacé ont traversé la limite K-Pg. De plus, les six familles de tortues qui existaient à la fin du Crétacé ont survécu au Tertiaire et sont représentées par des espèces actuelles[59].
Les lépidosauriens vivants incluent les rhynchocéphales et les squamates. Les Rhynchocephalia, qui regroupent aujourd'hui les seuls Tuataras, étaient un groupe répandu et relativement prospère de lépidosauriens au début du Mésozoïque, mais qui ont commencé à diminuer à partir du milieu du Crétacé. Ils sont représentés aujourd'hui par un genre unique localisé exclusivement en Nouvelle-Zélande[60].
L'ordre des squamates, qui est représenté aujourd'hui par les lézards, les serpents et les amphisbènes, a rayonné dans diverses niches écologiques pendant le Jurassique et a réussi à passer au travers du Crétacé. Ils ont survécu au passage de la limite K-Pg et sont actuellement le groupe le plus prospère et le plus diversifié de reptiles vivants avec plus de 6 000 espèces existantes. Aucune famille connue des squamates terrestres ne s'est éteinte à la limite, et les fossiles indiquent qu'ils n'ont souffert d'aucun déclin significatif dans leurs effectifs. Leur petite taille, leur métabolisme adaptable, et leur capacité à changer d'habitat pour trouver des conditions plus favorables ont été des facteurs clefs dans leur survie pendant la fin du Crétacé et le début du Paléocène[8],[59].
Les reptiles marins non archosauriens comprenant les mosasaures et les plésiosaures, les reptiles aquatiques géants qui étaient les prédateurs marins supérieurs, se sont éteints vers la fin du Crétacé.
Archosauriens[modifier | modifier le code]
Le clade des archosauriens inclut deux ordres vivants : les crocodiliens (dont les Alligatoridae, les Crocodylidae et les Gavialidae sont les seules familles survivantes) et les oiseaux ; alors que les dinosaures non aviens et les ptérosaures sont éteints.
Crocodiliens[modifier | modifier le code]
Dix familles des crocodiliens ou de leurs proches parents sont déjà représentées dans les fossiles du Maastrichtien. Alors que cinq se sont éteintes avant la limite K-Pg[61], cinq autres familles ont des représentants fossiles jusqu'au Paléocène.
Toutes les familles de crocodiliens survivantes habitaient des environnements d'eau douce et terrestres, excepté les Dyrosauridae à la fois marins et dulçaquicoles. La seule tendance apparente étant qu'aucun des grands crocodiles, tel que le crocodile nord-américain géant Deinosuchus, ne survécurent[8]. La survie des crocodiliens à ces événements a pu simplement résulter de la persistance de leur niche aquatique et de leur capacité à creuser, qui a réduit leur susceptibilité aux effets négatifs sur l'environnement de la limite K-Pg[49].
En 2008, Stéphane Jouve et ses collègues ont suggéré que les juvéniles de Dyrosauridae auraient vécu dans l'eau douce comme les juvéniles des crocodiles marins modernes, ce qui les aurait aidés à survivre là où d'autres reptiles marins se sont éteints ; les environnements d'eau douce n'ayant pas été aussi fortement affectés par des événements K-Pg que les environnements marins[62].
Ptérosauriens[modifier | modifier le code]

La seule famille de ptérosauriens dont la présence au Maastrichtien (entre 72,1 ± 0,2 et 66,0 Ma) est certaine, les Azhdarchidae, s'est éteinte à la limite K-Pg. Ces grands ptérosauriens étaient les derniers représentants d'un groupe en déclin qui comprenait dix familles durant le Crétacé moyen. Les ptérosauriens de plus petite taille s'étaient éteints avant le Maastrichtien au cours d'une période qui avait vu le déclin des espèces animales de petite taille au profit des espèces de grande taille. Simultanément, les oiseaux modernes avaient connu une forte diversification et avaient remplacé des oiseaux archaïques et des groupes de ptérosauriens, probablement en raison de la concurrence directe, ou simplement en remplissant des niches vides[49],[63],[64].
Oiseaux[modifier | modifier le code]
La plupart des paléontologues considèrent les oiseaux comme les seuls survivants des dinosaures. Cependant, tous les oiseaux non néornithes se sont éteints, y compris des groupes florissants comme les enantiornithines et les hesperornithiformes[65]. Plusieurs analyses de fossiles d'oiseaux montrent une divergence d'espèces avant la limite K-Pg, et que des parents du canard, du poulet et des autruches ont coexisté avec les dinosaures[66]. Les oiseaux néornithes ont survécu à la limite K-Pg peut-être en raison de leurs capacités de plonger, nager, ou chercher un abri dans l'eau et les marécages. Beaucoup d'espèces d'oiseaux peuvent construire des terriers, ou des nids dans les trous d'arbre ou les termitières, ce qui les a mis à l'abri des effets sur l'environnement à la limite K-Pg[49]. Une autre hypothèse est que leur survie serait due à leur régime alimentaire à base de graines, l'une des rares ressources en nourriture disponibles alors[67]. La survie à long terme après la limite a été garantie par la possibilité de remplir les nombreuses niches écologiques laissées vides par l'extinction des dinosaures non aviens[49].
Dinosaures non aviens[modifier | modifier le code]

L'extinction des dinosaures au passage de la limite K-Pg a donné lieu à plus de publications que n'importe quel autre groupe d'organismes. À l'exception de quelques revendications controversées, on convient que tous les dinosaures non aviens de l'époque se sont éteints à la limite K-Pg. Les fossiles de dinosaures ont été interprétés à la fois pour montrer un déclin dans la diversité et aucun déclin dans la diversité pendant les derniers millions d'années du Crétacé, et il se peut que la qualité des fossiles de dinosaures ne soit simplement pas assez bonne pour permettre à des chercheurs de distinguer les choix[68]. Puisqu'il n'y a aucune preuve que les dinosaures de la fin du Maastrichtien aient pu creuser, nager ou plonger, ils ne pouvaient pas s'abriter pendant les plus mauvais moments du stress environnemental qui se sont produits à la limite K-Pg. Il est possible que les petits dinosaures non aviens aient survécu, mais ils auraient été privés de nourriture car des dinosaures herbivores auraient trouvé la matière végétale rare, et les carnivores se seraient rapidement trouvés à court de proies[49]. Le consensus croissant au sujet du caractère endotherme des dinosaures (voir Physiologie des dinosaures) aide à comprendre leur extinction complète par rapport à la survie de leurs parents proches, les crocodiliens. Les crocodiles, étant ectothermes (animaux à « sang froid »), ont des besoins très limités en nourriture (ils peuvent vivre plusieurs mois sans manger) tandis que des animaux de taille semblable mais endothermes (à « sang chaud ») ont besoin de beaucoup plus de nourriture afin de soutenir leur métabolisme plus rapide. Ainsi, dans les circonstances de la rupture de chaine alimentaire précédemment mentionnées, les dinosaures non aviens se sont éteints[19] tandis que certains crocodiles ont survécu. Dans ce contexte, la survie d'autres animaux endothermiques, tels que quelques oiseaux et mammifères, est peut-être due, entre autres raisons, à leur plus petit besoin en nourriture, de par leur petite taille à l'époque de l'extinction des dinosaures[69].
Plusieurs chercheurs pensent que l'extinction des dinosaures a été progressive, de sorte qu'il y aurait encore eu des dinosaures au Paléocène. Ces arguments se fondent sur la découverte de restes de dinosaures dans la formation de Hell Creek jusqu'à 1,3 m au-dessus et 40 000 années après la limite K-Pg[4]. Des échantillons de pollen prélevés près d'un fémur fossilisé d'hadrosaure découvert dans du grès à Ojo Alamo près de la rivière de San Juan indiquent que l'animal a vécu pendant le Tertiaire, approximativement 64,5 Ma (environ 1 million d'années après l'événement K-Pg). Si leur existence après la limite K-Pg est confirmée, ces hadrosaures doivent être considérés comme un clade « mort-vivant ». Les recherches actuelles suggèrent que ces fossiles auraient été érodés de leurs endroits originaux puis réensevelis par des sédiments très postérieurs (retouchés)[6].
Mammifères[modifier | modifier le code]

Les groupes de mammifères existant aujourd'hui étaient déjà présents au Crétacé, qu'il s'agisse des monotrèmes qui pondent des œufs, des marsupiaux ou des placentaires, mais aussi d'autres groupes disparus comme les multituberculés, Dryolestoidea (en)[71], et les Gondwanatheria[72]. Tous ont survécu à l'événement K-Pg, bien qu'ils aient enregistré des pertes. Beaucoup de marsupiaux ont disparu, en particulier ceux d'Amérique du Nord et plus particulièrement encore les espèces asiatiques regroupées dans le taxon des deltatheroïdes (en)[73]. Dans les gisements de fossiles de la formation de Hell Creek, au-dessus de la limite K/T, on ne trouve plus de trace d'au moins la moitié des dix espèces de multituberculés ni d'aucune espèce marsupiale parmi les onze présentes avant la limite[68].
Les espèces de mammifères ont commencé à se diversifier approximativement 30 millions d'années avant la limite du Crétacé et du Tertiaire. Une radiation évolutive de mammifères s'est produite dans les quelques millions d'années qui ont suivi[74]. La recherche actuelle indique que les mammifères n'ont pas eu d'explosion de diversification au passage de la limite K-Pg, en dépit des niches écologiques libérées par l'extinction des dinosaures[75]. Plusieurs ordres de mammifères ont été interprétés comme se diversifiant juste après la limite K-Pg, comme les Chiroptera (chauves-souris) et les Cetartiodactyla (un groupe divers qui inclut aujourd'hui les baleines et dauphins et les Artiodactyla)[75], mais des recherches plus récentes concluent que seuls les ordres de marsupiaux se sont diversifiés directement après la limite K-Pg[74].
Les espèces mammifères qui existaient à la limite K-Pg étaient généralement petites, de taille comparable aux rats, en grande majorité (mais pas exclusivement) insectivores nocturnes (le fait que plus de la moitié des mammifères actuels et la majorité des petits mammifères ont un mode de vie nocturne est révélateur)[76] ; cette petite taille les aurait aidées à trouver des abris dans des environnements protégés mais d'autres facteurs peuvent expliquer leur survie : capacités d'adaptation et de diversification écologique grâce à leur cerveau développé, la variété de leurs régimes alimentaires (ce qui explique l'augmentation progressive de leur taille dans les millions d'années qui ont suivi cette extinction)[77] ; homéothermie qui les protège des mycoses dues au « pic fongique »[78] ; simple contingence[79]? En outre, on postule que quelques monotrèmes, marsupiaux, et placentaires primitifs étaient semi-aquatiques ou fouisseurs, car il existe encore de nombreuses lignées de mammifères ayant conservé de tels comportements aujourd'hui. De plus, n'importe quel mammifère semi-aquatique ou creusant des terriers aurait eu la protection additionnelle contre le stress environnemental de la limite K-Pg[49].
Données paléontologiques[modifier | modifier le code]
Fossiles nord-américains[modifier | modifier le code]
Dans les dépôts géologiques d'Amérique du Nord, l'événement d'extinction est particulièrement bien représenté par la différence marquée entre le palynomorphe riche et relativement abondant du Maastrichtien supérieur par rapport à l'abondance de fougères succédant à la limite[52].
Dans l'état actuel des découvertes, les gisements de fossiles de dinosaures les plus instructifs sur la limite K-Pg se trouvent à l'ouest de l'Amérique du Nord, en particulier la Formation de Hell Creek dans le Montana, États-Unis qui date du Maastrichtien supérieur. En comparant cette formation avec celles de Judith River au Montana et de Dinosaur Park en Alberta (Canada), qui sont plus anciennes d'environ 75 Ma, on obtient des informations sur les changements dans les populations de dinosaures au cours des 10 derniers millions d'années du Crétacé. Ces gisements de fossiles sont géographiquement limités, couvrant seulement une partie d'un continent[68].
Les formations du Campanien moyen présentent une diversité de dinosaures plus grande que n'importe quelle autre couche de roches. Les roches du Maastrichtien supérieur contiennent les plus grands membres de plusieurs clades importants : Tyrannosaurus, Ankylosaurus, Pachycephalosaurus, Triceratops et Torosaurus[80], ce qui suggère que la nourriture était abondante immédiatement avant l'extinction.
Ces gisements sont non seulement riches en fossiles de dinosaures, mais comprennent également des fossiles de plantes qui illustrent la réduction du nombre d'espèces de plantes au passage de la limite K-Pg. Dans les sédiments au-dessous de la limite K-Pg, les grains de pollen angiosperme dominent, alors que la couche correspondant à la limite contient peu de pollen et est dominée par des spores de fougères[81]. Les niveaux normaux de pollen reprennent graduellement au-dessus de la couche limite. Cela rappelle les secteurs touchés par des éruptions volcaniques, où le rétablissement est mené par les fougères qui plus tard sont remplacées par de grandes quantités d'angiospermes[82].
En avril 2019, une étude publiée dans les PNAS[83] montre qu'une couche importante de dépôts au Dakota du Nord témoigne d'un tsunami dû à l'impact de la météorite de Chicxulub, et contient en particulier des fossiles très bien conservés de poissons et de dinosaures tués à ce moment, ce qui permet de reconstituer avec précision les circonstances exactes de l'extinction[18].
Fossiles marins[modifier | modifier le code]
L'extinction de masse du plancton marin semble avoir été brusque et correspondre exactement à la limite K-Pg[84]. Les genres d'ammonites se sont éteints exactement à la limite K-Pg ou juste après ; il faut cependant noter qu'une décroissance plus modérée et plus lente des genres d'ammonites avait commencé avant la limite en raison d'une régression des espèces marines au Crétacé supérieur. L'extinction progressive de la plupart des bivalves inocérames avait commencé bien avant la limite K-Pg et une réduction légère et progressive de la diversité des ammonites s'est produite à la fin du Crétacé supérieur[85]. Des analyses plus approfondies montrent que plusieurs processus étaient en cours dans les océans à la fin du Crétacé (certains se chevauchant temporellement en partie) et qu'ils ont pris fin brusquement avec l'extinction de masse[85].
Chronologie[modifier | modifier le code]

Dernier jour du Crétacé[modifier | modifier le code]
L'impact de Chicxulub, dans les quelques heures qui l'ont suivi, a laissé un enregistrement géologique et paléontologique dans le Dakota du Nord (États-Unis), environ 3 050 km au nord-ouest de Chicxulub. Le site de Tanis, au sein de la formation de Hell Creek, est constitué de sédiments dont la structure montre qu'ils ont été déposés rapidement et de façon turbulente et, pour l'essentiel, en direction de l'intérieur des terres de l'époque (un courant de retour a aussi été enregistré). Ces sédiments renferment des fossiles de végétaux et d'animaux marins aussi bien que continentaux, ce qui indique l'irruption d'une grande vague qui a déferlé sur le rivage. Ces sédiments sont surmontés d'une fine couche de gore blanc enrichi en iridium, classique à l'interface Crétacé-Paléogène. Le sédiment contient toute une série d'éjectas de différents types, et notamment des sphérules vitreux que l'on retrouve dans les branchies des poissons fossilisés et, inaltérés, dans de l'ambre. L'arrivée de ces éjectas n'est a priori postérieure à l'impact que d'au maximum quelques heures, compte tenu de la distance parcourue. La vague, contemporaine de l'arrivée des éjectas, n'est pas attribuée au tsunami généré par l'impact (qui ne serait arrivé que 18 h après l'impact selon les calculs, et très atténué), mais à une seiche engendrée localement par l'arrivée des ondes sismiques (6, 10 et 13 minutes après l'impact pour les ondes P, S et de Rayleigh, respectivement)[86]. Début 2022, des investigations utilisant les rayons X du synchrotron de Grenoble sur des arêtes de poissons provenant du site de Tanis ont confirmé l'hypothèse que l'impact s'était produit pendant le printemps de l'hémisphère nord[87],[88].
Durée de l'extinction[modifier | modifier le code]
La période de temps sur laquelle s'est déroulée l'extinction fait l'objet de controverses, parce que certaines théories de la cause de l'extinction exigent une extinction rapide sur une période relativement courte (de quelques années à quelques milliers d'années) tandis que d'autres nécessitent de plus longues périodes. Le problème est difficile à résoudre en raison de l'effet Signor–Lipps ; c'est-à-dire que les données fossiles ne sont que très partielles ce qui fait que la plupart des espèces qui se sont éteintes ne se sont probablement réellement éteintes que longtemps après le fossile le plus récent qui a été trouvé[89]. De plus, les scientifiques n'ont trouvé que très peu de gisements de fossiles couvrant de manière continue un intervalle de temps s'étalant de plusieurs millions d'années avant l'extinction K-Pg à quelques millions d'années après[8].
Théories[modifier | modifier le code]
Plusieurs théories expliquent la limite K-Pg et les causes de l'extinction massive[90]. À la base de ces théories figurent des impacts de météorites ou un volcanisme accru ; certaines théories intègrent les deux éléments. On a aussi proposé un scénario combinant trois causes : le volcanisme, la régression marine, et un impact cosmique. Dans ce dernier scénario, les communautés terrestres et marines auraient été perturbées par les changements dans leurs écosystèmes et par des pertes d'habitats. Les dinosaures, ainsi que les plus grands vertébrés, auraient été les premiers affectés par les changements environnementaux, en conséquence leur diversité aurait diminué. En même temps, des particules en suspension provenant du volcanisme auraient refroidi et asséché certains secteurs du globe. Puis, un impact cosmique se serait produit, ce qui aurait causé un effondrement des chaines alimentaires fondées sur la photosynthèse, affectant à la fois les chaines alimentaires terrestres déjà perturbées et les chaines alimentaires marines. La différence principale entre cette théorie et les théories reposant sur une cause unique est que ses partisans pensent qu'aucune cause unique n'est suffisante pour expliquer l'ampleur des extinctions ni pour produire le modèle taxonomique de l'extinction[68].
Théories anciennes[modifier | modifier le code]

Avant les années 1970, les causes envisagées pour la disparition des dinosaures étaient :
- l'élimination des dinosaures par la sélection naturelle ;
- la destruction des nids de dinosaures par des mammifères mangeurs d'œufs ;
- une épidémie fulgurante ;
- l'intoxication des dinosaures par les alcaloïdes contenus dans de nouvelles lignées de plantes à fleurs qui sont en extension vers la fin de l'ère secondaire, au détriment des conifères et fougères arborescentes (les dinosaures n'appréciant pas l'amertume de ces plantes et n'ayant pas un système de détoxification au niveau du foie)[91] ;
- une inversion du champ magnétique terrestre.
Ces anciennes théories sont aujourd'hui très minoritaires dans le monde scientifique, voire complètement abandonnées, car :
- l'extinction K-Pg a été planétaire ;
- un groupe qui perdure pendant 155 millions d'années peut être considéré comme solidement adapté ; de plus, leur disparition aurait été beaucoup plus progressive ;
- il est peu vraisemblable que toute une classe d'espèces ait disparu aussi rapidement et à l'échelle terrestre à la suite d'une prédation de ses nids. D'autant plus que cette disparition en masse ne touche pas que les dinosaures ;
- il est peu crédible qu'une épidémie se soit propagée à l'échelle intercontinentale, touchant autant d'espèces différentes, y compris des animaux marins ;
- les dinosaures n'étaient pas tous végétariens. De plus, une telle disparition n'aurait pas été aussi rapide ;
- des inversions du champ magnétique terrestre se sont produites maintes fois avant et après dans l'histoire géologique de la Terre, sans catastrophe de grande ampleur.
Impact cosmique[modifier | modifier le code]

À la fin des années 1970, l'exploration de certaines couches géologiques a révélé une couche d'argile de quelques centimètres d'épaisseur entre les strates du Crétacé et du Tertiaire[93]. On parle d'elle sous le nom de limite Crétacé-Paléogène, de limite CT ou de limite K-Pg. Cette limite géologique, bien visible en certains points du globe, présente un taux anormal d'iridium (30 fois et 130 fois plus élevé que la normale dans les deux sections étudiées à l'origine). L'iridium est extrêmement rare dans la croûte terrestre parce que c'est un élément sidérophile, ce qui signifie qu'il a migré avec le fer pendant la différenciation planétaire et se trouve donc principalement dans le noyau. Cet élément est donc rare sur Terre mais abondant dans certaines météorites.
En 1980, un groupe de scientifiques composé du professeur de science planétaire de l'université de Berkeley et prix Nobel de physique Luis Alvarez, de son fils le géologue Walter Alvarez et des chimistes Frank Asaro et Helen Michel a alors émis l'hypothèse de la chute d'une météorite (astéroïde ou comète) à cette période[94],[h],[95]. L'hypothèse d'un impact cosmique avait été publiée auparavant (Whiston 1696[96], Schindewolf 1955[97]), mais selon Laubenfels (en) l'hypothèse ne s'appuyait pas sur des découvertes concrètes[98].
L'impact aurait formé un large cratère d'impact au fond de la mer. La conséquence d'un tel choc aurait été qu'un nuage de poussière se serait formé et aurait entouré la Terre, ce qui aurait bloqué la lumière du Soleil sur une majeure partie du globe pour une année ou moins, et une augmentation des aérosols soufrés dans la stratosphère, menant à une réduction de 10-20 % du rayonnement solaire atteignant la surface de la Terre et empêchant ainsi la photosynthèse. Cela aurait pris au moins dix ans pour que ces aérosols se soient déposés, expliquant donc l'extinction des plantes, du phytoplancton et des organismes dépendant de ces derniers (comprenant les prédateurs aussi bien que les herbivores). Les petites créatures ayant un régime alimentaire à base de détritus ont eu de meilleures chances de survie[69],[84]. Les conséquences de la ré-entrée des éjectas dans l'atmosphère terrestre aurait causé une brève (quelques heures) mais intense augmentation du rayonnement infrarouge, tuant les organismes y étant exposés[49]. Des tempêtes de feu globales ont pu résulter de l'augmentation de chaleur et de la chute sur Terre de fragments incendiaires provenant de l'explosion. Les niveaux élevés d'oxygène pendant le Crétacé supérieur auraient maintenu une combustion intense. Le niveau de l'oxygène atmosphérique est descendu au début de la période Tertiaire. Si des feux de grande ampleur se sont produits, ils ont augmenté la teneur en CO2 de l'atmosphère et ont causé un effet de serre temporaire une fois que le nuage de poussière s'était résorbé, et ceci aurait exterminé les organismes les plus vulnérables qui avaient survécu à la période juste après l'impact[99].
L'impact a pu également avoir produit des pluies acides, selon le type de roche sur lequel l'astéroïde a frappé. Cependant, la recherche récente suggère que cet effet aurait été relativement mineur, ne durant qu'approximativement 12 ans[84]. L'acidité était neutralisée par l'environnement, et la survie des animaux vulnérables aux effets des pluies acides (comme les grenouilles) indiquent que cet effet n'a pas contribué de façon importante à l'extinction. Les théories d'un impact cosmique peuvent seulement expliquer des extinctions très rapides, puisque les nuages de poussière et les aérosols sulfurés potentiels seraient éliminés de l'atmosphère dans un temps assez court (moins de 10 ans)[100].

Des recherches ultérieures ont identifié le cratère de Chicxulub[101] enterré sous Chicxulub sur la côte du Yucatán, au Mexique, comme cratère d'impact qui était concordant avec la datation de l'hypothèse d'Alvarez. Identifié en 1990 à la suite du travail de Glen Penfield effectué en 1978, ce cratère est ovale, avec un diamètre moyen d'environ 177 km[95], soit une taille proche de celle calculée par l'équipe d'Alvarez[102]. La forme et la localisation du cratère indiquent d'autres causes de dévastation en plus du nuage de poussière. L'astéroïde a atterri dans l'océan ce qui aurait causé des tsunamis, dont les traces ont été trouvées dans plusieurs endroits dans les Caraïbes et à l'est des États-Unis – du sable marin en des endroits qui n'étaient alors pas côtiers, et des débris de végétation et des roches terrestres dans des sédiments marins datant de la période de l'impact. L'astéroïde a atterri dans un lit de gypse (sulfate de calcium), ce qui aurait produit un dégagement d'anhydride sulfureux sous forme d'aérosols. Cela aurait réduit encore plus l'intensité lumineuse du Soleil à la surface de la Terre puis aurait provoqué des pluies acides, tuant la végétation, le plancton et les organismes qui possèdent des coquilles de carbonate de calcium (les coccolithophoridés et les mollusques). En février 2008, une équipe de chercheurs a utilisé des images séismiques du cratère pour déterminer que le projectile a atteint l'eau plus profondément que ce que l'on avait supposé précédemment. Ceci aurait eu comme conséquence que les aérosols dans l'atmosphère auraient été plus riches en sulfates, augmentant la mortalité de l'impact par des changements de climat et des pluies acides[103].
La plupart des paléontologues s'accordent maintenant pour dire qu'un astéroïde a frappé la Terre il y a 65 Ma, mais il n'y a pas de consensus sur le fait que l'impact soit ou non la cause unique des extinctions[34],[104]. On a montré qu'il y a un intervalle d'environ 300 000 ans entre l'impact et l'extinction de masse[105]. En 1997, le paléontologue Sankar Chatterjee a attiré l'attention sur une structure géologique appelée cratère Shiva, qu'on suppose lié à un impact de taille plus importante (600 km), et a émis l'hypothèse d'un scénario d'impacts multiples[106].
En 2007, des chercheurs ont émis l'hypothèse que le projectile qui a tué les dinosaures il y a 65 Ma appartenait à la famille d'astéroïdes de Baptistina[107]. Le lien entre les deux événements a été mis en doute, en partie parce qu'on possède très peu d'observations de l'astéroïde ou de la famille[108]. En effet, on a récemment découvert que les astéroïdes de « 298 Baptistina » ne partagent pas la même signature chimique que la source de l'impact K-Pg. Ceci affaiblit la connexion possible entre la famille de Baptistina et le projectile de K-Pg[109].
Selon une nouvelle étude publiée le dans la revue américaine Science, la chute de la météorite au Mexique aurait bien porté un coup fatal aux dinosaures il y a 66 millions d'années. Il est estimé que l'objet impacteur mesurait près de dix kilomètres de diamètre. En utilisant des techniques de datation radiométrique de haute précision, la collision se serait produite il y a 66 038 000 ans, soit 33 000 ans avant l'extinction des dinosaures (laquelle daterait donc d'il y a 66 005 000 ans)[95].
Comme l'indique Paul Renne (en), professeur à l'université de Berkeley et principal auteur de cette étude, le faible écart temporel entre les deux événements semble indiquer que l'impact a eu un rôle important dans l'extinction des dinosaures. Cependant, il précise que « si l'impact a porté le coup fatal aux dinosaures, ça n'a probablement pas été le seul facteur », citant par exemple de fortes variations climatiques pendant le million d'années précédant leur disparition, dont de longues périodes froides, causées notamment par une série d'énormes éruptions volcaniques en Inde (voir section suivante)[95].
Ces travaux de 2013 permettent de préciser les estimations données par les précédentes études sur la date de cette extinction, déduites à partir de l'étude des fossiles. Jusqu'alors, il était en effet estimé que cet impact avait eu lieu 300 000 ans avant la disparition des dinosaures[95].
Début 2019, Mark Richards de l'Université de Berkeley annonce que des fossiles ensevelis le jour de la collision ont été découverts dans le Dakota du Nord[110],[18].
En octobre 2019, une étude des variations de la proportion des isotopes 11B du bore dans les coquilles de foraminifères marins des sédiments de plusieurs sites à travers le monde, sur un intervalle de temps d'environ 800 000 ans, entre 66,4 et 65,6 Ma (millions d'années), encadrant ainsi la date de l'impact (66,04 Ma), a montré[111] :
- l'absence de baisse progressive du pH dans les océans avant l'impact ;
- une chute rapide du pH de surface des océans liée à l'acidification de l'océan juste après l'impact ;
- un rebond assez rapide (de l'ordre de 20 000 ans) du pH à la suite de l'extinction des organismes marins calcifiants ;
- une période de transition 60 000 ans au cours de laquelle la vie marine se rétablit et le pH retrouve son niveau d'avant l'impact.
Les auteurs, Michael J. Henehan et ses collègues, en concluent que rien n'indique un rôle majeur de l'activité volcanique avant l'impact[112].
Épanchement des trapps du Deccan[modifier | modifier le code]
Des couches de lave gigantesques ont été retrouvées en Inde. Celles-ci portent le nom de Trapps du Deccan. Il peut y avoir jusqu'à 2 400 mètres d'épaisseur de basalte, et la surface actuellement couverte dépasse les 500 000 km2 (à partir d'une surface originelle sans doute supérieure à 1 500 000 km2). Avant l'an 2000, l'argument qu'il y avait un lien avec l'extinction n'était évoqué que dans l'hypothèse d'une extinction progressive, car on pensait que l'intense activité volcanique avait commencé autour de 68 Ma et avait duré plus de deux millions d'années. Plus récemment, on a déterminé que les énormes éruptions volcaniques se produisirent sur une période de 800 000 ans comprenant la limite K-Pg, et pourraient donc être responsables de l'extinction et du rétablissement biotique ralenti qui a suivi[113].
Les éruptions responsables des Trapps du Deccan pourraient avoir causé l'extinction par plusieurs mécanismes, y compris le dégagement de poussières, de cendres et d'aérosols soufrés dans l'air qui pourraient avoir bloqué la lumière du Soleil et réduit ainsi la photosynthèse pour les plantes. Selon Duncan & Pyle 1988, le volcanisme du Deccan pourrait en outre avoir eu comme conséquence des émissions de gaz carbonique qui auraient augmenté l'effet de serre déjà produit par les poussières et les aérosols présents dans l'atmosphère[114]. Mais Pope et al. 1994 montrent que pour les 8 à 13 ans suivant l'éruption, la densité importante des particules atmosphériques réduit fortement la transmission solaire, qui tombe à 10–20 % de son intensité normale ; ce qui amène des températures très froides qui compensent plus que largement l'effet de serre[115].
Dans les années où l'hypothèse des Trapps de Deccan était liée à une extinction progressive, Luis Alvarez (qui est mort en 1988) a répondu que les paléontologues se trompaient car les gisements fossiles ne constituent qu'un échantillon biaisé. Bien que cette affirmation n'ait au départ pas bien été reçue, les études intensives sur le terrain des gisements fossiles effectuées par la suite ont donné du poids à ses arguments. Ultérieurement, la plupart des paléontologues ont commencé à accepter l'idée que les extinctions de masse à la fin du Crétacé aient été au moins partiellement dues à un impact cosmique sur la Terre. Cependant, même Walter Alvarez a reconnu que d'autres changements importants sur Terre avaient eu lieu avant l'impact, tel qu'une baisse du niveau de la mer et les éruptions volcaniques massives qui ont produit les Trapps du Deccan en Inde, et ceux-ci avaient pu avoir contribué aux extinctions[116].
Impacts cosmiques multiples[modifier | modifier le code]
Plusieurs autres cratères semblent s'être également formés au moment de la limite K-Pg. Ceci suggère la possibilité d'impacts multiples presque simultanés, peut-être provenant des fragments d'un unique objet cosmique, à l'image de la collision de la comète Shoemaker-Levy 9 avec Jupiter. En plus du cratère de Chicxulub de 180 km, il y a le cratère de Boltysh en Ukraine de 24 km daté à 65,17 ± 0,64 Ma, le cratère de Silverpit de 20 km, un cratère d'impact suspecté dans la Mer du Nord daté à 60-65 Ma, et le cratère de Shiva et ses 600 km controversés. D'autres cratères pourraient s'être formés dans l'océan Téthys et avoir été effacés par des événements tectoniques comme la dérive de l'Afrique et de l'Inde vers le nord[117],[118],[119].
Régression marine[modifier | modifier le code]

Des indications claires montrent que le niveau des mers s'est abaissé à la fin du Crétacé plus qu'à n'importe quel autre moment de l'ère mésozoïque. Dans certains étages stratigraphiques du Maastrichtien de diverses régions du monde, les plus récents sont terrestres ; on trouve ensuite des rivages et les étages les plus anciens correspondent à la mer. Ces couches ne montrent pas l'inclinaison et la déformation liées à la construction de montagne, donc, l'explication la plus probable est une régression, c'est-à-dire une baisse du niveau de la mer. On n'a pas de preuve directe de la cause de cette régression, mais l'explication qui est actuellement acceptée comme la plus probable est que les rides médio-océaniques sont devenues moins actives et sont donc descendues sous leur propre poids[8],[120].
Une régression sévère aurait considérablement réduit le plateau continental, qui est le secteur le plus riche en espèces marines, et pourrait donc avoir suffi pour causer une extinction de masse marine. Cependant, les recherches concluent que ce changement aurait été insuffisant pour causer le niveau d'extinction observé chez les ammonites. La régression aurait également causé des changements climatiques, en partie en perturbant des vents et des courants océaniques et en partie en réduisant l'albédo de la Terre entrainant donc des températures globales croissantes[85].
La régression marine a également eu comme conséquence la perte des mers épicontinentales, telles que la voie maritime intérieure de l'Ouest de l'Amérique du Nord. La perte de ces mers a considérablement changé des habitats, détruisant la plaine côtière qui avait accueilli dix millions d'années plus tôt les communautés diverses qu'on trouve dans les roches de la Formation de Dinosaur Park. Une autre conséquence était une expansion des environnements d'eau douce, puisque l'écoulement continental avait de plus longues distances à parcourir avant d'atteindre les océans. Tandis que ce changement était favorable aux vertébrés d'eau douce, ceux qui préfèrent les environnements maritimes, tels que les requins, ont souffert[68].
Causes multiples[modifier | modifier le code]
Dans The Dinosauria, J. David Archibald et David E. Fastovsky ont proposé un scénario combinant les trois causes : volcanisme, régression marine et impact cosmique. Dans ce scénario, les communautés terrestres et marines auraient été perturbées par les changements de leurs écosystèmes et par des pertes d'habitat. Les dinosaures, comme les plus grands vertébrés, auraient été les premiers affectés par les changements environnementaux, et leur diversité aurait diminué. En même temps, les particules causées par le volcanisme auraient refroidi et asséché certains secteurs du globe. Puis, un impact cosmique se serait produit, causant l'effondrement des chaînes alimentaires fondées sur la photosynthèse, à la fois dans les chaînes alimentaires terrestres déjà soumises à perturbations et dans les chaînes alimentaires marines. La différence principale entre cette théorie et les théories mettant en avant une cause unique est que ses partisans pensent que les causes simples qui sont avancées soit n'avaient pas la force nécessaire pour causer les extinctions, soit n'étaient pas susceptibles de produire le profil taxonomique des extinctions[68]. La difficulté à trancher de façon définitive vient de l'impossibilité actuelle de définir un biotope sur quelques milliers ou même millions d'années de façon très précise. Seule cette précision permettrait de dire si les groupes d'espèces ont disparu en quelques jours (ce qui confirmerait définitivement la thèse de la météorite comme cause dominante), ou en quelques centaines de milliers d'années (ce qui ferait plutôt pencher pour les éruptions du Deccan, ou pour un panachage Deccan — régression marine et météorite).
Autres extinctions de masse[modifier | modifier le code]
L'extinction de masse de la fin du Crétacé n'est pas la seule enregistrée. Les scientifiques estiment en avoir repéré au moins cinq autres comme celle du Dévonien où 50 % des espèces disparurent et celle qui marque la fin du Permien où plus de 90 % des espèces animales disparurent.
Notes et références[modifier | modifier le code]
Notes[modifier | modifier le code]
- K est l'initiale du mot allemand Kreidezeit (« Crétacé »).
- L'usage du terme Tertiaire est aujourd'hui déconseillé par la Commission internationale de stratigraphie[1] .
- T est l'initiale du mot allemand Tertiär (« tertiaire »), mais c'est aussi celle du mot français Tertiaire.
- La limite Crétacé-Paléogène est datée précisément à 66,043 ± 0,043 Ma[2]. Il s'agit là de l'âge de l'impact de Chicxulub, mais la plupart des extinctions ne se sont ensuite étalées que sur quelques milliers d'années.
- Le Cénozoïque est divisé en trois périodes : le Paléogène, le Néogène et le Quaternaire.
- Keller soutient que l'impact météoritique est antérieur à l'extinction de masse et que le volcanisme du Deccan et ses conséquences environnementales en sont la cause majeure, quoique probablement exacerbées par l'impact.
- Le principal pic fongique a lieu à l'extinction Permien-Trias.
- Voir aussi l'article sur la famille d'astéroïdes « Baptistina ».
Références[modifier | modifier le code]
- [Gradstein et al. 2004] (en) Felix M. Gradstein, James G. Ogg et Alan G. Smith, A Geologic Time Scale, Cambridge (Royaume-Uni), Cambridge University Press, , 589 p. (ISBN 978-0-521-78142-8 et 0-521-78142-6, présentation en ligne).
- [Renne et al. 2013] (en) Paul R. Renne, Alan L. Deino, Frederik J. Hilgen, Klaudia F. Kuiper, Darren F. Mark, William S. Mitchell, Leah E. Morgan, Roland Mundil et Jan Smit, « Time Scales of Critical Events Around the Cretaceous-Paleogene Boundary », Science, vol. 339, no 6120, , p. 684-687 (PMID 23393261, DOI 10.1126/science.1230492, Bibcode 2013Sci...339..684R, lire en ligne [PDF] sur eps.harvard.edu, consulté en ).
- [Buffetaut 2015] Éric Buffetaut, Idées reçues sur les Dinosaures, Le Cavalier Bleu, coll. « Idées reçues », (réimpr. 2019), 158 p. (ISBN 979-1031803562, présentation en ligne).
- [Sloan et al. 1986] (en) Robert E. Sloan, J. Keith Rigby, Leigh M. Van Valen et Diane Gabriel, « Gradual dinosaur extinction and simultaneous ungulate radiation in the Hell Creek formation », Science, vol. 232, no 4750, , p. 629–633 (PMID 17781415, DOI 10.1126/science.232.4750.629).
- [Fassett et al. 2001] (en) James E. Fassett, Spencer George Lucas, Robert A. Zielinski et James R. Budahn, « Compelling new evidence for Paleocene dinosaurs in the Ojo Alamo Sandstone San Juan Basin, New Mexico and Colorado, USA », International Conference on Catastrophic Events and Mass Extinctions: Impacts and Beyond, 9-12 July 2000, Vienna, Austria, vol. 1053, , p. 45–46 (lire en ligne [PDF] sur lpi.usra.edu, consulté en ).
- [Sullivan 2003] (en) Robert M. Sullivan, « No Paleocene dinosaurs in the San Juan Basin, New Mexico » (annales de la 55e rencontre annuelle, Rocky Mountain, 7-9 mai 2003), Geological Society of America Abstracts with Programs, vol. 35, no 5, , p. 15 (lire en ligne [archive du ] [sur gsa.confex.com], consulté en ).
- Laurent Sacco, « La première datation directe d'os de dinosaure », sur futura-sciences.com, (consulté en ).
- [MacLeod et al. 1997] (en) Norman MacLeod, Peter F. Rawson, Peter L. Forey, F. T. Banner, Marcelle K. Boudagher-Fadel, Paul R. Bown, Jackie A. Burnett-Lees, Peter Chambers, Steve J. Culver, Suzan E. Evans, Charlotte H. Jeffery, Michael A. Kaminski, Alan R. Lord, Angela C. Milner, Andrew R. Milner, Noel J. Morris, E. Owen, Brian Roy Rosen, Andrew B. Smith, Paul D. Taylor, Elspeth Urquhart et Jeremy R. Young, « The Cretaceous–Tertiary biotic transition », Journal of the Geological Society of London, vol. 154, no 2, , p. 265–292 (DOI 10.1144/gsjgs.154.2.0265, lire en ligne [PDF], consulté en ).
- JM Vallée, « Spores et pollens dans l'ouest des États-Unis et en Nouvelle-Zélande », sur l'anomalie en iridium et un changement soudain dans la proportion relative des spores de fougère par rapport aux pollens d’Angiosperme, sur acces.ens-lyon.fr, École normale supérieure de Lyon Institut français de l'Éducation - ACCES, (consulté en ).
- [Wolfe & Upchurch 1986] Jack A. Wolfe et Garland R. Upchurch Jr, « Vegetation, climate and Floral Changes at the Cretaceous Tertiary Boundary », Nature, vol. 324, , p. 148-152 (DOI 10.1038/324148a0).
- [Tshudy & Tshudy 1986] Robert H. Tshudy et Bernadine D. Tshudy, « Extinction and Survival of Plant Life following the Cretaceous Tertiary Boundary event, Western Interior, North America », Geology, vol. 14, no 8, , p. 667-670 (DOI 10.1130/0091-7613(1986)14<667:EASOPL>2.0.CO;2).
- [Willis & Mc Elwain 2002] (en) Kathy J. Willis et Jennifer C. Mc Elwain, The Evolution of Plants, Oxford University Press, (réimpr. déc. 2013), 425 p. (ISBN 978-0199292233, présentation en ligne), p. 244-249, fig 8.10.
- [Schulte et al. 2010] (en) Peter Schulte, Laia Alegret, Ignacio Arenillas, José Antonio Arz et al., « The Chicxulub Asteroid Impact and Mass Extinction at the Cretaceous-Paleogene Boundary », Science, vol. 327, no 5970, , p. 1214-1218 (DOI 10.1126/science.1177265, lire en ligne, consulté en ).
- Joel Achenbach, « The Dissenter: Most experts think an asteroid killed the dinosaurs. Not Gerta Keller », revue de l'université, sur paw.princeton.edu, Princeton Alumni Weekly, (consulté en ).
- [Schoene et al. 2014] Blair Schoene, Kyle M. Samperton, Michael P. Eddy, Gerta Keller, Thierry Adatte, Samuel A. Bowring, Syed F. R. Khadri et Brian Gertsch, « U-Pb geochronology of the Deccan Traps and relation to the end-Cretaceous mass extinction », Science, vol. 347, no 6218, , p. 182-184 (DOI 10.1126/science.aaa0118, lire en ligne [sur researchgate.net], consulté en ).
- [Renne et al. 2015] (en) Paul R. Renne, Courtney J. Sprain, Mark A. Richards, Stephen Self, Loÿc Vanderkluysen et Kanchan Pande, « State shift in Deccan volcanism at the Cretaceous-Paleogene boundary, possibly induced by impact », Science, vol. 350, no 6256, , p. 76-78 (DOI 10.1126/science.aac7549, lire en ligne [sur scinapse.io], consulté en ).
- Nathaniel Herzberg, « Le ciel et la terre, unis pour éliminer les dinosaures », sur lemonde.fr, Le Monde, (consulté en ).
- Auriane Guerithault, « Extinction des dinosaures : pourquoi la découverte de fossiles de poissons dans le Dakota du Nord est un événement scientifique majeur », sur francetvinfo.fr, (consulté en ).
- [Wilf & Johnson 2004] (en) Peter Wilf et Kirk R. Johnson, « Land plant extinction at the end of the Cretaceous: a quantitative analysis of the North Dakota megafloral record », Paleobiology, vol. 30, no 3, , p. 347–368 (DOI 10.1666/0094-8373(2004)030<0347:LPEATE>2.0.CO;2, lire en ligne [sur researchgate.net]).
- [Kauffman 2004] (en) Erle G. Kauffman, « Mosasaur Predation on Upper Cretaceous Nautiloids and Ammonites from the United States Pacific Coast », Palaios, Society for Sedimentary Geology, vol. 19, no 1, , p. 96–100 (DOI 10.1669/0883-1351(2004)019<0096:MPOUCN>2.0.CO;2, lire en ligne [PDF], consulté le ).
- [Sheehan & Hansen 1986] (en) Peter M. Sheehan et Thor A. Hansen, « Detritus feeding as a buffer to extinction at the end of the Cretaceous », Geology, vol. 14, no 10, , p. 868–870 (DOI 10.1130/0091-7613(1986)14<868:DFAABT>2.0.CO;2, lire en ligne [sur academia.edu], consulté en ).
- [Aberhan et al. 2007] (en) Martin Aberhan, Swen Weidemeyer, Wolfgang Kieesling, Roberto A. Scasso et Francisco A. Medina, « Faunal evidence for reduced productivity and uncoordinated recovery in Southern Hemisphere Cretaceous-Paleogene boundary sections », Geology, vol. 35, no 3, , p. 227–230 (DOI 10.1130/G23197A.1, lire en ligne [sur researchgate.net], consulté en ).
- [Sheehan & Fastovsky 1992] (en) Peter M. Sheehan et David E. Fastovsky, « Major extinctions of land-dwelling vertebrates at the Cretaceous–Tertiary boundary, eastern Montana », Geology, vol. 20, no 6, , p. 556–560 (DOI 10.1130/0091-7613(1992)020<0556:MEOLDV>2.3.CO;2, lire en ligne [sur researchgate.net], consulté en ).
- [Pospichal 1996] (en) James J. Pospichal, « Calcareous nannofossils and clastic sediments at the Cretaceous–Tertiary boundary, northeastern Mexico », Geology, vol. 24, no 3, , p. 255–258 (DOI 10.1130/0091-7613(1996)024<0255:CNACSA>2.3.CO;2).
- [Brown 2005] (en) Paul R. Bown, « Selective calcareous nannoplankton survivorship at the Cretaceous–Tertiary boundary », Geology, vol. 33, no 8, , p. 653–656 (DOI 10.1130/G21566.1).
- [Bambach, Knoll & Wang 2004] (en) Richard K. Bambach, Andrew H. Knoll et Steve C. Wang, « Origination, extinction, and mass depletions of marine diversity », Paleobiology, vol. 30, no 4, , p. 522–542 (DOI 10.1666/0094-8373(2004)030<0522:OEAMDO>2.0.CO;2, lire en ligne [sur researchgate.net], consulté en ).
- [Gedl 2004] (en) Przemysław Gedl, « Dinoflagellate cyst record of the deep-sea Cretaceous-Tertiary boundary at Uzgru, Carpathian Mountains, Czech Republic », Geological Society, London, Special Publications, vol. 230, , p. 257–273 (DOI 10.1144/GSL.SP.2004.230.01.13).
- [Braun et al. 2007] (en) Andreas Braun, Jian Chen, Dieter Waloszek et Andreas Maas, « First Early Cambrian Radiolaria », Geological Society, London, vol. 286 « The Rise and Fall of the Ediacaran Biota », no « Special Publications » édité par Patricia Vickers-Rich & Patricia Komarower, , p. 143-149 (DOI 10.1144/SP286.10, lire en ligne [sur researchgate.net], consulté en ).
- [MacLeod 1998] (en) Norman MacLeod, « Impacts and marine invertebrate extinctions », Geological Society, London, vol. 140 « Special Publications », , p. 217–246 (DOI 10.1144/GSL.SP.1998.140.01.16, résumé, lire en ligne [PDF] sur citeseerx.ist.psu.edu, consulté en ).
- [Courtillot 1999] (en) Vincent Courtillot, Evolutionary Catastrophes: The Science of Mass Extinction, Cambridge, Cambridge University Press, , 173 p., sur books.google.com (ISBN 0-521-58392-6, lire en ligne).
- [Glaessner 1937] (de) Martin Fritz Glaessner, « Studien über foraminiferen aus der kreide und dem Tertiär des Kaukasus. I. Die foraminiferen der ältesten Tertiärschichten des Nordwest-Kaukasus » [« Études des foraminifères du Crétacé et du Tertiaire du Caucase. I. Les foraminifères des plus anciennes strates tertiaires du Caucase du Nord-Ouest »], Problemy Paleontologii [Problems in Paleontology], éd. Paleontologicheskay Laboratoriya Moskovskogo Universiteta, vol. 2–3, , p. 349–410 (lire en ligne [sur books.google.pt]).
- [Arenillas et al. 2000] (en) Ignacio Arenillas, Jose Antonio Arz Sola, Enid Molina et Christian Dupuis, « An Independent Test of Planktic Foraminiferal Turnover across the Cretaceous/Paleogene (K/P) Boundary at El Kef, Tunisia: Catastrophic Mass Extinction and Possible Survivorship », Micropaleontology, vol. 46, no 1, , p. 31–49 (lire en ligne [sur researchgate.net], consulté en ).
- [MacLeod 1996] (en) Norman MacLeod, « Nature of the Cretaceous-Tertiary (K–T) planktonic foraminiferal record: stratigraphic confidence intervals, Signor-Lipps effect, and patterns of survivorship », dans Gerta Keller & Norman MacLeod (éds.), Cretaceous–Tertiary Mass Extinctions : Biotic and Environmental Changes, éd. W.W. Norton & Co, , 575 p. (ISBN 978-0-393-96657-2, présentation en ligne), p. 85–138.
- [Keller et al. 2004] (en) Gerta Keller, Thierry Adatte, Wolfgang Stinnesbeck, Mario Rebolledo-Vieyra, Jaime Urrutia Fucugauchi, Utz Kramar et Doris Stüben, « Chicxulub impact predates the K–T boundary mass extinction », PNAS, vol. 101, no 11, , p. 3753–3758 (PMID 15004276, PMCID 374316, DOI 10.1073/pnas.0400396101, lire en ligne [PDF] sur pnas.org, consulté en ).
- [Galeotti et al.] (en) Simone Galeotti, Miguel Bellagamba, Michael A. Kaminski et Alessandro Montanari, « Deep-sea benthic foraminiferal recolonisation following a volcaniclastic event in the lower Campanian of the Scaglia Rossa Formation (Umbria-Marche Basin, central Italy) », Marine Micropaleontology, vol. 44, , p. 57–76 (lire en ligne [sur academia.edu], consulté en ).
- [Kuhnt & Collins 1996] (en) Wolfgang Kuhnt et Eric S. Collins, « 8. Cretaceous to Paleogene benthic foraminifers from the Iberia abyssal plain », Proceedings of the Ocean Drilling Program, Scientific Results, vol. 149, no édité par Robert B. Whitmarsh, Dale S. Sawyer, Adam Klaus & Douglas G. Masson, , p. 203–216 (lire en ligne [PDF] sur citeseerx.ist.psu.edu, consulté en ).
- [Coles, Ayress & Whatley 1990] (en) Graham P. Coles, Michael A. Ayress et Robin C. Whatley, « A comparison of North Atlantic and 20 Pacific deep-sea Ostracoda », dans Robin Whatley & Caroline Maybury (éds.), Ostracoda and global events, Chapman & Hall, coll. « British Micropalaeontological Society publication series », , 621 p., sur researchgate.net (ISBN 978-0-442-31167-4, présentation en ligne, lire en ligne), p. 287–305.
- [Brouwers & Deckker 1993] (en) Elisabeth M. Brouwers et Patrick De Deckker, « Late Maastrichtian and Danian Ostracode Faunas from Northern Alaska: Reconstructions of Environment and Paleogeography », PALAIOS, vol. 8, no 2, , p. 140–154 (DOI 10.2307/3515168, résumé).
- [Vescsei & Moussavian 1997] (en) Adam Vescsei et Esmail Moussavian, « Paleocene reefs on the Maiella Platform Margin, Italy: An example of the effects of the cretaceous/tertiary boundary events on reefs and carbonate platforms », Facies, no 36, , p. 123–139 (DOI 10.1007/BF02536880).
- [Rosen & Turnšek 1989] (en) Brian R. Rosen et Dragica Turnšek, « Extinction patterns and biogeography of scleractinian corals across the Cretaceous/Tertiary boundary » (annales du 5e Symposium International sur le fossile Cnidaria [International Symposium on Fossil Cnidaria], y compris Archaeocyatha et Spongiomorphes, Brisbane, Queensland, Australia, 25-29 juillet 1988), Mémoire de l'Association of australasian palaeontologists, no 8 (Peter A. Jell & John W. Pickett éds.), , p. 355–370 (lire en ligne [PDF] sur piir.zrc-sazu.si, consulté en ).
- [Kiessling & Baron-Szabo 2004] (en) Wolfgang Kiessling et Rosemarie C. Baron-Szabo, « Extinction and recovery patterns of scleractinian corals at the Cretaceous-Tertiary boundary » (publications du groupe de travail sur les événements biologiques du Mésozoïque-Cénozoïque, Berlin, fin 2002), Palaeo, no 8 (éds. Wolfgang Kiessling, David Lazarus & Ulrich Zeller) « Mesozoic-Cenozoic Bioevents », , p. 195–223 (DOI 10.1016/j.palaeo.2004.05.025, lire en ligne [sur academia.edu], consulté en ).
- [Ward et al. 1991] (en) Peter D. Ward, W. Jim Kennedy, Kenneth G. MacLeod et Jeffrey F. Mount, « Ammonite and inoceramid bivalve extinction patterns in Cretaceous/Tertiary boundary sections of the Biscay region (southwestern France, northern Spain) », Geology, vol. 19, no 12, , p. 1181–1184 (DOI 10.1130/0091-7613(1991)019<1181:AAIBEP>2.3.CO;2).
- [Harries et al. 2002] (en) Peter Jürgen Harries, Kirk R. Johnson, William A. Cobban et Douglas J. Nichols, « Marine Cretaceous-Tertiary boundary section in southwestern South Dakota: Comment and Reply », Geology, vol. 30, no 10, , p. 954–955 (DOI 10.1130/0091-7613(2002)030<0955:MCTBSI>2.0.CO;2).
- [Neraudeau, Thierry & Moreau 1997] (en) Didier Neraudeau, Jacques Thierry et Pierre Moreau, « Variation in echinoid biodiversity during the Cenomanian–early Turonian transgressive episode in Charentes (France) » (séance spécialisée SGF-APF, Paris, 14-15 décembre 1995), Bulletin de la Société géologique de France, t. 168, no 1 « Faune, flore et stratigraphie séquentielle », , p. 51–61 (ISSN 0037-9409, présentation en ligne).
- [Raup & Jablonski 1993] (en) David M. Raup et David Jablonski, « Geography of end-Cretaceous marine bivalve extinctions », Science, vol. 260, no 5110, , p. 971–973 (PMID 11537491, DOI 10.1126/science.11537491, résumé).
- [MacLeod 1994] (en) Kenneth G. MacLeod, « Extinction of Inoceramid Bivalves in Maastrichtian Strata of the Bay of Biscay Region of France and Spain », Journal of Paleontology, vol. 68, no 5, , p. 1048–1066 (DOI 10.1017/S0022336000026652).
- [Patterson 1993] (en) Colin Patterson, « Osteichthyes : Teleostei », dans Michael J. Benton (éd.), The Fossil Record 2, London / Glasgow / New York etc., Springer, (réimpr. Chapman & Hall, 2007), 845 p. (ISBN 0-412-39380-8).
- [Zinsmeister 1998] (en) William J. Zinsmeister, « Discovery of fish mortality horizon at the K–T boundary on Seymour Island: Re-evaluation of events at the end of the Cretaceous », Journal of Paleontology, vol. 72, no 3, , p. 556–571 (DOI 10.1017/S0022336000024331).
- [Robertson et al. 2004] (en) Douglas S. Robertson, Malcolm C. McKenna, Owen B. Toon, Sylvia Hope et Jason A. Lillegraven, « Survival in the first hours of the Cenozoic », GSA Bulletin, vol. 116, nos 5–6, , p. 760–768 (DOI 10.1130/B25402.1, lire en ligne [sur yumpu.com], consulté en ).
- [Labandeira, Johnson & Wilf] (en) Conrad C. Labandeira, Kirk R. Johnson et Peter Wilf, « Impact of the terminal Cretaceous event on plant–insect associations », PNAS, vol. 99, no 4, , p. 2061–2066 (PMID 11854501, PMCID 122319, DOI 10.1073/pnas.042492999, lire en ligne [PDF] sur geosc.psu.edu, consulté en ).
- [Wilf et al. 2006] (en) Peter Wilf, Conrad C. Labandeira, Kirk R. Johnson et Beth Ellis, « Decoupled Plant and Insect Diversity After the End-Cretaceous Extinction », Science, vol. 313, no 5790, , p. 1112–1115 (PMID 16931760, DOI 10.1126/science.1129569, lire en ligne [sur academia.edu], consulté en ).
- [Vajda, Raine & Hollis 2001] (en) Vivi Vajda, J. Ian Raine et Christopher J. Hollis, « Indication of Global Deforestation at the Cretaceous–Tertiary Boundary by New Zealand Fern Spike », Science, vol. 294, no 5547, , p. 1700–1702 (PMID 11721051, DOI 10.1126/science.1064706, lire en ligne [sur researchgate.net], consulté en ).
- [Johnson & Hickey] Kirk R. Johnson et Leo J. Hickey, « Megafloral change across the Cretaceous Tertiary boundary in the northern Great Plains and Rocky Mountains », dans Virgil L. Sharpton & Peter D. Ward, Global Catastrophes in Earth History: an Interdisciplinary Conference on Impacts, Volcanism, and Mass Mortality, Geological Society of America, coll. « Special Paper » (no 247), , 631 p. (ISBN 978-0-8137-2247-4, résumé), p. 549–562.
- [Askin & Jacobson 1996] (en) R.A. Askin et S.R. Jacobson, « Palynological change across the Cretaceous–Tertiary boundary on Seymour Island, Antarctica : environmental and depositional factors », dans Gerta Keller & Norman MacLeod (éds.), Cretaceous–Tertiary Mass Extinctions : Biotic and Environmental Changes, éd. WW Norton, , 575 p. (ISBN 978-0-393-96657-2).
- [Schultz & D'Hondt 1996] (en) Peter H. Schultz (en) et Steven D'Hondt (en), « Cretaceous–Tertiary (Chicxulub) impact angle and its consequences », Geology, vol. 24, no 11, , p. 963–967 (DOI 10.1130/0091-7613(1996)024<0963:CTCIAA>2.3.CO;2).
- [Vajda & McLoughlin 2004] (en) Vivi Vajda et Stephen McLoughlin, « Fungal Proliferation at the Cretaceous–Tertiary Boundary », Science, vol. 303, no 5663, , p. 1489–1490 (PMID 15001770, DOI 10.1126/science.1093807, résumé, lire en ligne [PDF] sur nrm.diva-portal.org, consulté en ).
- [Fawcett, Maere & Peer 2009] (en) Jeffrey A. Fawcett, Steven Maere et Yves Van de Peer, « Plants with double genomes might have had a better chance to survive the Cretaceous-Tertiary extinction event », PNAS, vol. 106, no 14, , p. 5737-5742 (DOI 10.1073/pnas.0900906106, lire en ligne [sur pnas.org], consulté en ).
- [Archibald & Bryant 1990] (en) J. David Archibald et Laurie J. Bryant, « Differential Cretaceous–Tertiary extinction of nonmarine vertebrates; evidence from northeastern Montana », dans Virgil L. Sharpton & Peter D. Ward, Global Catastrophes in Earth History: an Interdisciplinary Conference on Impacts, Volcanism, and Mass Mortality, Geological Society of America, coll. « Special Paper » (no 247), , 631 p. (ISBN 9780813722474, résumé), p. 549–562.
- [Novacek 1999] (en) Michael J. Novacek, « 100 Million Years of Land Vertebrate Evolution: The Cretaceous-Early Tertiary Transition », Annals of the Missouri Botanical Garden, vol. 86, , p. 230–258 (DOI 10.2307/2666178, lire en ligne [sur ur.booksc.eu], consulté en ).
- [Lutz 2005] (en) Dick Lutz, Tuatara: A Living Fossil from before dinosaurs, DIMI Press, (ISBN 0-931625-43-2, présentation en ligne).
- [Brochu 2004] (en) Christopher A. Brochu, « Calibration age and quartet divergence date estimation », Evolution, vol. 58, no 6, , p. 1375–1382 (PMID 15266985, DOI 10.1554/03-509, lire en ligne [sur ur.booksc.eu], consulté en ).
- [Jouve et al. 2008] (en) Stéphane Jouve, Nathalie Bardet, Nour-Eddine Jalil, Xabier Pereda Suberbiola, Baâdi Bouya et Mbarek Amaghzaz, « The oldest African crocodylian: phylogeny, paleobiogeography, and differential survivorship of marine reptiles through the Cretaceous-Tertiary Boundary », Journal of Vertebrate Paleontology, vol. 28, no 2, , p. 409–421 (DOI 10.1671/0272-4634(2008)28[409:TOACPP]2.0.CO;2, lire en ligne [sur academia.edu]).
- [Slack et al. 2006] (en) Kerryn E. Slack, Craig M. Jones, Tatsuro Ando, G. L. (Abby) Harrison, R. Ewan Fordyce, Ulfur Arnason et David Penny, « Early Penguin Fossils, Plus Mitochondrial Genomes, Calibrate Avian Evolution », Molecular Biology and Evolution, vol. 23, no 6, , p. 1144–1155 (PMID 16533822, DOI 10.1093/molbev/msj124, lire en ligne [sur mbe.oxfordjournals.org]).
- [Penny & Phillips 2004] (en) David Penny et Matthew J. Phillips, « The rise of birds and mammals: are microevolutionary processes sufficient for macroevolution », Trends in ecology & evolution, vol. 19, no 10, , p. 516–522 (PMID 16701316, DOI 10.1016/j.tree.2004.07.015, lire en ligne [PDF] sur evolbiol.ru, consulté en ).
- [Hou et al. 1996] (en) Lianhai Hou, Larry D. Martin, Zhonghe Zhou et Alan Feduccia, « Early Adaptive Radiation of Birds: Evidence from Fossils from Northeastern China », Science, vol. 274, no 5290, , p. 1164–1167 (PMID 8895459, DOI 10.1126/science.274.5290.1164, lire en ligne [PDF] sur 119.78.100.205/bitstream, consulté en ).
- [Clarke et al. 2005] (en) Julia A. Clarke, Claudia P. Tambussi, Jorge I. Noriega, Gregory M. Erickson et Richard A. Ketcham, « Definitive fossil evidence for the extant avian radiation in the Cretaceous », Nature, vol. 433, no 7023, , p. 305–308 (PMID 15662422, DOI 10.1038/nature03150, lire en ligne [sur researchgate.net]).
- Véronique Marsollier, « Comment les oiseaux ont-ils survécu à la disparition des dinosaures ? »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur cite-sciences.fr, .
- [Archibald & Fastovsky 2004] (en) J. David Archibald et David E. Fastovsky, The Dinosauria, Berkeley, University of California Press, , 2e éd. (ISBN 0-520-24209-2), « Dinosaur Extinction », p. 672–684.
- [Ocampo, Vadja & Buffetaut 2006] (en) Adriana Ocampo, Vivi Vajda et Éric Buffetaut, « Unravelling the Cretaceous–Paleogene (K–T) turnover, evidence from flora, fauna and geology », dans Charles Cockell, Christian Koeberl & Iain Gilmour (éds.), Biological Processes Associated with Impact Events, SpringerLink, coll. « Impact Studies book series (IMPACTSTUD) », , sur books.google.fr (ISBN 978-3-540-25735-6, DOI 10.1007/3-540-25736-5_9, présentation en ligne, lire en ligne), p. 197–219.
- Charles Frankel, Extinctions. Du dinosaure à l'homme, Seuil, , p. 34.
- [Gelfo & Pascual 2001] (en) Javier N. Gelfo et Rosendo Pascual, « Peligrotherium tropicalis (Mammalia, Dryolestida) from the early Paleocene of Patagonia, a survival from a Mesozoic Gondwanan radiation », Geodiversitas, vol. 23, , p. 369–379 (lire en ligne [sur researchgate.net]).
- [Goin et al. 2006] (en) Francisco J. Goin, Marcelo A. Reguero, Rosendo Pascual et Wighart Von Koenigswald, « First gondwanatherian mammal from Antarctica », Geological Society, London, Special Publications, vol. 258, , p. 135–144 (DOI 10.1144/GSL.SP.2006.258.01.10, lire en ligne [sur researchgate.net]).
- [McKenna & Bell 1997] (en) Malcolm C. McKenna et Susan K. Bell, Classification of Mammals: Above the Species Level, Columbia University Press, , 631 p. (ISBN 978-0-231-11012-9, présentation en ligne).
- [Bidinda-Emonds et al. 2007] (en) Olaf R. P. Bininda-Emonds, Marcel Cardillo, Kate Elizabeth Jones, Ross D.E. Macphee, Robin M. Beck, Richard Grenyer, Samantha A. Price, Rutger A. Vos, John L Gittleman et Andy Purvis, « The delayed rise of present-day mammals », Nature, vol. 446, no 7135, , p. 507–512 (PMID 17392779, DOI 10.1038/nature05634, lire en ligne [sur researchgate.net], consulté en ).
- [Springer et al. 2003] (en) Mark S. Springer, William J. Murphy, Eduardo Eizirik et Stephen J. O'Brien, « Placental mammal diversification and the Cretaceous–Tertiary boundary », PNAS, vol. 100, no 3, , p. 1056–1061 (PMID 12552136, PMCID 298725, DOI 10.1073/pnas.0334222100, lire en ligne [PDF] sur pnas.org).
- [Kielan-Jaworowska, Cifelli & Luo 2004] (en) Zofia Kielan-Jaworowska, Richard L. Cifelli et Zhe-Xi Luo, Mammals from the age of Dinosaurs. Origins, evolution, and structure, Columbia University Press, , 700 p. (ISBN 9780231119184, présentation en ligne), p. 6.
- [Clausen & Métais 2013] Sébastien Clausen et Grégoire Métais, chap. 6, section 2 (p. 179-197) : « Diversifications et extinctions » : « Radiation », dans Thierry Tortosa (dir.) et al., Principes de paléontologie, Dunod, coll. « Sciences Sup », , 329 p. (ISBN 978-2-10-057993-8, présentation en ligne), p. 195.
- [Casadevall 2005] (en) Arturo Casadevall, « Fungal virulence, vertebrate endothermy, and dinosaur extinction: is there a connection? », Fungal Genetics and Biology, vol. 42, no 2, , p. 98–106 (DOI 10.1016/j.fgb.2004.11.008, lire en ligne [PDF] sur einsteinmed.org, consulté en ).
- [Allain 2012] Ronan Allain, Histoire des dinosaures, éd. Perrin, (réimpr. Flammarion, 2015, coll. Champs - Sciences), 229 p. (résumé, présentation en ligne), p. 87.
- [Dodson 1996] (en) Peter Dodson, The Horned Dinosaurs: A Natural History, Princeton, Princeton University Press, (ISBN 0-691-05900-4), p. 279–281.
- [Pillmore, Nichols & Fleming 2004] (en) C. L. Pillmore, D. J. Nichols et R. F. Fleming, « Online guide to the continental Cretaceous–Tertiary boundary in the Raton basin, Colorado and New Mexico », U.S. Geological Survey, (ISBN 9780813756011, DOI 10.1130/0-8137-0001-9.135, consulté le ).
- [Smathers & Mueller-Dombois 1972] (en) Garrett A. Smathers, Invasion and Recovery of Vegetation after a Volcanic Eruption in Hawaii, United States National Park Service, coll. « Scientific Monograph » (no 5), , sur nps.gov (lire en ligne).
- [De Palma et al. 2019] (en) Robert A. De Palma, Jan Smit, David A. Burnham, Klaudia Kuiper, Phillip L. Manning, Anton Oleinik, Peter Larson, Florentin J. Maurrasse, Johan Vellekoop, Mark A. Richards, Loren Gurche et Walter Alvarez, « A seismically induced onshore surge deposit at the KPg boundary, North Dakota », Proceedings of the National Academy of Sciences, vol. 116, no 17, , p. 8190-8199 (lire en ligne [sur pnas.org], consulté en ).
- [Pope, D'Hondt & Marshall 1998] (en) Kevin O. Pope, Steven L. D'Hondt (en) et Charles R. Marshall, « Meteorite impact and the mass extinction of species at the Cretaceous/Tertiary boundary », PNAS, vol. 95, no 19, , p. 11028–11029 (PMID 9736679, PMCID 33889, DOI 10.1073/pnas.95.19.11028, lire en ligne [sur pnas.org], consulté en ).
- [Marshall & Ward 1996] (en) Charles R. Marshall et Peter D. Ward, « Sudden and Gradual Molluscan Extinctions in the Latest Cretaceous of Western European Tethys », Science, vol. 274, no 5291, , p. 1360–1363 (PMID 8910273, DOI 10.1126/science.274.5291.1360).
- [DePalma et al. 2019] (en) Robert A. DePalma, Jan Smit, David A. Burnham, Klaudia Kuiper, Phillip L. Manning, Anton Oleinik, Peter Larson, Florentin J. Maurrasse, Johan Vellekoop, Mark A. Richards et Loren Gurche, « A seismically induced onshore surge deposit at the KPg boundary, North Dakota », PNAS, vol. 116, no 17, , p. 8190-8199 (DOI 10.1073/pnas.1817407116, lire en ligne [sur researchgate.net], consulté en ).
- Laurent Sacco, « L'astéroïde qui a tué les dinosaures est tombé au printemps », sur futura-sciences.com, Futura-Sciences, .
- Sophie Bécherel, « La fin des dinosaures s'est produite au printemps (on le sait grâce à des os de poissons) », sur franceinter.fr, France Inter, .
- [Signor & Lipps 1982] (en) Phillip W. Signor et Jere H. Lipps, « Sampling bias, gradual extinction patterns, and catastrophes in the fossil record », dans Leon T. Silver et Peter H. Schultz, Geological implications of impacts of large asteroids and comets on the Earth, coll. « Geological Society of America Special Publication » (no 190), , 291–296 p. (DOI 10.1130/SPE190-p291).
- [Fastovsky & Sheehan 2005] (en) David Fastovsky et Peter M. Sheehan, « The extinction of the dinosaurs in North America », GSA today, vol. 15, no 3., , p. 4-10 (DOI 10.1130/1052-5173(2005)15<4:TEOTDI>2.0.CO;2, lire en ligne [sur researchgate.net], consulté en ).
- [Swain 1976] (en) Tony Swain, « Reptile-angiosperm co-evolution », dans Martin Luckner, Kurt Mothes & Lutz Nover (éds.), Secondary Metabolism and Coevolution: Cellular, Intercellular, and Interorganismic Aspects (annales du Congrès de la Deutche Akademie der Naturforscher Leopoldina de Halle, 19-21 avril 1974), Deutche Akademie der Naturforscher Leopoldina, coll. « Nova acta Leopodina » (no 7), , 614 p. (ISSN 0232-8615 et 0232-8615, présentation en ligne), p. 551–561.
- [Montenat & Merle 2018] Christian Montenat et Didier Merle, Stratotype Danien, Paris, Muséum national d'Histoire naturelle, coll. « Patrimoine géologique » (no 9), , 480 p. (ISBN 978-2-85653-830-2, présentation en ligne), « La crise Crétacé-Tertiaire : le point sur la question », p. 394.
- [Fortey 1999] (en) Richard Fortey, Life: a natural history of the first four billion years of life on earth, Vintage Books, , 400 p. (ISBN 978-0-375-70261-7), p. 238-260.
- [Alvarez et al. 1980] (en) Luis W. Alvarez, Walter Alvarez, Frank Asaro et Helen V. Michel, « Extraterrestrial cause for the Cretaceous–Tertiary extinction », Science, vol. 208, no 4448, , p. 1095–1108 (PMID 17783054, DOI 10.1126/science.208.4448.1095, lire en ligne [PDF] sur websites.pmc.ucsc.edu, consulté en ).
- « La chute d'une météorite a bien été fatale aux dinosaures », sur lemonde.fr, (consulté en ).
- [Whiston 1696] William Whiston, A new Theory of the Earth (en) from its original to the consummation of all things, wherein the creation of the world in six days, the universal deluge, and the general conflagration, as lain down in the Holy Scriptures, are shewn to be prefectly agreeable to reason and philosophy, London, (réimpr. 1708, the University-Press, Cambridge), 388 p., sur gallica (lire en ligne). Cité par (en) Norman McLeod, « Dinosaur Extinction - Impact Hypothesis first proposed in Journalof Paleontology in 1956 », sur jerwood.nhm.ac.uk, (consulté en ), qui cite également [Stephen Jay Gould 1991, Dinosaur in a Haystack].
- [Schindewolf 1955] Otto Schindewolf, « Die Entfaltung des Lebens im Rahmen der geologischen Zeit », Studium Generale, Berlin / Göttingen / Heidelberg, Springer-Verlag, vol. 8, no 8, , p. 489-497. Cité par Norman McLeod, « Dinosaur Extinction - Impact Hypothesis first proposed in Journalof Paleontology in 1956 », sur jerwood.nhm.ac.uk, (consulté en ).
- [Laubenfels 1956] (en) De Laubenfels (en), « Dinosaur extinction: One more hypothesis », Journal of Paleontology, vol. 30, no 1, , p. 207–218 (résumé).
- [Pope et al. 1997] (en) Kevin O. Pope, Kevin H. Baines, Adriana C. Ocampo et Boris A. Ivanov, « Energy, volatile production, and climatic effects of the Chicxulub Cretaceous/Tertiary impact », Journal of Geophysical Research, vol. 102, no E9, , p. 21645–21664 (PMID 11541145, DOI 10.1029/97JE01743, lire en ligne, consulté en ).
- [Kring 2003] (en) David A. Kring, « Environmental consequences of impact cratering events as a function of ambient conditions on Earth », Astrobiology, vol. 3, no 1, , p. 133–152 (PMID 12809133, DOI 10.1089/153110703321632471, lire en ligne [sur ur.booksc.eu], consulté en ).
- [Courtillot 2002] (en) Vincent Courtillot (trad. du français par Joe McClinton), Evolutionary Catastrophes: The Science of Mass Extinction [« La Vie en catastrophes: Du hasard dans l'évolution des espèces »], Cambridge University Press, (1re éd. 1995, Fayard), 173 p. (ISBN 978-0-521-89118-9, présentation en ligne), « An asteroid impact - A general conflagration », p. 43.
- [Pope et al. 1996] (en) Kevin O. Pope, Adriana C. Ocampo, Gary L. Kinsland et Randy Smith, « Surface expression of the Chicxulub crater », Geology, vol. 24, no 6, , p. 527–530 (PMID 11539331, DOI 10.1130/0091-7613(1996)024<0527:SEOTCC>2.3.CO;2).
Voir aussi [Sharpton & Pope] (en) Virgil L. Sharpton et Kevin O. Pope, « Surface expression of the Chicxulub crater: Comment [par Virgil L. Sharpton] and Reply [par Kevin O. Pope] », Geology, , p. 567-569 (lire en ligne [PDF] sur ur.booksc.eu, consulté en ). - [Gulick et al. 2008] (en) Sean P. S. Gulick, Penny J. Barton, Gail L. Christeson, Joanna V. Morgan, Missy Mcdonald, Keren Mendoza, Zulmacristina F. Pearson, Anusha Surendra, J. Urrutia Fucugauchi, Peggy M. Vermeesch et Mike R. Warner, « Importance of pre-impact crustal structure for the asymmetry of the Chicxulub impact crater », Nature Geoscience, vol. 1, no 2, , p. 131–135 (DOI 10.1038/ngeo103, résumé).
- [Morgan et al. 2006] (en) Joanna V. Morgan, Cristiano Lana, Anton Kearsley, Barry Coles, Claire Belcher, Alessandro Montanari, Enrique Díaz-Martínez, Antonio Barbosa et Virginio Neumann, « Analyses of shocked quartz at the global K-P boundary indicate an origin from a single, high-angle, oblique impact at Chicxulub », Earth and Planetary Science Letters, vol. 251, nos 3–4, , p. 264–279 (DOI 10.1016/j.epsl.2006.09.009, lire en ligne [sur spiral.imperial.ac.uk], consulté en ).
- [Keller et al. 2009] (en) Gerta Keller, Sigal Abramovich, Zsolt Attila Berner et Thierry Adatte, « Biotic effects of the Chicxulub impact, K–T catastrophe and sea level change in Texas », Palaeogeography, Palaeoclimatology, Palaeoecology, vol. 271, nos 1-2, , p. 52–68 (DOI 10.1016/j.palaeo.2008.09.007, lire en ligne [sur academia.edu], consulté en ).
- [Chatterjee 1997] (en) Sankar Chatterjee, « Multiple impacts at the KT boundary and the death of the dinosaurs » (2 vol.), Proceedings of the 30th International Geological Congress, Beijing (China), août 1997, Utrecht (Netherlands), éd. VSP, vol. 26 (éds. Wang Hongzhen, D.F. Branagan, Ouyang Ziyuan & Wang Xunlian « Comparative Planetology, Geological Education, History of Geology », , p. 31-54 (lire en ligne [sur books.google.fr], consulté en ).
- [Bottke, Vokrouhlický & Nesvorný 2007] (en) William Bottke, David Vokrouhlický et David Nesvorný, « An asteroid breakup 160 Myr ago as the probable source of the K/T impactor », Nature, vol. 449, , p. 48-53 (lire en ligne [PDF] sur astro.mff.cuni.cz, consulté en ).
- [Majaess et al. 2008] (en) Daniel J. Majaess, David Higgins, Larry Molnar, Melissa Haegert, David J. Lane, David G. Turner et Inga Nielsen, « New Constraints on the Asteroid 298 Baptistina, the Alleged Family Member of the K/T Impactor », Journal of the Royal Astronomical Society of Canada, (lire en ligne [sur researchgate.net], consulté en ).
- [Reddy et al. 2009] (en) Vishnu Reddy, Michael S. Kelley, Joshua P. Emery, Michael J. Gaffey, William F. Bottke, David Nesvorny, Meagan Schaal, Abigail Cramer et Driss Takir, « Composition of 298 Baptistina: Implications for K–T Impactor Link » (conference, 2008), Meteoritics & Planetary Science, vol. 44, no 12 « Asteroids, Comets, Meteors », , p. 1917-1927 (lire en ligne [e-pdf sur onlinelibrary.wiley.com], consulté en ).
- « Extinction des dinosaures : découverte de fossiles du jour où un astéroïde a frappé la Terre », sur europe1.fr, (consulté en ).
- [Henehan et al. 2019] (en) Michael James Henehan, Andy Ridgwell, Ellen Thomas, Shuang Zhang, Laia Alegret, Daniela N. Schmidt, James W. B. Rae, James D. Witts, Neil H. Landman, Sarah E. Greene, Brian T. Huber, James R. Super, Noah J. Planavsky et Pincelli M. Hull, « Rapid ocean acidification and protracted Earth system recovery followed the end-Cretaceous Chicxulub impact », Proceedings of the National Academy of Sciences, vol. 116, no 45 « Global biogeochemical cycles Project », , p. 22500-22504 (DOI 10.1073/pnas.1905989116, lire en ligne [sur researchgate.net], consulté en ).
- (en) « Study: Asteroid Impact, Not Volcanism, was Key in Driving End-Cretaceous Mass Extinction », sur sci-news.com, (consulté en ).
- [Keller et al. 2008] (en) Gerta Keller, Thierry Adatte, Silvia Gardin, Annachiara Bartolini et Sunil Bajpai, « Main Deccan volcanism phase ends near the K–T boundary: Evidence from the Krishna-Godavari Basin, SE India », Earth and Planetary Science Letters, vol. 268, , p. 293–311 (DOI 10.1016/j.epsl.2008.01.015, lire en ligne [sur academia.edu], consulté en ).
- [Duncan & Pyle 1988] (en) Robert A. Duncan et Douglas G. Pyle, « Rapid eruption of the Deccan flood basalts at the Cretaceous/Tertiary boundary », Nature, vol. 333, , p. 841–843 (DOI 10.1038/333841a0, Bibcode 1988Natur.333..841D).
- [Pope et al. 1994] (en) Kevin O. Pope, Kevin H. Baines, Adriana C. Ocampo et Boris A. Ivanov, « Impact winter and the Cretaceous/Tertiary extinctions: Results of a Chicxulub asteroid impact model », Earth and Planetary Science Letters, vol. 128, nos 3-4, , p. 719-725 (DOI 10.1016/0012-821X(94)90186-4, lire en ligne [sur academia.edu], consulté en ).
- (en) Walter Alvarez, T. Rex and the Crater of Doom (en), Princeton University Press, , 130–146 p. (ISBN 978-0-691-01630-6).
- (en) L. Mullen, « Debating the Dinosaur Extinction »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur astrobio.net, Astrobiology Magazine (consulté le ).
- (en) L. Mullen, « Multiple impacts »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur astrobio.net, Astrobiology Magazine (consulté le ).
- (en) L. Mullen, « Shiva: Another K–T impact? »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur astrobio.net, Astrobiology Magazine (consulté le ).
- [Liangquan & Keller 1998] (en) Li Liangquan et Gerta Keller, « Abrupt deep-sea warming at the end of the Cretaceous », Geology, vol. 26, , p. 995–998 (DOI 10.1130/0091-7613(1998)026<0995:ADSWAT>2.3.CO;2, lire en ligne [sur academia.edu], consulté en ).
Voir aussi[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- (en) Adriana Ocampo, Vivi Vajda et Eric Buffetaut, « Unravelling the Cretaceous-Paleogene (KT) Turnover, Evidence from Flora, Fauna and Geology », dans Charles Cockell, Iain Gilmour et Christian Koeberl, Biological Processes Associated with Impact Events, Springer, coll. « Impact studies », (ISBN 978-3-540-25735-6 et 978-3-540-25736-3, DOI 10.1007/3-540-25736-5_9, lire en ligne), p. 197-219
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- Notice dans un dictionnaire ou une encyclopédie généraliste :
- Arnaud Salome, « Enquête sur la disparition des dinosaures », sur futura-sciences.com, Futura-Sciences, .
- André Holbecq, « La limite Crétacé/Tertiaire (KT) et l'extinction des dinosaures »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur geopolis.fr, Confédération Française des Acteurs des Sciences de la Terre
- (en) Manabu Sakamoto, Michael J. Benton et Chris Venditti, « Dinosaurs in decline tens of millions of years before their final extinction », sur PNAS,