Grippe espagnole
Pandémie grippale de 1918
(Pandémie grippale de 1918)
| Maladie | |
|---|---|
| Agent infectieux | |
| Origine |
Inconnue. Identifiée aux États-Unis |
| Date d'arrivée | |
| Date de fin | |
| Site web |
| Cas confirmés |
500 M[1] |
|---|---|
| Morts |
Entre 20 et 100 millions |
La grippe espagnole, également appelée « pandémie grippale de l'année 1918 », est une pandémie de grippe A (H1N1), due à une souche particulièrement virulente et contagieuse qui s'est répandue en et a fini par s'éteindre dans la seconde moitié de l'année 1919. Quelques derniers cas sporadiques ont eu lieu en Nouvelle-Calédonie en [2].
Bien que les premiers cas dûment répertoriés soient apparus en France et aux États-Unis, on lui a attribué le nom de « grippe espagnole » car l'Espagne (non impliquée dans la Première Guerre mondiale) fut le seul pays à publier librement les informations relatives à cette épidémie.
Cette pandémie a fait de 20 à 50 millions de morts selon l'Institut Pasteur, et peut-être jusqu'à 100 millions selon certaines réévaluations de 2020, soit 2,5 à 5 % de l'humanité et environ 4 à 20 % des malades (on estime le taux de létalité aux alentours de 10 %)[3].
Selon l'historien Niall Johnson qui se fonde sur la fourchette basse, les plus grandes pertes ont touché l'Inde (18,5 millions de morts, soit 6 % de la population), la Chine (4 à 9,5 millions de morts selon les estimations, soit 0,8 à 2 % de la population), l'Europe (2,3 millions de morts en Europe occidentale, soit 0,5 % de la population) et les États-Unis (entre 500 000 et 675 000 morts, soit 0,48 à 0,64 % de la population américaine).
Histoire
[modifier | modifier le code]Antécédents
[modifier | modifier le code]Avant cette grippe de 1918, des pandémies de grippe se produisaient dans le monde en moyenne trois fois par siècle[4]. Les flambées de grippe s'accélèrent au fur et à mesure des siècles : « de 1700 à 1889, l'intervalle moyen entre deux pandémies est de cinquante à soixante ans. À partir de 1889, cet intervalle n'est plus que de dix à quarante ans. Cette accélération peut correspondre à une plus facile propagation du virus, entre autres liée à l'accroissement de la population, à l'urbanisation et à la plus grande fréquence des échanges internationaux »[5].
Hypothèses sur l'origine géographique
[modifier | modifier le code]Comme la plupart des grippes, cette épidémie a d'abord été supposée d'origine asiatique. Au début du XXIe siècle, et de recherches s'appuyant sur la génétique du virus, cette hypothèse a perdu de sa crédibilité au profit d'autres, et c'est maintenant l'hypothèse d'une origine aux États-Unis, plus précisément au Kansas, qui est privilégiée :
- les cas précoces et mortels d’infections respiratoires signalés dès 1916-1917 dans le camp britannique d'Étaples dans le Pas-de-Calais (France) — où les Britanniques installèrent le plus grand complexe hospitalier de tous les temps — et à Aldershot au Royaume-Uni, pourraient être à l'origine de l'épidémie. Le camp d'Étaples en particulier concentrait « tous les ingrédients pouvant favoriser l'émergence d'une pandémie grippale : surpeuplement, cochons vivant à proximité d'oies, de canards, de poulets et de chevaux, et gaz (certains mutagènes) utilisés en grande quantité »[6]. L'historien Pierre Darmon enfin a signalé plusieurs épidémies de pneumonies ayant touché les travailleurs annamites en France en 1917 et 1918[7] ;
- un rapport de recherches en 2014 de Michael Worobey, Guan-Zhu Han et Andrew Rambaut, validées par Neil M. Ferguson de l'Imperial College de Londres, situe les premières souches entre 1889 et 1900, sur des jeunes Américains ayant développé des anticorps, invalidant de fait la thèse d'une épidémie qui aurait été importée de Canton en 1918[8]. Selon le Professeur Berche, « De mauvaises conditions sanitaires, des populations affaiblies et de grands rassemblements. ». « On pense que la grippe espagnole est apparue d'abord au Kansas où elle a contaminé de jeunes soldats américains, qui étaient réunis trois mois dans des camps de formation militaire, à raison de 50 000 à 70 000 individus, avant de traverser le pays et de prendre la mer pour l'Europe »[9]. Trois thèses récentes appuient cette origine géographique du virus : le rapport de l'Oxford Academy, publié dans le magazine Evolution, Medicine, and Public Health, volume 2019, étudie les trois thèses qui avaient, jusque-là, été évoquées (États-Unis, France et Chine) et réfute la Chine arguant que les écrits de l'époque s'appuyaient uniquement sur des données symptomatiques, et non sur la science, la microbiologie en 1918 étant peu développée. Le rapport valide donc, données à l'appui, une origine vraisemblable au Kansas[10]. Loring Miner, un médecin du Kansas rural, rencontra des cas dans les premières semaines de 1918. Miner, alerté par le taux de mortalité envoya un rapport aux autorités sanitaires. Quelques semaines plus tard, l'un des premiers foyers épidémiques aurait éclaté, vers la base militaire de Fort Riley au nord-est de l'État. L'épidémie se serait propagée ensuite à la fois en Amérique du Nord et vers l'Europe, lors du débarquement de la force expéditionnaire américaine à Bordeaux en [6].
Les premiers cas
[modifier | modifier le code]
Les débuts de cette pandémie sont discrets, car le virus n'est pas initialement mortel : l'origine du virus-père de la grippe de 1918, dite « grippe espagnole », reste toujours incertaine, notamment car, à l'époque, les pays asiatiques ne tenaient aucune statistique ou répertoire recensant les patients qui auraient pu souffrir des mêmes symptômes.
Pour l'Europe, dès les années 1916-1917, la « pneumonie des Annamites » fait des ravages parmi les ouvriers ou soldats d’origine indochinoise présents en France, qui meurent de façon fulgurante de syndromes respiratoires aigus. Il est suspecté que cela soit la première vague de cette grippe[11]. Les travailleurs chinois du Chinese Labour Corps, organisés en service d'assistance pour les troupes britanniques dans le Nord de la France, ont peut-être apporté la grippe en Europe. En avril 1918, elle est dûment répertoriée dans un cantonnement britannique à Rouen[12]. L'épidémie se répand rapidement, par le biais des mouvements de troupes alliées, d'abord à Glasgow en Grande-Bretagne, au mois de mai[13], puis aux États-Unis, et enfin en Italie et en Allemagne, atteignant son apogée durant le mois de juin 1918, moment où les premiers cas sont signalés en Nouvelle-Écosse (Canada)[13].
Le premier cas enregistré officiellement aux États-Unis le se trouve dans le camp militaire de Funston (en) dépendant de Fort Riley au Kansas. Le patient zéro à cet endroit aurait été un certain Albert Gitchell, un fermier appelé sous les drapeaux, contaminé par l'un de ses oiseaux, lui-même contaminé par un oiseau sauvage[14]. La maladie s'y étend rapidement.
Tous ces pays sont en guerre et censurent les informations sur la maladie pour ne pas affecter le moral des populations. Aussi, quand en mai 1918 la grippe atteint l'Espagne, la presse espagnole est la première à en décrire les effets[15]. C'est pour cette raison que l'épidémie a souvent été qualifiée en Europe de « grippe espagnole »[16],[17],[a], sauf en Espagne où elle porte le sobriquet de « Soldat napolitain »[15].
En juillet, l'Europe considère l'épidémie comme pratiquement terminée, bien qu'ayant atteint un nombre élevé d'individus, surtout dans les armées, mais s'étant manifestée sans gravité, étant de courte durée, et avec des symptômes classiques peu alarmants.
Simultanément à ces épidémies internationales, d'autres foyers épidémiques plus restreints sont observés en Inde et en Nouvelle-Zélande, en juillet, et en Afrique du Sud, en août. On ignore aujourd'hui encore s'il s'agit d'une seule ou de différentes souches, toutes n'engendrant cependant que des symptômes bénins.
Septembre 1918 : l'épidémie et le continent américain
[modifier | modifier le code]Aux États-Unis, c'est dans la région de Boston, aux environs du , que les premiers cas mortels d'une grippe, bientôt tristement connue sous le nom de « grippe espagnole », sont signalés.
À compter de cette date, cette vague virale, bien qu'étant dans la lignée directe de la précédente, se caractérise par une mortalité 10 à 30 fois plus élevée que les épidémies grippales habituelles, soit un taux de mortalité moyen situé entre 2,5 et 3 % des grippés. Les symptômes, auparavant décrits comme bénins par un journal de l'époque, sont « une tendance à l’hémorragie [et] des attaques aux poumons, dont le résultat était souvent fatal. L’épidémie sévit avec plus de sévérité au mois d’octobre[13]. »
Du fait de sa grande contagiosité, l'épidémie se répand partout où les voyageurs contaminés, civils ou militaires, vont au gré des transports ferroviaires et maritimes de cette époque, inconscients du danger et de la puissance meurtrière de ce qu'ils portent. Dès le , dans l'ensemble du Nord-Est des États-Unis, des côtes américaines du golfe du Mexique, ainsi qu'en Californie et dans la majorité des grandes villes de l'Est américain, sont signalés des décès dus à la grippe : c'est le début d'une augmentation significative et anormale du nombre de cas mortels. Dans le même temps, les premiers cas sont répertoriés en Europe, la souche américaine ayant encore probablement renforcé l'épidémie par le biais de renforts américains venus aider les armées alliées. Une semaine plus tard, début , c'est l'ensemble du territoire des États-Unis et de l'Amérique du Nord qui est atteint. Il aura suffi de 15 jours à ce virus pour être présent sur l'ensemble du sous-continent Nord-Américain.
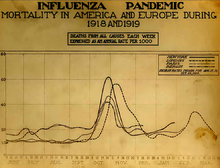
C'est alors seulement que l'épidémie prend réellement une ampleur considérable. En effet, si elle était déjà présente dans l'ensemble de ces territoires, le nombre de contaminés n'était pas encore très élevé. Et c'est seulement après sa dissémination que le nombre de contaminés explose.
Aussi, comme le montre le graphique ci-contre, c'est le mois d' qui voit le plus de cas mortels aux États-Unis : un taux de mortalité de près de 5 % chez les malades, soit, rapporté à la population entière (30 à 40 % de la population est atteinte), un taux de mortalité global de 2 %. L'État américain, ainsi que la population, prennent soudainement conscience de l'importance de cette épidémie.
C‘est sur le même schéma que l'Europe, puis le reste du monde, sont à leur tour atteints.
Octobre 1918 : l'épidémie devient pandémie
[modifier | modifier le code]


Les États-Unis sont brutalement submergés par cette épidémie nouvelle. Bon nombre de villes américaines sont paralysées du fait du grand nombre de malades, ainsi que du grand nombre de personnes refusant d'aller travailler. Alors que les médecins américains, désemparés, sans aucune information ou aide possible, font face à cette épidémie du mieux qu'ils le peuvent, une infirmière sur quatre meurt. Alors que cette épidémie, à son apogée de puissance aux États-Unis, y sème le chaos, le désarroi et surtout la mort, l'Europe compte ses premiers morts dans les rangs des militaires alliés. Avec son arrivée en Europe[23], ce virus devint international, ce qui annonce déjà son originalité.
Suivant la même évolution qu'aux États-Unis, la maladie, partant du Nord-Est de la France, conquiert bien vite l'ensemble des tranchées alliées ainsi que le territoire français et, du fait des mouvements de troupes britanniques, gagne la Grande-Bretagne.
Vers le , l'épidémie atteint, en France, puis en Angleterre, une importance considérable. Avec une à deux semaines de décalage, l'Espagne, l'Italie, l'Allemagne et l'ensemble des pays limitrophes comptent leurs premiers morts. De là, l'Europe étant à l'époque le centre colonisateur du monde, des bateaux, avec à leur bord des marins grippés, partent vers l'Afrique, l'Amérique du Sud, les Indes et la Chine, ainsi que vers l'Océanie, ces marins colportant vers ces terres alors encore épargnées une épidémie qui, de fait, devient alors pandémie.
Fin octobre et début novembre, d'abord en France et en Grande-Bretagne, ensuite dans l'Europe entière durant le mois de , l'épidémie devient aussi grave qu'aux États-Unis. Max C. Starkloff, médecin de la ville de Saint-Louis (Missouri) met en place un des premiers cas de distanciation sociale en médecine moderne[24], en ordonnant la limitation du nombre de personnes pouvant s'attrouper et en fermant les écoles. Saint-Louis a ainsi un des taux de mortalité les plus bas des États-Unis[25],[26] (moins de 60 pour 100 000 environ, six semaines après que les premiers cas ont été signalés[27]).
Cependant, les populations européennes, affaiblies par quatre ans de guerre et de pénuries, subissent des pertes, pires encore que celles des États-Unis, proportionnellement à leur population. Des villes entières sont paralysées, autant par la maladie que par sa crainte. Aux États-Unis, l'épidémie perd enfin de sa force, après deux mois de choc : septembre, mois de la propagation, et octobre, mois des morts.
En Europe, pour la France et la Grande-Bretagne, après une propagation en octobre (avec déjà un grand nombre de morts), c'est principalement novembre, en raison des infrastructures sanitaires débordées, qui voit les plus grandes vagues de mortalité. Pour les autres pays d'Europe, la période de propagation s'étend de mi-octobre à mi-novembre, celle du pic de mortalité, de mi-novembre à mi-décembre. La censure de guerre limite l'écho médiatique de la pandémie, les journaux annonçant qu'une nouvelle épidémie touchait surtout l'Espagne, pays neutre publiant librement les informations relatives à cette épidémie, alors que celle-ci fait déjà des ravages en France.
Parmi les comptoirs et colonies européennes, seule l'Australie est en mesure d'appliquer une quarantaine rigoureuse. Pour les autres, l'épidémie est inévitable : les Européens qui débarquent amènent avec eux le virus. À partir de début novembre 1918, le virus se répand très vite dans toute l'Afrique, l'Amérique latine, les Indes, la Chine ainsi qu'en Océanie. Le pourcentage de malades oscille entre 30 et 80 % de contaminés dans les populations locales, parmi lesquels de 1 à 20 % de cas mortels. Les vagues épidémiques, là aussi, durent de l'ordre de deux mois sur une région. La pandémie est donc enrayée vers le début de , avec un pic de mortalité en .
Après deux mois d'accalmie, de à , l'année 1919 voit étrangement une recrudescence importante du nombre de cas. Cette troisième « vague » est toutefois moins grave[28], les individus atteints lors des deux premières vagues présentant désormais une immunité et ne pouvant donc ni être contaminés ni colporter le virus. Ce retour de la pandémie déclenche des foyers épidémiques disséminés sur la planète, notamment dans les régions jusqu'alors épargnées, comme l'Australie, où il ne sera résorbé qu'en .
Certains pays seront encore touchés en 1919 et 1920 ; le dernier cas est signalé en , en Nouvelle-Calédonie[29].
En un peu plus d'un an, la pandémie aura fait finalement plus de victimes (voir les évaluations dans le chapeau) dans le monde que la Première Guerre mondiale entre et .
Propriétés
[modifier | modifier le code]Différentes mutations
[modifier | modifier le code]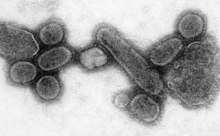
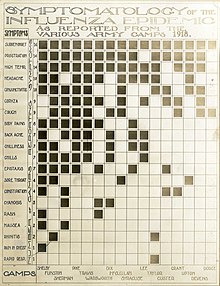
Les caractéristiques génétiques du virus ont pu être établies grâce à la conservation de tissus prélevés au cours d'autopsies récentes[Quand ?] sur des cadavres inuits et norvégiens conservés dans le pergélisol (sol gelé des pays nordiques). Ce virus est une grippe H1N1 dont l'origine aviaire est fortement suspectée à la suite de l'identification en 1999 de la séquence complète des 1 701 nucléotides du gène de l'hémagglutinine[30]. Le virus est à l'origine de trois vagues principales :
- « virus père », souche inconnue : virus de grippe source, à forte contagiosité mais à virulence normale (mortalité de 0,1 %) qui, par mutation, donna le virus de la grippe espagnole. Le virus père ne fut identifié qu'en par le médecin généraliste Loring Miner (de) du Comté de Haskell au Kansas et suivi rigoureusement qu'à partir d'avril (après une épidémie touchant des milliers de soldats américains dans le Camp Funston en mars), et jusqu'à (gagnant l'Europe lors du débarquement des troupes américaines à Brest, Bordeaux, Étaples), alors qu'il sévit probablement dès l'hiver 1917-1918 en Chine ;
- « virus de la grippe espagnole », souche H1N1 se révélant être de même origine que le « virus père » qui a muté, les personnes atteintes lors de la première vague sont en effet immunisées lors de la deuxième : virus à forte virulence apparu aux États-Unis (attesté à la parade de Philadelphie[31]) ; cette appellation inclut généralement aussi son « virus père ». Cette version plus létale (mortalité de 2 à 4 %) sévit en deux vagues meurtrières, l'une de mi-septembre à décembre 1918, l'autre de février à mai 1919. Tous les continents et toutes les populations ont été gravement touchés.
Origine du virus
[modifier | modifier le code]Du fait de l'absence d'étude sur des souches originales du virus de la grippe espagnole, aucune souche n'ayant pu être conservée, il est impossible de déclarer, aujourd'hui du moins, quelle est la source qui a vu apparaître le « virus père ». Il y a cependant deux hypothèses possibles concernant l'apparition du « virus père » de la grippe espagnole : la première est que ce virus proviendrait de la mutation d'un virus humain préexistant ; dans ce cas, il devrait n'être que faiblement différent de l'original et les populations humaines devraient, en bonne partie, être immunisées. La seconde est qu'il proviendrait d'une souche nouvelle, provenant d'une autre espèce, notamment les espèces aviaires, qui sont des réservoirs naturels de bon nombre de virus. C'est effectivement souvent ainsi qu'apparaissent les nouvelles souches de virus de la grippe : par l'interaction de populations humaines, porcines et aviaires.
Si cela demeurait inconnu à l'époque, il est désormais attesté que les différentes espèces d'oiseaux, notamment les canards domestiqués, sont des réservoirs naturels de quantité de virus et que ceux-ci peuvent, sous certaines conditions, se transmettre à d'autres espèces, tels les porcs. Or, le mode d'organisation traditionnel de la paysannerie mettait en contact direct et continuel les oiseaux de basse-cour, les porcs et les humains. Les populations porcines subissent ainsi continuellement l'assaut des virus grippaux aviaires, qu'ils ne craignent normalement pas du fait de la barrière des espèces. Mais ce contact continuel permet, le cas échéant, aux variantes des virus de s'adapter au système immunitaire mammalien. Et parce que le système immunitaire des porcs est proche de celui de l'homme, les virus grippaux aviaires peuvent donc atteindre ainsi l'homme.
Plusieurs études semblent pointer vers une origine aviaire du virus responsable de la grippe espagnole. En reconstituant le virus à partir d'un prélèvement issu d'une femme Inuit décédée en 1918 et conservée dans le pergélisol alaskain, des chercheurs américains ont découvert de fortes similitudes entre ce virus et des souches aviaires[32],[33],[34][source secondaire souhaitée]. Néanmoins, les chercheurs n'excluent pas la possibilité que le virus ait d'abord évolué parmi d'autres espèces de mammifères avant d'atteindre les populations humaines.
Ce que l'on sait de ce virus père tient en ses propriétés pathologiques. Il était somme toute assez commun : durée d'incubation très courte (de 1 à 2 jours), immense majorité de cas bénins et mortalité habituelle d'environ 0,15 %, soit un cas mortel sur 700 malades, particulièrement chez les vieillards et les nourrissons, comme c'est encore le cas aujourd'hui. Ces cas mortels n'étaient pas dus au virus lui-même mais, du fait de l'affaiblissement de l'organisme qu'il entraîne, à des complications de maladies normalement non mortelles (bronchite, pneumonie...).
Ce virus père ne diffère de ceux des autres grippes que par une contagiosité plus élevée qu'à l'accoutumée, lui permettant d'engendrer une épidémie timidement internationale, cela n'est pas encore assez pour être appelé pandémie.
Impact
[modifier | modifier le code]
Contagiosité
[modifier | modifier le code]Cette grippe se caractérise d'abord par une très forte contagiosité : deux fois plus élevée qu'une grippe saisonnière et légèrement supérieure à un simple rhume[35]. C'est cela qui lui permit de devenir une pandémie. Une fois arrivée en un lieu donné, l'épidémie s'étend rapidement car les malades transportent et propagent le virus durant les deux premiers jours de leur infection, tout en ne présentant aucun symptôme ; or dans ces cas, le virus avait contaminé dès la première semaine, avant même les premiers morts, une impressionnante partie de la population. La morbidité (proportion de cas de grippe dans une population) était extrême, près de 30 % de la population était atteinte après 15 jours.
Elle se caractérise ensuite par une période d'incubation de 2 à 3 jours, suivie de 3 à 5 jours de symptômes : fièvre, affaiblissement des défenses immunitaires, qui finalement permettent l'apparition de complications normalement bénignes, mais ici mortelles dans 3 % des cas, soit 20 fois plus que les grippes « normales ». Elle ne fait cependant qu'affaiblir les malades, qui meurent des complications qui en découlent.
Traitement médical
[modifier | modifier le code]Comme aucun vaccin adapté n'était disponible, ni de médicaments antiviraux pour traiter le virus, ni d'antibiotiques pour traiter les infections bactériennes secondaires[36],[37], les médecins s'appuyèrent sur un assortiment aléatoire de médicaments avec des degrés d'efficacité variables, tels que l'aspirine, la quinine, l'arsenic, la digitale, la strychnine, les sels d'Epsom, l'huile de ricin et certains dérivés de l'iode. Des traitements de médecine traditionnelle, telles que la saignée, la consommation d'alcool et de tabac, l'ayurveda en Inde, et le kanpo au Japon, ont également été pratiqués[12].
Mortalité
[modifier | modifier le code]
La mortalité importante était due à une surinfection bronchique bactérienne, mais aussi à une pneumonie due au virus. Le malade, prostré, se plaignait de douleurs dans la poitrine, son visage devenait violacé, une mousse sanguinolente s'échappait de ses lèvres. En quelques heures, plus de la moitié de ces cas se terminèrent par la mort[Information douteuse].
Un pic de mortalité de l'épidémie était observé du 15e au 30e jour de l'épidémie, suivi d'une décroissance lente du nombre de cas. Ce ne fut généralement qu'au bout de deux mois que l'épidémie s'essouffla, poursuivant ailleurs son œuvre.
Dans l'ensemble, ce ne fut non pas la grippe en elle-même, mais les complications pulmonaires qui la suivirent qui furent ainsi la cause principale des cas mortels. Avec les grippes précédentes, seuls 1 % des grippés présentaient des complications pulmonaires plus ou moins graves et, parmi ceux-ci, seuls 1 % des cas étaient mortels. Avec cette vague de grippe espagnole, ce fut près de 15 à 30 % des grippés qui présentèrent des complications pulmonaires, et environ 10 % de ces cas eurent une issue fatale. Soit, sur une population de 10 000 grippés, 100 complications pulmonaires, 1 décès pour les épidémies communes. Pour une épidémie de grippe espagnole, il y avait de 1 500 à 3 000 complications pulmonaires et de 150 à 300 décès. C'est-à-dire jusqu'à 300 fois plus de morts.
Immunisation des plus âgés
[modifier | modifier le code]Une spécificité de cette grippe est que le taux de mortalité a été anormalement haut pour la tranche d'âge de 20 à 40 ans, qui représentait 50 % des décès, avec un pic anormal de la mortalité autour de 30 ans[38], cette tranche d'âge étant habituellement et clairement la moins touchée.
L'atteinte préférentielle d'adultes jeunes pourrait peut-être s'expliquer par une relative immunisation des personnes plus âgées ayant été contaminées auparavant par un virus proche. Le Pr Julien Besançon[39] dans son livre Les jours de l'homme situe très précisément la date de cette immunisation. Il s'agit de l'épidémie de « grippe pneumonique » de 1885-1889 qui, à l'hôpital de la Pitié où il était interne, tua 2 malades sur 3.
Une autre hypothèse serait le système immunitaire de cette classe d'âge qui a trop vigoureusement réagi à ce nouveau virus, en déclenchant un choc cytokinique qui endommageait tous les organes, au point de tuer nombre de malades. D'autres chercheurs ont proposé que ce choc cytokinique était dû à une exposition à un tout jeune âge au virus de la « grippe russe » de 1889-1890[40],[38], peut-être causée par une souche d'influenza de type H3N8[41].
Bien que les personnes plus âgées (notamment vers 60 ans), les adolescents et les nourrissons aient subi une morbidité particulièrement élevée, ils ne subirent pourtant pas davantage de pertes (mortalité) qu'à l'accoutumée. Le nombre de complications pulmonaires ainsi que la mortalité restent étrangement faibles au regard de la virulence de cette épidémie et de leur grande vulnérabilité habituelle face aux grippes, telle celle de 1957, ou d'autres, même anodines. La cause de ces anomalies de répartition de la mortalité, ainsi que de sa forte mortalité, plus encore celle des adultes, reste aujourd'hui encore inconnue.
Autres conséquences
[modifier | modifier le code]Avec un système immunitaire très affaibli, pour les malades guéris de cette grippe entre fin 1918 et l'hiver 1918-1919, les complications au niveau de l'organisme restaient très présentes, des années après[réf. nécessaire] : ainsi, par exemple, une femme qui attendait un enfant en 1922 après avoir été malade durant l'hiver 1918-1919 pouvait décéder lors de l’accouchement. Les conséquences sanitaires de l'impact de cette pandémie furent ainsi mésestimées sur le long terme par les autorités sanitaires des pays concernés. Cependant, pour les chercheurs et les historiens, des données sont encore disponibles dans les archives médicales et sanitaires de certains pays.
Plusieurs études laissent penser que cette épidémie pourrait avoir été à l'origine d'un premier baby-boom (y compris dans des pays neutres) après la guerre[42].
Gestes barrières
[modifier | modifier le code]La grippe fut l'occasion de déployer certains gestes barrières : lavage des mains, interdiction de cracher dans la rue, interdiction des attroupements, « rester chez soi » (en anglais, « shelter-in-place (en) »), port du masque, mise en quarantaine, fermeture d'écoles, interdiction de services religieux, fermeture de divertissements publics, interdiction de l'affluence dans les commerces[43].
Toutefois, les réglementations des gestes barrières variaient selon les régions et les pays. Aux États-Unis par exemple, la ville de Seattle se protégea plus que Philadelphie[43], tandis qu'à San Francisco une controverse apparut autour de l'obligation de porter des masques, culminant dans la Ligue anti-masque qui parvint à faire lever cette obligation en février 1919, lors de la seconde vague d'infections dans la ville[44].
Autre exemple, en France, pays englué dans la Première Guerre mondiale depuis 1914, avec des combats sur une partie de son territoire, aucune mesure générale n'est prise par les autorités jusqu'en août 1918. Les premières décisions coercitives sont prises en automne 1918. L’État publie alors des circulaires invitant les préfets à prendre des mesures d’hygiène contre la propagation de l’épidémie : fermer les écoles et théâtres, éviter les rassemblements, désinfecter les transports, etc. Leur mode d'application concrète est laissé à l'initiative des préfets et des municipalités. Il paraît difficile d’ordonner des mesures générales alors que la circulation du virus est mal cernée : « Les autorités n’avaient pas de représentation exacte de la géographie de l’épidémie. ». De plus, toute mesure générale risque de devenir un signe de faiblesse en direction de l’ennemi. Les décisions locales sont plus discrètes. Des consignes de distanciation physique existent aussi, mais elles sont appliquées dans les hôpitaux et ne sont pas préconisées à l’ensemble de la population[45].
Bilan humain
[modifier | modifier le code]
On a par ailleurs constaté que la pandémie de 1918-1919 fut essentiellement caractérisée par trois faits :
- une proportion de population infectée élevée, évaluée à 500 millions soit 27 % de la population mondiale de 1,8 à 1,9 milliard d'habitants en 1918[46]. Ceci s'expliquant par le fait qu'il s'agissait d'un virus grippal de type nouveau vis-à-vis duquel la population ne possédait aucune immunité ;
- un taux de mortalité induit (ce n'est souvent pas la grippe qui tue directement) inhabituellement important pour une grippe, dans une fourchette estimée de 2 à 10 % des personnes infectées. De 20 à 50 millions de personnes selon le site de l'institut Pasteur[47], voire jusqu'à 100 millions selon certaines réévaluations récentes, en périrent[48],[49] ;
- une courbe de mortalité inhabituelle, avec un pic sur les 20–40 ans, notamment aux alentours de 30 ans[50],[51].
Un article dans le Lancet en 2006, réalisé par des chercheurs qui ont étudié les registres de décès de 27 pays, montre que la mortalité due à cette grippe varie d'un facteur 30 selon les régions, corrélée au revenu économique moyen par habitant : à 10 % de revenu moyen en plus par habitant correspond une baisse de 10 % de la mortalité (corrélation linéaire inversement proportionnelle). Le lien entre la mortalité de cette épidémie et la pauvreté est ainsi établi[52].
Plus précisément, au cours de ces différentes vagues, il y eut 549 000 décès aux États-Unis, premier pays touché. En France, une étude fait état de 240 000 morts dont 33 000 dans l'armée, au Royaume-Uni de 153 000, en Allemagne de 426 000 morts, au total 2 300 000 pour 14 pays d'Europe occidentale (donc vraisemblablement plus de 4 000 000 pour l'ensemble de l'Europe en comprenant l'Autriche-Hongrie, les autres pays d'Europe orientale et la Russie)[53]. Dans les principaux pays belligérants, à l'exception des États-Unis entrés tardivement le conflit, la pandémie survenue dans des sociétés meurtries depuis 4 ans, a été cependant moins meurtrière que la guerre qui a coûté, dans son ensemble, la vie à 18 600 000 personnes, y compris les victimes civiles, en grande majorité en Europe.
La grippe espagnole a frappé plus massivement les pays n'ayant pas ou peu participé au conflit. Dans l'ensemble du monde, la grippe a fait plus de morts que la guerre[54].
En Inde, il y aurait eu au minimum 18,5 millions de morts, soit 6 % de la population, en Chine, de 4 à 9,5 millions, soit 0,8 à 2 % de la population — ce nombre ne pouvant être estimé, dans ces deux pays, que dans une fourchette très large[55] —, au Japon, près de 250 000.
En Océanie, le bilan relatif varie selon les pays. Le gouvernement des Samoa américaines isola l'archipel et parvint à protéger sa population. À l'inverse, les autorités néo-zélandaises des Samoa occidentales firent preuve de négligence et 90 % de la population fut infectée. 30 % de la population adulte masculine, 22 % des femmes et 10 % des enfants périrent. Des navires quittant les ports néo-zélandais apportèrent la grippe aux Tonga, à Nauru et aux Fidji ; les taux de mortalité s'y élevèrent à 8 %, 16 % et 5 %, respectivement[56]. Le taux de mortalité en Nouvelle-Zélande elle-même fut de 5 %[57].
Pour les autres pays, tels que les colonies africaines, l'Amérique du Sud et la Russie (alors en pleine refonte communiste), il n'est fait mention nulle part de quelconques statistiques, mais on peut, en fonction des populations de l'époque et de la mortalité moyenne, y estimer le nombre de morts total à près de 6 millions. On obtient ainsi au minimum de 20,5 millions à 21,5 millions de morts dus à cette pandémie, des évaluations atteignant jusqu'à 100 millions.
Après plus de 50 millions de morts emportés par la guerre et cette grippe, la pandémie s'achève définitivement vers le début de l'été 1919. En fait, elle s'est scindée en une lignée spécifiquement porcine et une spécifiquement humaine puis est devenue par la suite une grippe saisonnière sous une forme beaucoup moins virulente, évoluant par vagues tous les ans jusqu'à aujourd'hui (le virus père H1N1 étant repéré jusqu'en 1957, date à partir de laquelle il s'est réassorti en virus de type A, souche H2N2 de la « grippe asiatique », puis virus de type A, souche H3N2 de la « grippe de Hong Kong » de 1968), les grippes humaines actuelles provenant toutes du virus de 1918 à partir de combinaisons, mutations ou réassortiments[58].
Répercussions scientifiques
[modifier | modifier le code]Du fait, sans doute, de la priorité militaire de l'époque, et malgré la virulence de cette pandémie mondiale, aucune étude scientifique approfondie ne fut entreprise. Seuls quelques médecins isolés comme Loring Miner (de) écrivirent de petits traités exposant les symptômes constatés, des statistiques de contamination ou de taux de mortalité. Les rares prélèvements conservés (par exemple dans de la paraffine solide) s'avèrent aujourd'hui dégradés et inutilisables[58].
Aucune souche n'ayant pu être conservée, aucune étude n'a pu être faite sur l'origine de sa contagiosité et de sa virulence, l'une comme l'autre restant inexpliquées jusqu'en 1950, date à laquelle le chercheur Johan Hultin (en) découvre des tissus contenant des traces du virus sur des corps d'Inuits enterrés dans le permafrost d'Alaska[59].
Cette pandémie a fait prendre conscience de la nature internationale de la menace des épidémies et maladies, et des impératifs de l'hygiène et d'un réseau de surveillance pour y faire face. Le Comité d'hygiène de la Société des Nations (SDN), ancêtre de l'OMS, a été créé à la suite de cette épidémie.
Victimes notables
[modifier | modifier le code]- Rodrigues Alves, président du Brésil[60].
- Guillaume Apollinaire, poète français[60].
- Louis Botha, Premier ministre de l'Union d'Afrique du Sud[60].
- Pascal Ceccaldi, journaliste et député français.
- John H. Collins, acteur, scénariste et réalisateur américain.
- Les frères John Francis Dodge et Horace Dodge, ingénieurs et constructeurs automobiles américains.
- Myrtle Gonzalez, actrice américaine.
- Joe Hall, joueur de hockey sur glace britannique.
- Vera Kholodnaïa, première « reine de l'écran » du cinéma russe.
- Marie Lenéru, dramaturge française.
- Meri Te Tai Mangakāhia, suffragette maorie néo-zélandaise.
- Jacinta Marto et Francisco Marto (tous deux canonisés en 2013), enfants portugais, témoins des apparitions mariales de Fátima.
- Léon Morane, pionnier français de l'aéronautique.
- Edmond Rostand, dramaturge, écrivain et metteur en scène français[60].
- Egon Schiele, peintre autrichien[60].
- Humbert de Savoie-Aoste, membre de la Maison royale d'Italie;
- Amadeo de Souza-Cardoso, peintre portugais.
- Erik de Suède, prince suédois.
- Iakov Sverdlov, homme d’État et révolutionnaire russe.
- Mark Sykes, conseiller britannique mort à Paris pendant les accords Sykes-Picot[60].
- Frederick Trump, homme d'affaires, grand-père de Donald Trump, président des États-Unis de 2017 à 2021.
- Max Weber, juriste, économiste et sociologue allemand considéré comme l'un des fondateurs de la sociologie[61].
Documentaire
[modifier | modifier le code]- 2005 : Les chroniques de l'insolite - La Grande Épidémie réalisé par Stéphane Bégoin.
- 2021 : La Grippe espagnole, la grande tueuse réalisé par Paul Le Grouyer et Lucie Pastor[62],[63].
Notes et références
[modifier | modifier le code]Notes
[modifier | modifier le code]- Également parce que le roi Alphonse XIII en est rapidement tombé malade. Le terme de grippe espagnole s'est répandu largement, mais en Espagne on l'a appelée grippe française[18], en Allemagne grippe des Flandres[19], au Sénégal grippe brésilienne, au Brésil grippe allemande, en Pologne grippe bolchévique et en Perse, grippe britannique[20],[21],[22].
Références
[modifier | modifier le code]- (en) Jeffery K Taubenberger et David M Morens, « 1918 Influenza: the mother of all pandemics », Emerging Infectious Diseases, CDC, vol. 12, no 1, , p. 15-22 (ISSN 1080-6040 et 1080-6059, OCLC 31848353, PMID 16494711, PMCID 3291398, DOI 10.3201/EID1201.050979)
- « La grippe espagnole de 1918, la plus grande pandémie de l'histoire de l'humanité », sur rcf.fr (consulté le )
- (en) « Why the coronavirus outbreak isn’t likely to be a repeat of the 1918 Spanish flu », sur latimes.com (consulté le )
- (en) Chris Patten, What Next ? Surviving the Twenty-first Century, Penguin UK, , p. 121.
- Patrick Berche, Faut-il encore avoir peur de la grippe ? Histoire des pandémies, Odile Jacob, , p. 128.
- Karl Feltgen 2007, p. 17.
- Pierre Darmon, « La grippe espagnole submerge la France », L'Histoire, no 281, novembre 2003, p. 79-85.
- Genesis and pathogenesis of the 1918 pandemic H1N1 influenza A virus, pnas.org du 28 avril 2014, consulté le 19 mars 2020.
- L'origine du virus de la grippe espagnole de 1918 enfin précisée, lefigaro.fr du 29 avril 2014, consulté le 19 mars 2020.
- (en) Michael Worobey, Jim Cox, Douglas Gill, « The origins of the great pandemic », oup.com, 21 janvier 2019, consulté le 19 mars 2020.
- « Retour sur la grippe espagnole : « On pensait en avoir fini avec les grandes épidémies. Et patatras, 240 000 morts » », Le Monde.fr, (lire en ligne, consulté le ).
- (en) « The 1918 Spanish Flu Pandemic, the Origins of the H1N1-virus Strain, a Glance in History ».
- « Leçons tirées de l'influenza pandémique », Le Pays, 20 septembre 2019, p. 4.
- « Comment la grippe espagnole a pu faire jusqu'à 100 millions de morts », documentaire de 2018 produit par la BBC et diffusé sur RMC Story.
- Spinney 2018, p. 63-64.
- « L'origine du virus de la grippe espagnole de 1918 enfin précisée », sur sante.lefigaro.fr, (consulté le ).
- « Grippe espagnole : le mystère de son origine enfin résolu », sur Science et Avenir, .
- Philippe Chassaigne, Les Sociétés, la Guerre, la Paix : 1911-1946, Sedes, , 286 p. (ISBN 978-2-301-00205-1, lire en ligne), « Glossaire ».
- Marine Dumeurger, « La grippe espagnole : le tueur invisible de 1918 », sur Geo.fr, (consulté le ).
- Spinney 2018, p. 64
- « La mère de toutes les pandémies », Courrier international, no 1528, 13-19 février 2020, p. 46-47.
- (de) Stefan Schmitt et Anna-Lena Scholz, « Die Mutter aller Pandemien », Die Zeit, nos 6/2020, (présentation en ligne).
- Les troupes confinées à bord des navires, dont le SS Leviathan, se contaminent rapidement. In La grande grippe 1918. La pire épidémie du siècle, Freddy Vinet - Présentation en ligne.
- (en) « How Public Health Policies Saved Citizens in St. Louis During the 1918 Flu Pandemic », bioMérieux Connection, (consulté le ).
- « St. Louis, Missouri and the 1918-1919 Influenza Epidemic », The American Influenza Epidemic of 1918: A Digital Encyclopedia, (consulté le ).
- Roos, « How U.S. Cities Tried to Halt the Spread of the 1918 Spanish Flu », HISTORY, (consulté le ).
- McKinsey, McKinsey et Enriquez, « The 1918 Influenza in Missouri: Centennial Remembrance of the Crisis », Missouri Medicine, vol. 115, no 4, jul–aug 2018, p. 319–324 (ISSN 0026-6620, OCLC 7850378090, PMID 30228752, lire en ligne, consulté le ).
- Freddy Vinet et Florent Georgesco, « Retour sur la grippe espagnole : On pensait en avoir fini avec les grandes épidémies. Et patatras, 240 000 morts », Le Monde, (lire en ligne)
- (en) G. Dennis Shanks, Nick Wilson, Rebecca Kippen, John F Brundage, « The unusually diverse mortality patterns in the Pacific region during the 1918–21 influenza pandemic: reflections at the pandemic's centenary », The Lancet, vol. 18, no 10, , p. 323 (ISSN 1473-3099, DOI 10.1016/S1473-3099(18)30178-6).
- (en) Mark J. Gibbs et Adrian J. Gibbs, « Molecular virology : Was the 1918 pandemic caused by a bird flu ? », Nature, vol. 440, no 7088, , E8-E8 (DOI 10.1038/nature04823).
- (en) Flu by Eileen A. Lynch. The devastating effect of the Spanish flu in the city of Philadelphia, PA, USA.
- (en) Ann H. Reid, Thomas G. Fanning, Johan V. Hultin et Jeffery K. Taubenberger, « Origin and evolution of the 1918 “Spanish” influenza virus hemagglutinin gene », Proceedings of the National Academy of Sciences, vol. 96, no 4, , p. 1651–1656 (ISSN 0027-8424 et 1091-6490, PMID 9990079, PMCID PMC15547, DOI 10.1073/pnas.96.4.1651, lire en ligne, consulté le )
- (en) Ann H. Reid, Thomas G. Fanning, Thomas A. Janczewski et Jeffery K. Taubenberger, « Characterization of the 1918 “Spanish” influenza virus neuraminidase gene », Proceedings of the National Academy of Sciences, vol. 97, no 12, , p. 6785–6790 (ISSN 0027-8424 et 1091-6490, PMID 10823895, PMCID PMC18739, DOI 10.1073/pnas.100140097, lire en ligne, consulté le )
- (en) Jeffery K. Taubenberger, Ann H. Reid, Raina M. Lourens et Ruixue Wang, « Characterization of the 1918 influenza virus polymerase genes », Nature, vol. 437, no 7060, , p. 889–893 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/nature04230, lire en ligne, consulté le )
- « Coronavirus : quelles sont la contagiosité et la létalité du virus ? », Le Monde.fr, (lire en ligne, consulté le ).
- (en) Amy Sarah Ginsburg et Keith P. Klugman, « COVID-19 pneumonia and the appropriate use of antibiotics », The Lancet Global Health, vol. 8, no 12, , e1453–e1454 (ISSN 2214-109X, PMID 33188730, DOI 10.1016/S2214-109X(20)30444-7, lire en ligne, consulté le )
- « Les surinfections bactériennes », sur Institut Pasteur de Lille (consulté le )
- Alain Gagnon, Matthew S. Miller, Stacey A. Hallman et Robert Bourbeau, « Age-Specific Mortality During the 1918 Influenza Pandemic: Unravelling the Mystery of High Young Adult Mortality », PLoS ONE, vol. 8, no 8, , e69586 (ISSN 1932-6203, DOI 10.1371/journal.pone.0069586, lire en ligne, consulté le ).
- https://www.idref.fr/06878063X
- G. Dennis Shanks et John F. Brundage, « Pathogenic Responses among Young Adults during the 1918 Influenza Pandemic », Emerging Infectious Diseases, vol. 18, no 2, , p. 201–207 (ISSN 1080-6040 et 1080-6059, DOI 10.3201/eid1802.102042, lire en ligne, consulté le )
- M. Worobey, G.-Z. Han et A. Rambaut, « Genesis and pathogenesis of the 1918 pandemic H1N1 influenza A virus », Proceedings of the National Academy of Sciences, vol. 111, no 22, , p. 8107–8112 (ISSN 0027-8424 et 1091-6490, DOI 10.1073/pnas.1324197111, lire en ligne, consulté le )
- S.-E. Mamelund, « La grippe espagnole de 1918 est-elle responsable du baby-boom de 1920 en Norvège ? Le cas d'un pays neutre », Population, vol. 59e année, no 2, , p. 269-301 (lire en ligne).
- (en) Nancy K. Bristow, « US responses 1918 flu pandemic offer Stark lessons coronavirus now », The Guardian, (lire en ligne).
- (en) Centre pour l'histoire de la médecine de l'Université du Michigan, « San Francisco, California and the 1918-1919 Influenza Epidemic | The American Influenza Epidemic of 1918: A Digital Encyclopedia », sur influenzaarchive.org (consulté le )
- Assma Maad, « Peut-on comparer les mesures prises face à la grippe espagnole de 1918 et face au Covid-19 ? », Le Monde, (lire en ligne)
- (en) Jeffery K. Taubenberger, David M. Morens, « 1918 Influenza: the Mother of All Pandemics », Emerging infecteous diseases journal, (lire en ligne).
- Site pasteur.fr, page "Grippe", consulté le 29 avril 2020
- Site rts.ch, page "Comment la grippe espagnole a pu faire jusqu'à 100 millions de morts", consulté le 29 avril 2020
- Site lejournaldumedecin.com, consulté le 29 avril 2020
- Institut Pasteur, « Grippe », sur pasteur.fr.
- Johnson N.P., Mueller J. « Updating the accounts: global mortality of the 1918-1920 “Spanish” influenza pandemic. », Bull Hist Med., printemps 2002, 76(1), p. 105-15. Citation : « This paper suggests that it was of the order of 50 million. However, it must be acknowledged that even this vast figure may be substantially lower than the real toll, perhaps as much as 100 % understated. » Résumé.
- (en) Christopher JL Murray et coll., « Estimation of potential global pandemic influenza mortality on the basis of vital registry data from the 1918—20 pandemic: a quantitative analysis », The lancet, vol. 368, no 9554, , p. 2211-2218 (lire en ligne).
- (en) Séverine Ansart, « Mortality burden of the 1918–1919 influenza pandemic in Europe », US National Library of Medecine National Institutes of Health, (lire en ligne).
- Anne Rasmussen, « Aucune autre pandémie dans l’histoire n’a autant tué» que la grippe espagnole », Le Temps, (lire en ligne).
- (en) Niall Johnson, Britain and the 1918-19 Influenza Pandemic, Routledge, , p. 77-80.
- (en) Donald Denoon, « New Economic Orders : Land, Labour and Dependency », The Cambridge History of the Pacific Islanders, Cambridge University Press, , p. 247 (ISBN 0-521-00354-7).
- (en) Malama Meleisea, Lagaga : A Short History of Western Samoa, University of the South Pacific, (ISBN 982-02-0029-6), p. 130.
- Patrick Berche, Faut-il encore avoir peur de la grippe ? Histoire des pandémies, Odile Jacob, , 278 p. (ISBN 2738127592).
- « (en) Researchers Reconstruct 1918 Pandemic Influenza Virus; Effort Designed to Advance Preparedness Retrieved », sur Center for Disease Control, .
- Charles de Saint-Sauveur, « : une saison en enfer avec la grippe espagnole », sur Le Parisien, (consulté le ).
- Louis Begley, Franz Kafka, Odile Jacob, , p. 227.
- « « La Grippe espagnole, la grande tueuse », sur France 2 : dix-huit mois d’enfer sur Terre », Le Monde.fr, (lire en ligne, consulté le )
- « La grippe espagnole, la grande tueuse » (consulté le )
Voir aussi
[modifier | modifier le code]Bibliographie
[modifier | modifier le code]- Documents de la conférence de l'Institut Pasteur : La Grippe espagnole de 1918.
- Avner Bar-Hen et Patrick Zylberman, « La presse parisienne et la grippe « espagnole » (1918-1920) », Les Tribunes de la santé, no 47 « La santé à la une », , p. 35-49 (lire en ligne).
- Pierre Darmon, « Une tragédie dans la tragédie : la grippe espagnole en France (avril 1918-avril 1919) », Annales de démographie historique, no 2, , p. 153-175 (lire en ligne).
- (en) Ryan A. Davis, The Spanish Flu : Narrative and Cultural Identity in Spain, 1918, Basingstoke, Palgrave Macmillan, , XIII-255 p. (ISBN 978-1-137-33920-1 et 978-1-349-46439-5).
- Karl Feltgen (docteur), « La grippe « espagnole » à Rouen », Études normandes, no 1 (56e année) « Images et Perspectives », , p. 15-30 (lire en ligne).
- Claude Hannoun, La Grippe, éd. Techniques EMC (Encyclopédie médico-chirurgicale), Maladies infectieuses, 8-069-A-10, 1993.
- Jacques Houdaille, « La grippe espagnole, la mal nommée », Population, Paris, Éditions de l'INED, no 1 (28e année), , p. 136-137 (lire en ligne).
- Olivier Lahaie, « L'épidémie de grippe dite « espagnole » et sa perception par l’armée française (1918-1919) », Revue historique des armées, no 262, , p. 102-109 (lire en ligne).
- Laura Spinney (trad. Patrizia Sirignano), La Grande tueuse : comment la grippe espagnole a changé le monde [« Pale Rider : The Spanish Flu of 1918 and How it Changed the World »], Paris, Albin Michel, , 414 p. (ISBN 978-2-226-43195-0).
- (en) J. Tautenberger et coll., « Characterization of the 1918 influenza virus polymerase genes », Nature, 6 octobre 2005.
- (en) T. Tumpey T et coll. « Characterization of the reconstructed 1918 spanish influenza pandemic virus », Science 2005, pp. 77-80.
- Freddy Vinet, La grande grippe : 1918, la pire épidémie du siècle : histoire de la grippe espagnole, Paris, Vendémiaire, coll. « Chroniques », , 259 p. (ISBN 978-2-36358-301-7).
- (en) Michael Worobey, Guan-Zhu Han et Andrew Rambaut, « Genesis and pathogenesis of the 1918 pandemic H1N1 influenza A virus » [« Genèse et pathogenèse du virus de la grippe pandémique A (H1N1) de »], Proceedings of the National Academy of Sciences, vol. 111, no 22, , p. 8107-8112 (PMID 24778238, PMCID PMC4050607, DOI 10.1073/pnas.1324197111, résumé, lire en ligne [PDF], consulté le ).
- André Minet, « La grippe espagnole en Pays Tarnais : quand le virus prenait le train … », Société culturelle du Pays castrais, Castres, t. cahier n° 48, (ISBN 978-2-904401-85-5)
Articles connexes
[modifier | modifier le code]- Grippe espagnole en Suisse
- Grippe asiatique
- Grippe de Hong Kong
- Grippe A (H1N1) de 2009
- Risque pandémique lié à la grippe aviaire
- Grippe aviaire
- Ligue anti-masque de San Francisco
- Pandémie de Covid-19
Liens externes
[modifier | modifier le code]
- Ressources relatives à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :
- "La grippe espagnole 1914-1918", Concordance des temps, France-culture, [1]
- (en) La grippe espagnole, État par État aux USA
- (en) Données historiques, témoignages. Un site bien réalisé de l'administration américaine.
- Deux rapports de 1919, riches en statistiques (tableaux, graphiques) concernant les taux de morbidité, mortalité, les dates et lieux de début des foyers dans la population militaire des États-Unis lors de la pandémie de 1918, dans la marine et l'armée américaines :


