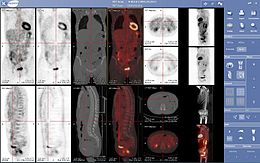
Médecine nucléaire
| Partie de |
Médecine, sciences cliniques (d), radiologie |
|---|---|
| Pratiqué par |
Médecin nucléaire (en) |
La médecine nucléaire comprend l'ensemble des applications médicales de la radioactivité en médecine.
Administrativement on parle de l'utilisation de sources radioactives non scellées.
On administre au patient (par injection intraveineuse, ingestion, inhalation...) des médicaments radiopharmaceutiques (MRP) ; ceux-ci peuvent être des radionucléides isolés (comme l'iode 123 pour la glande thyroïde) ou être constitués d'un vecteur et d'un radionucléide. Une molécule « vectrice » qui fait partie du métabolisme humain va être attirée vers un organe cible ou tracer une fonction de l'organisme. Le radionucléide-traceur rattaché émet des rayonnements ionisants qui peuvent être détectés (imagerie ou scintigraphie) ou servir à détruire des cellules (radiothérapie interne vectorisée). Cette méthode est très sensible et permet des diagnostics ou des traitements. Celle-ci vient souvent en complément d’une radio, échographie ou IRM.
Les différents domaines d'application sont :
- l'imagerie fonctionnelle in vivo qui consiste en l'administration d'un traceur radioactif au patient permettant sa détection externe. Ce sont les scintigraphies (émission de rayonnements gamma) ou les tomographies par émission de positons (TEP) ;
- la radiothérapie métabolique qui traite des maladies bénignes (hyperthyroïdie, polyglobulie de Vaquez...) ou des maladies malignes (cancers thyroïdiens, métastases de cancer de la prostate...) ;
- le diagnostic biologique in vitro : la radio-immunologie.
La médecine nucléaire est une spécialité médicale complète à la fois diagnostique (in vivo et in vitro) et thérapeutique.
Histoire[modifier | modifier le code]
La découverte en 1934 par Frédéric et Irène Joliot-Curie des isotopes radioactifs (radionucléides) produits artificiellement marque l’émergence de cette nouvelle discipline médicale.
Les premières applications des radio-isotopes ont été thérapeutiques. En 1936, le phosphore 32 est utilisé dans le but de traiter une leucémie[1]. En 1938, John Livingood et Glenn Seaborg réussissent à mettre au point la production d’iode 131. En 1941 de l’iode radioactif est administré à des patients souffrant d’hyperthyroïdie.
En 1946, Samuel Seidlin, Leonidas Marinelli et Eleanor Oshry montrent que l’ensemble des métastases d’un patient atteint d’un cancer de la thyroïde peuvent être détruites à la suite d'un traitement à l’iode 131. Ce traitement reste aujourd’hui encore la méthode la plus efficace dans ce cas de cancer.
La première gamma caméra est développée en 1957 par Hal Anger et permet de mesurer la radioactivité de toute une surface en une fois.
En 1963 Henri Wagner réalise les premières images pulmonaires en utilisant des agrégats d’albumine radiomarqués. En 1978, David Goldenberg utilise des anticorps marqués pour l’imagerie de tumeurs chez l’homme. La scintigraphie émerge en 1962 sous l’impulsion de David Kuhl.
En 1971, la médecine nucléaire est reconnue comme une spécialité médicale par l’American Medical Association[2].
Actuellement en France la médecine nucléaire est une spécialité médicale reconnue.
Diagnostic[modifier | modifier le code]
Principe général[modifier | modifier le code]
En médecine nucléaire le patient reçoit un radiopharmaceutique par voie intraveineuse, par voie orale, ou par inhalation suivant l'examen ou la thérapie à réaliser.
En scintigraphie (imagerie de médecine nucléaire), les images (pour le diagnostic) sont réalisées à l'aide de détecteurs externes (les gamma-caméras) qui sont des détecteurs proportionnels des rayonnements ionisants (émetteurs de photons) et permettent la réalisation d'image mais aussi des quantifications. Ce procédé est différent du diagnostic par rayons X, où le rayonnement est externe et traverse le corps pour former une image. L'imagerie nucléaire permet d’observer une fonction de l'organisme alors que la radiologie (et notamment le scanner X) fournit des informations sur la structure. Il s'agit d'une imagerie fonctionnelle, par opposition à l'imagerie anatomique.
Actuellement on couple de plus en plus des gamma-caméras avec des scanners ou des IRM permettant la réalisation d'images de fusion donnant en un seul examen l'information structurelle et l'information physiologique ou métabolique.
On peut ainsi explorer la plupart des métabolismes : hépato-biliaire, thyroïdien, ventilation et perfusion pulmonaire, structure et fonctionnement du rein et de l'arbre urinaire, métabolisme osseux (recherche de fractures, métastases, algoneurodystrophie), métabolisme du cerveau, du tube digestif (notamment la vidange gastrique), fonction ventriculaire gauche, fonction du tissu myocardique du ventricule gauche... L'apport récent des scintigraphies par émetteurs de positrons a encore accru les possibilités diagnostiques.
La médecine nucléaire se prête à la quantification. En effet le résultat de la mesure de la radioactivité lors d'un examen est proportionnel au volume ou à l'activité fonctionnelle.
Certaines techniques permettent une reconstruction dynamique (mouvement) par superposition d'images prises à des temps différents (cœur, rein).
Deux techniques de scintigraphie sont actuellement utilisées :
- la tomographie par émission monophotonique (TEMP) ;
- la tomographie par émission de positons (TEP).
Elles n'ont cependant pas fait totalement disparaître les scintigraphie planaires, dynamiques.
La scintigraphie[modifier | modifier le code]
Le principe de la scintigraphie, consiste en l'administration au patient d'une très petite quantité de radiopharmaceutique. Les rayonnements photoniques émis par le radiopharmaceutique, concentrés dans un organe ou tracés dans une fonction sont détectés par une gamma caméra. En scintigraphie, on utilise des radiopharmaceutiques contenant un radio-isotope émetteur de rayons gamma.
Une fois fixé sur la partie ciblée, le radiopharmaceutique émet les rayons gamma qui sont détectés par une caméra à scintillation communément appelé gamma caméra. Ces informations sont ensuite traitées par ordinateur à l’aide d’un algorithme de reconstruction afin d'obtenir l’image 2D ou 3D de la partie du corps ciblée.
On distingue notamment les explorations suivantes :
- la scintigraphie myocardique permet d’étudier la perfusion du myocarde, c'est-à-dire le flux sanguin arrivant dans le muscle cardiaque, notamment du ventricule gauche (permettant le diagnostic d'angor ou de séquelles d'infarctus du myocarde) ;
- la scintigraphie des cavités cardiaques qui permet de mesurer la fraction d'éjection ventriculaire (notamment gauche) paramètre important dans le suivi de certains traitements chimiothérapeutiques cardiotoxiques ;
- la scintigraphie pulmonaire permet d'imager les fonctions de ventilation et perfusion du poumon, afin de diagnostiquer une embolie pulmonaire. C'est actuellement la méthode de référence de ce diagnostic en particulier chez la femme enceinte ;
- la scintigraphie osseuse permet de visualiser l'augmentation du renouvellement osseux. Elle est indiquée dans les recherches de fractures (syndrome de Silverman ou des enfants battus, fractures passées inaperçues à la radiographie...), de neuro-algo-dystrophie ou la recherche en un seul examen de métastases osseuses des cancers ostéophiles (sein, rein, thyroïde, prostate, poumon) ;
- la scintigraphie rénale dynamique permet d’étudier la captation et l'évacuation par les reins d'un traceur. La scintigraphie au DMSA permet de visualiser les séquelles ou cicatrices post infection ;
- la scintigraphie cérébrale permet d’analyser la distribution d’une perfusion dans le cerveau. Or dans certaines maladies dégénératives (Alzheimer, démences fronto-temporales) , les anomalies de perfusion intéressent des zones précises du cerveau, ce qui permet d'orienter le diagnostic. On peut utiliser aussi la scintigraphie au Datscan pour faire le diagnostic dans les syndromes Parkinsonniens ;
- la scintigraphie thyroïdienne est aussi utilisée pour distinguer les différentes formes d'hyperthyroïdies (maladie de Basedow, goitre basedowifié, nodules chauds, nodules toxiques...) ;
- la scintigraphie digestive est réalisée pour apprécier la vidange gastrique (notamment dans le bilan du diabète) ;
- la scintigraphie hépatobiliaire est réalisée pour étudier le transit biliaire.
Il existe d'autres scintigraphies possibles (lymphatiques, certains cancers neuro-endocrines...)
La TEMP[modifier | modifier le code]
La tomographie d’émission monophotonique (TEMP) est une technique d’imagerie fonctionnelle basée sur la scintigraphie. La gamma caméra effectue une rotation de 180 ou 360 degrés autour du patient pour capter des images. À l’aide d'un algorithme de reconstruction, l’ordinateur reconstruit les images de la distribution à trois dimensions des radionucléides dans l'organe. La TEMP exige un collimateur afin de sélectionner les photons perpendiculaires à l'organe ou la fonction ciblée. Ce collimateur doit être adapté à l'énergie des photons émis par le radionucléides (collimateur à haute énergie pour l'iode 131 par exemple). Ce procédé induit la perte d’une grande quantité de photons et explique la mauvaise qualité relative des images. Cependant la sensibilité du signal photonique est telle que ce type d'imagerie est très performant.
La TEP[modifier | modifier le code]
La tomographie par émission de positons (TEP) est une scintigraphie consistant à administrer au patient un radiopharmaceutique marqué par un radionucléide émetteur de positons (béta+). Une fois émis et après un court parcours de l’ordre du millimètre, le positron va s’annihiler avec un électron du milieu donnant lieu à l’émission de deux photons gamma de 511 keV dans des directions opposées (à 180°). La détection de ces photons se fait par coïncidence et à l’aide d’une caméra TEP ; ce qui permet de localiser la position de l’émission et la concentration du traceur en chaque point. Les coïncidences sont converties en images tomographiques en utilisant un algorithme de reconstruction et l’image de l’organe en 3D est ainsi reconstituée.
Les traceurs les plus communs sont des radionucléides (de demi-vie très courtes) couplés à des molécules de glucose qui vont se fixer aux tissus qui consomment le plus de sucre, en particulier les cellules cancéreuses. Le fluor 18 (18F) est l'émetteur de positrons actuellement le plus utilisé. Mais on retrouve aussi d’autres radionucléides utilisables tels que 15O, 13N et 11C. Cependant la période très courte de ces éléments fait qu'ils ne peuvent être utilisés que lorsqu'un cyclotron de production est à proximité de l'installation de médecine nucléaire.
La TEP a été initialement développée pour la neurologie (déceler des lésions cérébrales qui causent l’épilepsie, la maladie de Parkinson ou d’Alzheimer) et la cardiologie (détection de malformations des muscles du cœur) ; actuellement, la TEP est essentiellement développée pour la cancérologie.
Imagerie couplée[modifier | modifier le code]
Actuellement la plupart des gamma-caméras (TEMP ou TEP) sont liées à un scanner X (ou dans le futur une IRM) permettant l'association ou plutôt la fusion de l'information structurelle apportée par le scanner à l'information métabolique ou physiologique apportée par la scintigraphie.
La scintigraphie en France[modifier | modifier le code]
Il y a en France en 2013 un peu plus de 460 gamma caméras et environ 118 TEP-TDM répartis dans 220 centres de médecine nucléaire.
Plus d'un million de scintigraphies et près de 250 000 TEP sont réalisées chaque année en France dans les centres de Médecine Nucléaire (données SFMN 2013).
Comparaison avec d’autres méthodes de diagnostic[modifier | modifier le code]
L’imagerie en médecine nucléaire est une imagerie fonctionnelle, qui ne donne pas les mêmes résultats qu’une simple imagerie anatomique. Mais l'examen ne remplace pas les scanners et l'IRM, il les complète seulement dans certains cas (pour les tumeurs cérébrales, pour la suspicion de récidive…). Le PET-scan donne cependant au médecin des informations sur le métabolisme des tissus. La TEP peut faire apparaître de petites tumeurs non visibles au scanner ou à l'IRM dont le diagnostic devra être ensuite confirmé. La TEP peut aussi donner une indication sur l'activité d'une chimiothérapie[3].
Le tableau suivant récapitule ces informations :
| Type d’imagerie médicale | Échographie | Imagerie par rayon X | IRM | Imagerie par radio-isotopes |
|---|---|---|---|---|
| Principe | Un faisceau d’ultrasons est émis par une sonde vers une partie du corps, il peut être transmis, absorbé ou réfléchi selon le tissu qu'il rencontre. L'analyse des modifications du faisceau permet de former une image | Un faisceau de rayons X est envoyé à travers le corps. Plus la partie traversée est dense, plus les rayons sont absorbés. Les rayons transmis sont captés par un film. | Un champ magnétique puissant et stable crée une magnétisation des tissus, des champs magnétiques oscillants plus faibles produisent un phénomène de précession qui donne lieu à un signal électromagnétique mesurable. | |
| Application | Structure de l’abdomen, des organes génitaux, des muscles, fonctionnement du cœur. | Structure des os, des poumons. | cardiologie, neurologie, structure de l’abdomen. | toute exploration fonctionnelle |
| Durée de l’examen (min) | 5 à 15 | 5 à 15 | 20 à 60 | dépend de l'examen. Il y a souvent un temps d'attente entre l'administration du radionucléide et la réalisation des images. |
| sensibilité | La sensibilité décroit avec la profondeur. Imagerie 3D. | sensibles sauf pour les tissus mous. Imagerie 2D (3D pour un scanner) | sensibles pour les tissus mous. Imagerie 3D. | Ciblé et précis. Imagerie 3D. |
| Risques | Échauffement des tissus. | faible exposition aux rayonnements ionisants en radiologie conventionnelle. L'exposition est un peu plus importante en scanner. Elle est à balancer avec le bénéfice diagnostic très important de la méthode. | Échauffement des tissus. | faible exposition aux rayonnements ionisants. Lors des examens couplés il faut ajouter l'exposition liée au scanner réalisé |
Applications thérapeutiques[modifier | modifier le code]
La radiothérapie interne vectorisée (anciennement radiothérapie métabolique)[modifier | modifier le code]
Les applications thérapeutiques de la médecine nucléaire sont importantes.
La RIV est couramment utilisée
Radiothérapie à l'iode 131[modifier | modifier le code]
Une source radioactive d'iode 131 est spécialement commandée pour chaque patient selon l'activité nécessaire au traitement. Cette source est le plus souvent administrée sous la forme d'une gélule. Dans les rares cas d'impossibilité pour le patient d'avaler, des formes liquides sont possibles.
Pour traiter les hyperthyroïdies (que ce soit de type maladie de Basedow ou nodulaire toxique).[modifier | modifier le code]
Pour cela on utilise des sources dont l'activité est de l'ordre de 300 à 800 MBq d'iode 131.
La formule de Marinelli permet un calcul théorique. Cependant on cherche le plus souvent à mettre le patient en hypothyroïdie (traitée par l'hormonothérapie à la LT4) qu'en euthyroïdie du fait du risque de récidive de la maladie.
Pour traiter les cancers de la thyroïde.[modifier | modifier le code]
Après thyroïdectomie totale et selon les résultats de l'anatomopathologie il peut être indiqué un traitement par l'iode 131. Ce traitement vise à détruire les résidus thyroïdiens (pratiquement toujours existants) et à explorer et traiter les éventuelles métastases. Les activités administrées vont de 1.1 GBq à 5.5 GBq. Cependant l'activité la plus administrée est celle de 3.7 GBq. Ce traitement se fait en stimulant la production de TSH par l'hypophyse pour stimuler au maximum les cellules thyroïdiennes restantes. Cette stimulation peut se faire par un sevrage de l'hormonothérapie (arrêt de la LT4 pendant environ un mois) ou par injection de TSH endogène (TyrogenΘ) dans les 48 heures précédant la prise de l'iode.
Traitement des autres pathologies bénignes[modifier | modifier le code]
La polyglobulie de Vaquez est traitée par le 32P.
On peut aussi réaliser des synoviorthèses (traitement de la pathologie des articulations) en administrant par voie d'injection intra-articulaire des radionucléides adaptés à la taille de l'articulation.
Traitement des autres pathologies malignes (cancéreuses)[modifier | modifier le code]
On peut citer les sphères marquées à l'90Y pour traiter les hépatocarcinomes, les traitements par la MIBG-131I des phéochromocytomes, le traitement par le 223Ra des métastases osseuses algiques, l'immunoradiothérapie...
Les applications thérapeutiques de la médecine nucléaire sont en expansion avec l'utilisation de nouveaux radionucléides comme le 177Lu ou le 223Ra.
Les isotopes utilisés et l'exposition médicale[modifier | modifier le code]
| Utilisation | Isotope | Radiation | Temps de demi-vie |
|---|---|---|---|
| Imagerie | 18F | 2 photons de 511 keV | 110 minutes |
| 99mTc | Gamma 140 keV | 6 heures | |
| 123I | Gamma 159 keV | 13 heures | |
| 111mIn | Gamma 171 et 245 keV | 2,8 jours | |
| 201TI | Gamma 167 keV | 3 jours | |
| 67Ga | Gamma 92 keV | 3,3 jours | |
| Traitement | 188Re | Bêta | 1 jour |
| 153Sm | Bêta et gamma | 1,9 jour | |
| 90Y | Bêta 2 300 keV | 2,7 jours | |
| 177Lu | Bêta | 6,7 jours | |
| 131I | Bêta et gamma | 8,2 jours | |
| 32P | Bêta | 14.4 jours | |
| 192Ir | Bêta | 74 jours |
99mTc[modifier | modifier le code]
Le technétium 99m est le radioisotope le plus utile en imagerie médicale nucléaire. Ses caractéristiques physiques sont presque idéales pour cette fin :
- la demi-vie de 6 heures est assez longue pour permettre de suivre les processus physiologiques d'intérêt, mais assez courte pour limiter l'irradiation inutile ;
- L'énergie du photon gamma, 140 keV, est idéale puisqu'assez énergétique pour traverser les tissus vivants, mais assez faible pour pouvoir être détectée commodément : elle peut être interceptée efficacement par un cristal d'iodure de sodium dont l'épaisseur typique sera de l'ordre de 10 à 15 mm ;
- L'abondance de photons gamma est grande, environ 98 % des désintégrations. Peu de particules non pénétrantes sont émises, limitant la dose d'énergie reçue par les tissus vivants.
Le technétium est habituellement obtenu sous forme de pertechnétate sodique : NaTcO4. Il peut être utilisé sous cette forme pour ses propriétés anioniques. Sous cette forme, en effet, son comportement biologique mimera celui des anions Cl- ou encore I-. Ainsi, on pourra par exemple faire des recherches des diverticules de Meckel ou encore imager la glande thyroïde.
Cependant, son principal usage se fera comme marqueur de molécules biologiquement actives. En liant un atome de 99mTc :
- à divers phosphates ou phosphonates, on pourra imager le métabolisme osseux (HDP, HMDP, DPD...) ;
- à certains chélateurs tel le DTPA , on imagera la fonction rénale. Le même DTPA, sous forme d'aérosol sera inhalé pour cartographier la ventilation pulmonaire ;
- à des macro-agrégats d'albumine qui permettront d'imager la perfusion pulmonaire ;
- à l'acide diimino-acétique ou ses dérivés, on imagera la fonction hépato-biliaire ;
- à des colloïdes divers, habituellement de soufre, pour cartographier la distribution des cellules hépatiques de Kupffer ;
- aux globules rouges du patient, pour rechercher des hémangiomes ou des saignements digestifs ;
- à certaines molécules lipophiles tel le MIBI ou la tetrofosmine, pour cartographier la perfusion sanguine régionale; utile notamment pour l'évaluation de l'ischémie myocardique ou la recherche de certaines tumeurs.
18F[modifier | modifier le code]
Le Fluor 18 est un isotope émetteur de positons; la désintégration du fluor 18F sera détectée par les 2 photons de 511 keV émis à 180° par annihilation lors de la rencontre du positon avec un électron du milieu.
L'atome de fluor a une densité équivalente à celui d'hydrogène. Son T1/2 est de 109 minutes. Les avantages en médecine tiennent au faible parcours du bêta+ (meilleure résolution spatiale), à la petite taille de l'atome et à la demi-vie courte (faible durée d'exposition).
Il est en particulier d'un grand intérêt en neurologie, cardiologie et oncologie, par marquage de la molécule de déoxyglucose, appelé alors 18FDG (proposé initialement par l’équipe du Brookhaven National Laboratory en 1976). Le 18FDG, ou 2-[18F]fluoro-2-désoxy-D-glucose, est un analogue du glucose qui sera absorbé en quantités importantes par les cellules tumorales en développement rapide et nécessitant un apport énergétique accru, alors que la dégradation en fructose sera bloquée par le remplacement du 2e groupement hydroxyle par le fluor, la non-métabolisation résultant en une accumulation dans les cellules tumorales (ou autres cellules absorbant rapidement du glucose : inflammations, activité musculaire, activité neuronale)...
Le 18FDG est le plus important médicament radiopharmaceutique marqué par un émetteur de positons. C'est le 1er traceur avec autorisation de mise sur le marché (AMM) utilisé en Tomographie par émission de positons (TEP), pour les explorations en oncologie.
La détection est en coïncidence, par caméra de type TEP en général (voire caméra type Anger à doubles têtes CDET, quasiment abandonné).
L'émission bêta+ impose la mise en place de mesures de radioprotection plus importantes que pour le 99mTc.
201Tl[modifier | modifier le code]
Le thallium 201 est un isotope du thallium qui possède des propriétés chimiques similaires à celles du potassium. Absorbé par les cellules via la pompe Na-K Atpase, il se distribuera en fonction de la perfusion sanguine régionale. Longtemps utilisé, notamment pour évaluer la perfusion sanguine myocardique, il tend à être délaissé au profit des marqueurs lipophiliques technétiés (MIBI, tetrofosmine).
En effet, ses propriétés physiques sont moins optimales : l'énergie de ses photons gamma est faible et la période un peu longue. Les images obtenues sont donc sujettes à la dégradation causée par l'atténuation et la diffusion.
123I[modifier | modifier le code]
L'iode 123 est un isotope de l'iode utilisé pour étudier le métabolisme thyroïdien. Ses radiations riches en photons gamma et sa demi-vie de 13 heures en font un agent bien adapté à l'imagerie. Il est notamment utilisé pour la scintigraphie thyroïdienne, pour marquer l'iobenguane utilisé en scintigraphie (MIBG) et l'ioflupane (DaTSCAN) pour la scintigraphie des voies dopaminergiques.
131I[modifier | modifier le code]
L'iode 131 est un autre isotope de l'iode, ses radiations riches en particules bêta et sa demi-vie relativement longue de 8,2 jours en font un élément très propice au traitement. On l'utilise pour l'ablation de nodules thyroïdiens hyperactifs, pour le traitement de certaines formes d'hyperthyroïdie, par exemple la maladie de Graves-Basedow ou la maladie de Plummer, ou pour la recherche et l'ablation de métastases de carcinomes thyroïdiens bien différenciés (papillaires ou vésiculaires). Il était aussi utilisé pour marquer l'iobenguane en scintigraphie (MIBG) remplacé par l'iode 123 aujourd'hui.
Il n'a sauf exception plus d'utilisation en diagnostic.
67Ga[modifier | modifier le code]
Le gallium 67 est un isotope du gallium qui mime le métabolisme du fer. Utile pour imager la fonction de la moelle osseuse et pour la recherche de certaines infections ou maladie inflammatoires. Il a été abandonné pour les lymphomes ou certaines tumeurs, supplanté par la TEP au FDG.
111mIn[modifier | modifier le code]
Le DTPA marqué à l'indium peut être injecté dans l'espace sous-arachnoïdien, par ponction lombaire, afin d'imager la production, la migration et la réabsorption du liquide céphalo-rachidien.
On peut aussi retrouver le DTPA à l'indium ou au technétium joint aux globules blancs (in vitro) du patient dans un cas de recherche d'infection (plus efficace que le gallium).
Il est surtout utilisé pour marquer un analogue de la somatostatine : l'Octreoscan.
Radioprotection[modifier | modifier le code]
En médecine nucléaire on utilise les rayonnements ionisants. On applique donc les règles de la radioprotection pour protéger les patients, les travailleurs, le public et l'environnement. (application de directives européennes).
Les radiopharmaceutiques utilisés sont administrés en très petite quantité et ne posent aucun problème pharmacologique. (On n'a noté aucune allergie, pratiquement aucune réaction adverse prouvée).
Le paramètre important est la demi-vie ou période efficace du radiopharmaceutique. Elle combine la décroissance radioactive (caractérisée par la période ou demi-vie physique) et la sortie physiologique du médicament et de la radioactivité le plus souvent par voie urinaire ou dans les selles (caractérisée par la période ou demi-vie biologique).
Les deux grandes règles de radioprotection doivent s'appliquer comme pour tous les examens et traitements utilisant les rayonnements ionisants :
- justification : balance entre bénéfice et risque ;
- optimisation : utilisation de la quantité de rayonnements juste nécessaire pour obtenir l'information diagnostique souhaitée ou l'effet thérapeutique recherché.
Les activités administrées peuvent dépendre de l'âge (on réalise des scintigraphies et des thérapeutiques chez les enfants dès la naissance) du poids et de la taille. Il arrive aussi qu'on administre la même quantité de radioactivité pour tous les patients permettant ainsi une « calibration » donnant accès à des informations quantitatives (fixation de l'iode par la thyroïde par exemple).
Les traitements utilisant des plus hautes activités nécessitent l'hospitalisation (en général de l'ordre de 48h) des patients dans des chambres (dites plombées) dont les sanitaires sont reliées à un système de cuve de rétention.
Des conseils de radioprotection doivent être donnés par le médecin nucléaire à la sortie de l'unité de médecine nucléaire pour permettre de diminuer l'exposition des proches, du public et de l'environnement.
Production d'isotopes médicaux[modifier | modifier le code]
L'isotope servant à la grande majorité des scintigraphies est le technétium (99mTc). La demande de technétium augmente alors que les réacteurs permettant de le produire vieillissent. Ces réacteurs nucléaires fissionnent de l'uranium hautement enrichi de qualité militaire. L'un des sous produits de fission, le molybdène est vendu pour être conditionné par des laboratoires pharmaceutiques en générateurs de technétium. En effet le molybdène est l'élément père du Tc, il se désintègre en Tc. Ces générateurs sont ensuite livrés de façon hebdomadaire ou bi-hebdomadaire dans les services de médecine nucléaire où sont préparés les radiopharmaceutiques administrés aux patients pour leurs scintigraphies.
En 2007 et 2008, à la suite de pannes ou de révisions des réacteurs canadien et néerlandais, le monde a manqué d'isotopes médicaux durant quelques mois.
En 2009, alors que la plupart des réacteurs produisant les radioisotopes utilisés par la médecine nucléaire ont plus de 40 ans, l'Autorité de sûreté nucléaire française (ASN) a rappelé les risques en amont d'une production mal sécurisée de radioisotopes : « Le risque de pénurie de radioéléments à usage médical ne doit pas conduire à faire l'impasse sur la sûreté des réacteurs qui les produisent » .L'Agence invite à ne pas prolonger l'exploitation des réacteurs dangereusement anciens mais à initier une nouvelle approche internationale concertée[4] ; l'ASN invite les autorités médicales à « optimiser » l'utilisation du technétium 99m, et à trouver des méthodes alternatives pour le produire, par exemple avec un accélérateur, ainsi qu'à étudier le recours à d'autres méthodes d'imagerie médicale ; construire un modèle économique robuste de production de ces radioéléments. En effet, le modèle actuel n'intègre pas le coût complet de fabrication des radioéléments et notamment le coût de fabrication du molybdène produit dans des réacteurs de recherche publics.
Les principaux réacteurs produisant le molybdène sont des réacteurs de recherche et sont anciens. Ce sont[4] :
- le National Research Universal Reactor (NRU) aux Laboratoires nucléaires de Chalk River (Canada) ; en service depuis 1957, a connu en 2007 un arrêt pour maintenance, prolongé, après un redémarrage autorisé par le Parlement, contre l'avis de l'Autorité de sûreté canadienne (ce réacteur produit environ 40 % de la production mondiale) ;
- le High Flux Reactor (HFR) à Petten (Pays-Bas) ; en service depuis 1961, il a connu une panne en 2008, qui a entraîné une pénurie (ce réacteur produit environ 30 % de la production mondiale), il a encore été arrêté à la mi- et au moins jusqu'au printemps 2010 ;
- le réacteur Safari à Pelindaba (Afrique du Sud) ; en service depuis 1965 (~10 % de la production mondiale) ;
- Belgian Reactor-2 (BR2) dans l'institut SCK•CEN situé à Mol (Belgique) ; en service depuis 1961 (~9 % de la production mondiale) ;
- le réacteur OSIRIS au Centre CEA de Saclay) (France) ; en service depuis 1965 et soumis par l'ASN à un arrêt avant 2015, à condition qu'un programme important d'amélioration de la sûreté soit mis en œuvre (ce réacteur assure environ 5 % de la production mondiale, et il aurait dû être révisé et donc arrêté de mars à ).
La construction prochaine du RJH (réacteur Jules Horowitz) en France à Cadarache selon le Commissariat à l'énergie atomique et aux énergies alternatives (CEA) doit venir pallier la défaillance des principaux réacteurs mais ne sera pas opérationnel avant 2025.
En revanche, il est important de noter que la production de certains isotopes : tous les isotopes pour la TEP (essentiellement le fluor 18) et certains isotopes pour la scintigraphie classique (comme l'iode 123 ou le thallium 201), sont produits par des cyclotrons beaucoup plus nombreux, répartis dans différents pays. Ce mode de production décentralisé n'est pas concerné par les risques de pénurie cités plus haut ne faisant pas appel aux réacteurs nucléaires. Des études très avancées permettent d'envisager la production, par les cyclotrons, du molybdène 99 servant à la préparation du technétium 99m[5],[6].
Notes et références[modifier | modifier le code]
- Zimmermann, Richard., La Médecine nucléaire (La radioactivité au service du diagnostic et de la thérapie)., EDP Sciences, , 192 p. (ISBN 978-2-7598-0228-9, OCLC 476159980, lire en ligne), page 26
- « MÉDECINE NUCLÉAIRE », sur universalis.fr (consulté le ).
- « Tep ou Pet-Scan (Scanner par image de rayons gamma) », sur gfme.free.fr (consulté le ).
- Communiqué de presse à la suite de la Prise de position du collège sur les radioéléments à usage médical. « Le risque de pénurie de radioéléments à usage médical ne doit pas conduire à faire l'impasse sur la sûreté des réacteurs qui les produisent. » 16 septembre 2009
- (en) Abrams DN, Adelfang P, Alldred K et al., Non-HEU production technologies for Molybdenum-99 and Technetium-99m, Vienne, International atomic energy agency, coll. « IAEA Nuclear Energy Series / No. NF-T-5.4 », , 75 p. (ISBN 978-92-0-137710-4 et 920137710X, OCLC 830370852, lire en ligne [PDF])
- http://meteopolitique.com/fiches/depistage/actualite/35/est-de-la-fin-du-nucleaire-medical.htm « Vers la fin du nucléaire médical. »