Métastase (médecine)
| Spécialité | Oncologie |
|---|
| ICD-O | 8000/6 |
|---|---|
| DiseasesDB | 28954 |
| MedlinePlus | 002260 |
| MeSH | D009362 |
Une métastase (du grec ancien : μετάστασις / metástasis, de μεθίστημι / methístēmi, « je change de place ») est, au sens large, une croissance cellulaire qui se produit à distance du site primaire de cette croissance et sans contact direct avec elle — cette définition inclut en principe les métastases infectieuses — microbiennes, virales ou parasitaires — ou tumorales, qu’elles s’effectuent par voie hématogène ou lymphatique mais en clinique courante, l’usage du terme est restreint à la métastase cancéreuse[1].
La métastase présente une importance diagnostique en tant qu’indice de malignité, et pronostique en tant que composante de diverses classifications, dont la classification TNM.
Généralités sur les métastases en cancérologie[modifier | modifier le code]
Les organes les plus fréquemment concernés par le développement de métastases sont toujours les mêmes, certaines tumeurs tendant à essaimer dans des organes particuliers, comme l'a suggéré il y a plus d’un siècle, en 1889, la « théorie de la graine et du sol » due à Stéphane Paget.
Le cancer de la prostate, par exemple, métastase généralement dans les os. De la même façon, le cancer du côlon tend à métastaser dans le foie. Chez les femmes, le cancer de l'estomac métastase souvent dans les ovaires, où il forme une tumeur de Krukenberg. On avait remarqué que le plus souvent les principaux organes-cibles des métastases sont ceux qui jouent un rôle de filtre dans le corps sain (ex. : foie) ou dans le système immunitaire (ex. : glandes surrénales).
- Le foie accueille le plus de métastases d'adénocarcinomes, même quand ces derniers se développent dans l'enfance. On pensait que c'était surtout parce qu'il filtre la circulation digestive, en provenance de la veine porte, mais une étude[2] publiée en 2010 laisse penser que le système immunitaire pourrait en être la raison principale ; cette étude a utilisé des souris mutantes comme modèle animal. Une souche mutante développait spontanément un cancer du pancréas, une autre présentait un cancer avancé du côlon, se propageant à l'abdomen. Les chercheurs ont observé dans le foie — dès les premiers stades de développement du cancer — une expansion de deux types de cellules immunitaires myeloïdes suppressives dans le foie présentant des phénotypes (CD11b+ Gr1+) et caractéristiques fonctionnelles différentes. Ces cellules deviennent alors les leucocytes hépatiques dominants, concomitamment aux phénomènes de cancérisation du foie. Lutter contre ces cellules immunitaires de suppression (tueuses de lymphocytes T) dans le foie lors du développement d'un cancer pourrait empêcher la propagation du cancer au foie[2].
- Après le foie, ce sont les poumons qui sont le plus touchés (ils voient passer toute la circulation du corps).
- Mais les os, le cerveau, et bien que moins souvent, la plupart des autres organes peuvent également être touchés.
Les métastases sont souvent groupées, réalisant, lors des examens (radiographie de poumons, échographie hépatique, etc.), un véritable lâcher de ballons.
Les métastases font toute la gravité du cancer car l'extirpation chirurgicale complète d'une tumeur cancéreuse ne permet pas d'avoir la certitude qu'une métastase ne se découvrira pas, des mois ou des années plus tard[3].
À partir d’une tumeur primaire, les cellules cancéreuses peuvent pénétrer dans les vaisseaux lymphatiques et sanguins puis circuler ailleurs dans le corps grâce au système sanguin jusqu’à un centre éloigné et croître (« métastaser ») dans des tissus normaux.
La métastase définit la tumeur qui est soit bénigne, soit maligne : les tumeurs malignes sont celles qui peuvent se propager par invasion et métastases tandis que des tumeurs bénignes ne peuvent que grandir sur place. Par définition, le terme « cancer » ne s’applique qu’aux tumeurs malignes. Cependant, quelques tumeurs avec histologie bénigne peuvent se comporter comme des tumeurs malignes, par exemple dans le cas de tumeurs cérébrales, et là le traitement doit être aussi agressif qu’avec la forme maligne.
C’est la capacité de s’étendre à d’autres tissus et d’autres organes qui fait du cancer une maladie potentiellement mortelle. C’est pourquoi il y a grand intérêt à comprendre ce qui rend possible des métastases dans le cas d'une tumeur cancéreuse maligne. En effet, l'apparition de métastases traduit en général l'entrée de la maladie cancéreuse dans sa phase terminale.
Quand les cellules cancéreuses diffusent pour former une nouvelle tumeur, on parle de tumeur secondaire ou métastatique. Bien que les cellules métastatiques soient originaires de la tumeur primitive, elles ne sont pas exactement identiques aux cellules de cette dernière. En effet, ces cellules doivent acquérir un certain nombre de caractères (perte d'adhésion cellulaire, migration, invasion, etc.) leur permettant de passer du phénotype cancéreux à métastatique. Ces cellules se caractérisent par un comportement similaires aux cellules souches et peuvent alors être qualifiées de cellules souches cancéreuses. Ainsi, si le cancer du sein métastase dans le poumon, la tumeur secondaire est composée de cellules de sein malade (et non des cellules de poumon malade). La maladie dans le poumon est le cancer du sein métastatique (et non le cancer de poumon).
Les cellules cancéreuses peuvent s’étendre aux ganglions lymphatiques (ganglions lymphatiques régionaux) dans la zone de drainage de la tumeur primaire. On parle alors d’envahissement ganglionnaire, de ganglions envahis, ou de maladie régionale. La diffusion dont la localisation se limite aux ganglions lymphatiques régionaux près de la tumeur primaire n’est pas normalement comptée comme métastase, bien que ce soit une indication de pronostic plus mauvais.
Facteurs entrant en jeu[modifier | modifier le code]
Le phénomène de métastase est une série complexe d’étapes au cours desquelles des cellules cancéreuses quittent le site originel (tumeur primaire) et migrent vers d'autres parties du corps en utilisant le système lymphatique et/ou le système sanguin. Pour ce faire, des cellules malignes se séparent de la tumeur primaire et s’attachent en les dégradant aux protéines qui composent la matrice extracellulaire (ECM), laquelle sépare la tumeur des tissus voisins. En dégradant ces protéines, les cellules cancéreuses sont capables de briser l'ECM et de s’évader. Quand des formations cancéreuses orales métastasent, elles voyagent généralement par le système lymphatique vers les ganglions lymphatiques du cou. On dit alors que le cancer est « métastasé ».
En étudiant les conditions nécessaires pour la métastase des cancers, des chercheurs[Qui ?] ont découvert qu'un des événements critiques requis est la croissance d'un nouveau réseau de vaisseaux sanguins. Ce processus de formation de nouveaux vaisseaux sanguins est appelé angiogenèse tumorale.

L’angiogenèse tumorale est la prolifération d'un réseau des vaisseaux sanguins qui pénètrent dans les croissances cancéreuses, fournissant des substances nutritives et de l'oxygène et enlevant les déchets : le chercheur Judah Folkman montre en 1971 que la tumeur ne peut grossir sans angiogenèse au-delà de 2 mm3[4]. La tumeur angiogénétique commence en réalité lorsque des cellules de tumeur cancéreuses laissent échapper des molécules qui envoient des signaux au tissu hôte normal qui l’entoure. Cette signalisation active certains gènes dans le tissu hôte, lequel, à son tour, permet aux protéines de susciter la croissance de nouveaux vaisseaux sanguins.
Patricia Steeg, de l'Institut national du cancer de Bethesda (Maryland) a donné ce commentaire : « Les auteurs montrent que les cellules cancéreuses peuvent mobiliser des cellules de moelle osseuse normales, les amenant à migrer vers des régions particulières et à modifier l'environnement local afin d'attirer une métastase et de l’aider à se développer. » Les cellules se multiplient sur le site de la métastase et produisent une protéine appelée fibronectine, qui agit comme une sorte de glu pour attirer et prendre au piège les cellules de moelle osseuse, créant ainsi un terrain d’accueil ou un nid pour les cellules cancéreuses. « Ces nids fournissent aux cellules cancéreuses la possibilité de s’attacher ; elles peuvent ainsi s’implanter et croître. C’est non seulement une occasion de se lier ensemble mais de proliférer. Une fois que tout cela s’est produit, nous sommes en présence d’un site métastatique entièrement formé, c’est-à-dire d’une tumeur secondaire », a dit Lyden. « C'est la première fois que quelqu’un a découvert ce que nous appelons la niche prémétastatique ».
Différentes étapes conduisant à la métastase cancéreuse[modifier | modifier le code]
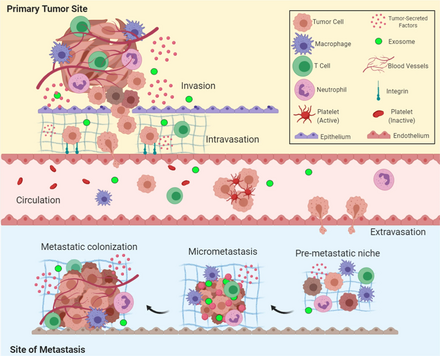
Dissémination[modifier | modifier le code]
Élément déclencheur: l'instabilité chromosomique[modifier | modifier le code]
La dissémination des cellules cancéreuses précède les étapes initiales de la cascade invasion-métastase[5]. Cette cascade est la conséquence de l'instabilité chromosomique provoquée par des erreurs continues dans la ségrégation des chromosomes au cours de la mitose[6]. Les défauts de ségrégation chromosomique provoquent la rupture des micronoyaux et la sécrétion d'ADN génomique dans le cytosol, qui active ensuite les voies de détection de l'ADN cytosolique[7].
La recherche suggère que la nature de la cellule cancéreuse primaire détermine les différentes propriétés métastatiques comme la croissance et la réponse au traitement[8],[9].
Transition épithélio-mésenchymateuse[modifier | modifier le code]

La transition épithélio-mésenchymateuse est le processus d'acquisition des cellules épithéliales qui développent la capacité d'envahir, de résister et de se disséminer[10]. Les cellules épithéliales sont étroitement liées les unes aux autres et à la matrice extracellulaire[11]. La transition épithélio-mésenchymateuse régit les altérations biochimiques réversibles qui permettent à une cellule épithéliale d'atteindre un phénotype mésenchymateux et confère une plasticité épithéliale-mésenchymateuse à la cellule épithéliale[12], ce qui est crucial pour la progression du cancer et des métastases. Cependant, toutes les cellules provenant du site tumoral primaire ne contribuent pas au développement de métastases.
La transition épithélio-mésenchymateuse est un spectre d'étapes de transition entre les phénotypes épithéliaux et mésenchymateux[13], et elle est régie par un certain nombre de facteurs de croissance[14] et de voies de signalisation[15]. La transition épithélio-mésenchymateuse spontanée dans les cellules tumorales primaires se déplace entre différents stades intermédiaires présentant différentes caractéristiques invasives, métastatiques et de différenciation[16]. Les cellules tumorales qui expriment un mélange de phénotypes épithéliaux et mésenchymateux sont plus efficace dans la circulation, la colonisation et le développement de métastases[16]. Le séquençage transcriptionnel de la chromatine et de l'ARN unicellulaire montre des expressions géniques différentes qui sont régulées par des facteurs de transcription et des voies de signalisation communs et distincts. Les différents stades de la transition épithélio-mésenchymateuse sont situés dans divers microenvironnements et en contact avec diverses cellules stromales. Les cellules tumorales libèrent de grandes quantités de chimiokines pour attirer les cellules immunitaires et stimuler l'angiogenèse, favorisant ainsi le développement d'une niche inflammatoire unique et hautement vascularisée[16]. Les fibroblastes associés aux cancers conduisent et dirigent la migration des cellules cancéreuses via l'alignement de la fibronectine[17]. L’hypoxie[18], les facteurs de stress métaboliques et la rigidité matricielle[19] déclenchent la transition épithélio-mésenchymateuse dans les cellules cancéreuses.
Il existe un débat important sur l'importance de la transition épithélio-mésenchymateuse dans les métastases du cancer et la résistance à la chimiothérapie[20],[21],[22]. Elle ne semble pas essentielle aux métastases des cancers du pancréas et du poumon mais elle contribue à la chimiorésistance[23],[21].
Bien que la transition épithélio-mésenchymateuse n'est peut être pas indispensable puisse être nécessaire pour l'initiation des métastases, le processus inverse de transition mésenchymateuse-épithéliale est nécessaire pour la progression métastatique. Dans les métastases osseuses, la sélectine-E dans le système vasculaire osseux induit l'activation de transition mésenchymateuse-épithéliale et l'activation de la protéine Wnt dans les cellules cancéreuses est nécessaire la formation de tumeurs métastatiques[24].
Amorçage de la niche prémétastatique[modifier | modifier le code]
Les sites secondaires ne reçoivent pas passivement les cellules cancéreuses. En fait, le microenvironnement tumoral sélectionne une zone appelée niche prémétastatique avant même l'initiation des métastases[25]. Le développement d'un niche pré-métastatique est un processus en plusieurs étapes impliquant des facteurs de sécrétion et des vésicules extracellulaires induisant un remodelage de la matrice extracellulaire et une immunosuppression locale[25]. Les microscopes à haute définition ont obtenu des images de cellules cancéreuses partageant du matériel biologique avec des cellules moins cancéreuses rendant ces cellules plus cancéreuses[26]. Les cellules cancéreuses libèrent des vésicules qui transportent l'ARN messager transcrit à partir de gènes impliqués dans la migration cellulaire et métastases, qui sont ensuite acceptées par d'autres cellules[26],[27]. Une fois que les cellules saines ont englouti ces vésicules, les cellules qui n'expriment pas de phénotype malin commencent à migrer plus rapidement. Les gènes transférés améliorent également la capacité des cellules à envahir d’autres organes[26]. Ainsi, les caractéristiques métastatiques peuvent être transférées par échange de vésicules extracellulaires[26].
Rôle des exosomes[modifier | modifier le code]
Les tumeurs primaires libèrent des quantités importantes d'exosomes qui transfèrent des facteurs favorisant l'invasion, tels que les micro-ARNs , aux cellules cancéreuses tumorigènes[28],[29],[30]. Par exemple,le micro-ARN-10b est transporté et libéré par les exosomes et détermine les propriétés métastatiques dans le cancer du sein. cellules[31]. invasion de cellules cancéreuses[32],[33] De plus, les exosomes sécrètent des inducteurs de transition épithélio-mésenchymateuse qui stimulent la progression de la transition épithélio-mésenchymateuse des cellules épithéliales de l'hôte, leur fournissant ainsi la capacité d'envahir et de métastaser[34],[35],[36],[37]. Les exosomes ont la capacité de remodeler la matrice extra-cellulaire en interagissant avec les fibroblastes, les cellules stromales et les cellules endothéliales pour dégrader les composants associés à la protéase tels que le collagène, la laminine et la fibronectine[38]. La matrice cellulaire extra-cellulaire altérée par les exosomes présente une prolifération accrue des cellules stromales, et la résistance des cellules tumorales aux signaux apoptotiques. Ceci, associé à l'effet des chimiokines et des facteurs de croissance, conduit à la formation d'un nouveau microenvironnement pour les cellules cancéreuses, les cellules immunitaires et d'autres constituants stromaux, appelé niche pré-métastatique[39],[40],[41],[42]dans lequel les cellules métastatiques s'arrêtent, extravasent et finalement colonisent[43],[44],[45].
En plus de leur rôle dans l’amorçage de la niche pré-métastatique, les exosomes participent à l’organotropisme des cellules cancéreuses. Cette affinité envers certains organes provient de l'avidité exosomale pour des cellules hôtes spécifiques[46]. L'étude de l'expression protéomique exosomale du cancer des os a montré différents modèles d'intégrines, dans lesquels les intégrines exosomales α6β4 et α6β1 étaient corrélées aux métastases pulmonaires, tandis que l'intégrine exosomale αvβ5 était associée aux métastases hépatiques[47]. L'absorption des intégrines dans le site secondaire a conduit à la phosphorylation de la protéine oncogène Src et à l'expression du gène pro-inflammatoire S100 [47]. Le ciblage de ces intégrines a diminué l'absorption exosomale et diminue le nombre de métastases pulmonaires et hépatiques par diminution de l’absorption des exosomes[47]. Les autres protéines et lipides membranaires associés à la matrice extra-cellulaire influencent le ciblage spécifique des exosomes sur leurs cellules hôtes spécifiques[47],[48],[49],[50],[51]. De plus, l'internalisation exosomale par les cellules hôtes cibles active des voies endocytaires hétérogènes telles que la clathrine, le radeau lipidique et l'absorption médiée par la cavéoline[52],[53].
Les métastases médiées par les exosomes ne dépendent pas uniquement des exosomes libérés par la tumeur. En fait, les exosomes dérivés des astrocytes assurent le transfert intercellulaire des micro-ARNs qui ciblent le gène suppresseur de tumeur PTEN vers les cellules cancéreuses métastatiques, favorisant ainsi l'invasion et les métastases cérébrales[53]. Cela conduit à son tour à la sécrétion accrue du ligand de chimiokine 2 , qui recrute des cellules myéloïdes, améliorant la croissance des cellules métastatiques cérébrales et réduisant l'effet de la signalisation apoptotique[53]. L'inhibition de la libération exosomale astrocytaire prévient la perte de PTEN et supprime les métastases cérébrales[53].
Modification de la matrice extracellulaire[modifier | modifier le code]
La matrice extracellulaire est un échafaudage de macromolécules interconnectées formant un réseau qui englobe les cellules présentes dans les tissus et les organes[54]. Cette environnement spécialisé modifie les propriétés des cellules et affecte leur propension à proliférer, à migrer et à survivre[55],[56]. Suite à des déclencheurs physiologiques et pathologiques, la protéolyse partielles des macromolécules libèrent des peptides , appelées matrikines, sont libérées pour remodeler la matrice extra-cellulaire, rétablir un maillage fonctionnel et maintenir l'homéostasie des tissus[56],[57]. Dans les métastases cancéreuses, le remodelage de la matrice extra-cellulaire est détourné, conduisant à une tumorigenèse stromale[58],[59],[60],[61]. Une variété de composants majeurs de la matrice extra-cellulaire, comme les protéoglycanes, le collagène, les laminines, la fibronectine, l'élastine, d'autres glycoprotéines et les protéinases, sont impliqués dans les processus invasifs et métastatiques des cellules cancéreuses.
Une étape importante de l’invasion est le désassemblage de la matrice extra-cellulaire et de ses constituants grâce à des enzymes telles que les métalloprotéinases matricielles[62]. Les métalloprotéinases matricielles jouent un rôle majeur dans l’invasion, la prolifération cellulaire, la survie, la réponse immunitaire et l’angiogenèse[63],[64]. Les métalloprotéinases matricielles sont élevés dans la plupart des types de cancer et sont continuellement associés à un mauvais pronostic[65],[66]. Les cellules cancéreuses ajustent la niche métastatique pour stimuler la croissance en remodelant la matrice extra-cellulaire. Les changements dans l’accessibilité des nutriments et les réactions métaboliques dans les tissus déterminent la probabilité que les cellules cancéreuses se métastasent. Par exemple, les cellules métastatiques du cancer du sein métabolisent le pyruvate, qui est abondant dans les poumons, pour piloter le remodelage de la matrice extra-cellulaire à base de collagène dans la niche métastatique pulmonaire[67].
Autres facteurs[modifier | modifier le code]
Facteur épigénétique[modifier | modifier le code]
Microbiote[modifier | modifier le code]
Le concept de « microbiote tumoral » vient du fait que des bactéries ont été détectées au sein des tumeurs elles-mêmes. Bien qu’aucun lien avec les résultats thérapeutiques des patients et la survie n’ait été établi, les bactéries confèreraient une vulnérabilité à des cancers spécifiques[68].
Les bactéries ciblent sélectivement les tumeurs dotées de réseaux vasculaires riches et sont attirées par chomiotactisme chimiotactique. Les bactéries anaérobies strictes ou facultatives, en particulier, survivent vigoureusement dans les microenvironnements tumoraux hypoxiques[69],[70]. Les bactéries sont métaboliquement actives entrainant des altérations de la structure chimique de certains agents chimiothérapeutiques et affecte la réponse au traitement[71],[72]. Les gammaprotéobactéries situées dans le cancer du pancréas confèrent une résistance à la gemcitabine, un médicament couramment utilisé dans les cancers gastro-intestinaux[72],[73]. Fusobacterium nucleatum favorise également la résistance au cancer colorectal en initiant l'autophagie et en activant les récepteurs de type Toll sur les cellules cancéreuses[74].
Rythme circadien[modifier | modifier le code]
Pénétration dans le système vasculaire ou intravasion[modifier | modifier le code]
L'intravasation ou la traversée des cellules cancéreuses de la paroi du système vasculaire, est médiée activement ou passivement[11],[75] et dépend du type de tumeur, du microenvironnement et du système vasculaire[76]. Cette intravasation des cellules tumorales est régulée par des facteurs présents dans le microenvironnement tumoral[77]. Les cellules tumorales situées le long de la périphérie du vaisseau perturbent l'endothélium du vaisseau et pénétrentnt dans la circulation[78]. De plus, les contraintes architecturales du tissu imposent certaines pressions mécaniques sur les cellules tumorales envahissantes pendant l'intravasation[79]. La compression nucléaire est particulièrement importante menaçant l'intégrité du noyau de la cellule envahie responsable d'un réarrangement génomique, ce qui augmente le potentiel métastatique[79].
Les intégrines sont les principaux récepteurs d'adhésion cellulaire qui sont impliqués dans presque toutes les étapes de la progression du cancer, depuis le développement de la tumeur primaire jusqu'aux métastases[80]. Une expression altérée des intégrines est fréquemment détectée dans les tumeurs, où les intégrines jouent un rôle dans l'activation de la signalisation du récepteur du facteur de croissance épidermique[80]. De plus, les intégrines régulent le processus de colonisation en facilitant la survie indépendamment de l'ancrage des cellules tumorales circulantes. Les cellules métastatiques utilisent la cadhérine E dans les sites métastatiques pour se détacher, se disséminer et coloniser[81]. Cela favorise la survie des cellules métastatiques et bloque l'apoptose réactive médiée par l'oxygène[81].
Circulation[modifier | modifier le code]

Les interactions entre les cellules tumorales circulantes et les composants de la circulation déterminent la survie et la capacité des cellules tumorales circulantes à éventuellement s'extravaser dans des sites distants[82],[83],[84]. La plupart des cellules tumorales circulantes circulent sous forme de cellules individuelles, tandis que d'autres se déplacent en grappes. Cependant, les amas en circulation sont beaucoup plus susceptibles de former des métastases[85]. En plus des cellules cancéreuses envahissantes, les amas contiennent des cellules stromales et des composants immunitaires du microenvironnement tumoral d'origine qui améliorent sa survie[85],[86],[87]. Les neutrophiles participent à l'amas et suppriment l'activation immunitaire des leucocytes, ce qui augmente les chances de survie des cellules tumorales circulantes[88]. De plus, l'interaction des cellules tumorales circulantes avec les plaquettes conduit à la formation d'un bouclier de plaquettes autour des cellules cancéreuses qui empêche la détection des cellules tumorales circulantes par les cellules immunitaires et fournit la structure nécessaire pour supporter les contraintes physiques de la circulation[89],[90],[91]. Un facteur important dans le processus métastatique est la capacité des cellules tumorales circulantes à adhérer et à extravaser à travers les cellules endothéliales et à coloniser les niches pré métastatiques[92]. Dès que les cellules tumorales circulantes s'arrêtent dans les capillaires, soit ils s'extravasent par migration transendothéliale, soit ils se développent dans le vaisseau avant une éventuelle extravasation et colonisation de la niche pré-métastatique[93],[94],[95],[96].
Résistance aux forces vasculaires et à la pression mécanique[modifier | modifier le code]
Les cellules tumorales circulantes détectent et réagissent à la mécanique des tissus et provoquent des altérations tissulaires brèves ou durables, notamment le raidissement, la compression et la déformation de la matrice extra-cellulaire, le déploiement des protéines, le remodelage protéolytique[97].
Des pressions mécaniques sont susceptibles d'être détectées lors de l'arrêt des cellules tumorales circulantes sur des sites distants, lorsque à la sortie des vaisseaux (extravasation) et pendant la croissance métastatique. Les vitesses d'écoulement dans les régions vasculaires jouent un rôle important dans le processus de métastase à distance[98]. Le passage des cellules tumorales circulantes dans la circulation sanguine est interrompu lorsque leur capacité d'adhésion devient supérieure aux forces de cisaillement. qui leur sont imposés par le flux sanguin[98]. Par conséquent, les régions à faible flux hémodynamique sont les régions où la plupart des cellules tumorales circulantes se stabilisent et interagissent avec les cellules endothéliales. C'est dans de telles régions qu'individuellement des cellules tumorales circulantes uniques peuvent former des amas intravasculaires[99]. Une fois les cellules tumorales circulantes fixées dans la microvascularisation, elles sont fragmentées par le flux sanguin. Cela génère une interaction immunitaire qui favorisent l'extravasation et le développement des métastases à partir des cellules tumorales circulantes survivantes.Par conséquent, les forces de cisaillement jouent un rôle important dans les métastases hématogènes et dans la détermination du lieu de l'arrêt terminal[98],[100].
Rôle des chimiokines et des cytokines dans la circulation les cellules tumorales[modifier | modifier le code]
La migration des cellules métastatiques dans la circulation repose souvent sur les chimiokines , le système du complément et sur des facteurs métaboliques à effet antioxydant[101] qui dirigent les cellules tumorales à travers le système vasculaire[102],[103]. Les cellules cancéreuses, quand elles circulent en très grand nombre, stimulent la production d'interleukine 6 et d'interleukine 8 qui stimulent les voies biochimiques et faciliter la migration des tumeurs[104]. Dans les modèles murins de cancer du sein, le blocage des récepteurs de l'IL-6 et de l'IL-8 a minimisé les métastases au niveau des ganglions lymphatiques, des poumons et du foie par rapport à celles des groupes témoins[104].
D'autres données suggèrent que les tumeurs métastatiques induisent le libération d'interleukine 1 bêta , qui induit la libération d'interleukine 17 par les lymphocytes T gamma delta), supprimant les lymphocytes T CD8+ cytotoxiques et favorisant les métastases[105]. La perte de la protéine P53 dans les cellules cancéreuses induit la sécrétion de ligands WNT qui stimulent la production d’interleukine 1 bêta, provoquant ainsi une inflammation neutrophile prométastatique[106].
Extravasion[modifier | modifier le code]

Lorsque les cellules tumorales circulantes traversent de petits capillaires, elles sont piégée conduisant soit à une rupture microvasculaire, soit à une extravasation[107]. Comme les organes tels que le foie et les os possèdent des vaisseaux sinusoïdaux très perméables, les cellules tumorales circulantes colonisent plus facilement ces organes[108]. Dans d'autres organes, les cellules tumorales circulantes sont confrontées à des barrières étanches et des membranes basales qui nécessitent une médiation génétique et moléculaire pour pouvoir extravaser.
L'extravasation est un processus complexe qui implique des interactions ligand-récepteur, des chimiokines et des cellules non tumorales en circulation[75],[109]. Les intégrines, encore une fois, jouent un rôle essentiel dans la détermination des sites où l'extravasation et la colonisation[110].
L'hypothése que l’extravasation des cellules cancéreuses se produit de la même manière que la migration transendothéliale des leucocytes[75],[111],[112] a été réfuté par la mise en évidence que les cellules cancéreuses induisent une nécrose programmée des cellules endothéliales, entraînant l’extravasation des cellules métastatiques. Le traitement par la nécrostatine-1, un inhibiteur de la RIPK1 (Receptor-interacting serine/threonine-protein kinase 1)interagissant avec les récepteurs, ou par la délétion spécifique des cellules endothéliales de RIPK3 (Receptor-interacting serine/threonine-protein kinase 3) a réduit la nécroptose endothéliale et l'extravasation métastatique[113].
L'organotropisme a été abordé pour la première fois par Paget dans le cadre de l'hypothèse des « graines et du sol »[114]. La recherche sur le cancer du sein a soutenu cette hypothèse[115],[116], les chercheurs élucidant les bases génétiques de la colonisation du cancer dans des organes distants[117]. De plus, le microenvironnement de l'hôte joue un rôle dans l’extravasation et la colonisation des cellules cancéreuses à des sites spécifiques.Par exemple, dans le cancer du sein, Le flux de calcium, par exemple, a été identifié comme un mécanisme interactif entre la niche ostéogénique et les cellules tumrales , qui favorise la progression des métastases osseuses[118].
Colonisation[modifier | modifier le code]
Les cellules circulantes qui extravasent au niveau du site cible sont confrontées à des conditions de survie difficile [119]. Un certain nombre de facteurs sécrétés de la tumeur et de cellules de la moelle osseuse signalent la formation de la niche pré-métastatique dans laquelle les cellules tumorales colonisent et se développent [108],[120],[121],[122]. Outre les facteurs sécrétés de la tumeur, les exosomes jouent encore un rôle majeur. Les exosomes jouent un rôle dans l’éducation des cellules progénitrices de la moelle osseuse pour qu’elles deviennent métastatiques [122]. Des recherches ont montré des résultats similaires dans le cancer du pancréas, dans lesquels les exosomes ont initié la formation de niche pré-métastatique dans le foie [123]. Les interactions entre cellules cancéreuses et cellules hôtes sont également importantes pour une colonisation appropriée. Les hépatocytes contrôlent l’accumulation de cellules myéloïdes et la fibrose dans le foie augmentant ainsi la susceptibilité du foie à la colonisation métastatique. Dans les modèles murins de cancer du pancréas, les hépatocytes induisent la signalisation STAT3 médiée par l'interleukine 6 et augmentent la sécrétion d'amyloïde sérique A1 et A2. L'inhibition de la signalisation interleukine 6-STAT3-Amyloïde sérique empêche l'établissement d'une niche pré-métastasique et inhibe les métastases hépatiques [124].
L’établissement d’un réseau vasculaire est crucial pour une bonne colonisation métastatique. Le mimétisme vasculaire détermine la capacité de certaines cellules cancéreuses du sein à contribuer aux métastases à distance via la surexpression de serpine 2 et la secretory leukocyte protease inhibitor (SLPI) [125]. Ces deux gènes sont surexprimés préférentiellement chez les patientes humaines présentant des métastases pulmonaires du cancer du sein, ce qui suggère leur potentiel de progression métastatique [125].
Les cellules cancéreuses colonisatrices sont également capables d’utiliser les voies de signalisation neuronale pour leur croissance et leur adaptation. La proximité des cellules cancéreuses du sein avec les synapses neuronales permet aux cellules cancéreuses de détourner la signalisation du récepteur N-méthyl-D-aspartate pour favoriser les métastases cérébrales [126]. La protocadhérine 7 est une protéine qui favorise l'assemblage des jonctions lacunaires cellules cancéreuses-astrocytes composées de connexine 43. Les cellules cancéreuses métastatiques utilisent ces jonctions pour transférer le deuxième messager cGAMP vers les astrocytes, activant ainsi la voie du stimulateur des gènes de l'interféron et produisant des cytokines inflammatoires telles que l'interféron alpha et le facteur de nécrose tumorale. À leur tour, ces facteurs activent les voies STAT1 et NF-κB dans les cellules métastatiques du cerveau, favorisant ainsi la croissance tumorale et la chimiorésistance [127].
Les cellules dormantes[modifier | modifier le code]
Par définition, la dormance du cancer est une phase d'arrêt de la progression du cancer qui survient pendant la phase de formation de la tumeur primaire ou après l'invasion de sites secondaires [128]. La dormance métastatique se produit spécifiquement en raison de l'acclimatation retardée des cellules cancéreuses en diffusion vers leurs niches secondaires [129] et affecte des cellules envahissantes uniques. ou des grappes de cancer après circulation.
Chez de nombreux survivants du cancer, les cellules cancéreuses dormantes sont présentes longtemps après l'ablation radicale de la tumeur primitive et seraient responsables de rechutes tardives [129]. Deux mécanismes de dormance existeraient: la dormance angiogénique dans laquelle un équilibre est réalisé entre la division cellulaire et la mort cellulaire par absence de vascularisation des cellules cancéreuses et la dormance à médiation immunitaire dans laquelle la masse tumorale est préservée de la cytotoxicité des cellules immunitaires [130],[11]. Certains pensent que le microenvironnement de l'organe cible ordonne aux cellules tumorales circulantes d'entrer en dormance, tandis que d'autres pensent que les tumeurs primaires précodent une signature de dormance sur les cellules tumorales circulantes qui s'activent lorsque les cellules tumorales circulantes pénètrent dans le microenvironnement hôte. Une autre explication possible est que la dissémination précoce engendre des cellules tumorales circulantes qui répondent aux signaux induisant la dormance et entrent en dormance dans les organes cibles [131].
Mécanismes moléculaires de la dormance[modifier | modifier le code]

La régulation de la dormance des cellules tumorales implique des interactions réciproques entre l'environnement et les mécanismes qui contrôlent les programmes transcriptionnels [132]. La dormance unicellulaire décrit l'état de quiétude réversible dans lequel la cellule métastatique entre en réponse à des stimuli stressants, tout en exprimant le marqueur de prolifération Ki67 [128]. L'homéostasie métabolique est maintenue à l’état dormant grâce à la régulation négative de deux des voies les plus étudiées qui sont activées au cours de l’oncogenèse, les voies de signalisation RAS – MEK – ERK/MAPK et PI3K-AKT, qui jouent un rôle essentiel dans la gouvernance de la dormance des cellules cancéreuses [133].
Les facteurs sécrétés par les niches pré-métastatiques , tels que les protéines morphogénétiques osseuses dérivées des cellules mésenchymateuses et le growth arrest – specific 6 (GAS6), déplacent les cellules cancéreuses vers la dormance [134],[135]. Le facteur de croissance BMP7 active le gène suppresseur métastatique NMYC, gène régulant négativement la proteine NDRG1, entraînant une augmentation de l’activation de la kinase p38 , de l’expression de l’inhibiteur du cycle cellulaire p21 entraimant l’arrêt du cycle cellulaire [134].
Les interactions moléculaires entre la signalisation induite par les mitogènes et celle induite par le stress sont essentielles à la régulation de l'état de dormance/activation des cellules cancéreuses métastatiques. Le rapport entre le signal extracellulaire ERK1/2 et la la kinase p38 régule le cycle cellulaire. Des niveaux élevés d'activité ERK1/2 favorisent la prolifération, tandis que des niveaux élevés de p38 favorisent la dormance. L'activité accrue de la kinase p38 déclenche l'activation de la réponse protéique , qui régule positivement l'activation du facteur de transcription 6, favorisant ainsi l'arrêt et la survie des cellules [136],[137]. L'activation des voies de signalisation du stress induit un état de quiétude soutenu lié à dormance.
Cellules dormantes en cluster[modifier | modifier le code]
La dormance dans les grappes de cancers métastatiques se produit lorsque le taux de prolifération cellulaire au sein de la grappe est égal au taux d'apoptose. En tant que tel, le groupe tumoral ne se développe pas en micrométastase. Cet équilibre est obtenu grâce à une signalisation génique suppressive, une angiogenèse restreinte et/ou un microenvironnement immunitaire actif [128].
La signalisation génique suppressive peut être obtenue grâce à l'induction du gène DEC2, un gène suppresseur de tumeur. Le facteur de croissance transformant induit DEC2, qui inhibe la kinase dépendante des cyclines 4 et active p27, forçant la cellule à entrer dans un état de quiescence [138]. Bloquer la formation de vaisseaux sanguins par l'activation de la thrombospondine-1 [139] ou par l'inhibition des protéines chaperons, tels que la protéine de choc thermique de 27 kDa , pousse les amas métastatiques dans un état dormant [140].
Le système immunitaire est également un facteur majeur dans du contrôle du cancer. Les cellules T et les cellules NK, en plus des macrophages, éliminent les cellules métastatiques par cytolyse [141]. Les cellules tumorales dormantes expriment des antigènes faibles pour échapper au système immunitaire, ce qui pourrait être à l'origine d'une rechute après une immunothérapie [132].
Réveil des cellules dormantes[modifier | modifier le code]

Les chercheurs ont commencé à comprendre le processus qui permet à certaines cellules cancéreuses de devenir dormantes pendant un certain temps et de réapparaître plus tard avec une maladie récurrente. Ces cellules cancéreuses entrent dans un état de latence et de division lente en inhibant une voie de signalisation pilotée par la protéine WNT [142].De plus, ces cellules présentent des niveaux accrus des gènes de cellules souches SRY-box et SOX9, qui permettent la croissance de nouvelles tumeurs si certaines conditions existent. Pour réduire la capacité du système immunitaire à les identifier, ces cellules cancéreuses dormantes régulent négativement l’expression de molécules reconnaissables par les cellules immunitaires [142]. Cela permet aux cellules tumorales d’échapper à une réponse immunitaire jusqu’à ce que les conditions permettent le développement de métastases. Une inflammation persistante de l’organe hôte et l’établissement de pièges extracellulaires neutrophiles peuvent transformer les cellules cancéreuses dormantes en métastases agressives [143]. D’autres pensent que le passage de la dormance à l’activation se produit en ce qui concerne l’organotropisme [144] , indiquant que le microenvironnement de l’hôte joue un rôle dans le réveil des cellules. de leur état de dormance [145].Plus important encore, il a été établi que des niveaux élevés d'ERK1/2 par rapport à p38 MAPK favorisent la réactivation.
La progression tumorale[modifier | modifier le code]
La plasticité des cellules cancéreuses facilite le développement de la résistance au traitement et la progression maligne. La plasticité confère aux cellules cancéreuses la capacité de basculer dynamiquement entre un état différencié, avec un potentiel tumorigène limité, et un état de cellules indifférenciées, responsable de la croissance tumorale à long terme. Cependant, les chercheurs gardent espoir que la plasticité des cellules cancéreuses puisse être exploitée à des fins thérapeutiques. Certains ont forcé la trans différenciation des cellules cancéreuses du sein dans leur microenvironnement tumoral en adipocytes post-mitotiques et fonctionnels en utilisant une thérapie combinée d'inhibiteurs de la mitogen-activated protein kinase kinase (MEKK) et de rosiglitazone, un médicament antidiabétique, inhibant ainsi le processus métastatique [146]. Les criblages in vivo à l'échelle du génome peuvent identifier de nouveaux hôtes. régulateurs de la colonisation métastatique. Des études in vivo ont identifié plusieurs gènes qui, lorsqu'ils sont perturbés, modifient la capacité des cellules tumorales à établir des métastases [147]. Souvent, les cellules progénitrices endovasculaires fonctionnent comme des précurseurs des cellules endothéliales [148]. Ces cellules progénitrices expriment le facteur de transcription SOX18 et ne sont donc pas affectées par les thérapies. qui ciblent le facteur de croissance de l’endothélium vasculaire. En supprimant la signalisation Notch, SOX18 est inhibée, ce qui arrête ensuite les métastases du mélanome dans les modèles murins .
Dans de nombreux cas, les glucocorticoïdes sont utilisés pour traiter les patients présentant des complications liées au cancer. La progression du cancer du sein est initiée par l’augmentation des taux d’hormones de stress et de glucocorticoïdes, qui activent ensuite les récepteurs glucocorticoïdes du site secondaire, améliorent la colonisation du cancer et diminuent les taux de survie [149].Cela suggère la prudence lors du traitement par corticothérapie des patientes atteintes d’un cancer.
Malgré l’efficacité affichée de la chimiothérapie cytotoxique dans le traitement du cancer du sein invasif, il a été démontré que le traitement présente des effets prométastatiques [150]. Le paclitaxel et la doxorubicine déclenchent la production de vésicules extracellulaires dérivées de la tumeur dans des modèles de cancer du sein chimiorésistant chez la souris. Ces vésicules facilitent la colonisation de tumeurs sur des sites métastatiques dans les poumons [150].
Traitement par suppresseur de métastases[modifier | modifier le code]

Les suppresseurs de métastases inhibent la croissance et la prolifération du cancer au niveau du site métastatique sans affecter la tumeur primaire [151],[152]. Ils ciblent les voies oncogènes et les protéines impliquées dans l'invasion et l'éventuelle colonisation métastatique. Par exemple, la A-kinase-anchoring protein 8 est un facteur régulateur d'épissage qui supprime le microenvirronement tumoral et les métastases du cancer du sein [153]. Dans les cellules hautement métastatiques, les suppresseurs de métastases sont généralement régulés négativement par rapport aux cellules tumorales primaires [154],[155],[151]. Au cours de la dernière décennie, un nombre important de des suppresseurs de métastases ont été identifiés . Plus particulièrement, les micro-ARNs qui suppriment les oncogènes et inhibent la signalisation tumorigène ont été reconnus et explorés comme biomarqueurs potentiels et cibles des métastases .
Métastase et cancer primaire[modifier | modifier le code]
Théoriquement, une métastase est toujours la conséquence d’un cancer primaire, puisqu’il s’agit d’une tumeur dont le point de départ se trouve dans une ou plusieurs cellules cancéreuses situées dans une autre partie du corps. Malgré tout, plus de 10 % des patients qui se présentent aux services de cancérologie ont des métastases sans qu’on trouve une tumeur primaire. Dans ce cas, les médecins parlent d’une tumeur primaire « inconnue » ou « occulte ». Les études ont montré que si des questions simples ne permettent pas de connaître la source du cancer (quand on crache du sang, c’est probablement le poumon ; quand on urine du sang c’est probablement la vessie), une imagerie complexe ne fera pas mieux. Dans certains de ces cas, un cancer primaire apparaîtra par la suite.
L'utilisation de l'immunohistochimie permet aux anatomopathologistes de mettre un nom sur un grand nombre de ces métastases. Cependant, l'imagerie de la zone indiquée ne révèle que de temps en temps un cancer primaire. Dans des cas rares (de mélanome, par exemple), aucune tumeur primaire ne peut être trouvée, même à l'autopsie. On a donc été amené à penser que certaines tumeurs primaires peuvent régresser complètement tout en laissant leurs métastases derrière elles.
Diagnostic des tumeurs cancéreuses primaires et secondaires[modifier | modifier le code]
Dans une tumeur métastatique les cellules ressemblent à celles de la tumeur primaire. Une fois que le tissu cancéreux a été examiné au microscope pour déterminer le type de cellule, un médecin peut dire généralement si ce type de cellule se trouve normalement dans la partie du corps dont provient le tissu prélevé.
Par exemple, les cellules de cancer du sein ont le même aspect si on les trouve dans le sein ou si elles ont gagné une autre partie du corps. Ainsi, si un échantillon de tissu prélevé dans une tumeur du poumon contient les cellules qui ressemblent à des cellules de sein, le médecin jugera que la tumeur du poumon est une tumeur secondaire. Cependant, il peut être souvent très difficile de déterminer la tumeur primaire, et le pathologiste doit employer plusieurs mesures techniques associées, comme l’immunohistochimie, le FISH (hybridation fluorescente in situ) et quelques autres. Malgré les techniques utilisées, dans certains cas il n’est pas possible d’identifier la tumeur primaire.
On peut trouver des cancers métastatiques en même temps que la tumeur primaire, ou bien des mois voire des années plus tard. Quand on trouve une deuxième tumeur chez un patient qui a déjà été traité pour un cancer dans le passé, il s’agit plus souvent d’une métastase que d'une nouvelle tumeur primaire.
Traitements des cancers métastatiques[modifier | modifier le code]
Quand le cancer s’est métastasé, on peut le traiter par la chimiothérapie, la radiothérapie, la biothérapie, l’hormonothérapie, l'immunothérapie, la chirurgie, ou une combinaison de ces méthodes. Le choix du traitement dépend généralement du type de cancer primaire, de la taille et de l'emplacement de la métastase, de l'âge du patient et de sa santé générale, ainsi que des types de traitements employés précédemment. Pour les patients chez qui on a diagnostiqué une tumeur primaire occulte, il est toujours possible de traiter la maladie même si cette tumeur primaire ne peut pas être localisée.
Les traitements actuels n'aboutissent pas souvent à une guérison définitive. Toutefois certaines tumeurs comme le cancer des testicules restent curables dans la plupart des cas même au stade métastatique.
Notes et références[modifier | modifier le code]
- Yves Bécouarn et Bernard Hoerni (dir.), Cancérologie et hématologie, Paris, Masson, coll. « Pour le praticien », , XII-315 p., ill., couv. ill. ; 28 cm (ISBN 2-225-83393-1 et 978-2-225-83393-9, BNF 37704980, lire en ligne), p. 47.
- (en) Michael K. Connolly, Jon Mallen-St. Clair, Andrea S. Bedrosian, Ashim Malhotra, Valery Vera, Junaid Ibrahim, Justin Henning, H. Leon Pachter, Dafna Bar-Sagi, Alan B. Frey et George Miller, « Distinct populations of metastases-enabling myeloid cells expand in the liver of mice harboring invasive and preinvasive intra-abdominal tumor », Journal of Leukocyte Biology, vol. 87, no 4, , p. 713-725 (ISSN 0741-5400 et 1938-3673, DOI 10.1189/jlb.0909607, résumé, lire en ligne).
- Maryse Delehedde et Frédéric Denhez, Que sait-on du cancer ?, EDP Sciences, , 207 p. (ISBN 978-2-86883-834-6, OCLC 300319375, lire en ligne), p. 35
- (en) Judah Folkman, « Tumor Angiogenesis : Therapeutic Implications », The New England Journal of Medicine, vol. 285, no 21, , p. 1182-1186 (ISSN 1533-4406 et 0028-4793, PMID 4938153, DOI 10.1056/NEJM197111182852108, résumé).
- Arthur W. Lambert, Diwakar R. Pattabiraman et Robert A. Weinberg, « Emerging Biological Principles of Metastasis », Cell, vol. 168, no 4, , p. 670–691 (ISSN 0092-8674, PMID 28187288, PMCID PMC5308465, DOI 10.1016/j.cell.2016.11.037, lire en ligne, consulté le )
- Arthur W. Lambert, Diwakar R. Pattabiraman et Robert A. Weinberg, « Emerging Biological Principles of Metastasis », Cell, vol. 168, no 4, , p. 670–691 (ISSN 0092-8674, PMID 28187288, PMCID PMC5308465, DOI 10.1016/j.cell.2016.11.037, lire en ligne, consulté le )
- (en) Samuel F. Bakhoum, Bryan Ngo, Ashley M. Laughney et Julie-Ann Cavallo, « Chromosomal instability drives metastasis through a cytosolic DNA response », Nature, vol. 553, no 7689, , p. 467–472 (ISSN 1476-4687, PMID 29342134, PMCID PMC5785464, DOI 10.1038/nature25432, lire en ligne, consulté le )
- (en) Doris P. Tabassum et Kornelia Polyak, « Tumorigenesis: it takes a village », Nature Reviews Cancer, vol. 15, no 8, , p. 473–483 (ISSN 1474-1768, DOI 10.1038/nrc3971, lire en ligne, consulté le )
- (en) Gunes Gundem, Peter Van Loo, Barbara Kremeyer et Ludmil B. Alexandrov, « The evolutionary history of lethal metastatic prostate cancer », Nature, vol. 520, no 7547, , p. 353–357 (ISSN 1476-4687, PMID 25830880, PMCID PMC4413032, DOI 10.1038/nature14347, lire en ligne, consulté le )
- Hanahan, D. & Weinberg, R. A. Hallmarks of cancer: the next generation. Cell 144, 646–674 (2011).
- Fouad, Y. A. & Aanei, C. Revisiting the hallmarks of cancer. Am. J. Cancer Res. 7, 1016–1036 (2017)
- Ye, X. & Weinberg, R. A. Epithelial-mesenchymal plasticity: a central regulator of cancer progression. Trends Cell Biol. 25, 675–686 (2015).
- Nieto, M. A., Huang, R. Y. J., Jackson, R. A. & Thiery, J. P. Emt: 2016. Cell 166, 21–45 (2016).
- Katsuno, Y., Lamouille, S. & Derynck, R. TGF-beta signaling and epithelial-mesenchymal transition in cancer progression. Curr. Opin. Oncol. 25, 76–84 (2013).
- De Craene, B. & Berx, G. Regulatory networks defining EMT during cancer initiation and progression. Nat. Rev. Cancer 13, 97–110 (2013)
- Pastushenko, I. et al. Identification of the tumour transition states occurring during EMT. Nature 556, 463 (2018).
- Erdogan, B. et al. Cancer-associated fibroblasts promote directional cancer cell migration by aligning fibronectin. J. Cell Biol. 216, 3799–3816 (2017).
- Rankin, E. B. & Giaccia, A. J. Hypoxic control of metastasis. Science 352, 175–180 (2016).
- Lamouille, S., Xu, J. & Derynck, R. Molecular mechanisms of epithelial-mesenchymal transition. Nat. Rev. Mol. Cell Biol. 15, 178–196 (2014).
- Diepenbruck, M. & Christofori, G. Epithelial-mesenchymal transition (EMT) and metastasis: yes, no, maybe? Curr. Opin. Cell Biol. 43, 7–13 (2016).
- Fischer, K. R. et al. Epithelial-to-mesenchymal transition is not required for lung metastasis but contributes to chemoresistance. Nature 527, 472–476 (2015).
- De Craene, B. & Berx, G. Regulatory networks defining EMT during cancer initiation and progression. Nat. Rev. Cancer 13, 97–110 (2013).
- Zheng, X. F. et al. Epithelial-to-mesenchymal transition is dispensable for metastasis but induces chemoresistance in pancreatic cancer. Nature 527, 525 (2015).
- Esposito, M. et al. Bone vascular niche E-selectin induces mesenchymal-epithelial transition and Wnt activation in cancer cells to promote bone metastasis. Nat. Cell Biol. 21, 627–639 (2019).
- (en) Héctor Peinado, Haiying Zhang, Irina R. Matei et Bruno Costa-Silva, « Pre-metastatic niches: organ-specific homes for metastases », Nature Reviews Cancer, vol. 17, no 5, , p. 302–317 (ISSN 1474-1768, DOI 10.1038/nrc.2017.6, lire en ligne, consulté le )
- Anoek Zomer, Carrie Maynard, Frederik Johannes Verweij et Alwin Kamermans, « In Vivo Imaging Reveals Extracellular Vesicle-Mediated Phenocopying of Metastatic Behavior », Cell, vol. 161, no 5, , p. 1046–1057 (ISSN 0092-8674, PMID 26000481, PMCID PMC4448148, DOI 10.1016/j.cell.2015.04.042, lire en ligne, consulté le )
- (en) « Cancer-cell transfer filmed », Nature, vol. 521, no 7553, , p. 396–396 (ISSN 1476-4687, DOI 10.1038/521396d, lire en ligne, consulté le )
- (en) Ulrich H. Weidle, Fabian Birzele, Gwen Kollmorgen et Rüdiger Rüger, « The Multiple Roles of Exosomes in Metastasis », Cancer Genomics & Proteomics, vol. 14, no 1, , p. 1–15 (ISSN 1109-6535 et 1790-6245, PMID 28031234, lire en ligne, consulté le )
- Jacob A. Tickner, Aaron J. Urquhart, Sally-Anne Stephenson et Derek J. Richard, « Functions and Therapeutic Roles of Exosomes in Cancer », Frontiers in Oncology, vol. 4, (ISSN 2234-943X, PMID 24904836, PMCID PMC4034415, DOI 10.3389/fonc.2014.00127, lire en ligne, consulté le )
- (en) Dinari A. Harris, Sajni H. Patel, Marjan Gucek et An Hendrix, « Exosomes Released from Breast Cancer Carcinomas Stimulate Cell Movement », PLOS ONE, vol. 10, no 3, , e0117495 (ISSN 1932-6203, PMID 25798887, PMCID PMC4370373, DOI 10.1371/journal.pone.0117495, lire en ligne, consulté le )
- Ramesh Singh, Radhika Pochampally, Kounosuke Watabe et Zhaohui Lu, « Exosome-mediated transfer of miR-10b promotes cell invasion in breast cancer », Molecular Cancer, vol. 13, no 1, , p. 256 (ISSN 1476-4598, PMID 25428807, PMCID PMC4258287, DOI 10.1186/1476-4598-13-256, lire en ligne, consulté le )
- McCready, J., Sims, J. D., Chan, D. & Jay, D. G. Secretion of extracellular hsp90alpha via exosomes increases cancer cell motility: a role for plasminogen activation. BMC Cancer 10, 294 (2010).
- Fu, H., Yang, H., Zhang, X. & Xu, W. The emerging roles of exosomes in tumor-stroma interaction. J. Cancer Res Clin. Oncol. 142, 1897–1907 (2016).
- Syn, N. et al. Exosome-mediated metastasis: from epithelial-mesenchymal transition to escape from immunosurveillance. Trends Pharm. Sci. 37, 606–617 (2016).
- (en) M. Aga, G. L. Bentz, S. Raffa et M. R. Torrisi, « Exosomal HIF1α supports invasive potential of nasopharyngeal carcinoma-associated LMP1-positive exosomes », Oncogene, vol. 33, no 37, , p. 4613–4622 (ISSN 1476-5594, PMID 24662828, PMCID PMC4162459, DOI 10.1038/onc.2014.66, lire en ligne, consulté le )
- (en) Yiwen You, Ying Shan, Jing Chen et Huijun Yue, « Matrix metalloproteinase 13‐containing exosomes promote nasopharyngeal carcinoma metastasis », Cancer Science, vol. 106, no 12, , p. 1669–1677 (ISSN 1347-9032 et 1349-7006, PMID 26362844, PMCID PMC4714673, DOI 10.1111/cas.12818, lire en ligne, consulté le )
- (en) C. A. Franzen, R. H. Blackwell, V. Todorovic et K. A. Greco, « Urothelial cells undergo epithelial-to-mesenchymal transition after exposure to muscle invasive bladder cancer exosomes », Oncogenesis, vol. 4, no 8, , e163–e163 (ISSN 2157-9024, PMID 26280654, PMCID PMC4632072, DOI 10.1038/oncsis.2015.21, lire en ligne, consulté le )
- Tarbe, N. et al. Identification of rat pancreatic carcinoma genes associated with lymphogenous metastasis. Anticancer Res. 22, 2015–2027 (2002).
- Wei Mu, Sanyukta Rana et Margot Zöller, « Host Matrix Modulation by Tumor Exosomes Promotes Motility and Invasiveness », Neoplasia, vol. 15, no 8, , p. 875–IN4 (ISSN 1476-5586, PMID 23908589, PMCID PMC3730040, DOI 10.1593/neo.13786, lire en ligne, consulté le )
- (en) Muller Fabbri, Alessio Paone, Federica Calore et Roberta Galli, « MicroRNAs bind to Toll-like receptors to induce prometastatic inflammatory response », Proceedings of the National Academy of Sciences, vol. 109, no 31, (ISSN 0027-8424 et 1091-6490, PMID 22753494, PMCID PMC3412003, DOI 10.1073/pnas.1209414109, lire en ligne, consulté le )
- (en) Shu-biao Ye, Ze-Lei Li, Dong-hua Luo et Bi-jun Huang, « Tumor-derived exosomes promote tumor progression and T-cell dysfunction through the regulation of enriched exosomal microRNAs in human nasopharyngeal carcinoma », Oncotarget, vol. 5, no 14, , p. 5439–5452 (ISSN 1949-2553, PMID 24978137, PMCID PMC4170615, DOI 10.18632/oncotarget.2118, lire en ligne, consulté le )
- Aled Clayton, Saly Al-Taei, Jason Webber et Malcolm D. Mason, « Cancer Exosomes Express CD39 and CD73, Which Suppress T Cells through Adenosine Production », The Journal of Immunology, vol. 187, no 2, , p. 676–683 (ISSN 0022-1767 et 1550-6606, DOI 10.4049/jimmunol.1003884, lire en ligne, consulté le )
- (en) Héctor Peinado, Maša Alečković, Simon Lavotshkin et Irina Matei, « Melanoma exosomes educate bone marrow progenitor cells toward a pro-metastatic phenotype through MET », Nature Medicine, vol. 18, no 6, , p. 883–891 (ISSN 1546-170X, PMID 22635005, PMCID PMC3645291, DOI 10.1038/nm.2753, lire en ligne, consulté le )
- Hood, J. L., San, R. S. & Wickline, S. A. Exosomes released by melanoma cells prepare sentinel lymph nodes for tumor metastasis. Cancer Res. 71, 3792–3801 (2011).
- (en) Bruno Costa-Silva, Nicole M. Aiello, Allyson J. Ocean et Swarnima Singh, « Pancreatic cancer exosomes initiate pre-metastatic niche formation in the liver », Nature Cell Biology, vol. 17, no 6, , p. 816–826 (ISSN 1476-4679, PMID 25985394, PMCID PMC5769922, DOI 10.1038/ncb3169, lire en ligne, consulté le )
- Nicholas Syn, Lingzhi Wang, Gautam Sethi et Jean-Paul Thiery, « Exosome-Mediated Metastasis: From Epithelial–Mesenchymal Transition to Escape from Immunosurveillance », Trends in Pharmacological Sciences, vol. 37, no 7, , p. 606–617 (ISSN 0165-6147, DOI 10.1016/j.tips.2016.04.006, lire en ligne, consulté le )
- (en) Ayuko Hoshino, Bruno Costa-Silva, Tang-Long Shen et Goncalo Rodrigues, « Tumour exosome integrins determine organotropic metastasis », Nature, vol. 527, no 7578, , p. 329–335 (ISSN 1476-4687, PMID 26524530, PMCID PMC4788391, DOI 10.1038/nature15756, lire en ligne, consulté le )
- Yue, S., Mu, W., Erb, U. & Zöller, M. The tetraspanins CD151 and Tspan8 are essential exosome components for the crosstalk between cancer initiating cells and their surrounding. Oncotarget 6, 2366 (2015).
- Valbona Luga, Liang Zhang, Alicia M. Viloria-Petit et Abiodun A. Ogunjimi, « Exosomes Mediate Stromal Mobilization of Autocrine Wnt-PCP Signaling in Breast Cancer Cell Migration », Cell, vol. 151, no 7, , p. 1542–1556 (ISSN 0092-8674, DOI 10.1016/j.cell.2012.11.024, lire en ligne, consulté le )
- Tyson J. Smyth, Jasmina S. Redzic, Michael W. Graner et Thomas J. Anchordoquy, « Examination of the specificity of tumor cell derived exosomes with tumor cells in vitro », Biochimica et Biophysica Acta (BBA) - Biomembranes, vol. 1838, no 11, , p. 2954–2965 (ISSN 0005-2736, PMID 25102470, PMCID PMC5657189, DOI 10.1016/j.bbamem.2014.07.026, lire en ligne, consulté le )
- (en) Margot Zöller, « Tetraspanins: push and pull in suppressing and promoting metastasis », Nature Reviews Cancer, vol. 9, no 1, , p. 40–55 (ISSN 1474-1768, DOI 10.1038/nrc2543, lire en ligne, consulté le )
- (en) Asuka Nanbo, Eri Kawanishi, Ryuji Yoshida et Hironori Yoshiyama, « Exosomes Derived from Epstein-Barr Virus-Infected Cells Are Internalized via Caveola-Dependent Endocytosis and Promote Phenotypic Modulation in Target Cells », Journal of Virology, vol. 87, no 18, , p. 10334–10347 (ISSN 0022-538X et 1098-5514, PMID 23864627, PMCID PMC3753980, DOI 10.1128/JVI.01310-13, lire en ligne, consulté le )
- (en) Lin Zhang, Siyuan Zhang, Jun Yao et Frank J. Lowery, « Microenvironment-induced PTEN loss by exosomal microRNA primes brain metastasis outgrowth », Nature, vol. 527, no 7576, , p. 100–104 (ISSN 1476-4687, PMID 26479035, PMCID PMC4819404, DOI 10.1038/nature15376, lire en ligne, consulté le )
- Karamanos, N. K. et al. Proteoglycan chemical diversity drives multifunctional cell regulation and therapeutics. Chem. Rev. 118, 9152–9232 (2018).
- Frantz, C., Stewart, K. M. & Weaver, V. M. The extracellular matrix at a glance. J. Cell Sci. 123, 4195–4200 (2010).
- Theocharis, A. D., Skandalis, S. S., Gialeli, C. & Karamanos, N. K. Extracellular matrix structure. Adv. Drug Deliv. Rev. 97, 4–27 (2016).
- Maquart, F.-X. et al. An introduction to matrikines: extracellular matrix-derived peptides which regulate cell activity: implication in tumor invasion. Crit. Rev. Oncol. Hematol. 49, 199–202 (2004).
- Sonnenschein, C. & Soto, A. M. Carcinogenesis explained within the context of a theory of organisms. Prog. Biophys. Mol. Biol. 122, 70–76 (2016).
- Maffini, M. V. et al. The stroma as a crucial target in rat mammary gland carcinogenesis. J. Cell Sci. 117, 1495–1502 (2004).
- Barcellos-Hoff, M. H. & Ravani, S. A. Irradiated mammary gland stroma promotes the expression of tumorigenic potential by unirradiated epithelial cells. Cancer Res. 60, 1254–1260 (2000)
- Guerra, L., Odorisio, T., Zambruno, G. & Castiglia, D. Stromal microenvironment in type VII collagen-deficient skin: The ground for squamous cell carcinoma development. Matrix Biol. 63, 1–10 (2017).
- S Curran et G.I Murray, « Matrix metalloproteinases », European Journal of Cancer, vol. 36, no 13, , p. 1621–1630 (ISSN 0959-8049, DOI 10.1016/s0959-8049(00)00156-8, lire en ligne, consulté le )
- Kai Kessenbrock, Vicki Plaks et Zena Werb, « Matrix Metalloproteinases: Regulators of the Tumor Microenvironment », Cell, vol. 141, no 1, , p. 52–67 (ISSN 0092-8674, PMID 20371345, PMCID PMC2862057, DOI 10.1016/j.cell.2010.03.015, lire en ligne, consulté le )
- (en) Laurie A. Shuman Moss, Sandra Jensen-Taubman et William G. Stetler-Stevenson, « Matrix Metalloproteinases: Changing Roles in Tumor Progression and Metastasis », The American Journal of Pathology, vol. 181, no 6, , p. 1895–1899 (ISSN 0002-9440 et 1525-2191, PMID 23063657, PMCID PMC3506216, DOI 10.1016/j.ajpath.2012.08.044, lire en ligne, consulté le )
- (en) Mikala Egeblad et Zena Werb, « New functions for the matrix metalloproteinases in cancer progression », Nature Reviews Cancer, vol. 2, no 3, , p. 161–174 (ISSN 1474-1768, DOI 10.1038/nrc745, lire en ligne, consulté le )
- (en) Elin Hadler-Olsen, Jan-Olof Winberg et Lars Uhlin-Hansen, « Matrix metalloproteinases in cancer: their value as diagnostic and prognostic markers and therapeutic targets », Tumor Biology, vol. 34, no 4, , p. 2041–2051 (ISSN 1423-0380, DOI 10.1007/s13277-013-0842-8, lire en ligne, consulté le )
- (en) Ilaria Elia, Matteo Rossi, Steve Stegen et Dorien Broekaert, « Breast cancer cells rely on environmental pyruvate to shape the metastatic niche », Nature, vol. 568, no 7750, , p. 117–121 (ISSN 1476-4687, PMID 30814728, PMCID PMC6451642, DOI 10.1038/s41586-019-0977-x, lire en ligne, consulté le )
- (en) Beth A. Helmink, M. A. Wadud Khan, Amanda Hermann et Vancheswaran Gopalakrishnan, « The microbiome, cancer, and cancer therapy », Nature Medicine, vol. 25, no 3, , p. 377–388 (ISSN 1546-170X, DOI 10.1038/s41591-019-0377-7, lire en ligne, consulté le )
- Pushalkar, S. et al. The pancreatic cancer microbiome promotes oncogenesis by induction of innate and adaptive immune suppression. Cancer Discov. 8, 403–416 (2018).
- Cronin, M. et al. Orally administered bifidobacteria as vehicles for delivery of agents to systemic tumors. Mol. Ther. 18, 1397–1407 (2010).
- Panebianco, C., Andriulli, A. & Pazienza, V. Pharmacomicrobiomics: exploiting the drug-microbiota interactions in anticancer therapies. Microbiome 6, 92 (2018).
- Lehouritis, P. et al. Local bacteria affect the efficacy of chemotherapeutic drugs. Sci. Rep. 5, 14554 (2015).
- (en) Leore T. Geller, Michal Barzily-Rokni, Tal Danino et Oliver H. Jonas, « Potential role of intratumor bacteria in mediating tumor resistance to the chemotherapeutic drug gemcitabine », Science, vol. 357, no 6356, , p. 1156–1160 (ISSN 0036-8075 et 1095-9203, PMID 28912244, PMCID PMC5727343, DOI 10.1126/science.aah5043, lire en ligne, consulté le )
- (en) TaChung Yu, Fangfang Guo, Yanan Yu et Tiantian Sun, « Fusobacterium nucleatum Promotes Chemoresistance to Colorectal Cancer by Modulating Autophagy », Cell, vol. 170, no 3, , p. 548–563.e16 (PMID 28753429, PMCID PMC5767127, DOI 10.1016/j.cell.2017.07.008, lire en ligne, consulté le )
- Reymond, N., d’Agua, B. B. & Ridley, A. J. Crossing the endothelial barrier during metastasis. Nat. Rev. Cancer 13, 858–870 (2013).
- Bockhorn, M., Jain, R. K. & Munn, L. L. Active versus passive mechanisms in metastasis: do cancer cells crawl into vessels, or are they pushed? Lancet Oncol. 8, 444–448 (2007).
- Zervantonakis, I. K. et al. Three-dimensional microfluidic model for tumor cell intravasation and endothelial barrier function. Proc. Natl Acad. Sci. USA 109, 13515–13520 (2012).
- Wong, A. D. & Searson, P. C. Mitosis-mediated intravasation in a tissue-engineered tumor-microvessel platform. Cancer Res. 77, 6453–6461 (2017).
- Denais, C. M. et al. Nuclear envelope rupture and repair during cancer cell migration. Science 352, 353–358 (2016).
- Hamidi, H. & Ivaska, J. Every step of the way: integrins in cancer progression and metastasis. Nat. Rev. Cancer 18, 532–547 (2018).
- Padmanaban, V. et al. E-cadherin is required for metastasis in multiple models of breast cancer. Nature 573, 439–444 (2019).
- Pantel, K. & Speicher, M. R. The biology of circulating tumor cells. Oncogene 35, 1216–1224 (2016).
- Gao, H. et al. The BMP inhibitor Coco reactivates breast cancer cells at lung metastatic sites. Cell 150, 764–779 (2012).
- Lu, X. et al. VCAM-1 promotes osteolytic expansion of indolent bone micrometastasis of breast cancer by engaging alpha4beta1-positive osteoclast progenitors. Cancer Cell. 20, 701–714 (2011).
- (en) Nicola Aceto, Aditya Bardia, David T. Miyamoto et Maria C. Donaldson, « Circulating Tumor Cell Clusters Are Oligoclonal Precursors of Breast Cancer Metastasis », Cell, vol. 158, no 5, , p. 1110–1122 (PMID 25171411, PMCID PMC4149753, DOI 10.1016/j.cell.2014.07.013, lire en ligne, consulté le )
- (en) Min Yu, Aditya Bardia, Ben S. Wittner et Shannon L. Stott, « Circulating Breast Tumor Cells Exhibit Dynamic Changes in Epithelial and Mesenchymal Composition », Science, vol. 339, no 6119, , p. 580–584 (ISSN 0036-8075 et 1095-9203, PMID 23372014, PMCID PMC3760262, DOI 10.1126/science.1228522, lire en ligne, consulté le )
- (en) Dan G. Duda, Annique M. M. J. Duyverman, Mitsutomo Kohno et Matija Snuderl, « Malignant cells facilitate lung metastasis by bringing their own soil », Proceedings of the National Academy of Sciences, vol. 107, no 50, , p. 21677–21682 (ISSN 0027-8424 et 1091-6490, PMID 21098274, PMCID PMC3003109, DOI 10.1073/pnas.1016234107, lire en ligne, consulté le )
- Joshua Leach, Jennifer P. Morton et Owen J. Sansom, « Neutrophils: Homing in on the myeloid mechanisms of metastasis », Molecular Immunology, vol. 110, , p. 69–76 (ISSN 0161-5890, PMID 29269005, PMCID PMC6544568, DOI 10.1016/j.molimm.2017.12.013, lire en ligne, consulté le )
- (en) Laurie J. Gay et Brunhilde Felding-Habermann, « Contribution of platelets to tumour metastasis », Nature Reviews Cancer, vol. 11, no 2, , p. 123–134 (ISSN 1474-1768, PMID 21258396, PMCID PMC6894505, DOI 10.1038/nrc3004, lire en ligne, consulté le )
- Placke, T. et al. Platelet-derived MHC class I confers a pseudonormal phenotype to cancer cells that subverts the antitumor reactivity of natural killer immune cells. Cancer Res. 72, 440–448 (2012).
- Changyuan Hu, Renpin Chen, Wenjing Chen et Wenyang Pang, « Thrombocytosis is a significant indictor of hypercoagulability, prognosis and recurrence in gastric cancer », Experimental and Therapeutic Medicine, vol. 8, no 1, , p. 125–132 (ISSN 1792-0981, PMID 24944610, PMCID PMC4061185, DOI 10.3892/etm.2014.1699, lire en ligne, consulté le )
- Boris Strilic et Stefan Offermanns, « Intravascular Survival and Extravasation of Tumor Cells », Cancer Cell, vol. 32, no 3, , p. 282–293 (ISSN 1535-6108, DOI 10.1016/j.ccell.2017.07.001, lire en ligne, consulté le )
- Hon S. Leong, Amy E. Robertson, Konstantin Stoletov et Sean J. Leith, « Invadopodia Are Required for Cancer Cell Extravasation and Are a Therapeutic Target for Metastasis », Cell Reports, vol. 8, no 5, , p. 1558–1570 (ISSN 2211-1247, DOI 10.1016/j.celrep.2014.07.050, lire en ligne, consulté le )
- Konstantin Stoletov, Hisashi Kato, Erin Zardouzian et Jonathan Kelber, « Visualizing extravasation dynamics of metastatic tumor cells », Journal of Cell Science, vol. 123, no 13, , p. 2332–2341 (ISSN 1477-9137 et 0021-9533, PMID 20530574, PMCID PMC2886748, DOI 10.1242/jcs.069443, lire en ligne, consulté le )
- Dagmar Schumacher, Boris Strilic, Kishor Kumar Sivaraj et Nina Wettschureck, « Platelet-Derived Nucleotides Promote Tumor-Cell Transendothelial Migration and Metastasis via P2Y2 Receptor », Cancer Cell, vol. 24, no 1, , p. 130–137 (ISSN 1535-6108, DOI 10.1016/j.ccr.2013.05.008, lire en ligne, consulté le )
- (en) Hans Raskov, Adile Orhan, Ali Salanti et Ismail Gögenur, « Premetastatic niches, exosomes and circulating tumor cells: Early mechanisms of tumor dissemination and the relation to surgery », International Journal of Cancer, vol. 146, no 12, , p. 3244–3255 (ISSN 0020-7136 et 1097-0215, DOI 10.1002/ijc.32820, lire en ligne, consulté le )
- (en) Sjoerd van Helvert, Cornelis Storm et Peter Friedl, « Mechanoreciprocity in cell migration », Nature Cell Biology, vol. 20, no 1, , p. 8–20 (ISSN 1476-4679, PMID 29269951, PMCID PMC5943039, DOI 10.1038/s41556-017-0012-0, lire en ligne, consulté le )
- Gautier Follain, Naël Osmani, Ana Sofia Azevedo et Guillaume Allio, « Hemodynamic Forces Tune the Arrest, Adhesion, and Extravasation of Circulating Tumor Cells », Developmental Cell, vol. 45, no 1, , p. 33–52.e12 (ISSN 1534-5807, DOI 10.1016/j.devcel.2018.02.015, lire en ligne, consulté le )
- Entenberg, D. et al. A permanent window for the murine lung enables high-resolution imaging of cancer metastasis. Nat. Methods 15, 73 (2018).
- Goetz, J. G. Metastases go with the flow. Science 362, 999–1000 (2018).
- Le Gal, K. et al. Antioxidants can increase melanoma metastasis in mice. Sci. Transl. Med. 7, 308re8 (2015).R
- Adrienne Boire, Yilong Zou, Jason Shieh et Danilo G. Macalinao, « Complement Component 3 Adapts the Cerebrospinal Fluid for Leptomeningeal Metastasis », Cell, vol. 168, no 6, , p. 1101–1113.e13 (ISSN 0092-8674, PMID 28283064, PMCID PMC5405733, DOI 10.1016/j.cell.2017.02.025, lire en ligne, consulté le )
- Raffaella Bonecchi, Emanuela Galliera, Elena M. Borroni et Massimiliano M. Corsi, « Chemokines and chemokine receptors: an overview », Frontiers in Bioscience-Landmark, vol. 14, no 2, , p. 540–551 (ISSN 2768-6701, DOI 10.2741/3261, lire en ligne, consulté le )
- Jayatilaka, H. et al. Synergistic IL-6 and IL-8 paracrine signalling pathway infers a strategy to inhibit tumour cell migration. Nat. Commun. 8, 15584 (2017).
- (en) Seth B. Coffelt, Kelly Kersten, Chris W. Doornebal et Jorieke Weiden, « IL-17-producing γδ T cells and neutrophils conspire to promote breast cancer metastasis », Nature, vol. 522, no 7556, , p. 345–348 (ISSN 1476-4687, PMID 25822788, PMCID PMC4475637, DOI 10.1038/nature14282, lire en ligne, consulté le )
- Wellenstein, M. D. et al. Loss of p53 triggers WNT-dependent systemic inflammation to drive breast cancer metastasis. Nature 572, 538–542, (2019).
- (en) Joan Massagué et Anna C. Obenauf, « Metastatic colonization by circulating tumour cells », Nature, vol. 529, no 7586, , p. 298–306 (ISSN 1476-4687, PMID 26791720, PMCID PMC5029466, DOI 10.1038/nature17038, lire en ligne, consulté le )
- Fouad, Y. A. & Aanei, C. Revisiting the hallmarks of cancer. Am. J. Cancer Res. 7, 1016–1036 (2017).
- Alix-Panabieres, C. & Pantel, K. Clinical applications of circulating tumor cells and circulating tumor DNA as liquid biopsy. Cancer Discov. 6, 479–491 (2016).
- (en) Hellyeh Hamidi et Johanna Ivaska, « Every step of the way: integrins in cancer progression and metastasis », Nature Reviews Cancer, vol. 18, no 9, , p. 533–548 (ISSN 1474-1768, PMID 30002479, PMCID PMC6629548, DOI 10.1038/s41568-018-0038-z, lire en ligne, consulté le )
- Labelle, M. & Hynes, R. O. The initial hours of metastasis: the importance of cooperative host-tumor cell interactions during hematogenous dissemination. Cancer Discov. 2, 1091–1099 (2012).
- Joyce, J. A. & Pollard, J. W. Microenvironmental regulation of metastasis. Nat. Rev. Cancer 9, 239–252 (2009)
- (en) Boris Strilic, Lida Yang, Julián Albarrán-Juárez et Laurens Wachsmuth, « Tumour-cell-induced endothelial cell necroptosis via death receptor 6 promotes metastasis », Nature, vol. 536, no 7615, , p. 215–218 (ISSN 1476-4687, DOI 10.1038/nature19076, lire en ligne, consulté le )
- Langley, R. R. & Fidler, I. J. The seed and soil hypothesis revisited–the role of tumor-stroma interactions in metastasis to different organs. Int. J. Cancer 128, 2527–2535 (2011).
- Minn, A. J. et al. Distinct organ-specific metastatic potential of individual breast cancer cells and primary tumors. J. Clin. Invest. 115, 44–55 (2005).
- Girieca Lorusso et Curzio Rüegg, « New insights into the mechanisms of organ-specific breast cancer metastasis », Seminars in Cancer Biology, vol. 22, no 3, , p. 226–233 (ISSN 1044-579X, DOI 10.1016/j.semcancer.2012.03.007, lire en ligne, consulté le )
- Nguyen, D. X. & Massague, J. Genetic determinants of cancer metastasis. Nat. Rev. Genet. 8, 341–352 (2007).
- (en) Hai Wang, Lin Tian, Jun Liu et Amit Goldstein, « The Osteogenic Niche Is a Calcium Reservoir of Bone Micrometastases and Confers Unexpected Therapeutic Vulnerability », Cancer Cell, vol. 34, no 5, , p. 823–839.e7 (PMID 30423299, PMCID PMC6239211, DOI 10.1016/j.ccell.2018.10.002, lire en ligne, consulté le )
- Scott Valastyan et Robert A. Weinberg, « Tumor Metastasis: Molecular Insights and Evolving Paradigms », Cell, vol. 147, no 2, , p. 275–292 (ISSN 0092-8674, PMID 22000009, PMCID PMC3261217, DOI 10.1016/j.cell.2011.09.024, lire en ligne, consulté le )
- Fernando Salvador, Alberto Martin, Celia López-Menéndez et Gema Moreno-Bueno, « Lysyl Oxidase–like Protein LOXL2 Promotes Lung Metastasis of Breast Cancer », Cancer Research, vol. 77, no 21, , p. 5846–5859 (ISSN 0008-5472 et 1538-7445, PMID 28720577, PMCID PMC5656180, DOI 10.1158/0008-5472.can-16-3152, lire en ligne, consulté le )
- Bethan Psaila, Rosandra N. Kaplan, Elisa R. Port et David Lyden, « Priming the ‘Soil’ for Breast Cancer Metastasis: The Pre-Metastatic Niche », Breast Disease, vol. 26, no 1, , p. 65–74 (DOI 10.3233/BD-2007-26106, lire en ligne, consulté le )
- Héctor Peinado, Simon Lavotshkin et David Lyden, « The secreted factors responsible for pre-metastatic niche formation: Old sayings and new thoughts », Seminars in Cancer Biology, vol. 21, no 2, , p. 139–146 (ISSN 1044-579X, DOI 10.1016/j.semcancer.2011.01.002, lire en ligne, consulté le )
- Costa-Silva, B. et al. Pancreatic cancer exosomes initiate pre-metastatic niche formation in the liver. Nat. Cell Biol. 17, 816–826 (2015).
- (en) Jae W. Lee, Meredith L. Stone, Paige M. Porrett et Stacy K. Thomas, « Hepatocytes direct the formation of a pro-metastatic niche in the liver », Nature, vol. 567, no 7747, , p. 249–252 (ISSN 1476-4687, PMID 30842658, PMCID PMC6430113, DOI 10.1038/s41586-019-1004-y, lire en ligne, consulté le )
- (en) Elvin Wagenblast, Mar Soto, Sara Gutiérrez-Ángel et Christina A. Hartl, « A model of breast cancer heterogeneity reveals vascular mimicry as a driver of metastasis », Nature, vol. 520, no 7547, , p. 358–362 (ISSN 1476-4687, PMID 25855289, PMCID PMC4634366, DOI 10.1038/nature14403, lire en ligne, consulté le )
- (en) Qiqun Zeng, Iacovos P. Michael, Peng Zhang et Sadegh Saghafinia, « Synaptic proximity enables NMDAR signalling to promote brain metastasis », Nature, vol. 573, no 7775, , p. 526–531 (ISSN 1476-4687, PMID 31534217, PMCID PMC6837873, DOI 10.1038/s41586-019-1576-6, lire en ligne, consulté le )
- (en) Qing Chen, Adrienne Boire, Xin Jin et Manuel Valiente, « Carcinoma–astrocyte gap junctions promote brain metastasis by cGAMP transfer », Nature, vol. 533, no 7604, , p. 493–498 (ISSN 1476-4687, PMID 27225120, PMCID PMC5021195, DOI 10.1038/nature18268, lire en ligne, consulté le )
- (en) Roger R. Gomis et Sylwia Gawrzak, « Tumor cell dormancy », Molecular Oncology, vol. 11, no 1, , p. 62–78 (ISSN 1574-7891 et 1878-0261, PMID 28017284, PMCID PMC5423221, DOI 10.1016/j.molonc.2016.09.009, lire en ligne, consulté le )
- Filippo G. Giancotti, « Mechanisms Governing Metastatic Dormancy and Reactivation », Cell, vol. 155, no 4, , p. 750–764 (ISSN 0092-8674, PMID 24209616, PMCID PMC4354734, DOI 10.1016/j.cell.2013.10.029, lire en ligne, consulté le )
- (en) María Soledad Sosa, Paloma Bragado et Julio A. Aguirre-Ghiso, « Mechanisms of disseminated cancer cell dormancy: an awakening field », Nature Reviews Cancer, vol. 14, no 9, , p. 611–622 (ISSN 1474-1768, PMID 25118602, PMCID PMC4230700, DOI 10.1038/nrc3793, lire en ligne, consulté le )
- (en) Julio A. Aguirre-Ghiso et Maria Soledad Sosa, « Emerging Topics on Disseminated Cancer Cell Dormancy and the Paradigm of Metastasis », Annual Review of Cancer Biology, vol. 2, no 1, , p. 377–393 (ISSN 2472-3428 et 2472-3428, DOI 10.1146/annurev-cancerbio-030617-050446, lire en ligne, consulté le )
- Sosa, M. S., Bernstein, E. & Aguirre-Ghiso, J. A. in Tumor Dormancy and Recurrence (eds Yuzhuo Wang & Francesco Crea) 1–16 (Springer International Publishing, 2017).
- Albert C. Yeh et Sridhar Ramaswamy, « Mechanisms of Cancer Cell Dormancy—Another Hallmark of Cancer? », Cancer Research, vol. 75, no 23, , p. 5014–5022 (ISSN 0008-5472 et 1538-7445, PMID 26354021, PMCID PMC4668214, DOI 10.1158/0008-5472.can-15-1370, lire en ligne, consulté le )
- Aya Kobayashi, Hiroshi Okuda, Fei Xing et Puspa R. Pandey, « Bone morphogenetic protein 7 in dormancy and metastasis of prostate cancer stem-like cells in bone », Journal of Experimental Medicine, vol. 208, no 13, , p. 2641–2655 (ISSN 1540-9538 et 0022-1007, PMID 22124112, PMCID PMC3244043, DOI 10.1084/jem.20110840, lire en ligne, consulté le )
- Yusuke Shiozawa, Elisabeth A. Pedersen, Lalit R. Patel et Anne M. Ziegler, « GAS6/AXL Axis Regulates Prostate Cancer Invasion, Proliferation, and Survival in the Bone Marrow Niche », Neoplasia, vol. 12, no 2, , p. 116–IN4 (ISSN 1476-5586, PMID 20126470, PMCID PMC2814350, DOI 10.1593/neo.91384, lire en ligne, consulté le )
- (en) Julio A. Aguirre-Ghiso, David Liu, Andrea Mignatti et Katherine Kovalski, « Urokinase Receptor and Fibronectin Regulate the ERK MAPK to p38 MAPK Activity Ratios That Determine Carcinoma Cell Proliferation or Dormancy In Vivo », Molecular Biology of the Cell, vol. 12, no 4, , p. 863–879 (ISSN 1059-1524 et 1939-4586, PMID 11294892, PMCID PMC32272, DOI 10.1091/mbc.12.4.863, lire en ligne, consulté le )
- Aguirre-Ghiso, J. A., Estrada, Y., Liu, D. & Ossowski, L. ERKMAPK activity as a determinant of tumor growth and dormancy; regulation by p38SAPK. Cancer Res. 63, 1684–1695 (2003).
- (en) Paloma Bragado, Yeriel Estrada, Falguni Parikh et Sarah Krause, « TGF-β2 dictates disseminated tumour cell fate in target organs through TGF-β-RIII and p38α/β signalling », Nature Cell Biology, vol. 15, no 11, , p. 1351–1361 (ISSN 1476-4679, PMID 24161934, PMCID PMC4006312, DOI 10.1038/ncb2861, lire en ligne, consulté le )
- (en) Cyrus M. Ghajar, Héctor Peinado, Hidetoshi Mori et Irina R. Matei, « The perivascular niche regulates breast tumour dormancy », Nature Cell Biology, vol. 15, no 7, , p. 807–817 (ISSN 1476-4679, PMID 23728425, PMCID PMC3826912, DOI 10.1038/ncb2767, lire en ligne, consulté le )
- (en) Oddbjørn Straume, Takeshi Shimamura, Michael J. G. Lampa et Julian Carretero, « Suppression of heat shock protein 27 induces long-term dormancy in human breast cancer », Proceedings of the National Academy of Sciences, vol. 109, no 22, , p. 8699–8704 (ISSN 0027-8424 et 1091-6490, PMID 22589302, PMCID PMC3365195, DOI 10.1073/pnas.1017909109, lire en ligne, consulté le )
- (en) Hiroko Endo et Masahiro Inoue, « Dormancy in cancer », Cancer Science, vol. 110, no 2, , p. 474–480 (ISSN 1347-9032 et 1349-7006, PMID 30575231, PMCID PMC6361606, DOI 10.1111/cas.13917, lire en ligne, consulté le )
- Giancotti, F. G. Mechanisms governing metastatic dormancy and Reactivation. Cell 155, 750–764 (2013).
- (en) Jean Albrengues, Mario A. Shields, David Ng et Chun Gwon Park, « Neutrophil extracellular traps produced during inflammation awaken dormant cancer cells in mice », Science, vol. 361, no 6409, (ISSN 0036-8075 et 1095-9203, PMID 30262472, PMCID PMC6777850, DOI 10.1126/science.aao4227, lire en ligne, consulté le )
- (en) Joan Massagué et Anna C. Obenauf, « Metastatic colonization by circulating tumour cells », Nature, vol. 529, no 7586, , p. 298–306 (ISSN 1476-4687, PMID 26791720, PMCID PMC5029466, DOI 10.1038/nature17038, lire en ligne, consulté le )
- Gay, L. J. & Malanchi, I. The sleeping ugly: tumour microenvironment’s act to make or break the spell of dormancy. BBA Rev. Cancer 1868, 231–238 (2017).
- Dana Ishay-Ronen, Maren Diepenbruck, Ravi Kiran Reddy Kalathur et Nami Sugiyama, « Gain Fat—Lose Metastasis: Converting Invasive Breast Cancer Cells into Adipocytes Inhibits Cancer Metastasis », Cancer Cell, vol. 35, no 1, , p. 17–32.e6 (ISSN 1535-6108, DOI 10.1016/j.ccell.2018.12.002, lire en ligne, consulté le )
- van der Weyden, L. et al. Genome-wide in vivo screen identifies novel host regulators of metastatic colonization. Nature 541, 233–236 (2017).
- Donovan, P. et al. Endovascular progenitors infiltrate melanomas and differentiate towards a variety of vascular beds promoting tumor metastasis. Nat. Commun. 10, 18 (2019).
- (en) Milan M. S. Obradović, Baptiste Hamelin, Nenad Manevski et Joana Pinto Couto, « Glucocorticoids promote breast cancer metastasis », Nature, vol. 567, no 7749, , p. 540–544 (ISSN 1476-4687, DOI 10.1038/s41586-019-1019-4, lire en ligne, consulté le )
- (en) Ioanna Keklikoglou, Chiara Cianciaruso, Esra Güç et Mario Leonardo Squadrito, « Chemotherapy elicits pro-metastatic extracellular vesicles in breast cancer models », Nature Cell Biology, vol. 21, no 2, , p. 190–202 (ISSN 1476-4679, PMID 30598531, PMCID PMC6525097, DOI 10.1038/s41556-018-0256-3, lire en ligne, consulté le )
- Imran Khan et Patricia S Steeg, « Metastasis suppressors: functional pathways », Laboratory Investigation, vol. 98, no 2, , p. 198–210 (ISSN 0023-6837, PMID 28967874, PMCID PMC6545599, DOI 10.1038/labinvest.2017.104, lire en ligne, consulté le )
- Lalita A. Shevde et Danny R. Welch, « Metastasis suppressor pathways—an evolving paradigm », Cancer Letters, vol. 198, no 1, , p. 1–20 (ISSN 0304-3835, DOI 10.1016/S0304-3835(03)00304-5, lire en ligne, consulté le )
- (en) Xiaohui Hu, Samuel E. Harvey, Rong Zheng et Jingyi Lyu, « The RNA-binding protein AKAP8 suppresses tumor metastasis by antagonizing EMT-associated alternative splicing », Nature Communications, vol. 11, no 1, , p. 486 (ISSN 2041-1723, PMID 31980632, PMCID PMC6981122, DOI 10.1038/s41467-020-14304-1, lire en ligne, consulté le )
- (en) Patricia S. Steeg, « Metastasis suppressors alter the signal transduction of cancer cells », Nature Reviews Cancer, vol. 3, no 1, , p. 55–63 (ISSN 1474-1768, DOI 10.1038/nrc967, lire en ligne, consulté le )
- (en) Liyuan Mao, Yan-yan Zhan, Bin Wu et Qiang Yu, « ULK1 phosphorylates Exo70 to suppress breast cancer metastasis », Nature Communications, vol. 11, no 1, , p. 117 (ISSN 2041-1723, PMID 31913283, PMCID PMC6949295, DOI 10.1038/s41467-019-13923-7, lire en ligne, consulté le )
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- Ressources relatives à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :
- «Métastases, la grande invasion», La Méthode scientifique, France Culture, 15 juin 2020.

