Autophagie
L’autophagie (du grec αυτο : « soi-même » et φαγειν « manger »), autolyse ou autophagocytose, est un mécanisme physiologique, intracellulaire, de protection et de recyclage d'éléments cellulaires : les organites indésirables ou endommagés, un pathogène introduit dans la cellule, des protéines mal repliées... sont ainsi collectés et transportés vers les lysosomes pour être dégradés. Une partie du cytoplasme est ainsi recyclée par ses propres lysosomes[1]. Ce mécanisme est aussi une source d’énergie et d’acides aminés en conditions stressantes pour la cellule, comme l’hypoxie, le manque de nutriments (jeûne) ou l’exposition à des traitements médicamenteux[2],[3].
Le terme autophagie regroupe plusieurs voies de dégradation lysosomale des constituants cellulaires. Ces voies diffèrent surtout par le site de séquestration du « fret » et par le type et la taille de la « cargaison » concernée[4]. Elles sont notamment la microautophagie, l’autophagie réalisée par des protéines chaperonnes et la macroautophagie (la forme principale)[5],[6].
La macroautophagie, appelée couramment autophagie, est la capture dans une double membrane lipidique (appelée « autophagosome ») de protéines ou composés cellulaires, puis la dégradation de ces composés après fusion avec un lysosome. C’est la seule voie qui puisse dégrader massivement des macromolécules et des organites. C’est une voie de dégradation alternative à celle du protéasome. En permettant le renouvellement de composants cytoplasmiques endommagés, ce mécanisme est essentiel à l'homéostasie cellulaire et évite parfois l'apoptose.
L'histolyse (du grec ἱστος signifiant « tissu ») désigne le même processus mais quand il est mobilisé par une métamorphose, par exemple chez les amphibiens quand le têtard se transforme en grenouille[7]. L'histolyse est également présente au cours du développement embryonnaire[8]. L'autophagie est aussi nécessaire à la réussite de processus de mobilisation de cellules souches totipotentes nécessaires à la régénération d'organes coupés ou endommagés.
Le dysfonctionnement de l'autophagie est source de maladies graves (neurodégénérescence, cancer...)[4].
Yoshinori Ohsumi a obtenu le prix Nobel de physiologie ou médecine en 2016 pour avoir découvert des marqueurs biologiques de l'autophagie.
Historique[modifier | modifier le code]
Le processus de régénération de la cellule a été découvert par le Belge Christian de Duve en 1963. Ce dernier a créé le terme d'autophagie et reçu le prix Nobel en 1974[9].
Trente ans plus tard, Yoshinori Ohsumi, grâce à ses expériences sur la levure de boulanger, montre que les mêmes mécanismes peuvent être observés dans le corps humain et qu’ils peuvent, en cas de dysfonctionnement, déclencher certaines maladies comme le cancer, la maladie de Parkinson, le diabète et certaines maladies génétiques et neurologiques[9].
Ohsumi a développé des souches de levure dépourvues d'enzymes-clés soupçonnées de jouer un rôle dans l'autophagie, espérant voir ce qu'il advient des cellules lorsque le processus ne fonctionne pas comme il le devrait. En affamant la levure, les scientifiques ont découvert que les cellules développaient des vacuoles inhabituellement grandes, jouant un rôle de « décharges cellulaires » collectant les matériaux à recycler[10].
En 1993, Ohsumi et son équipe publient la liste des 15 gènes essentiels impliqués dans le processus[10].
Depuis lors, lui et d'autres ont montré que l'autophagie joue un rôle crucial dans le développement de l'embryon, la différenciation des cellules et le système immunitaire. Une défaillance de l'autophagie peut entraîner une grande variété de maladies, notamment le cancer, le diabète et la maladie de Huntington. Un système d'autophagie sain est lié à la longévité et un système défectueux peut accélérer les symptômes du vieillissement[10].
La découverte des gènes Atg (autophagy related genes) dans la levure, au milieu des années 1990, a été importante, non seulement pour la dissection en termes moléculaires de la macroautophagie, mais aussi pour comprendre son importance en physiologie et en physiopathologie. Il existe plus de trente gènes Atg dont plus de la moitié est impliquée dans l’autophagie. Ces gènes sont présents aussi bien dans la levure que dans les cellules de mammifères[réf. nécessaire].
Mode de fonctionnement[modifier | modifier le code]
Les cinq étapes de l'autophagie sont l'initiation, la nucléation, l'expansion, la maturation puis la dégradation.
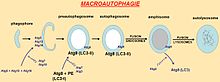
Au plan cellulaire, la macroautophagie, la forme principale[11], débute par la formation d’une double membrane phospholipidique dans la cellule, dite phagophore, qui s’allonge, séquestre des constituants du cytoplasme avant de se refermer sur elle-même. L’autophagosome ainsi formé va ensuite fusionner avec un lysosome pour dégrader les composés capturés. Plusieurs compartiments cellulaires (le réticulum endoplasmique, l'appareil de Golgi et le réseau trans-golgien formant le système endomembranaire) et la membrane plasmique participeraient probablement à la formation de l’autophagosome.
Une quinzaine de protéines Atg sont nécessaires à sa biogenèse.
Mécanisme moléculaire[modifier | modifier le code]
Le déroulement du processus autophagique repose essentiellement sur deux systèmes de conjugaison, analogues aux systèmes d'ubiquitination des protéines :
- le premier conjugué, formé des protéines Atg5-Atg12, permet le recrutement du deuxième complexe sur l'autophagosome en formation, puis est recyclé vers le cytosol.
- le deuxième résulte de la conjugaison de la protéine Atg8 (MAP-LC3 chez les mammifères) à la phosphatidyléthanolamine (PE) et s’incorpore dans la membrane du pré-autophagosome. LC3 existe donc sous forme cytosolique (LC3-I) ou associé au phagosome (LC3-II = Atg8-PE). LC3-II pourrait jouer une fonction structurale permettant l’élongation et la formation de l’autophagosome mature et il constitue un marqueur cellulaire d'identification des autophagosomes.
L'autophagie sélective de constituants cellulaires est réalisée grâce à des protéines-cargos, notamment SQSTM1/p62. p62 se lie aux protéines et composés ubiquitinés et les fixe/séquestre à la membrane du phagophore grâce à sa liaison avec LC3-II[12]. p62 est dégradé une fois que l'autophagosome a fusionné avec un lysosome, ce qui fait de lui un bon marqueur pour estimer l'activité autophagique de la cellule[13].
Déclenchement[modifier | modifier le code]
L’autophagie peut être stimulée en conditions de stress, telles que la carence en nutriments, l’absence de facteurs de croissance ou l’hypoxie. La protéine mTOR (mammalian target of rapamycin) joue un rôle-clé dans l’intégration de ces signaux et la régulation de l’autophagie. Lorsqu’elle est activée, mTor inhibe la voie de l’autophagie mais son inactivation (à la suite d'une carence en nutriments, par exemple) permet de lever l'inhibition et donc de lancer l’autophagie. Cette enzyme est la cible de la rapamycine (une drogue classiquement utilisée pour induire l’autophagie). Une autre voie déclenchant l'autophagie fait intervenir le complexe Atg6 (aussi appelé Bécline 1)/PI3 kinase de classe III. Ce complexe participe à l’induction de l’autophagie, à l’incurvation du pré-autophagosome et à la formation de l’autophagosome.
Rôles physiologiques[modifier | modifier le code]
L’autophagie joue un rôle important dans :
- le maintien de l’homéostasie car cette voie catabolique permet l’élimination et le remplacement continuel des protéines et des organites non fonctionnels ;
- l’adaptation et la survie des cellules soumises à des conditions de stress ;
- l’immunité innée à l’échelle de la cellule car elle permet de directement éliminer des pathogènes intracellulaires, y compris des virus intrus (on parle alors de « virophagie ») ; l'autophagie est liée à la présentation d'antigènes bactériens ou viraux, à l'aptitude de cellules immunitaires et contribue à inhiber des réactions inflammatoires excessives[14]
- l'immunité adaptative car la dégradation des protéines par autophagie génère des peptides qui seront ensuite présentés sur le complexe majeur d'histocompatibilité (CMH) ;
- le vieillissement cellulaire. En effet, l'autophagie des mitochondries, appelée mitophagie, permet la recyclage des mitochondries dysfonctionnelles[15] , lesquelles génèrent notamment du stress oxydatif causant des dommages à la cellule. Par ce biais, elle a un rôle protecteur contre le vieillissement cellulaire[16].
- le fonctionnement des neurones. Les mitochondries étant particulièrement actives dans ces cellules, leur renouvellement joue un rôle essentiel pour empêcher un stress oxydatif trop important et la dégénérescence[17],[18].
Rôle contre les virus[modifier | modifier le code]
Le virus est obligé d'utiliser le matériel cellulaire pour se faire dupliquer. L'autophagie (virophagie) est l'une des voies majeures de la défense de l'organisme (unicellulaire ou pluricellulaire) contre les virus.
Certains virus ont cependant, au cours de l'évolution ou en co-évolulant avec leur hôte, développé des mécanismes de contournement de l'immunité, dont en inhibant le processus autophagique ou en lui échappant.
Certains virus (coronavirus par exemple)[19] exploitent même tout ou partie du mécanisme d'autophagie pour leur réplication. Quand c'est le cas, l'autophagie pourrait peut-être devenir l'une des cibles d'interventions thérapeutiques nouvelles, comme l'ont proposé Didac Carmona-Gutierrez & al. (2020) dans le cadre de la lutte médicamenteuse contre le SARS-CoV-2 responsable de la pandémie de Covid-19[14].
Rôle dans le cancer[modifier | modifier le code]
L’identification de molécules impliquées dans le contrôle et l’exécution de l’autophagie a mis en lumière une étroite relation entre l’autophagie et la progression tumorale. Les cellules cancéreuses présentaient généralement une capacité autophagique plus réduite que les cellules normales. Le rôle anti-tumoral de l’autophagie est suggéré par son implication dans la réduction de l’instabilité chromosomique, de la prolifération et de l’inflammation des cellules tumorales. L’autophagie peut aussi être un mécanisme pro-tumoral en permettant la survie des cellules tumorales exposées à des variations de leur micro-environnement (hypoxie, carence nutritionnelle…). Le processus autophagique est induit en réponse à divers traitements anti-cancéreux. Cette réponse peut s'avérer être un mécanisme permettant la survie des cellules, ou favorisant et amplifiant la mort induite par ces traitements.
Une étude publiée en 2018 montre que le jeûne intermittent peut protéger les cellules normales de la toxicité des agents anticancéreux, en réduisant les effets secondaires chez les patients et en augmentant les effets néfastes de la chimiothérapie, de la radiothérapie et de la thérapie ciblée sur les cellules tumorales[20].
Rôle contre les maladies neurodégénératives[modifier | modifier le code]
Une caractéristique commune à de nombreuses maladies neurodégénératives est l’accumulation de protéines mutées ou toxiques et leur agrégation dans le cytoplasme. Ces maladies sont désignées sous le terme de « protéinopathies » et comprennent notamment la maladie de Huntington, la maladie d'Alzheimer, la maladie de Parkinson ou la maladie de Machado-Joseph (SCA-3). Ces agrégats de protéines anormales se formeraient, par exemple, à la suite d'une diminution de l’activité du protéasome. Leur présence entraîne une augmentation de cette autophagie induite qui, dans les premiers stades de la maladie, est assez efficace pour assurer leur élimination. Cependant, à un stade plus avancé, l’autophagie induite n’est plus suffisante et des inclusions protéiques se forment dans les cellules ; la stimulation de l’autophagie (par un agent pharmacologique) pourrait s’avérer efficace pour éliminer ces inclusions et ainsi lutter contre la neurodégénérescence[21]. Des perturbations initiales de la voie autophagique ont aussi été étudiées, par exemple dans le cas de la maladie de Machado-Joseph, avec la mise en évidence d'un niveau insuffisant de la protéine bécline 1 [22].
Notes et références[modifier | modifier le code]
- (en) NY Lin, C Beyer, A Gießl et al., « Autophagy regulates TNFα-mediated joint destruction in experimental arthritis », Ann. Rheum. Dis., (PMID 22975756, DOI 10.1136/annrheumdis-2012-201671, lire en ligne).
- (en) Michael N. Moore, J. Icarus Allen et Paul J. Somerfield, « Autophagy: Role in surviving environmental stress », Marine Environmental Research, vol. 62, , S420–S425 (DOI 10.1016/j.marenvres.2006.04.055, lire en ligne, consulté le )
- (en) Noboru Mizushima, Akitsugu Yamamoto, Makoto Matsui et Tamotsu Yoshimori, « In Vivo Analysis of Autophagy in Response to Nutrient Starvation Using Transgenic Mice Expressing a Fluorescent Autophagosome Marker », Molecular Biology of the Cell, vol. 15, no 3, , p. 1101–1111 (ISSN 1059-1524 et 1939-4586, PMID 14699058, PMCID PMC363084, DOI 10.1091/mbc.e03-09-0704, lire en ligne, consulté le )
- (en) Sahar Abo ElFadl, « AUTOPHAGY; Recent Advances in Health and Disease », Journal of Medical Histology, vol. 2, no 1, , p. 1–10 (ISSN 2536-930X, DOI 10.21608/jmh.2018.5225.1040, lire en ligne, consulté le )
- (en) J Lee, S Giordano et J Zhang, « Autophagy, mitochondria and oxidative stress: cross-talk and redox signalling », Biochem. J., vol. 441, no 2, , p. 523–540 (PMID 22187934, PMCID 3258656, DOI 10.1042/BJ20111451, lire en ligne).
- (en) Mizushima N, Ohsumi Y, Yoshimori T, « Autophagosome formation in mammalian cells », Cell Struct. Funct., (PMID 12576635), p. 421–429.
- D. L. Stocum, « Amphibian Regeneration and Stem Cells », dans Regeneration: Stem Cells and Beyond, vol. 280, Springer Berlin Heidelberg, (ISBN 978-3-642-62321-9, DOI 10.1007/978-3-642-18846-6_1, lire en ligne), p. 1–70
- (en) F.J. Edwards, « Development and histolysis of the indirect flight muscles in Dysdercus intermedius », Journal of Insect Physiology, vol. 15, no 9, , p. 1591–1599 (DOI 10.1016/0022-1910(69)90179-6, lire en ligne, consulté le )
- « Nobel de médecine : mais qu'est-ce que l'autophagie ? », sur France Culture, (consulté le )
- (en) Science News StaffOct. 3 et 2016, « Nobel honors discoveries on how cells eat themselves », sur Science | AAAS, (consulté le )
- (en) B Levine, N Mizushima et HW Virgin, « Autophagy in immunity and inflammation », Nature, vol. 469, no 7330, , p. 323–335 (PMID 21248839, PMCID 3131688, DOI 10.1038/nature09782).
- (en) Serhiy Pankiv, Terje Høyvarde Clausen, Trond Lamark et Andreas Brech, « p62/SQSTM1 Binds Directly to Atg8/LC3 to Facilitate Degradation of Ubiquitinated Protein Aggregates by Autophagy », Journal of Biological Chemistry, vol. 282, no 33, , p. 24131–24145 (ISSN 0021-9258 et 1083-351X, PMID 17580304, DOI 10.1074/jbc.M702824200, lire en ligne, consulté le )
- Karolina Pircs, Peter Nagy, Agnes Varga et Zsolt Venkei, « Advantages and Limitations of Different p62-Based Assays for Estimating Autophagic Activity in Drosophila », PLoS ONE, vol. 7, no 8, (ISSN 1932-6203, PMID 22952930, PMCID 3432079, DOI 10.1371/journal.pone.0044214, lire en ligne, consulté le )
- Didac Carmona-Gutierrez et Maria A. Bauer, « Digesting the crisis: autophagy and coronaviruses », sur Microbial Cell, (PMID 32391393, PMCID PMC7199282, DOI 10.15698/mic2020.05.715, consulté le ), p. 119–128
- (en) Sarah Pickles, Pierre Vigié et Richard J. Youle, « Mitophagy and Quality Control Mechanisms in Mitochondrial Maintenance », Current Biology, vol. 28, no 4, , R170–R185 (DOI 10.1016/j.cub.2018.01.004, lire en ligne, consulté le )
- (en) Ruoyang Shi, Matthew Guberman et Lorrie A. Kirshenbaum, « Mitochondrial quality control: The role of mitophagy in aging », Trends in Cardiovascular Medicine, vol. 28, no 4, , p. 246–260 (DOI 10.1016/j.tcm.2017.11.008, lire en ligne, consulté le )
- (en) Elayne M. Fivenson, Sofie Lautrup, Nuo Sun et Morten Scheibye-Knudsen, « Mitophagy in neurodegeneration and aging », Neurochemistry International, vol. 109, , p. 202–209 (PMID 28235551, PMCID PMC5565781, DOI 10.1016/j.neuint.2017.02.007, lire en ligne, consulté le )
- (en) H. Chen et D. C. Chan, « Mitochondrial dynamics-fusion, fission, movement, and mitophagy-in neurodegenerative diseases », Human Molecular Genetics, vol. 18, no R2, , R169–R176 (ISSN 0964-6906 et 1460-2083, PMID 19808793, PMCID PMC2758711, DOI 10.1093/hmg/ddp326, lire en ligne, consulté le )
- (en) Eleanor M. Cottam et Helena J. Maier, « Coronavirus nsp6 proteins generate autophagosomes from the endoplasmic reticulum via an omegasome intermediate », sur Autophagy, (ISSN 1554-8627, PMID 21799305, PMCID PMC3242798, DOI 10.4161/auto.7.11.16642, consulté le ), p. 1335–1347
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6257056//
- Mathieu Bourdenx et Benjamin Dehay, « Autophagie et cerveau: Le cas des maladies neurodégénératives », médecine/sciences, vol. 33, no 3, , p. 268–274 (ISSN 0767-0974 et 1958-5381, DOI 10.1051/medsci/20173303013, lire en ligne, consulté le )
- (en) Isabel Nascimento-Ferreira, Tiago Santos-Ferreira, Lígia Sousa-Ferreira et Gwennaëlle Auregan, « Overexpression of the autophagic beclin-1 protein clears mutant ataxin-3 and alleviates Machado–Joseph disease », Brain, vol. 134, no 5, , p. 1400–1415 (ISSN 0006-8950, DOI 10.1093/brain/awr047, lire en ligne, consulté le )
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- « Club francophone de l'autophagie (CFATG) » (consulté le )
- HADb, une base de données dédiée à l'autophagie
- L'autophagie : un nouveau concept en cancérologie, magazine Bull Cancer, volume 95, no 1, p. 43-50
- L'autophagie remplaçant de luxe du protéasome, magazine Médecine Sciences, volume 24, no 1, p. 19-21
- Les deux visages de l'autophagie dans le système nerveux, magazine Médecine Sciences, volume 25, no 4, p. 383-388
Bibliographie[modifier | modifier le code]
- Zhangyuan Yin et Clarence Pascual, « Autophagy: machinery and regulation », sur Microbial Cell, (PMID 28357331, PMCID PMC5348978, DOI 10.15698/mic2016.12.546, consulté le ), p. 588–596
- (en) Tobias Eisenberg et Heide Knauer, « Induction of autophagy by spermidine promotes longevity », sur Nature Cell Biology, (ISSN 1465-7392, DOI 10.1038/ncb1975, consulté le ), p. 1305–1314
- (en) Didac Carmona-Gutierrez et Andreas Zimmermann, « The flavonoid 4,4′-dimethoxychalcone promotes autophagy-dependent longevity across species », sur Nature Communications, (ISSN 2041-1723, PMID 30783116, PMCID PMC6381180, DOI 10.1038/s41467-019-08555-w, consulté le ), p. 651
