Peste porcine africaine
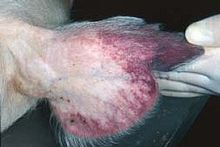
La peste porcine africaine ou PPA (en anglais, African swine fever ou ASF) est une maladie animale qui touche les porcs, mais aussi les sangliers[1], les phacochères, les potamochères et les tiques, qui en sont le vecteur probable.
La PPA est une maladie virale, causée par le virus de la peste porcine africaine qui est endémique dans le milieu naturel en Afrique subsaharienne. C'est un Asfivirus, un grand virus à ADN double-brin qui se réplique dans le cytoplasme des cellules infectées. C'est en 2022 le seul représentant officiel de la famille des Asfarviridae (mais Faustovirus, au positionnement discuté[2], est parfois attribué à cette famille[3]). C'est le seul virus à ADN double brin connu à être transmis par des arthropodes. Attaquant certaines cellules du système immunitaire, il cause des hémorragies mortelles chez les porcs domestiques. Certains isolats sont retrouvés dans tous les organes du porcelet seulement 30 h après l'inoculation[4] et ils peuvent provoquer leur mort en à peine une semaine. Le cycle d'infection implique les tiques (du genre Ornithodoros), les potamochères, phacochères et hylochères. Ces espèces-réservoir sont des porteurs asymptomatiques.
Le virus ne menace pas la santé humaine, mais étant hautement mortel pour les cochons et sangliers[5], il est source d'importants dégâts socioéconomiques. C'est donc une maladie à enjeu vétérinaire et à déclaration obligatoire. Une seule détection faite dans un pays peut justifier des interdictions d'exporter vers d'autres pays.
La PPA est détectée depuis plusieurs décennies en Sardaigne chez des sangliers et des porcs semi-sauvages. Au début des années 2000 pour la première fois des sangliers sont touchés, et en grand nombre, de même que des porcs en Europe de l’Est (Pologne, Lituanie, Lettonie, Estonie, Tchéquie, Moldavie, Ukraine, Biélorussie, Russie), faisant craindre qu'ils ne véhiculent le virus vers toute l'Europe, et que des chasseurs ou leurs chiens ou des charcuteries contaminées[6],[7] puissent involontairement le véhiculer[1].
En 2018, une épidémie de peste porcine africaine en Chine a conduit à l'abattage de 20 000 bêtes[8]. Idem en Roumanie où plus d'une centaine de milliers de porcs sont tués durant l'été après la survenue de nombreux foyers d'infection. En , neuf sangliers porteurs du virus sont retrouvés morts en Belgique, dans le sud de la Wallonie[9]. Depuis lors, la maladie progresse en Chine, en Europe de l'Est et en Belgique malgré les moyens mis en œuvre pour tenter de limiter sa propagation.
Aucun vaccin n'étant attendu avant 2027[réf. nécessaire], les chercheurs ont tenté de comprendre pourquoi et comment cette maladie mortelle persiste chez le sanglier et comment limiter si cela est possible la circulation du virus[1]. La découverte sérendipiteuse, en 2017, d'un sanglier immunisé naturellement a cependant permis la distribution en 2019 d'un vaccin administrable oralement, qui semble efficace[10].
Histoire
[modifier | modifier le code]Elle a été décrite pour la première fois lorsque des colons européens ont introduit des porcs domestiques dans les régions affectées, ce qui en fait un bon exemple de maladie émergente.
La peste porcine africaine était limitée au continent africain jusqu'en 1957, quand elle a été signalée à Lisbonne, au Portugal. Une autre éruption y a eu lieu en 1960. Après ces introductions, la maladie s'est installée dans la péninsule ibérique et des éruptions sporadiques ont eu lieu en France, en Belgique et dans d'autres pays d'Europe dans les années 1980. L'Espagne et le Portugal ont réussi à éradiquer la maladie au milieu des années 1990 grâce à une politique d'abattage.
La maladie a traversé l'Océan Atlantique et des éruptions ont été signalées dans plusieurs îles des Caraïbes, notamment en République dominicaine. En 1971, le régime cubain a dû faire abattre 500 000 porcs pour éviter une épizootie à l'échelle nationale. Cet épisode a été qualifié d'« événement le plus inquiétant » de 1971 par l'Organisation des Nations unies pour l'alimentation et l'agriculture (FAO). Il a été avancé que le virus avait été introduit dans le pays par des opposants anti-castristes, avec le soutien tacite de membres de la CIA, pour déstabiliser l'économie du pays et encourager l'opposition interne à Fidel Castro. Le virus leur aurait été fourni depuis une base de l'armée américaine de la zone du canal de Panama par un agent américain anonyme[11]. Cependant l'accusation de complot n'est apparue que six ans après les faits, dans le journal Newsday, citant des sources invérifiables[12],[13].
D'importantes épidémies en Afrique sont régulièrement déclarées à l'Organisation mondiale de la santé animale (OIE, ex-Office international des épizooties). La maladie s'étend particulièrement en Afrique depuis la fin des années 1990, mais passe relativement inaperçue[14].

La plus récente épizootie hors d'Afrique s'est déclaré début 2007 en Géorgie. De là elle a gagné l'Arménie, l'Azerbaïdjan, l'Iran et la Russie. Le virus a été signalé en Lituanie en 2014 (1ère apparition dans l'Union européenne) puis s'est répandu dans les États baltes (alors qu'il progressait aussi en Extrême-Orient, décimant de nombreux élevages de porcs). L'été 2017, il était en République tchèque puis en novembre 2017 près de Varsovie en Pologne, inquiétant l'Allemagne et le Danemark deux grands producteurs de porcs. En , 9 cas de sangliers porteurs du virus sont découverts dans le sud de la Belgique en Province de Luxembourg, une zone de confinement de 63 000 hectares de forêts avec interdiction de circuler et de chasser est immédiatement instaurée en accord avec les autorités européennes[15],[16]. En 2022, un élevage allemand est touché à Forchheim am Kaiserstuhl[17].
Sous l'égide de l'AFSCA en Europe les mesures sanitaires ont été renforcées, et il est interdit d'importer de la viande de porc ou de sanglier ou des produits de viande de porc ou de sanglier d'un pays ou de zones où sévissent la PPA vers des zones indemnes. Les visites d'exploitations porcines et tout contact avec des porcs dans les 72 h suivant le retour d’une zone à risque sont également interdits[18]. La chasse au sanglier n'est pas interdite dans les pays où le virus est endémique, mais dans certains pays (belgique par ex) les chasseurs ne doivent pas utiliser de chien au cours de la chasse et diverses mesures de désinfections et nettoyage sont ensuite obligatoire ;
Symptômes
[modifier | modifier le code]
Les symptômes de la maladie sont très proches de ceux de la peste porcine classique ; Seuls des examens de laboratoire permettent normalement de les distinguer. De plus dans les deux cas, les symptômes cliniques et visuels varient considérablement selon les souches et leurs virulence[1]. De même chez le porc, comme chez le sanglier selon la souche l'animal sera porteur sain (sans maladie apparente) ou pourra mourir en quelques dizaines d'heures.
Les infections aigües dues à des souches hautement pathogènes du virus conduisent à une présentation clinique évoquant une fièvre hémorragique virale, caractérisée par[1] :
- une déplétion prononcée des tissus lymphoïdes ;
- une apoptose des sous-populations lymphocytaires ;
- une altération de l'hémostase ;
- une dégradation des fonctions immunitaires.
On admet généralement qu'un grande partie des lésions résulte indirectement des effets des cytokines produites par les monocytes et des macrophages infectés, plutôt que des effets directs du virus sur les cellules[1].
Structure du virus et réplication
[modifier | modifier le code]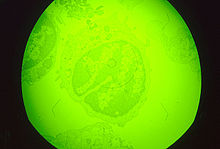
L'agent de la peste porcine africaine est un grand virus à ADN double-brin (groupe I) possédant un génome d'au moins 150 gènes (le nombre de gènes varie légèrement selon les isolats viraux considérés). Il ressemble aux autres grands virus à ADN comme les poxvirus, les iridovirus et les mimivirus. Comme dans les autres fièvres hémorragiques virales, ses principales cellules-cibles sont celles de la lignée des monocytes et macrophages.
Le virus cause chez les porcs une fièvre hémorragique avec un fort taux de mortalité (souvent proche de 100 %), tout en infectant ses hôtes naturels (les phacochères, les potamochères et les tiques du genre Ornithodoros) de manière chronique et sans signe clinique[19].
Le virus code les enzymes nécessaires à la réplication et à la transcription de son génome, notamment les éléments de son système de réparation par excision de base, ses protéines structurelles et beaucoup d'autres qui ne sont pas essentielles à sa réplication, mais jouent un rôle dans sa survie et dans sa transmission.
La réplication du virus a lieu dans les régions entourant le noyau cellulaire. Sa capside icosaédrale est assemblée sur des membranes modifiées du réticulum endoplasmique. Des produits issus de polyprotéines protéolysées forment l'enveloppe entre la membrane interne et le centre nucléoprotéique. Une membrane extérieure supplémentaire est ajoutée à partir de particules de la membrane plasmique. Le virus code des protéines qui inhibent la transmission du signal des macrophages infectés et régulent ainsi l'activation des gènes de la réponse immunitaire. Il code en outre des protéines inhibant l'apoptose (la mort) des cellules infectées, ce qui facilite la production des virions. Des protéines membranaires virales possédant des similitudes avec des protéines d'adhésion cellulaire régulent l'interaction des cellules infectées et des virions extracellulaires avec les organes de l'hôte[3].
Génotypes
[modifier | modifier le code]En 2012, 22 génotypes avaient déjà été identifiés (sur la base des variations de la séquence de la région C-terminale du gène p72[20]). Le génotype VIII est limité à quatre pays d'Afrique orientale.
Épizooties
[modifier | modifier le code]Europe du Sud à partir de 1960
[modifier | modifier le code]La maladie touche à partir de 1960 l'Espagne et le Portugal, où elle est finalement éradiquée respectivement en 1995 et 1993[21].
Enzootie en Sardaigne
[modifier | modifier le code]En Sardaigne, la maladie est une enzootie présente depuis 1978, avec plusieurs pics épizootiques en 1995, 2004, 2005 et depuis 2012[22].
Expansion en Europe de L'Est
[modifier | modifier le code]

La maladie est originaire d'Afrique, et est arrivée en Géorgie en 2007. La souche retrouvée en Géorgie est considérée comme beaucoup plus virulente que les épidémies connues jusqu'alors[23]. De là, elle s'est répandue en Russie, puis dans les Pays baltes à partir de 2014[24]. En 2016, elle frappe, en plus de la Russie et des Pays baltes, l'Ukraine, la Moldavie, la Biélorussie et la Pologne[25]. À l'été 2017, la maladie arrive en Tchéquie, mais est contenue notamment grâce à de nombreux abattages préventifs de porcs et de sangliers[26]. Le , la Hongrie connaît son premier cas, à proximité de la frontière slovaque[27]. La maladie est détectée pour la première fois en Roumanie en [28], et en , 110 000 porcs y sont abattus préventivement en raison de plusieurs foyers d'épidémie[29]. En Pologne, la maladie progresse vers l'ouest de 3 à 5 kilomètres par mois, et risque d'arriver prochainement en Allemagne[30].
En prévision de l'arrivée de la maladie en Allemagne, le Danemark décide en la construction d'une palissage le long de sa frontière, afin de se protéger de l'arrivée du virus[31].
Afin de tenter d'enrayer la maladie, la Pologne décide des destructions massives de sangliers[32]. 168 000 bêtes ont ainsi été abattues en 2018, alors que la population était estimée à 210 000 au début de l'année. Des scientifiques et des citoyens s'inquiètent cependant des conséquences négatives d'une quasi-disparition de l'espèce pour l'environnement, d'autant plus que les campagnes d'abattage massives, menées depuis 2014, n'ont pas montré leur efficacité pour lutter contre la propagation de la maladie. Pour un spécialiste du sujet, si les grands élevages de porcs sont aux normes sanitaires, ce n'est pas le cas des petites exploitations polonaises, qui sont un réservoir viral important[33].
En , un cas est signalé à Nowogród Bobrzański, à 40 km de la frontière allemande. Les autorités allemandes se préparent par conséquent, en formant les chasseurs, les vétérinaires et les secouristes, et en s'équipant de drones ou de caméras infrarouges[34].
La peste porcine africaine touche particulièrement le nord de la Bulgarie à l'été 2019, nécessitant l'abattage de 120 000 bêtes, soit 20 % des porcs du pays[35]. Les pertes financières sont estimées à 300 millions d'euros, et le manque à gagner à un milliard.
Le premier cas est constaté en Slovaquie en , près de la frontière hongroise[36].
Le premier cas est constaté en Grèce, à proximité de la frontière avec la Bulgarie, en . Cela porte à neuf le nombre de pays européens frappés par la maladie. La chasse massive des sangliers afin de diminuer leur population est souvent pratiquée, afin de prévenir la propagation de la maladie[37].
Le premier cas allemand est annoncé le sur un cadavre de sanglier retrouvé dans l'arrondissement d'Oder-Spree, dans le land de Brandebourg, à sept kilomètres de la frontière polonaise[38],[39]. Cinq nouveaux cas sont détectés à proximité le . En réaction, Argentine, Brésil, République populaire de Chine, Corée du Sud et Japon suspendent leurs importations en provenance de l'Allemagne[40].
Julia Klöckner, ministre de l'agriculture allemande annonce avoir donné des pouvoirs importants aux Länder, leur permettant notamment de construire des clôtures, avoir mobilisé la Bundeswehr et la Technisches Hilfswerk, et mis en place une organisation tripartite avec la Pologne et la Tchéquie[41].
Au , le nombre de 1031 cas cumulés de PPA en Allemagne est constaté, à 90 % en Brandebourg et 10 % en Saxe. La Bavière reste alors indemne de la maladie[42].
Extrême-Orient à partir de 2018
[modifier | modifier le code]
En Chine, pour freiner une épidémie qui a émergé à l'été 2018, 38 000 porcs sont abattus[43]. Le premier foyer d'épidémie est détecté le . Le , les premiers cas dans l'agglomération de Pékin ont été détectés. À cette date, 73 cas dans une vingtaine de provinces ont été signalés pour cette maladie, qui a tué ou nécessité l'abattage préventif de 600 000 porcs[44]. Au début de , les autorités signalent un ralentissement des contaminations, avec seulement cinq cas recensés en janvier, et les mesures d'isolement sont levées dans plusieurs provinces touchées par le virus[45]. À la mi-février, toutes les provinces étaient touchées, sauf Guangxi, Shandong, Tibet et Xinjiang[46]. Les trois quarts de la production porcine étant le fait de petites exploitations, celles-ci n'ont souvent pas les moyens ou les compétences pour mettre en place les mesures strictes nécessaires pour lutter contre la prolifération du virus. Le transport des animaux se fait souvent sur de longues distances dans des véhicules rarement désinfectés, ce qui favorise la propagation. Par ailleurs, devant le faible montant compensatoire en cas d'abattage et la peur de sanctions du gouvernement, de nombreux fermiers procèdent à des abattages à la va-vite et ne déclarent pas les porcs malades, contribuant également au manque de contrôle de la peste porcine africaine[47]. Au début du mois de , les autorités considèrent que le pire de l'épidémie est passé, et que le nombre de porcs recommence à augmenter[48].
Les premiers cas sont détectés au nord du Viêt Nam le , le virus étant probablement originaire de Chine[49]. En , on estime à plus d'un million le nombre de porcs abattus en Chine pour contenir la maladie, faisant baisser le cheptel porcin du pays de 15 %[50]. Cependant, cela ne permet pas d'enrayer la maladie, qui s'étend à la majorité des provinces du pays pendant la première moitié de l'année 2019. De nombreux élevages sont très petits, ce qui explique la difficulté de lutter contre la propagation[51]. En septembre, les 58 provinces et 5 municipalités sont toutes touchées par la peste porcine africaine[52].
Le Cambodge signale ses premiers cas le , dans la province frontalière de Rotanah Kiri[53].
Le , les premiers cas sont identifiés au Laos, dans la province de Saravane[54]. La maladie progresse rapidement, et à la fin du mois d'août, quinze des dix-huit provinces sont touchées par la peste porcine africaine[55].
Le , la présence de la maladie en Birmanie (Myanmar) est confirmée, dans une zone frontalière avec la province chinoise du Yunnan[56].
Le , les premiers cas de peste porcine africaine sont signalés aux Philippines, près de Manille[57]. La maladie se répand dans le reste de l'île de Luçon. Le premier cas est détecté dans l'île de Mindanao en [58].
En Russie, la maladie est détectée dans l'Oblast autonome juif le [59], et le un nouveau foyer est détecté dans le Kraï du Primorié, probablement en provenance de Chine[60].
Le , la Corée du Sud fait état des premiers cas de peste porcine africaine dans le village de Paju, proche de la frontière intercoréenne[61]. Le , alors que 15 000 porcs ont été abattus préventivement, quatre foyers ont été détectés, tous proches de la Corée du Nord. La maladie est suspectée d'avoir contaminé tout le pays, mais les autorités nord-coréennes refusent de communiquer sur ce sujet. Il est probable, si c'est le cas, que la maladie nuise à l'alimentation de la population nord-coréenne[62]. Le National Intelligence Service, service de renseignement sud-coréen, rapporte que la maladie est arrivée en en Corée du Nord, et s'étend depuis à tout le pays en décimant les élevages porcins[63]. Devant le silence nord-coréen, le ministère de l'Unification décide de donner de l'argent à des ONG pour qu'elles aident à contenir l'épizootie au nord[64].
Le Timor oriental rapporte les premiers cas le , dans la ville de Dili[65].
Le , la maladie est identifiée en Indonésie, dans la province de Sumatra du Nord[66].
En , des cas sont signalés dans l'Inde du Nord-Est, et il est demandé aux producteurs de ne plus transporter de porcs d'un État à l'autre[67].
Conséquences économiques
[modifier | modifier le code]La Chine abattant une grande quantité de porcs, elle doit en importer massivement pour sa consommation interne, ce qui fait fortement augmenter le prix sur le marché mondial[68]. Selon une estimation de , 200 millions de porcs, soit près de la moitié de la population, vont devoir être abattus en Chine. En un an, la production de viande de porc a chuté de 30 %, et le prix d'achat grimpé de 40 %[69]. En août, la FAO annonce que 5 millions de porcs ont été abattus ou sont décédés en Asie à la suite de cette épidémie[70].
La peste porcine africaine a pour conséquence un effondrement de la production de viande de porc chinoise, estimé à 40 % en 2019. Les prix ont grimpé de 46,7 % au de cette même année[71]. Le gouvernement dégèle 10 000 tonnes de viande issues de ses réserves stratégiques, afin d'éviter une situation de pénurie, notamment dans le contexte des célébrations du septantième anniversaire de la République populaire de Chine[72]. L'Asie est en effet une des régions où la viande consommée est le plus souvent du porc : 46 % contre 36 % à l'échelle mondiale. En Chine, ce taux monte à 62 %, et à 57 % pour le Vietnam[73]. Le cours du porc est affecté à une échelle mondiale, les prix devant monter de 5 à 15 % en France pour le jambon et les saucisses en [74]. En réaction face à la pénurie de viande, certains éleveurs chinois élèvent des porcs de plus en plus gros[75].
En , les prix du porc ont augmenté de 69 % sur un an en Chine continentale, entraînant également à la hausse le prix des autres viandes consommées en substitution, comme le bœuf ou l'agneau. L'inflation globale est également affectée, et atteint 3 %, soit son plus haut niveau depuis [76].
Les gros éleveurs de porc chinois s'enrichissent fortement en raison de la hausse des prix, et des faillites des plus petits producteurs touchés par la maladie[77].
En , le gouvernement chinois dévoile un plan en trois ans pour rétablir la production de porc. L'objectif est de reconstituer le cheptel en 2020, et de retrouver des niveaux de production pré-épidémiques en 2021. Des mesures sont prises pour faciliter la mise en place de nouvelles fermes porcines. Cependant, l'épidémie de maladie à coronavirus de 2019-2020 paralyse certains secteurs de l'économie, et pourrait retarder ce plan[78].
Belgique de 2018 à 2020
[modifier | modifier le code]

La peste porcine africaine est détectée sur le cadavre de deux sangliers la première fois en Belgique le [79]. De nouveaux cadavres de sangliers porteurs du virus sont ensuite retrouvés les jours suivants, le bilan étant de 18 au [80]. En réaction, le ministre fédéral de l'agriculture décide l'abattage préventif de tous les porcs dans un périmètre de 630 km2 situé au sud de la province du Luxembourg où tous les sangliers porteurs du virus ont été retrouvés[81]. Cela concerne un élevage de 1 000 animaux, un de 400 et cinq ou six élevages d'une cinquantaine de têtes[82]. De façon préventive, la Chine continentale, la République de Chine (Taïwan), la Corée du Sud, les Philippines et la Biélorussie décident de cesser leurs importations de viande de porc belge[83].
Dans les deux départements français contigus au périmètre concerné, la Meuse et la Meurthe-et-Moselle, une zone d'observation renforcée est mise en place le , concernant 41 communes. Dans celles-ci, tout déplacement et activité forestière, y compris exploitation du bois et chasse, est interdite[84]. De même, le Grand-Duché de Luxembourg a mis en place une zone de surveillance délimitée par les frontières française et belge, ainsi que par les autoroutes A4 et A6. Dans cette zone, la chasse reste autorisée, mais les porcs doivent rester confinés[85].
Au , 79 sangliers viropositifs ont été découverts, tous autour des villages de Buzenol, Ethe ou du camp militaire Lagland, à l'ouest d'Arlon. La pose de clôtures visant à isoler les massifs forestiers doit alors commencer le [86].
Le périmètre d'exclusion est subdivisé en une zone noyau où se trouvent l'essentiel des cadavres contaminés, une zone tampon autour, et une zone d'observation renforcée exempte. Au , 155 cadavres de sangliers viropositifs ont été retrouvés, 148 dans la zone noyau et 7 dans la zone tampon[87].
Au , 281 animaux ont été trouvés porteurs du virus, qui progresse vers l'ouest et se rapproche de la frontière française. Une nouvelle clôture doit être installée, au niveau de Meix-devant-Virton, le piégeage et les tirs de nuit mis en place[88]. Du côté français de la frontière, une « zone blanche », dans laquelle tous les sangliers doivent être abattus, est mise en place[89], et l'armée est par la suite appelée pour une aide logistique[90]. Le , deux sangliers sont abattus entre Meix-devant-Virton et Sommethonne, à quelques centaines de mètres de la frontière française, et sont contrôlés positifs au virus après analyse[91].
La maladie progresse également vers l'est, puisqu'un sanglier positif est découvert le à Differt, ce qui laisse craindre une expansion du virus dans le Grand-Duché du Luxembourg tout proche[92]. En réaction, les autorités luxembourgeoises décident d'ouvrir la chasse jusqu'au dans la zone de surveillance, de contrôler systématiquement tout sanglier retrouvé mort et prévoient la pose de nouvelles clôtures[93].
En conséquence, le prix du porc belge s'effondre, passant sous les 0,85 €/kg, ce qui est inférieur au coût de revient[94]. La région wallonne souhaite aider les éleveurs, notamment via des réductions de cotisations sociales. Le ministre fédéral de l'Agriculture, Denis Ducarme, reconnaît le la filière porcine comme « secteur en crise »[95], ce qui permet notamment un assouplissement des cotisations sociales pour les quatre trimestres de 2019.
Par ailleurs, la filière bois est lourdement affectée, puisqu'il est interdit de pénétrer dans la forêt. Les scolytes nuisent aux forêts, aidés par un été 2018 particulièrement sec. Le gouvernement wallon décide de mobilier quatre millions d'euros pour soutenir la filière[96].
Le , le parquet du Luxembourg annonce avoir arrêté quatre personnes, dont un agent du département de la nature et des forêts (DNF), qui doivent être interrogées afin d'éclaircir les circonstances de l'apparition de la maladie en Belgique[97].
À partir du , une partie de la forêt, soit 16 000 ha, est rouverte à la circulation, à condition de rester dans les sentiers, de ne pas laisser divaguer d'animal de compagnie, et de ne pas se rendre dans une exploitation agricole dans les trois jours suivant la visite[98]. Cette décision est critiquée par le syndicat agricole flamand Boerenbond[99], ainsi que par la Fédération wallonne de l'agriculture qui juge cette réouverture prématurée[100]. Cependant, cette zone est de nouveau fermée à partir du , par crainte de contagion par des sangliers porteurs du virus, mais non touchés par la maladie[101].
En , le nombre de cadavres retrouvés semble en forte diminution, ce qui laisse espérer une maladie sous contrôle pour le mois de décembre[102]. À cette date, 10,5 millions d'euros ont été dépensés pour contenir la maladie. Le , un nouveau cas positif est relevé sur les ossements d'un sanglier mort depuis un certain temps, dans le camp militaire de Lagland. Avant cette date, le dernier cas remontait au [103]. Le , les ossements d'un sanglier mort depuis trois à six mois sont retrouvés à proximité d'Assenois[104]. Par conséquent, la zone de surveillance, considérée comme infectée, est étendue jusqu'au sud de Neufchâteau[105].
À partir du , les sentiers forestiers de la zone d'exclusion doivent de nouveau être accessibles. Il reste interdit de s'enfoncer dans la forêt ou d'y circuler la nuit. De plus, dans un contexte de pandémie de Covid-19, les restrictions sont levées uniquement pour les résidents à proximité[106],[107].
À la fin du mois d', la Wallonie demande à l'Union européenne d'être de nouveau classée comme zone indemne de la maladie. Les clôtures doivent cependant rester en place au moins jusqu'à , et les restrictions de circulation jusqu'à [108]. La Commission européenne reconnaît en la Belgique indemne du virus[109].
| Date | Nombre de sangliers (cumul) |
|---|---|
| 18[80] | |
| 28[110] | |
| 32[111] | |
| 70[112] | |
| 79[86] | |
| 104[113] | |
| 155[87] | |
| 161[114] | |
| 167[115] | |
| 181[116] | |
| 184[117] | |
| 205[118] | |
| 281[88] | |
| 345[119] | |
| 389[120] | |
| 406[94] | |
| 439[121] | |
| 494[122] | |
| 573[123] | |
| 619[124] | |
| 687[125] | |
| 694[126] | |
| 708[127] | |
| 719[98] | |
| 815[128] | |
| 824[129] | |
| 825[130] | |
| 826[102] |
Vaccination
[modifier | modifier le code]Le développement d'un vaccin a été entravé par la complexité génétique du virus de la peste porcine africaine, par un manque de compréhension de son mode d'infection, par l'absence de développement d'anticorps neutralisant le virus, et aussi par des difficultés techniques telles que l'absence de lignées cellulaires stables, si bien qu'aucun vaccin n'était attendu avant 2027[réf. nécessaire].
En 2017, un sanglier abattu en Lettonie s'est révélé être porteur du virus sans présenter de symptômes de la maladie. La culture de son sérum a permis de produire un vaccin vivant. Il s'agit d'une souche faiblement virulente : inoculée à des sangliers en captivité, elle n'a entraîné aucun symptôme de la maladie, mais en revanche la production d'anticorps efficaces, non seulement contre cette souche virale mais aussi contre la forme la plus dangereuse. Le vaccin peut être administré oralement (dans des appâts pour ce qui est des animaux sauvages), et il est apparu que des sangliers pouvaient aussi être immunisés après un simple contact avec des sangliers vaccinés. Des études de sécurité et de stabilité génétique doivent encore être conduites avant de généraliser la vaccination aux animaux domestiques et à toutes les zones infectées[131],[132].
En 2020, un vaccin expérimental développé au Royaume-Uni pourrait servir de base au développement d'un vaccin efficace contre la peste porcine africaine, et ce malgré une protection limitée à ce stade des travaux[133],[134].
Notes et références
[modifier | modifier le code]- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « African swine fever virus » (voir la liste des auteurs).
- Blome S, Gabriel C & Beer M (2013). Pathogenesis of African swine fever in domestic pigs and European wild boar. Virus research, 173(1), 122-130|PDF, 9 pp
- (en) « Unclassified Viruses », sur ictv.global (consulté le ).
- (en) Dixon et al., Animal Viruses : Molecular Biology, Caister Academic Press, , 531 p. (ISBN 978-1-904455-22-6, lire en ligne), « African Swine Fever Virus »
- Colgrove et al. (1969) cités par le rapport scientifique de l'EFSA de 2009
- « Peste porcine africaine : une modélisation pour prévoir la circulation de la maladie chez les sangliers », sur Anses - Agence nationale de sécurité…, (consulté le ).
- le virus persiste dans certaines denrées alimentaires à base de produits et/ou viande de porc contaminés (charcuteries notamment) ; source AFSCA [http://www.afsca.be/santeanimale/pesteporcineafricaine/Peste porcine africaine , Fiche consultée 12 mars 2018
- « Peste porcine africaine : Actualité en Europe et dans le monde », sur afsca.be (consulté le ).
- « La Chine contrainte d'abattre des milliers de porcs atteints de la peste », FIGARO, (lire en ligne, consulté le )
- « Les 3 nouveaux cas de peste porcine africaine en Belgique ont été confirmés », Le Soir, (lire en ligne, consulté le )
- Jose Angel Barasona et al., « First Oral Vaccination of Eurasian Wild Boar Against African Swine Fever Virus Genotype II », (consulté le )
- (en) Howard Zinn, A People's History of the United States, chapitre 20.
- (en) Critical Reviews in Microbiology, 25(3):173–227 (1999)
- (en) Mark Wheelis, A Short History of Biological Warfare and Weapons
- José Manuel Sánchez-Vizcaíno et Lina Mur Gil, « La peste porcine africaine : brève vision du passé, du présent...et du futur? », sur 3trois3.com, (consulté le )
- « Peste porcine africaine : interdiction de chasse sur 63.000 hectares », sur wallonie.be via Wikiwix (consulté le ).
- « Peste porcine africaine: voici ce qui serait la cause de la contamination », La Libre Belgique, (lire en ligne, consulté le ).
- Le Monde avec AFP, « Peste porcine africaine : un foyer détecté dans l’ouest de l’Allemagne, près de la frontière française », Le Monde, (lire en ligne, consulté le ).
- AFSCA [http://www.afsca.be/santeanimale/pesteporcineafricaine/Peste porcine africaine , Fiche consultée 12 mars 2018
- Galindo, Inmaculada; Alonso, Covadonga. 2017. "African Swine Fever Virus: A Review." Viruses 9, no. 5: 103. |résumé
- Leblanc N, Cortey M, Fernandez Pinero J, Gallardo C, Masembe C, Okurut AR, Heath L, van Heerden J, Sánchez-Vizcaino JM, Ståhl K, Belák S (2012) Development of a suspension microarray for the genotyping of African swine fever virus targeting the SNPs in the C-terminal end of the p72 gene region of the Genome. Transbound Emerg Dis doi: 10.1111/j.1865-1682.2012.01359.x.
- Christophe Violette, « Le retour de la peste porcine menace l’Europe », sur Ouest-France, (consulté le )
- Elena Arsevska, « Peste porcine africaine en Sardaigne en 2014 – de l’enzootie à l’épizootie ? », (consulté le )
- Loïc Chauveau, « Comment la peste porcine africaine s'est frayée (sic) un chemin jusqu'à la frontière française », sur sciencesetavenir.fr, (consulté le )
- Bruno Poussard, « Alsace: Faut-il s'inquiéter de l'épidémie de peste porcine africaine en Europe de l'Est? », sur 20 minutes, (consulté le )
- Christophe Violette et Romain Su, « Peste porcine. Les sangliers polonais terrorisent les éleveurs en France », sur Ouest-France, (consulté le )
- Alexis Rosenzweig, « Limiter la propagation de la peste porcine: l'exemple de la Tchéquie », sur RTBF, (consulté le )
- « La Hongrie est touchée », sur La France agricole,
- Alizé MERCIER, « Déclaration d’un premier foyer de peste porcine africaine en Roumanie », sur Plateforme ESA, (consulté le )
- AFP, « Peste porcine africaine en Roumanie, plus de 110.000 porcs abattus », sur Europe1, (consulté le )
- Thomas Giraudeau, « Pologne: la peste porcine africaine ravage les élevages », sur RFI, (consulté le )
- Le Figaro et AFP, « Danemark: une palissade à la frontière allemande contre la peste porcine », sur Le Figaro, (consulté le )
- Nelly Didelot, « Les sangliers polonais au bord de la disparition programmée », sur Libération, (consulté le )
- « La Pologne, un "véritable réservoir" pour la peste porcine africaine », sur Ouest-France, (consulté le )
- AFP, « Les autorités allemandes sur le qui-vive », sur lafranceagricole.fr, .
- Damian Vodénitcharov, « La peste porcine ravage la Bulgarie », sur RFI, (consulté le ).
- « Première apparition de la PPA en Slovaquie », sur 3trois3.com, (consulté le ).
- Loïc Chauveau, « La peste porcine africaine continue de s’étendre en Europe », sur sciencesetavenir.fr, (consulté le ).
- Belga, « Peste porcine africaine : l'Allemagne enregistre un premier cas sur une carcasse de sanglier », sur RTBF.be, (consulté le ).
- (de) « Afrikanische Schweinepest: Wie lange bleibt sie? », sur welt.de, (consulté le ).
- Maxime Magnier et AFP, « Allemagne : cinq nouveaux cas de peste porcine africaine », sur rtl.fr, (consulté le ).
- (de) Stefan Lange, « Landwirtschaftsministern Klöckner: „Afrikanische Schweinepest rausbekommen aus Deutschland“ », sur augsburger-allgemeine.de, (consulté le ).
- Vincent Guyot, « Plus de 1 000 cas de peste porcine africaine en Allemagne », sur lafranceagricole.fr, .
- RTS Info, « L'épidémie de peste porcine s'étend en Chine et menace d'autres pays », Radio télévision suisse, 2 septembre 2018 (page consultée le 2 septembre 2018).
- FRÉDÉRIC SCHAEFFER, « Cette nuit en Asie : la peste porcine africaine aux portes de Pékin », sur Les Échos, (consulté le )
- Gao Ke et Yishuang Liu, « La Chine signale moins de cas de peste porcine africaine », sur Le Quotidien du Peuple, (consulté le )
- Stéphane Lagarde, « Des traces de peste porcine africaine retrouvées dans les raviolis en Chin », sur rfi.fr, (consulté le )
- Frédéric Schaeffer, « En Chine, les ravages de la peste porcine », sur Les Échos, (consulté le ).
- (en) « Worst of China’s African Swine Fever Over, Says Ministry Official », sur bloomberg.com, (consulté le ).
- « Des foyers épidémiques de peste porcine africaine découvertes à Hung Yen et Thai Binh », sur vietnamplus.vn, (consulté le )
- Pierre Demoux, « Ce virus tueur de cochon qui fait trembler le marché mondial du soja », sur Les Echos,
- (en) « African swine fever spreads to South-East Asia », sur economist.com, (consulté le ).
- (en) « Swine fever: How is Asia coping with the outbreak? », sur bcc.com, (consulté le ).
- (en) Sybille de La Hamaide et Gus Trompiz, « Cambodia reports first outbreak of African swine fever: OIE », sur Reuters, (consulté le ).
- (en) « Laos confirms first cases of African swine fever Read more at https://www.channelnewsasia.com/news/asia/laos-african-swine-fever-pork-pigs-first-cases-oie-11646256 », sur channelnewsasia.com, (consulté le ).
- (en) Vincent ter Beek, « ASF Laos: Virus spreads to most of the country », sur pigprogress.net, (consulté le ).
- « La PPA arrive au Myanmar », sur 3trois3.com, (consulté le ).
- AFP, « Les Philippines confirment de premiers cas de peste porcine », sur lalibre.be, (consulté le ).
- (en) « Philippines detects first African swine fever outbreak in southern province », sur reuters.com, (consulté le ).
- (ru) « Африканская чума свиней найдена в селе Дежнево в ЕАО », sur aif.ru.
- (ru) « В Приморье нашли новый очаг африканской чумы свиней », sur ria.ru, (consulté le ).
- « Un premier foyer de peste porcine en Corée du Sud », sur lessentiel.lu, (consulté le ).
- AFP, « Séoul confirme un 4e cas de peste porcine, demande à Pyongyang de coopérer », sur nouvelobs.com, (consulté le ).
- (en) « African Swine Fever 'Decimates N.Korean Pigs' », sur chosun.com, (consulté le ).
- Kim So-hyun, « Seoul seeks to support swine fever control in NK via NGOs », sur koreaherald.com, (consulté le ).
- (en) Matt Brann, « African swine fever on Australia's doorstep, with outbreaks confirmed in Timor-Leste pig farms », sur abc.net.au (consulté le ).
- (en) Jennifer Shike, « Indonesia Confirms African Swine Fever in North Sumatra », sur porkbusiness.com, (consulté le ).
- (en) Rajeev Bhattacharyya, « India’s Northeast Hit By the African Swine Fever », sur thediplomat.com, (consulté le ).
- François Lenglet et Quentin Marchal, « La Chine bouleverse le marché mondial du porc », sur RTL, (consulté le ).
- AFP, « "La plus grande épidémie animale jamais vue" : des experts alertent sur la peste porcine africaine qui fait rage en Asie », sur France Info, (consulté le ).
- Anne-Sophie Tassart, « 5 millions de porcs morts en Asie à cause de la peste porcine africaine », sur Science et Avenir,
- Simon Leplâtre, « En Chine, la flambée du prix du porc, une crise majeure pour les autorités », sur Le Monde, (consulté le ).
- « La Chine décongèle 10'000 tonnes de viande », sur Tribune de Genève, (consulté le ).
- (en) « African Swine Fever continues to spread », sur miragenews.com, (consulté le ).
- MARINE THORON, « VERS UNE AUGMENTATION CONSIDÉRABLE DES PRIX DU JAMBON », sur Capital, (consulté le ).
- Anne-Sophie Tassart, « Peste porcine : la Chine élève des porcs géants pour faire face à la pénurie », sur sciencesetavenir.fr, (consulté le ).
- « Chine: la crise du porc fait bondir l'inflation au plus haut depuis 6 ans », sur bfmtv.com, (consulté le ).
- (en) Bloomberg, « Chinese pig farming kings thrive as African swine fever sends prices soaring », sur scmp.com, (consulté le ).
- Vincent Guyot, « Porc Le coronavirus perturbe les échanges », La France agricole, no 3840, (lire en ligne, consulté le ).
- « Deux cas de peste porcine africaine identifiés à Etalle », (consulté le )
- « Peste porcine africaine : trois nouveaux cas de contamination de sangliers, 18 au total », sur La Libre
- Isabelle Lemaire, « Peste porcine: voici l'arrêté ministériel d'ordre d'abattage des porcs », sur La Libre
- Alizé MERCIER, « Point de situation sur la peste porcine africaine en Belgique », sur plateforme épidémiosurveillance santé animal, (consulté le )
- « Peste porcine africaine : six pays cessent d'importer du porc de Belgique », sur Europe1,
- « Peste porcine africaine – Nouvelles mesures contre la peste porcine dans le nord de la France », sur Metro Belgique, (consulté le )
- Ioanna Schmizzi, « La Grande Région face à la peste porcine africaine », sur paperjam, (consulté le )
- « Peste porcine africaine: la pose de clôtures débutera ce mardi », sur RTBF,
- « Peste porcine africaine: 155 sangliers contrôlés positifs au virus », sur Le Soir, (consulté le )
- Nadia Lallemant, « Peste porcine africaine : une clôture supplémentair », sur dh.be, (consulté le )
- Hugo Septier et AFP, « Peste porcine: création d'une "zone blanche" vide de sangliers à la frontière de la Belgique », sur bfmtv.com, (consulté le )
- AFP, « Peste porcine africaine: l'armée en appui logistique, zone blanche étendue », sur L'Express, (consulté le )
- JP, « Peste porcine africaine: des sangliers infectés pourraient avoir franchi la frontière française », sur RTBF, (consulté le )
- LQ, « Un cas de peste porcine à 3 km de la frontière luxembourgeoise », sur lequotidien.lu, (consulté le ).
- « La chasse restera ouverte jusqu'au 15 avril », sur lessentiel.lu, (consulté le ).
- Jordane Meyer, « Nouveau bilan sur le front de la Peste porcine africaine », sur RTBF, (consulté le )
- Belga, « Suite à la peste porcine, le ministre de l'Agriculture reconnaît la filière porcine comme secteur en crise », sur rtlinfo.be, (consulté le )
- « Peste porcine africaine: 4 millions d’euros pour la filière bois », sur sudinfo.be, (consulté le )
- RTBF, « Quatre personnes privées de liberté pour être auditionnées dans le cadre de la Peste Porcine Africaine », sur RTBF, (consulté le )
- Nicoals Poës, « Peste porcine : une partie de la forêt rouverte », sur dhnet.be, (consulté le ).
- Belga, « Peste porcine africaine: le Boerendond juge «irresponsable et incompréhensible» la réouverture de 16.000 ha », sur sudinfo.be, (consulté le ).
- Belga, « Peste porcine africaine: la réouverture de certains sentiers forestiers inquiète », sur Le Soir, (consulté le ).
- Laurent Van de Berg, « Peste porcine africaine : la zone infectée fermée aux promeneurs et cyclistes », sur RTBF.be, (consulté le ).
- « Bientôt la fin de la peste porcine africaine ? "On trouve beaucoup moins de cadavres infectés" », sur RTBF, (consulté le ).
- Belga, « Un nouveau cas positif de peste porcine africaine découvert dans la zone infectée », sur RTBF.be, (consulté le ).
- Belga, « Peste porcine africaine: des ossements d'un sanglier viropositif découverts au sud de Neufchâteau », sur rtbf.be, (consulté le ).
- Belga, « La zone infectée par la peste porcine s’agrandit », sur lesoir.be, (consulté le ).
- Jean-Luc Bodeux, « Peste porcine africaine : les sentiers forestiers gaumais enfin déconfinés le 15 mai », sur lesoir.be, (consulté le ).
- Nadia Lallemant, « PPA : réouverture de la forêt en zone infectée dès le 15 mai », sur dhnet.be, (consulté le ).
- Philippe Herman, « La Gaume pratiquement débarassée [sic] de la Peste Porcine Africaine mais la vigilance reste de mise », sur rtbf.be, (consulté le ).
- Vincent Guyot, « La Belgique est désormais indemne de peste porcine africaine », sur lafranceagricole.fr, .
- N.L., « Sanglier braconné à Tintigny : il n’était pas infecté ! », sur dhnet.be, (consulté le )
- N.L., « Peste porcine africaine : 32 sangliers contrôlés positifs ! », sur dhnet.be, (consulté le )
- N.L., « Peste porcine africaine : 70 sangliers viropositifs », sur dhnet.be, (consulté le )
- Belga, « Peste porcine africaine: un nouveau bilan mentionne 104 sangliers positifs au virus », sur dhnet.be, (consulté le )
- N.L., « Peste porcine africaine: 161 sangliers viropositifs », sur dhnet.be, (consulté le )
- N.L., « Peste porcine africaine : la zone noyau s’agrandit », sur dhnet.be, (consulté le )
- N.L., « Peste porcine africaine : une "zone de vigilance" s’ajoute aux 63.000 hectares », sur dhnet.be, (consulté le )
- N.L., « Peste porcine africaine : le forfait de 50 euros par sanglier accordé », sur dhnet.be, (consulté le )
- « PPA Belgique : Nombre de sangliers infectés », sur 3trois3, (consulté le )
- « Peste porcine africaine: à ce jour, 345 carcasses de sangliers positives au virus de la peste porcine africaine », sur dhnet.be, (consulté le )
- Belga, « Peste porcine: les chasseurs autorisés à tuer des sangliers en zone tampon », sur RTBF, (consulté le )
- Belga, « Peste porcine africaine: deux sangliers abattus lundi à Habay, une première dans cette commune », sur lavenir.net, (consulté le )
- N.L., « Peste porcine africaine : 494 sangliers viropositifs », sur dhnet.be, (consulté le )
- N.L., « Peste Porcine Africaine : 573 sangliers viropositifs », sur dhnet.be, (consulté le ).
- Belga, « Peste porcine africaine: le nombre de sangliers infectés continue à augmenter », sur lesoir.be, (consulté le )
- « Peste porcine africaine : 687 carcasses se sont révélées viropositives », sur sudinfo.be, (consulté le )
- « Peste porcine africaine: les sentiers en forêt gaumaise bientôt rouverts aux promeneurs », sur RTBF, (consulté le )
- Nadia Lallemant, « Peste porcine africaine : 708 carcasses viropositives », sur dhnet.be, (consulté le )
- « La peste porcine africaine est toujours présente dans le Luxembourg: une situation préoccupante pour le secteur forestier », sur sudinfo.be, (consulté le ).
- « Peste porcine : la Belgique étend son périmètre d’interdiction des forêts », sur Républicain lorrain, (consulté le ).
- « Peste porcine africaine: 825 sangliers positifs à ce jour », sur sudinfo.be, (consulté le ).
- (en) « Vaccine for African swine fever may save our bacon », sur Frontiers. Science News, (consulté le ).
- (en) Jose A. Barasona, Carmina Gallardo, Estefanía Cadenas-Fernández, Cristina Jurado, Belén Rivera et al., « First Oral Vaccination of Eurasian Wild Boar Against African Swine Fever Virus Genotype II », Frontiers in Veterinary Science, (DOI 10.3389/fvets.2019.00137).
- A Pool of Eight Virally Vectored African Swine Fever Antigens Protect Pigs Against Fatal Disease, Goatley, L. C., Reis, A. L., Portugal, R., Goldswain, H., Shimmon, G. L., Hargreaves, Z., Ho, C. S., Montoya, M., Sánchez-Cordón, P. J., Taylor, G., Dixon, L. K., & Netherton, C. L. (2020). Vaccines, 8(2), 234 , DOI : 10.3390/vaccines8020234
- Philippines to join field trials for swine vaccine, BusinessWorld, May 26, 2020 (Consulté le 16/03/2021)
Voir aussi
[modifier | modifier le code]Bibliographie
[modifier | modifier le code]- Achenbach J.E.; Gallardo, C.; Nieto-Pelegrin, E.; Rivera-Arroyo, B.; Degefa-Negi, T.; Arias, M.; Jenberie, S.; Mulisa, D.D.; Gizaw, D.; Gelaye, E.; et al. Identification of a new genotype of african swine fever virus in domestic pigs from Ethiopia. Transbound. Emerg. Dis. 2016.
- Alcami, A.; Carrascosa, A.L.; Vinuela, E. Interaction of African swine fever virus with macrophages. Virus Res. 1990, 17, 93–104
- Alcami, A.; Carrascosa, A.L.; Vinuela, E. Saturable binding sites mediate the entry of African swine fever virus into vero cells. Virology 1989, 168, 393–398
- Alcami, A.; Carrascosa, A.L.; Vinuela, E. The entry of African swine fever virus into vero cells. Virology 1989, 171, 68–75.
- Almazan, F.; Rodriguez, J.M.; Andres, G.; Perez, R.; Vinuela, E.; Rodriguez, J.F. Transcriptional analysis of multigene family 110 of african swine fever virus J. Virol. 1992, 66, 6655–6667.
- Alonso, C.; Miskin, J.; Hernaez, B.; Fernandez-Zapatero, P.; Soto, L.; Canto, C.; Rodriguez-Crespo, I.; Dixon, L.; Escribano, J.M. African swine fever virus protein p54 interacts with the microtubular motor complex through direct binding to light-chain dynein. J. Virol. 2001, 75, 9819–9827.
- Anderson, E.C.; Hutchings, G.H.; Mukarati, N.; Wilkinson, P.J. African swine fever virus infection of the bushpig (Potamochoerus porcus) and its significance in the epidemiology of the disease. Vet. Microbiol. 1998, 62, 1–15.
- Andres, G.; Garcia-Escudero, R.; Vinuela, E.; Salas, M.L.; Rodriguez, J.M. African swine fever virus structural protein pE120R is essential for virus transport from assembly sites to plasma membrane but not for infectivity. J. Virol. 2001, 75, 6758–6768.
- Angulo, A.; Vinuela, E.; Alcami, A. Inhibition of African swine fever virus binding and infectivity by purified recombinant virus attachment protein p12. J. Virol. 1993, 67, 5463–5471.
- Ballester, M.; Rodriguez-Carino, C.; Perez, M.; Gallardo, C.; Rodriguez, J.M.; Salas, M.L.; Rodriguez, F. Disruption of nuclear organization during the initial phase of african swine fever virus infection. J. Virol. 2011, 85, 8263–8269.
- Basta, S.; Gerber, H.; Schaub, A.; Summerfield, A.; McCullough, K.C. Cellular processes essential for African swine fever virus to infect and replicate in primary macrophages. Vet. Microbiol. 2010, 140, 9–17.
- Bastos, A.D.; Penrith, M.L.; Cruciere, C.; Edrich, J.L.; Hutchings, G.; Roger, F.; Couacy-Hymann, E.; Thomson, G.R. Genotyping field strains of african swine fever virus by partial p72 gene characterisation. Arch. Virol. 2003, 148, 693–706.
- Benedict, C.A.; Norris, P.S.; Ware, C.F. To kill or be killed: Viral evasion of apoptosis. Nat. Immunol. 2002, 3, 1013–1018.
- Boshoff, C.I.; Bastos, A.D.; Gerber, L.J.; Vosloo, W. Genetic characterisation of african swine fever viruses from outbreaks in southern Africa (1973–1999). Vet. Microbiol. 2007, 121, 45–55.
- Breese, S.S., Jr.; de Boer, C.J. Electron microscope observations of African swine fever virus in tissue culture cells. Virology 1966, 28, 420–428
- Brun, A.; Rivas, C.; Esteban, M.; Escribano, J.M.; Alonso, C. African swine fever virus gene a179l, a viral homologue of BCL-2, protects cells from programmed cell death. Virology 1996, 225, 227–230
- Carvalho, Z.G.; de Matos, A.P.; Rodrigues-Pousada, C. Association of African swine fever virus with the cytoskeleton. Virus Res. 1988, 11, 175–192.
- Chacon, M.R.; Almazan, F.; Nogal, M.L.; Vinuela, E.; Rodriguez, J.F. The African swine fever virus IAP homolog is a late structural polypeptide. Virology 1995, 214, 670–674.
- Cubillos, C.; Gomez-Sebastian, S.; Moreno, N.; Nunez, M.C.; Mulumba-Mfumu, L.K.; Quembo, C.J.; Heath, L.; Etter, E.M.; Jori, F.; Escribano, J.M.; et al. African swine fever virus serodiagnosis: A general review with a focus on the analyses of african serum samples. Virus Res. 2013, 173, 159–167.
- Cuesta-Geijo, M.A.; Chiappi, M.; Galindo, I.; Barrado-Gil, L.; Munoz-Moreno, R.; Carrascosa, J.L.; Alonso, C. Cholesterol flux is required for endosomal progression of african swine fever virions during the initial establishment of infection. J. Virol. 2015, 90, 1534–1543.
- Cuesta-Geijo, M.A.; Galindo, I.; Hernaez, B.; Quetglas, J.I.; Dalmau-Mena, I.; Alonso, C. Endosomal maturation, Rab7 GTPase and phosphoinositides in African swine fever virus entry. PLoS ONE 2012, 7, e48853.
- De Matos, A.P.; Carvalho, Z.G. African swine fever virus interaction with microtubules. Biol. Cell 1993, 78, 229–234.
- Dixon, L.K.; Escribano, J.M.; Martins, C.; Rock, D.L.; Salas, M.L.; Wilkinson, P.J. Asfarviridae. In Virus Taxonomy. VIIIth Report of the ICTV; Fauquet, C.M., Mayo, M.A., Maniloff, J., Desselberger, U., Ball, L.A., Eds.; Elsevier/Academic Press: London, UK, 2005; pp. 135–143
- Fabregas, J.; Garcia, D.; Fernandez-Alonso, M.; Rocha, A.I.; Gomez-Puertas, P.; Escribano, J.M.; Otero, A.; Coll, J.M. In vitro inhibition of the replication of haemorrhagic septicaemia virus (VHSV) and African swine fever virus (ASFV) by extracts from marine microalgae. Antivir. Res. 1999, 44, 67–73.
- Galindo, I.; Cuesta-Geijo, M.A.; Hlavova, K.; Munoz-Moreno, R.; Barrado-Gil, L.; Dominguez, J.; Alonso, C. African swine fever virus infects macrophages, the natural host cells, via clathrin and cholesterol-dependent endocytosis. Virus Res. 2015, 200, 45–55
- Galindo, I.; Hernaez, B.; Berna, J.; Fenoll, J.; Cenis, J.L.; Escribano, J.M.; Alonso, C. Comparative inhibitory activity of the stilbenes resveratrol and oxyresveratrol on african swine fever virus replication. Antivir. Res. 2011, 91, 57–63.
- Galindo, I.; Hernaez, B.; Diaz-Gil, G.; Escribano, J.M.; Alonso, C. A179l, a viral BCL-2 homologue, targets the core BCL-2 apoptotic machinery and its upstream BH3 activators with selective binding restrictions for bid and noxa. Virology 2008, 375, 561–572.
- Galindo, I.; Hernaez, B.; Munoz-Moreno, R.; Cuesta-Geijo, M.A.; Dalmau-Mena, I.; Alonso, C. The ATF6 branch of unfolded protein response and apoptosis are activated to promote African swine fever virus infection. Cell Death Dis. 2012, 3, e341.
- Galindo, Inmaculada; Alonso, Covadonga. 2017. "African Swine Fever Virus: A Review." Viruses 9, no. 5: 103.
Articles connexes
[modifier | modifier le code]Liens externes
[modifier | modifier le code]- Fiche de la maladie sur le site de l'Office international des épizooties.
- Peste porcine africaine - Fiche de renseignements sur le site de l'Agence canadienne d'inspection des aliments (ACIA).
- (en) Présentation de la maladie sur ThePigSite.com
Législation européenne
[modifier | modifier le code]- Directive 2002/60/CE du Conseil du 27 juin 2002 établissant des dispositions spécifiques pour la lutte contre la peste porcine africaine et modifiant la directive 92/119/CEE, en ce qui concerne la maladie de Teschen et la peste porcine africaine (J.O. du 20/07/2002)
- Décision 2014/709/EU de la Commission du 9 octobre 2014 concernant des mesures zoosanitaires de lutte contre la peste porcine africaine dans certains États membres (J.O. du 11/10/2014)
- sur le site de la Commission Européenne : http://ec.europa.eu/food/animal/diseases/controlmeasures/asf_en.htm
