Acide trifluorométhanesulfonique
| Acide trifluorométhanesulfonique | |

| |
| Structure de l'acide trifluorométhanesulfonique. | |
| Identification | |
|---|---|
| Nom UICPA | acide trifluorométhanesulfonique |
| Synonymes |
acide triflique, |
| No CAS | |
| No ECHA | 100.014.625 |
| No CE | 216-087-5 |
| No RTECS | PB2771000 |
| PubChem | 62406 |
| ChEBI | 48511 |
| SMILES | |
| InChI | |
| Apparence | liquide clair[1] de couleur jaune à l'odeur piquante[2] |
| Propriétés chimiques | |
| Formule | CHF3O3S |
| Masse molaire[3] | 150,077 ± 0,007 g/mol C 8 %, H 0,67 %, F 37,98 %, O 31,98 %, S 21,37 %, |
| Propriétés physiques | |
| T° fusion | −40 °C[2] |
| T° ébullition | 162 °C[2] |
| Solubilité | 1 600 g/L[1] dans l'eau à 20 °C |
| Masse volumique | 1,71 g/cm3[2] à 20 °C |
| Pression de vapeur saturante | 3,2 hPa[1] à 25 °C 10 hPa[2] à 55 °C |
| Précautions | |
| SGH[2] | |
| H290, H302, H314, H335, P280, P310, P301+P330+P331, P303+P361+P353, P304+P340 et P305+P351+P338 |
|
| SIMDUT[4] | |
 E, |
|
| NFPA 704[5] | |
| Transport[2] | |
| Écotoxicologie | |
| LogP | < 0,3[1] (octanol/eau) à 25 °C |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'acide trifluorométhanesulfonique, ou acide triflique, abrégé TfOH, est un acide sulfonique de formule CF3SO3H. Il est parfois considéré comme un des plus puissants acides, et fait partie de ceux qualifiés de superacides. Il est essentiellement utilisé en chimie organique comme catalyseur en recherche dans des réactions d'estérification[6],[7]. Base conjuguée d'un acide fort, l'anion trifluorométhanesulfonate CF3SO3−, ou triflate, est particulièrement stable[8]. L'acide trifluorométhanesulfonique est utilisé de diverses manières en chimie organique, le groupe triflate intervient souvent comme groupe partant et ses sels sont utilisés comme catalyseurs. Dans les publications spécialisées, l'abréviation « OTf » est principalement utilisée pour le groupe triflate –OSO2CF3 tandis que l'abréviation « Tf » désigne le groupe trifluorométhanesulfonyle –SO2CF3, également appelé groupe triflyle.
Propriétés[modifier | modifier le code]
L'acide triflique est un liquide hygroscopique incolore et légèrement visqueux à température ambiante. Il est soluble dans les solvants polaires tels que le N,N-diméthylformamide (DMF), le diméthylsulfoxyde (DMSO), l'acétonitrile ou encore le méthyl-sulfonyl-méthane (MSM, ou diméthylsulfone). Cependant, son addition à ces solvants polaires peut être dangereusement exothermique.
Au laboratoire, l'acide triflique est utile pour réaliser des protonations car sa base conjuguée est non nucléophile. Il est utilisé également pour le titrage acido-basique non aqueux car il se comporte comme un acide fort dans de nombreux solvants comme l'acétonitrile et l'acide acétique alors que des acides minéraux courants tels que l'acide chlorhydrique HCl et l'acide sulfurique H2SO4 ne sont que modérément forts.
Avec un Ka égal à 5,0 × 1014, d'où un pKa = −14,7 ± 2,0[9], l'acide triflique est un superacide. Il doit ses propriétés utiles à sa grande stabilité thermique et chimique. L'acide et sa base conjuguée CF3SO3− (triflate) résistent aux réactions d'oxydoréduction, alors que de nombreux acides forts sont oxydants, comme l'acide perchlorique HClO4 et l'acide nitrique HNO3. L'anion triflate est non réactif aux attaques de nucléophiles, même puissants. En raison de sa résistance à l'oxydation et à la réduction, l'acide triflique constitue un réactif à la fois utile et multi-usages. De plus, il ne sulfonate pas les substrats, ce qui peut constituer un avantage par rapport à l'acide sulfurique H2SO4, l'acide fluorosulfurique HSO3F et l'acide chlorosulfurique HSO3Cl ; la sulfonation du benzène en acide benzènesulfonique est possible par exemple avec l'acide sulfurique mais pas avec l'acide triflique :
L'acide triflique fume dans un air humide et forme un monohydrate solide stable CF3SO3H·H2O dont le point de fusion vaut 34 °C.
Historique et synthèses[modifier | modifier le code]
L'acide trifluorométhanesulfonique a été préparé pour la première fois en 1954 par la réaction suivante[6],[10] :
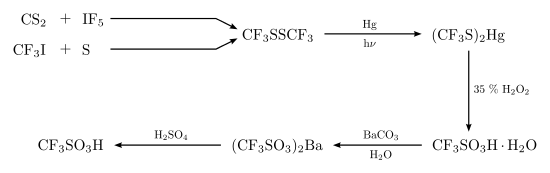
La synthèse industrielle implique l'hydrolyse de fluorure de triflyle CF3SO2F suivie d'une acidification. L'acide triflique peut également être produit par oxydation de chlorure de trifluorométhylsulfényle CF3SCl :
L'acide triflique est ensuite purifié par distillation avec une faible quantité d'anhydride triflique (CF3SO2)2O[7].
Une voie alternative de synthèse de l'acide triflique est la fluoration électrochimique[6] (ECF) :

Une autre solution est également l'oxydation du sulfure de trifluorométhyle méthyle[6] CF3SCH3 :

La production industrielle de l'acide triflique fait intervenir la fluoration électrochimique de chlorure de méthanesulfonyle CH3SO2Cl. Cette procédure est coûteuse de sorte qu'on en recherche des alternatives. Il est par exemple possible de produire de l'acide triflique à partir de trifluorométhane CHF3 dans une solution fortement acide ou fortement basique. Il s'agit d'une réaction radicalaire, par exemple avec le trioxyde de soufre SO3 ou le chlorure de sulfuryle SO2Cl2. Les rendements restent cependant assez faibles[11].
Utilisations[modifier | modifier le code]
Sels et complexes[modifier | modifier le code]
Le ligand triflate −SO2CF3 est labile, ce qui reflète sa faible basicité. L'acide triflique réagit de manière exothermique avec les carbonates, d'hydroxydes et d'oxydes de métaux. Ceci peut être illustré par la synthèse du triflate de cuivre(II) (en) Cu(OSO2CF3)2[12] :
- Cu2CO3(OH)2 (en) + 4 CF3SO3H ⟶ 2 Cu(OSO2CF3)2 (en) + 3 H2O + CO2.
La conversion de chlorures en triflates offre des perspectives intéressantes, comme la production de [Co(NH3)5OSO2CF3]2+ :
- 3 CF3SO3H + [Co(NH3)5Cl]Cl2 ⟶ [Co(NH3)5OSO2CF3](OSO2CF3)2 + 3 HCl.
Cette conversion est réalisée dans l'acide triflique pur à 100 °C suivie par la précipitation du sel par addition d'éther.
Réactions organiques[modifier | modifier le code]
L'acide triflique réagit avec les halogénures d'acyles pour donner des anhydrides mixtes, lesquels sont des agents puissants d'acylation, comme dans la réaction de Friedel-Crafts[6] :
L'acide triflique catalyse la réaction des composés aromatiques avec les chlorures de sulfonyle, probablement aussi par l'intermédiaire d'un anhydride mixte[6].
Une réaction très similaire existe si l'on souhaite effectuer une polymérisation avec une synthèse utilisant l'acide triflique. Il existe d'autres réactions de type Friedel-Crafts utilisant l'acide triflique comme le craquage des alcanes ou l'alkylation des alcènes, très importantes dans l'industrie pétrolière. Ces catalyseurs dérivés de l'acide triflique sont très efficaces dans l'isomérisation d'hydrocarbures à chaînes droites ou faiblement ramifiées, accroissant de fait l'indice d'octane de carburants pétroliers particuliers.
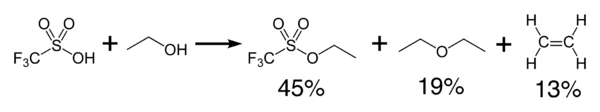
L'acide triflique réagit exothermiquement avec les alcools pour produire des éthers et des oléfines[6]. Il peut être utilisé comme catalyseur pour la condensation des alcools et des acides carboxyliques.
Références[modifier | modifier le code]
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Trifluoromethanesulfonic acid » (voir la liste des auteurs).
- Fiche Sigma-Aldrich du composé Trifluoromethanesulfonic acid, consultée le 6 novembre 2022.
FDS : (en) « Trifluoromethanesulfonic acid » [PDF], sur sigmaaldrich.com, (consulté le ) - Entrée « Trifluoromethanesulfonic acid » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 novembre 2022 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Acide trifluorométhanesulfonique » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009
- « Fiche du composé Trifluoromethanesulfonic acid, 98+% », sur Alfa Aesar (consulté le ).
- (en) R. D. Howells et J. D. Mc Cown, « Trifluoromethanesulfonic acid and derivatives », Chemical Reviews, vol. 77, no 1, , p. 69-92 (DOI 10.1021/cr60305a005, lire en ligne).
- (en) Lakshminarayanapuram R. Subramanian, Antonio García Martínez, Michael Hanack, G. K. Surya Prakash et Jinbo Hu, « Trifluoromethanesulfonic Acid », Encyclopedia of Reagents for Organic Synthesis, (DOI 10.1002/047084289X.rt246.pub2, lire en ligne).
- (en) A. Streitwieser Jr., C. Wilkins et E. Kiehlmann, « Kinetics and Isotope Effects in Solvolyses of Ethyl Trifluoromethanesulfonate », Journal of the American Chemical Society, vol. 90, no 6, , p. 1598-1601 (DOI 10.1021/ja01008a601, lire en ligne).
- (en) Aleksander Trummal, Lauri Lipping, Ivari Kaljurand, Ilmar A. Koppel et Ivo Leito, « Acidity of Strong Acids in Water and Dimethyl Sulfoxide », The Journal of Physical Chemistry A, vol. 120, no 20, , p. 3663-3669 (DOI 10.1021/acs.jpca.6b02253, lire en ligne).
- (en) R. N. Haszeldine et J. M. Kidd, « Perfluoroalkyl derivatives of sulphur. Part I. Trifluoromethanesulphonic acid », Journal of the Chemical Society (Resumed), , p. 4228-4232 (DOI 10.1039/jr9540004228, lire en ligne).
- (en) Sudip Mukhopadhyay, Alexis T. Bell, R. Vijay Srinivas et Gary S. Smith, « Synthesis of Trifluoromethanesulfonic Acid from CHF3 », Organic Process Research & Development, vol. 8, no 4, , p. 660-662 (DOI 10.1021/op040007r, lire en ligne).
- (en) Nicholas E. Dixon, Geoffrey A. Lawrance, Peter A. Lay, Alan M. Sargeson et Henry Taube, « Trifluoromethanesulfonates and Trifluoromethanesulfonato-O Complexes », Inorganic Syntheses: Reagents for Transition Metal Complex and Organometallic Syntheses, vol. 28, , p. 70-76 (DOI 10.1002/9780470132593.ch16, lire en ligne).
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- Dixon, N. E. ; Lawrance, G. A. ; Lay, P. A. ; Sargeson, A. M. et Taube, H., Trifluoromethanesulfonates and trifluoromethanesulfonato-O complexes, Inorganic Syntheses, 1990, vol. 28, p. 70-6.
- Fiche de sécurité Fischer et Sigma Aldrich




