N,N-Diméthylformamide
| N,N-Diméthylformamide | |
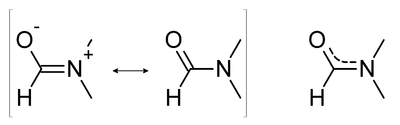
  Structure du diméthylformamide. |
|
| Identification | |
|---|---|
| Nom UICPA | N,N-Diméthylformamide |
| Synonymes |
DMF |
| No CAS | |
| No ECHA | 100.000.617 |
| No CE | 200-679-5 |
| DrugBank | DB01844 |
| PubChem | 6228 |
| ChEBI | 17741 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore à jaune, d'odeur caractéristique[1] |
| Propriétés chimiques | |
| Formule | C3H7NO [Isomères] |
| Masse molaire[3] | 73,093 8 ± 0,003 4 g/mol C 49,3 %, H 9,65 %, N 19,16 %, O 21,89 %, |
| Moment dipolaire | 3,86 D (25 °C) |
| Diamètre moléculaire | 0,595 nm[2] |
| Propriétés physiques | |
| T° fusion | −61 °C[1] |
| T° ébullition | 153 °C[1] |
| Paramètre de solubilité δ | 24,8 MPa1/2 (25 °C)[4] ; 11,5 cal1/2·cm-3/2[5] |
| Miscibilité | dans l'eau : miscible[1] |
| Masse volumique | |
| T° d'auto-inflammation | 445 °C[1] |
| Point d’éclair | 58 °C (coupelle fermée)[1] |
| Limites d’explosivité dans l’air | 2,2–15,2 %vol[7] |
| Pression de vapeur saturante | 3,77 mbar à 20 °C 6,5 mbar à 30 °C 23 mbar à 50 °C 45 mbar à 65 °C[7] |
| Viscosité dynamique | 0,92 mPa s à 20 °C |
| Thermochimie | |
| ΔfH0liquide | −239,4 kJ mol−1[8] |
| ΔfusH° | 8,950 kJ mol−1 à −60,3 °C[8] |
| ΔvapH° | 47,75 kJ mol−1 à 25 °C[8] |
| Cp | 146,05 J K−1 mol−1 à 25 °C[8]
|
| PCI | −1 941,6 kJ mol−1[8] |
| Propriétés électroniques | |
| Bande interdite | |
| Constante dielectrique | 36,70 |
| Précautions | |
| SGH[11] | |
| H312, H319, H332 et H360D |
|
| NFPA 704 | |
| Transport[7] | |
| Classification du CIRC | |
| Groupe 2A : Cancérogène probable pour l'Homme[10] | |
| Écotoxicologie | |
| LogP | −1,01[7] |
| Seuil de l’odorat | bas : 0,47 ppm haut : 100 ppm[12] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le N,N-diméthylformamide ou DMF est un solvant courant en chimie organique de formule HCO-N(CH3)2
Ce liquide incolore est miscible à l'eau et à la majorité des liquides organiques. C'est un solvant aprotique polaire à haut point de fusion/ébullition utilisé couramment pour les réactions chimiques. Le DMF est un amide dérivé de l'acide formique et de la diméthylamine. Il facilite les réactions de SN2 notamment.
Il peut être synthétisé à partir de l'acide formique et de la diméthylamine. Il n'est pas stable en présence de base forte comme la soude (hydroxyde de sodium) ou d'acide fort comme l'acide sulfurique, ou encore l'acide chlorhydrique. À haute température, il se décompose en acide formique et diméthylamine. Le DMF pur est inodore tandis qu'il acquiert souvent une odeur de poisson lors de sa dégradation, en raison de la présence de diméthylamine.
Structure et propriétés[modifier | modifier le code]
Du fait de la contribution de deux formes de résonance possibles, l'indice de liaison de la liaison carbonyle C=O est diminuée, tandis que celui de la liaison carbone-azote est augmenté. Ainsi, le spectre infrarouge du DMF laisse apparaître une bande plus basse (de fréquence 1 675 cm−1[13]) que celle d'un groupe carbonyle (C=O) non substitué. Aussi, à cause du caractère partiellement double de la liaison C-N, la rotation autour de son axe est gênée, et lente. Les deux méthyles ne sont donc pas équivalents en spectroscopie RMN (faisant apparaître deux singulets de trois protons, au lieu d'un seul singulet de six protons).
Applications[modifier | modifier le code]
On utilise tout d'abord le DMF en tant que solvant, en raison de son haut point d'ébullition. Il est aussi utilisé dans la production de fibres acryliques et de plastiques. On l'utilise également afin de coupler des peptides dans l'industrie pharmaceutique, dans la production de pesticides, colles, cuirs synthétiques, fibres, films, et revêtements[14].
Le DMF est un réactif pour la synthèse des aldéhydes de Bouveault, ainsi que dans la réaction de Vilsmeier-Haack, une des méthodes les plus employées dans la formation d'aldéhydes aromatiques. Le DMF pénètre beaucoup de matières plastiques et les fait gonfler. Il est donc fréquemment utilisé comme composant des dissolvants de peintures.
Production[modifier | modifier le code]
Il est produit par la réaction de la diméthylamine et du monoxyde de carbone à basses pression et température en conditions catalytiques[réf. nécessaire].
Précautions[modifier | modifier le code]
La réaction entre l'hydrure de sodium et le DMF est quelque peu dangereuse[réf. nécessaire] ; dès 26 °C, on observe une décomposition exothermique. En laboratoire, tout dégagement de chaleur est (en principe) rapidement compensé et mis sous contrôle par un bain de glace et ceci reste une combinaison de réactifs courante. On a recensé plusieurs accidents.
Toxicité[modifier | modifier le code]
Le DMF a été corrélé au cancer chez l'humain[réf. nécessaire], et on le suppose à l'origine de défauts de naissance. Dans certains secteurs de l'industrie, les femmes sont écartées de l'utilisation du DMF. Pour beaucoup de réactions, il peut être remplacé par le DMSO (diméthylsulfoxyde), le DMAC (diméthylacétamide) ou la NMP (N-méthyl-2-pyrrolidone). Attention cependant : la NMP a récemment été classée reprotoxique par l'European Chemicals Bureau (en)[15]. D'après le Centre international de recherche sur le cancer (International Agency for Research on Cancer, IARC), le DMF pourrait être une substance cancérigène, bien que l'agence de protection de l'environnement ne le considère pas comme un risque de cancer.
Codes de classement[modifier | modifier le code]
- ICSC : 0457 04
- PGCH : 0226
Notes et références[modifier | modifier le code]
- N, N - DIMETHYLFORMAMIDE, Fiches internationales de sécurité chimique .
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, Angleterre, John Wiley & Sons, , 239 p. (ISBN 0-471-98369-1).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Christian Reichardt, Solvents and Solvent Effects in Organic Chemistry, Wiley-VCH, , 3e éd., 629 p. (ISBN 3-527-30618-8), p. 66.
- (en) Șerban Moldoveanu, Sample preparation in chromatography, Amsterdam/Boston, Elsevier, , 930 p. (ISBN 0-444-50394-3), p. 258.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50.
- Entrée « Dimethyl formamide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 1 octobre 2009 (JavaScript nécessaire).
- (en) « Formamide, N,N-dimethyl- », sur NIST/WebBook (consulté le ).
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 1, Huston, Texas, Gulf Pub., , 396 p. (ISBN 0-88415-857-8).
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Évaluations Globales de la Cancérogénicité pour l'Homme, Groupe 2A : Cancérogène probable pour l'Homme », sur monographs.iarc.fr, CIRC, (consulté le ).
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008).
- « Dimethylformamide », sur hazmap.nlm.nih.gov (consulté le ).
- Spectral Database for Organic Compounds, « Dimethylformamide »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) (consulté le ).
- Redlich, C ; Beckett, W. S. ; Sparer, J. ; Barwick, K. W. ; Riely, C. A. ; Miller, H. ; Sigal, S. L. ; Shalat, S. L. et Cullen, M. R. (1988), Liver disease associated with occupational exposure to the solvent dimethylformamide, Ann. Intern. Med., 108:680-686, .
- http://ecb.jrc.ec.europa.eu/esis/ Taper le numéro CAS 872-50-4 dans le champ de recherche.
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- (en) Dimethylformamide usage on Organic Syntheses
- (en) Concise International Chemical Assessment Document 31: N,N-Dimethylformamide
- (en) Material Safety Data Sheet for DMF
- (en) DMF Chronic Toxicity Summary [PDF]
- INRS, Fiche













