Céramique technique


La céramique technique est une branche de la science des matériaux traitant de la science et de la technologie de matériaux minéraux non métalliques ayant des applications industrielles ou militaires. Elle se distingue radicalement des créations artisanales (poterie) ou artistiques (céramique d'art) ainsi que des porcelaines à usage domestique. Cette discipline traite notamment de la recherche et du développement de céramiques présentant les propriétés physiques particulières, ce qui recouvre la purification de la matière première, l'étude et la production des composés chimiques nécessaires à la production du matériau fini, leur formation dans les constituants, et l'étude de leur structure, de leur composition et de leurs propriétés physiques et chimiques. Ces matériaux sont par exemple des oxydes, comme l'alumine Al2O3 et le dioxyde de zirconium ZrO2, des non-oxydes, qui sont souvent des céramiques ultraréfractaires (borures, carbures et nitrures de métaux réfractaires, céramiques renforcées de silicium voire de magnésium), ou encore des céramiques composites, qui sont des combinaisons des deux précédents.
Une céramique technique peut être entièrement cristalline ou partiellement cristallisée, avec une organisation à grande échelle au niveau atomique ; les céramiques vitreuses peuvent également avoir une structure amorphe dépourvue d'organisation à l'échelle atomique, ou avoir un degré d'organisation limité. L'ASTM définit une céramique comme « une pièce ayant un corps vitrifié ou non, de structure cristalline ou partiellement cristalline, ou en verre, dont le corps est formé de substances essentiellement minérales et non métalliques, et qui est formé par une masse en fusion qui se solidifie en se refroidissant, ou qui est formé et porté à maturité, en même temps ou ultérieurement, par l'action de la chaleur »[1] ; on peut également ajouter un mode d'obtention à basse température par précipitation de solutions chimiques hautement purifiées, comme la synthèse hydrothermale (en), ou par polymérisation, comme le procédé sol-gel.
Les propriétés particulières recherchées pour les céramiques techniques peuvent être par exemple de nature mécanique, électrique, magnétique, optique, piézoélectrique, ferroélectrique ou supraconductrice, ce qui rend compte de la très grande variété d'applications de ce type de matériaux, que ce soit en génie des matériaux, en génie électrique, en génie chimique et en génie mécanique. Les céramiques étant thermostables, elles peuvent remplir des fonctions auxquelles les polymères et les métaux sont impropres. C'est la raison pour laquelle on les retrouve dans des domaines aussi variés que l'industrie minière, l'industrie aérospatiale, la médecine, l'industrie agroalimentaire, l'industrie chimique, l'industrie des semiconducteurs, l'industrie nucléaire, le transport de l'électricité et les guides d'ondes électromagnétiques[2].
Généralités[modifier | modifier le code]
Les céramiques demeurent solides à température élevée, résistent bien aux chocs thermiques (comme les « tuiles » de la navette spatiale américaine) ainsi qu'au vieillissement et aux agressions climatiques ou chimiques. Les objets en céramique possèdent généralement une bonne résistance mécanique, une faible masse volumique, une dureté élevée et une bonne résistance à l'usure. Des imperfections dans le matériau, comme des fissures résultant d'un frittage incomplet, peuvent toutefois altérer ces propriétés. Leur utilisation est sans danger pour l'homme, et nombreuses sont celles qui sont biocompatibles, comme l'hydroxyapatite Ca5(PO4)3(OH) ; elles sont ainsi utilisées comme équipements sanitaires, médicaux ou alimentaires.
Les céramiques ont généralement une faible conductivité thermique. Elles sont généralement opaques ou translucides (verres amorphes), mais peuvent aussi être transparentes, comme l'alumine Al2O3, le nitrure d'aluminium AlN, l'oxyde d'yttrium(III) Y2O3 et le YAG Y3Al5O12, par exemple pour jumelles de vision nocturne ou systèmes de guidage de missile par infrarouge. Ce sont d'excellents isolants électriques et elles sont utilisées par exemple comme isolateurs pour circuits électriques ou lignes à haute tension. Dans certaines conditions, notamment des températures cryogéniques (quelques dizaines de kelvins), certaines céramiques deviennent supraconductrices.
Dans les céramiques, les liaisons entre atomes ont un caractère iono-covalent. Les liaisons ioniques ne sont pas directionnelles, elles tendent à maximiser les attractions coulombiennes et minimiser les répulsions isocharges, ce qui conduit à des arrangements d'anions et de cations compacts ; les liaisons covalentes sont directionnelles et conduisent quant à elles à des arrangements atomiques plus étendus. Le caractère plutôt ionique ou plutôt covalent d'une liaison chimique dépend de la différence d'électronégativité des atomes formant la céramique : d'une manière générale, une différence d'électronégativité élevée favorise les liaisons ioniques tandis qu'une différence faible favorise les liaisons covalentes ; ainsi, le fluorure de calcium CaF2 est essentiellement ionique tandis que le carbure de silicium SiC est essentiellement covalent, le dioxyde de silicium SiO2 étant intermédiaire.
Synthèse[modifier | modifier le code]
Les deux grands types de synthèse des matériaux céramiques sont dits par voie sèche et par voie humide, selon les conditions expérimentales et la mise en forme souhaitée.
Par voie sèche[modifier | modifier le code]
On applique un traitement thermique approprié, typiquement autour de 1 200 °C, à un mélange de précurseurs solides en poudre afin d'obtenir le matériau céramique souhaité. Il s'agit d'une réaction en phase solide à haute température employée surtout pour l'obtention de pièces massives, c'est-à-dire d'au moins 1 mm d'épaisseur. Les poudres sont finement broyées et portées à une température élevée mais inférieure à leur point de fusion de sorte que la réaction chimique se déroule au niveau des surfaces de contact entre les grains. Ce sont par exemple les réactions :
Par ailleurs, les techniques d'ablation laser permettent la réalisation de couches minces de l'ordre du nanomètre.
Par voie humide[modifier | modifier le code]
Coprécipitation en solution[modifier | modifier le code]
Ce type de procédé est plus rapide et requiert des températures moins élevées que la voie sèche. Il permet de mieux contrôler la texture des poudres formées et peut être utilisé pour réaliser des couches minces de l'ordre du micromètre. Il consiste notamment en la précipitation simultanée en phase aqueuse de sels métalliques sous l'action d'une base forte, donnant des hydroxydes hydratés M1M2(OH)x·zH2O, ou sous l'action de l'acide oxalique HOOC–COOH, donnant des oxalates hydratés M1M2(C2O4)x·zH2O, l'eau de ces composés étant ensuite éliminée par chauffage. Dans la voie des hydroxydes métalliques obtenus sous l'action d'une base forte, il est important de se placer à un pH auquel ces hydroxydes coexistent, dans le cas présent à un pH de l'ordre de 9 à 10, afin qu'il y ait bien coprécipitation.
Par exemple, le ferrite de cobalt CoFe2O4 peut être obtenu en faisant coprécipiter des chlorures métalliques sous l'action de l'hydroxyde de sodium NaOH puis en chauffant les hydroxydes obtenus à environ 700 °C :
- CoCl2 + 2 FeCl3·6H2O + 6 NaOH ⟶ Co(OH)2↓ + 2 Fe(OH)3↓ + 6 NaCl + 6 H2O ;
- Co(OH)2 + 2 Fe(OH)3 ⟶ CoFe2O4 + 4 H2O↑ à 700 °C.
Le ferrite spinelle mixte Ni0,5Zn0,5Fe2O4 peut être obtenu de manière semblable :
- 0,5 NiCl2·6H2O + 0,5 ZnCl2 + 2 FeCl3·6H2O + 8 NaOH ⟶ 0,5 Ni(OH)2↓ + 0,5 Zn(OH)2↓ + 2 Fe(OH)3↓ + 8 NaCl + 12 H2O ;
- 0,5 Ni(OH)2 + 0,5 Zn(OH)2 + 2 Fe(OH)3 ⟶ Ni0,5Zn0,5Fe2O4 + 4 H2O↑ à 700 °C.
A contrario, le titanate de baryum BaTiO3 peut être obtenu en faisant coprécipiter des chlorures métalliques sous l'action de l'acide oxalique, écrit H2(C2O4) par commodité ci-dessous :
- TiCl3 + BaCl2·2H2O + 3 H2O + 2 H2(C2O4) ⟶ BaTiO(C2O4)2·4H2O↓ + 6 HCl ;
- BaTiO(C2O4)2·4H2O ⟶ BaTiO3 + 2 CO2↑ + 2 CO↑ à 700 °C.
Procédé sol-gel[modifier | modifier le code]
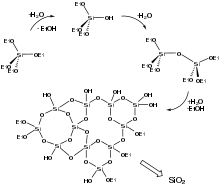
Le procédé sol-gel permet de fabriquer un polymère inorganique par des réactions chimiques simples et à une température relativement proche de la température ambiante, c'est-à-dire entre 20 et 150 °C. La synthèse s'effectue à partir d'alcoolates de formule M(OR)n, où M est un métal ou un atome de silicium, et R un groupe organique alkyle CnH2n+1, par exemple l'orthosilicate de tétraéthyle Si(OCH2CH3)4 (TEOS). L'un des intérêts de ce procédé est que ces précurseurs existent pour un grand nombre de métaux et de métalloïdes. Ils sont soit liquides soit solides, auquel cas ils sont, pour la plupart, solubles dans les solvants usuels. Il est donc possible de préparer des mélanges homogènes de monomères (précurseurs) ou d'oligomères. Les réactions chimiques simples à la base du procédé sont déclenchées lorsque les précurseurs sont mis en présence d'eau : l'hydrolyse des groupes alcoolate intervient en premier, puis la condensation des produits hydrolysés conduit à la gélification du système. Ceci peut être illustré par les réactions de production du dioxyde de silicium SiO2 à partir d'alcoolates de type Si(OR)4, amorcées par leur hydrolyse donnant un intermédiaire hydroxylé HOSi(OR)3 à partir duquel se propage la réaction de polymérisation formant une série de liaison siloxane Si–O–Si avec libération d'eau H2O et d'alcools ROH :
- Si(OR)4 + H2O ⟶ HOSi(OR)3 + ROH.
- (OR)3SiOH + HOSi(OR)3 ⟶ (OR)3Si–O–Si(OR)3 + H2O ;
- (OR)3SiOR + HOSi(OR)3 ⟶ (OR)3Si–O–Si(OR)3 + ROH.
L'hydrolyse complète des précurseurs peut être obtenue généralement à travers un excès d'eau ou l'utilisation de catalyseurs d'hydrolyse comme l'acide acétique CH3COOH ou l'acide chlorhydrique HCl. La formation d'intermédiaires tels que (OR)2Si(OH)2 ou (OR)3SiOH peut conduire à des hydrolyses partielles. Le procédé sol-gel permet de mettre le matériau final sous diverses formes, parmi lesquelles les monolithes, matériaux massifs de quelques millimètres cubes à quelques dizaines de centimètres cubes, et les couches minces, de quelques nanomètres à quelques dizaines de micromètres d'épaisseur.
Mise en forme[modifier | modifier le code]
À partir d'une poudre céramique[modifier | modifier le code]
- Frittage — Le frittage est un processus physique reposant sur la diffusion de la matière à travers les surfaces de contact entre grains de céramique pour aboutir à faire fusionner ces grains et obtenir une pièce solide formée d'un matériau céramique compact. Dans la mesure où ce procédé de mise en forme ne nécessite pas d'atteindre le point de fusion du matériau, il peut être employé en métallurgie des poudres pour traiter des métaux particulièrement réfractaires comme le tungstène, le rhénium, l'osmium, le tantale, ainsi que des céramiques ultraréfractaires comme les carbures d'hafnium, de tantale, de niobium ou de zirconium, dont le point de fusion dépasse les 2 000 °C, de sorte qu'ils ne peuvent être traités par coulage, extrusion ou moulage par injection de matière fondue, et dont la résistance aux déformations plastiques rend le forgeage et le laminage peu praticables.
- Pour un frittage donnant une céramique de bonne qualité, les poudres doivent préalablement être broyées le plus finement possibles afin d'en améliorer la granulométrie et d'homogénéité. Elles sont ensuite mises en forme par pressage, extrusion, injection, coulage ou d'autres techniques de façonnage dépendant de la forme désirée, du degré d'humidité des poudres, ou encore de la nature du matériau. Le traitement thermique peut dans un premier temps conduire au déliantage, à la décarbonatation et à la déshydratation des poudres, puis assure la diffusion du matériau responsable du processus de frittage et de la consolidation de la céramique. La finition peut faire intervenir des étapes d'usinage, de polissage ou de revêtement de la pièce obtenue.
- Pressage — Dans le pressage uniaxial, la poudre est compactée dans une matrice rigide à l'aide d'un poinçon. Le moule de pressage est métallique et les parties en contact avec la poudre peuvent être traitées pour résister à l'abrasion et à la corrosion. Cette technique conduit à la réalisation de pièces de forme simple, comme des joints ou des bagues de roulement mécanique. Dans le pressage isostatique, la poudre est compactée dans un contenant flexible maintenu par un moule support rigide. L'application de la pression se fait par l'intermédiaire d'un fluide à base d'huile et d'eau. Cette technique conduit à la réalisation de pièces de forme complexe, comme des tubes ou des bougies d'allumage.
- Le frittage de céramiques techniques peut faire également appel à des techniques de pressage à chaud, voire de pressage isostatique à chaud.
Avec un liant polymère[modifier | modifier le code]

Le mélange polymère-céramique permet de mettre en forme une poudre céramique, ce qui permet l'obtention d'une pièce composite. Il est nécessaire de faire une étape de frittage à postériori de ces méthodes pour obtenir une pièce en céramique seule.
- Extrusion — Le mélange préalablement plastifié et désaéré, est poussé à travers une filière de géométrie donnée à l'aide d'une vis. Après extrusion, les pièces sont coupées à la longueur désirée, puis subissent les traitements appropriés. Cette technique conduit à la réalisation de pièces aux formes complexes et de grandes dimensions, comme des tubes ou des tuyaux.
- Fabrication additive — Diverses techniques de fabrication additive peuvent être utilisées pour former des composants en céramique, mais la nature réfractaire des céramiques empêche l'utilisation des technologies à rayon (SLS, EBM). Cependant les procédés de fabrication additive par extrusion(FFF), similaires au procédé d'extrusion, permettent de créer une pièce en déplaçant la buse d'extrusion pour faire du volume[3]. Projeter une poudre céramique sur une résine photosensible ou inversement est aussi une technique adaptée aux céramiques (Binder Jetting ou Material Jetting)[4].
- Moulage par injection de poudre — Le mélange fluidifié est introduit dans un moule ayant la forme de la pièce à fabriquer. Le mélange thermofusible est chauffé dans une enceinte puis forcé à travers une buse dans le moule dont la température est inférieure au point de fusion du mélange. Après solidification, par abaissement de la température, la pièce est éjectée du moule. Cette technique conduit à la réalisation de pièces de formes simples ou complexes en série dont l'épaisseur maximale est de 1 cm.
Avec un liant liquide[modifier | modifier le code]
- Coulage — Dans le coulage en moule poreux, le mélange est versé dans un moule ayant la forme de la pièce à fabriquer. La pièce est laissée se solidifier. Cette technique conduit à la réalisation de pièces volumineuses. Dans le coulage sous pression, une pression est appliquée à la suspension de coulage dans un moule poreux. Le gradient de pression force le fluide à travers le moule poreux et à travers la couche en formation, ce qui permet de diminuer le temps de prise de la suspension par rapport au coulage classique. Cette technique, particulièrement utilisée dans le domaine des céramiques traditionnelles conduit à la réalisation de pièces volumineuses. La productivité peut être élevée.
Par enduction[modifier | modifier le code]


L'enduction se fait notamment à partir d'une pâte liquide issue du procédé sol-gel.
- Enduction par trempage — Dite dip coating en anglais, c'est une technique de mise en forme de couches minces qui consiste à immerger le substrat de la pièce dans une cuve contenant la céramique en pâte liquide, extraire la pièce de la cuve et laisser s'écouler la couche. La pièce enrobée est ensuite séchée. Ce processus se déroule donc généralement en trois étapes :
- immersion : le substrat est immergé dans la solution, contenant le matériau à mettre en forme, à une vitesse constante et préférablement sans secousses ;
- temps de séjour : le substrat est laissé complètement immergé et immobile pour permettre au matériau de bien s'y appliquer et l'enrober ;
- extraction : le substrat est extrait, de nouveau à vitesse constante et sans secousses. La vitesse d'extraction influe sur l'épaisseur de la couche : l'épaisseur de la couche est d'autant plus fine que la vitesse d'extraction du substrat est grande, mais elle dépend aussi de la concentration de soluté et du solvant.
- Enduction centrifuge — Dite spin coating en anglais, c'est une technique de mise en forme de couches minces qui consiste à poser un excès de matériau en solution, à mettre en forme sur le substrat — généralement un wafer de semiconducteur — et à faire tourner le tout à vitesse élevée pour étaler le fluide sur toute la surface par centrifugation. La rotation continue pendant que le fluide dépasse les bords du substrat, jusqu'à ce que la couche ait l'épaisseur voulue. Par conséquent, la couche est d'autant plus fine que la vitesse de rotation est élevée, mais elle dépend aussi de la concentration de soluté et du solvant.
Oxydes technologiques[modifier | modifier le code]
Les oxydes technologiques sont composés majoritairement d'éléments métalliques et d'oxygène, comme l'alumine Al2O3, l'oxyde de fer(III) Fe2O3, les spinelles MgAl2O4 et CoFe2O4, le titanate de baryum BaTiO3, le dioxyde de titane TiO2, etc.
À propriétés magnétiques[modifier | modifier le code]

Ce sont des oxydes technologiques présentant des propriétés magnétiques ou ferromagnétiques. La première céramique magnétique à avoir été découverte est l'oxyde de fer(II,III) Fe3O4, ou magnétite.
La structure la plus commune des oxydes technologiques à propriétés magnétiques est la structure spinelle où les anions forment un empilement compact de géométrie cubique à faces centrées ou hexagonal compact et les cations se placent dans les lacunes tétraédriques ou octaédriques selon leur taille. Elle est de la forme A(B)2O4 avec en rouge les métaux occupant les sites tétraédriques et en vert ceux octaédriques. Il existe deux types de structures spinelles :
- Spinelle directe : A2+(B3+)2O4. Exemple : MgAl2O4, Mg2+(Al3+)2O4.
- Spinelle inverse : A3+(B2+A3+)O4. Exemple : CoFe2O4, Fe3+(Co2+Fe3+)O4.

Le magnétisme de ces matériaux a pour origine le moment magnétique porté par les atomes, qui a deux composantes : le moment magnétique de spin et le moment cinétique orbital.
Chaque cation métallique porte un moment magnétique dû au spin de ses électrons de valence. Par exemple, le fer ferrique Fe3+ est un métal de type d5 et à haut spin, ce qui fait que son moment magnétique vaut de l'ordre de 5µB, où µB est le magnéton de Bohr. Or à cet effet s'ajoute l'effet du superéchange qui résulte du couplage antiferromagnétique induit par l'oxygène entre les cations dans les lacunes tétraédriques et ceux dans les lacunes octaédriques. Ce couplage est antiferromagnétique parce que l'oxygène implique que les spins de ces deux types de cations soient opposés. Mais la valeur absolue des deux moments magnétiques cationiques n'étant pas identique, le moment magnétique résultant n'est pas nul, par conséquent le matériau est magnétique.
Dans le cas de la magnétite Fe3O4, la structure est de type spinelle inverse Fe3+(Fe2+Fe3+)O4. Le moment magnétique du fer ferrique Fe3+ vaut 5µB, tandis que celui du fer ferreux Fe2+ vaut 4µB. En raison du superéchange, le moment magnétique total vaut (5 + 4 – 5) µB = 4 µB, car les moments magnétiques des deux types de cations sont opposés.
Les applications des oxydes technologiques à propriétés magnétiques dépendent en particulier de leur mise en forme, comme l'enregistrement magnétique (bandes magnétiques) ou le stockage d'information (disques durs, CD).
À propriétés piézoélectriques[modifier | modifier le code]

Les oxydes technologiques présentant des propriétés piézoélectriques ont la caractéristique de se polariser électriquement sous l’action d’une contrainte mécanique, et réciproquement de se déformer lorsqu’on leur applique un champ électrique. On parle d'effet direct et d'effet inverse, les deux étant indissociables : l'effet piézoélectrique direct induit une tension électrique sous l'effet d'une action mécanique, tandis que l'effet piézoélectrique inverse induit une action mécanique sous l'effet d'une tension électrique. Un cristal piézoélectrique est ferroélectrique s'il garde sa polarisation électrique après application d'un champ électrique. Très peu de matériaux sont ferroélectriques. Sans déformation, la structure pérovskite ne possède pas de moment dipolaire électrique car les anions et les cations sont disposés de manière symétrique, les cations étant au centre de leurs sites ; lorsque le réseau est déformé, par pression mécanique par exemple, les cations des lacunes octaèdriques sont décentrés, ce qui induit un moment dipolaire et donc une tension électrique.
La structure la plus commune des oxydes technologiques à propriétés piézoélectriques est un réseau cristallin orthorhombique formé par des octaèdres d'anions à l'intérieur desquels est emprisonné un cation relativement petit ; huit de ces octaèdres forment un cube possédant une lacune au centre de laquelle est emprisonné un autre cation relativement grand. Ce type de structure est appelé pérovskite. Un exemple en est le titanate de baryum BaTiO3, dont la structure cristalline est illustrée ci-contre. Dans cette illustration d'une pérovskite à haute température, la taille des ions n'est pas respectées afin de pourvoir visualiser clairement le polyèdre de coordination du titane. Le rayon de l'anion oxygène O2− est en réalité le plus grand.
Les oxydes technologiques piézoélectriques sont utilisés dans des capteurs (de pression, de température, microphones, microbalances, etc.) dans des actionneurs ou moteurs (microscope à force atomique, microscope à effet tunnel, optique adaptative en astronomie, autofocus des appareils photographiques, têtes d'écriture des imprimantes à jet d'encre, etc.).
Les oxydes technologiques ferroélectriques sont utilisés pour le stockage de l'information.
À propriétés électriques[modifier | modifier le code]
Les oxydes technologiques diélectriques sont utilisés comme isolants électriques, par exemple comme isolateurs de lignes à haute tension.
À propriétés optiques[modifier | modifier le code]
Les photocatalyseurs, par exemple, sont utilisés pour la catalyse en dépollution, comme le dioxyde de titane TiO2, qui peut ainsi être déposée sur les bâtiments vitrés pour en prévenir les salissures grâce à ses propriétés oxydantes, ou sur un miroir pour éviter la formation de buée car il a un très bon mouillage avec l'eau.
Les cristaux photoniques permettent par exemple de réaliser des colorations structurelles, des composants d'optique intégrée (utilisant par exemple du niobate de lithium LiNbO3) ou des fibres à cristaux photoniques, par exemple en verre de quartz (dioxyde de silicium SiO2).
Méthodes de caractérisation[modifier | modifier le code]
Les méthodes de caractérisation des céramiques, de la poudre initiale au produit fritté, sont nombreuses : techniques d'analyse de surface (RX, MEB, MET, MFA, etc.), mesure de la granulométrie, de la surface spécifique, de la densité (masse volumique), de la porosité, de la résistance mécanique, des paramètres rhéologiques et du comportement thermique.
- Diffractométrie de rayons X — C'est une technique d'analyse fondée sur la diffraction des rayons X sur la matière. Elle permet, dans le cas des céramiques, de savoir si on a obtenu la phase désirée et si la réaction a bien eu lieu.
- Microscopie électronique à balayage — La MEB est une technique de microscopie électronique fondée sur le principe des interactions électrons-matière. Elle permet, dans le cas des céramiques, de connaître la morphologie de la surface et de savoir si le frittage a eu lieu. Elle permet de voir par ailleurs que le frittage n'est jamais complet et qu'il reste toujours des microfissures appelées porosité résiduelle entre les plaques consolidées, ce qui rend les objets faits par voie céramique conventionnelle, cassants.
- Microscopie électronique en transmission — La MET est une technique de microscopie où un faisceau d'électrons est « transmis » à travers un échantillon très mince, elle est donc particulièrement indiquée pour l'analyse des céramiques en couches très minces issues de l'ablation laser par exemple.
- Microscopie à force atomique — La MFA est une technique de microscopie à champ proche, une sonde scanne la surface et est attirée ou repoussée selon la charge de la surface. Elle est donc particulièrement appropriée pour analyser les couches minces des oxydes à propriétés magnétiques.
Applications[modifier | modifier le code]
Les céramiques techniques tendent à remplacer les métaux dans un nombre croissant d'applications. Leur faiblesse majeure réside dans leur fragilité, liée à leur raideur, là où les métaux présentent une bonne résistance à la rupture en raison de leur ductilité. Elles tendent en revanche à réduire les contraintes locales accumulées sous l'effet de déformations élastiques et plastiques. Le développement de matériaux composites à fibres de céramiques a permis de réaliser des progrès significatifs en ce domaine et d'élargir sensiblement la gamme des applications des céramiques techniques.
On trouve des céramiques dans les roulements mécaniques et les joints d'étanchéité, comme des coques de paliers pour les turbines à gaz fonctionnant à plusieurs milliers de tours par minute et plus de 1 500 °C. Des garnitures mécaniques en céramique scellent les ouvertures permettant à des arbres à travers les pompes pour les protéger des agents corrosifs et abrasifs de l'environnement extérieur. C'est par exemple le cas dans les systèmes de désulfuration des fumées industrielles, où les paliers lisses en céramique des pompes sont exposés à du lait de chaux basique très concentré fortement chargé en sable. On retrouve des conditions semblables dans les systèmes de pompage pour le dessalement de l'eau de mer, dans lesquels des paliers lisses en céramique peuvent traiter de l'eau salée chargée de sable pendant plusieurs années sans être altérés par l'abrasion ni la corrosion.
La plupart des matériaux céramiques sont des isolants électriques, mais certains sont supraconducteurs, semiconducteurs ou sont utilisés comme éléments chauffants. Les céramiques semiconductrices sont utilisées pour les varistances (oxyde de zinc ZnO), les sondes thermiques, les démarreurs, la démagnétisation, les fusibles réarmables PTC.
Les céramiques sont généralement connues comme isolants, comme dans les bougies d'allumage et les isolateurs pour lignes à haute tension). Elles supportent des températures de 600 °C, par exemple dans le cas des bougies d'allumage ou des dispositifs d'allumage pour brûleurs à gaz. L'alumine Al2O3 des bougies d'allumage a une résistivité de 108 Ω cm à 600 °C. Les applications à chaud sont parmi les plus importantes des céramiques, notamment dans les poêles, les brûleurs et les éléments chauffants. Les céramiques ultraréfractaires peuvent fonctionner jusqu'à 2 500 °C sans déformation ni fatigue. La faible conductivité thermique et la très grande thermostabilité de ces matériaux, comme le diborure de zirconium ZrB2 et le diborure d'hafnium HfB2, font qu'ils sont utilisés comme isolants thermiques ou matériaux réfractaires, par exemple pour les tuiles des boucliers thermiques destinés à protéger les véhicules spatiaux et les missiles balistiques lors de leur rentrée atmosphérique, ou encore sur les bords d'attaque des aéronefs et des armes en vol hypersonique (en), voire pour recouvrir la structure métallique des aubes de turbines.
Avec les recherches sur les moteurs à combustion interne fonctionnant à des températures de plus en plus élevées, la demande en aubes de turbocompresseurs, pièces de moteurs et paliers en matériaux céramiques augmente significativement. Dès les années 1980, Toyota avait développé un moteur en céramique pouvant fonctionner à des températures élevées sans refroidissement, d'où un important gain de rendement et de poids par rapport aux moteurs à combustion interne classiques ; livré dans certaines motorisations de la 7e génération S120 de la Toyota Crown, il ne fut pas produit en grande série du fait de nombreuses difficultés industrielles, notamment du haut degré de pureté nécessaire.
L'utilisation des céramiques la plus importante en volume est sous forme de condensateurs céramiques (en). En raison de leur rigidité diélectrique élevée, les condensateurs de puissance (de) en céramique sont essentiels aux émetteurs d'ondes radioélectriques. Les propriétés optiques de certaines céramiques permettent leur utilisation dans les lampes à vapeur métallique (lampe à sodium, lampes à mercure), dans des diodes laser, ainsi que dans des détecteurs infrarouge. Leur inertie chimique et leur biocompatibilité en font des candidats valables pour les prothèses de la hanche et les prothèses dentaires. Les propriétés des céramiques peuvent également être utilisées pour réduire les frottements entre pièces mécaniques (roulements à billes céramiques par exemple) ou encore détecter des gaz, de l'humidité, agir comme catalyseur ou réaliser des électrodes. Des poudres céramiques à base de nitrure de titane TiN, par exemple, peuvent être utilisées comme lubrifiant solide.
Exemples de céramiques techniques[modifier | modifier le code]
Oxydes[modifier | modifier le code]
| Matériau | Formule chimique | Propriétés notables | Exemples d'applications |
|---|---|---|---|
| Alumine | Al2O3 | Bonne tenue mécanique aux températures élevées, bonne conductivité thermique, grande résistivité électrique, grande dureté, bonne résistance à l'usure, inertie chimique. | Isolateurs électriques, supports d'éléments chauffants, protections thermiques, éléments de broyage, composants mécaniques, bagues d'étanchéité, prothèses dentaires. |
| Sialon | Si12–m–nAlm+nOnN16–n Si6–nAlnOnN8–n Si2–nAlnO1+nN2–n |
Solution solide de nitrure de silicium Si3N4, de nitrure d'aluminium AlN et d'oxyde d'aluminium Al2O3. | |
| Cordiérite (silicate alumineux ferro-magnésien) | Mg2Al3AlSi5O18 | Bonne résistance aux chocs thermiques, bonne conductivité thermique. | Isolants électriques, échangeurs thermiques, éléments chauffants |
| Mullite | 3Al2O3·2SiO2 ou 2Al2O3·SiO2 | Bonne résistance aux chocs thermiques, conductivité thermique faible, résistivité électrique importante. | Produits réfractaires. |
| Dioxyde de zirconium | ZrO2 | Excellentes propriétés mécaniques aux températures élevées, conductivité thermique faible à température ambiante, conducteur électrique à T > 1 000 °C, grande dureté, bonne résistance à l'usure, bonne inertie chimique, bonne résistance aux attaques des métaux. Il existe deux types : zircone non stabilisée, utilisée en tant qu'additif, matériau de revêtement, poudre abrasive... et zircone stabilisée à l'yttrium (ZrO2/Y2O3 = TZP) ou à la magnésie (ZrO2/MgO = PSZ). | Creusets, buses de coulée, éléments chauffants, revêtement anti-thermique, conducteurs ioniques, prothèses dentaires. |
| Oxyde de zinc | ZnO | Utilisé dans les diodes pour ses propriétés électriques. Voir Varistance. | |
| Oxyde de fer(II,III) | Fe3O4 | Utilisé dans les transformateurs et le stockage magnétique des données. | |
| Pérovskites | (A)(B)O3 | Elles constituent une vaste famille de matériaux cristallins comprenant par exemple le titanate de baryum BaTiO3, le titanate de calcium CaTiO3 (pérovskite), le titanate de strontium SrTiO3, le (PbSr)TiO3 ou le Pb(Zr0,5Ti0,5)O3. | Diélectriques pour la fabrication de condensateurs multicouches, thermistances, transducteurs piézoélectriques... |
| Orthosilicate de magnésium | Mg2SiO4 | Bonne résistivité électrique. | Isolants électriques. |
| Oxyde de magnésium | MgO | Résistance aux métaux fondus, bonne résistance mécanique. | Traitement des matériaux piézoélectriques, réfractaires, composants optiques. |
| Dioxyde d'uranium | UO2 | Combustible dans les réacteurs nucléaires. |
Non-oxydes[modifier | modifier le code]
| Matériau | Formule chimique | Propriétés notables | Exemples d'applications |
|---|---|---|---|
| Nitrure de silicium | Si3N4 | Grande dureté, bonne résistance à l'usure et à l'abrasion, bonne inertie chimique, bonne résistance aux chocs thermiques. Il existe deux types de nitrure de silicium : lié par nitruration de poudre de silicium comprimée ou par pressage de la poudre de nitrure de silicium à température élevée (frittage). | Poudres abrasives, outils de coupe, réfractaire pour la sidérurgie, billes de roulement, bagues d'étanchéité pour le moulage des métaux, soupapes (automobile). |
| Carbure de bore | B4C | Blindage des tanks et des hélicoptères. | |
| Carbure de silicium | SiC | Grande dureté, bonne résistance aux chocs thermiques, grande conductivité thermique, faible dilatation thermique, excellente inertie chimique. | Réfractaires, résistances chauffantes, outils de coupe, pièces de frottement, joints d'étanchéité des pompes à eau, support de catalyseur. |
| Nitrure d'aluminium | AlN | Conductivité thermique élevée, bonne résistance électrique, transparent aux longueurs d'onde du visible et de l'infra-rouge. | Circuits imprimés, colonnes thermiques, fenêtres pour radar, creusets pour la fonderie. |
| Nitrure de bore | BN | Haute conductivité thermique, faible dilatation thermique, excellente résistance aux chocs thermiques, haute résistance diélectrique, faible constante diélectrique, inerte chimiquement, transparent aux micro-ondes, facilement usinable. | Isolants électriques à très hautes températures, creusets pour la fonderie, garnitures de fours, gaines de thermocouples, supports de résistances, lubrifiant à haute température. |
| Diborure d'aluminium | AlB2 | Matériau de renforcement dans les composites métalliques. |
Centres de formation et de recherche[modifier | modifier le code]
- École nationale supérieure de céramique industrielle de Limoges
- Lycée professionnel de la Céramique de Longchamp[7]
- Lycée Henri Brisson ex ENP de Vierzon[8]
- Lycée des Métiers Le Mas Jambost de Limoges[9]
- Centre de Transfert de Technologies Céramiques, centre de recherche appliquée[10]
- Pôle de compétitivité européen de la céramique (Limoges, Vierzon, Tarbes, Cavaillon)
Notes et références[modifier | modifier le code]
-
(en) « Ceramic article – ASTM C 242 », Ceramic Tile Institute of America (consulté le ) :
« An article having a glazed or unglazed body of crystalline or partly crystalline structure, or of glass, which body is produced from essentially inorganic, nonmetallic substances and either is formed from a molten mass which solidifies on cooling or is formed and simultaneously or subsequently matured by the action of the heat. » - (en) W. David Kingery, H. K. Bowen et Donald R. Uhlmann, Introduction to Ceramics, Wiley-Interscience, 2e éd., 1976, p. 690. (ISBN 978-0-471-47860-7)
- (en) « 3D printing of ceramics: A review », Journal of the European Ceramic Society, vol. 39, no 4, , p. 661–687 (ISSN 0955-2219, DOI 10.1016/j.jeurceramsoc.2018.11.013, lire en ligne, consulté le )
- (en) J. A. Gonzalez, J. Mireles, Y. Lin et R. B. Wicker, « Characterization of ceramic components fabricated using binder jetting additive manufacturing technology », Ceramics International, vol. 42, no 9, , p. 10559–10564 (ISSN 0272-8842, DOI 10.1016/j.ceramint.2016.03.079, lire en ligne, consulté le )
- (en) H. Sawada, « An electron density residual study of magnesium aluminum oxide spinel », Materials Research Bulletin, vol. 30, no 3, , p. 341-345 (DOI 10.1016/0025-5408(95)00010-0, lire en ligne)
- ICSD No. 43125 ; DOI Gotor F.J., Real C., Dianez M.J. & Criado J.M. ''Journal of Solid State Chemistry'' (1996) 123, 301–305
- Lycée professionnel de la Céramique.
- Lycée Henri Brisson ex ENP.
- Lycée des Métiers Le Mas Jambost.
- Centre de Transfert de Technologies Céramiques.
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
- Composite à matrice céramique
- Céramique ultraréfractaire
- Céramique
- Porcelaine
- École nationale supérieure de céramique industrielle
- Mousse céramique
Bibliographie[modifier | modifier le code]
- (en) Roger H. Mitchell, Perovskites : Modern and ancient, Thunder Bay, Almaz Press, , 318 p. (ISBN 978-0-9689411-0-2)
