Adénosine monophosphate
| Adénosine monophosphate | |
 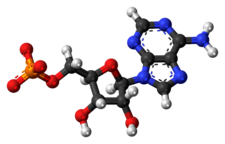 Structure de l'adénosine monophosphate. |
|
| Identification | |
|---|---|
| Nom UICPA | acide 5'-adénylique |
| Synonymes |
adenosine 5′-monophosphate |
| No CAS | |
| No ECHA | 100.000.455 |
| No CE | 200-500-0 |
| PubChem | 6083 |
| ChEBI | 16027 |
| SMILES | |
| InChI | |
| Apparence | cristal incolore, inodore[1] |
| Propriétés chimiques | |
| Formule | C10H14N5O7P [Isomères] |
| Masse molaire[2] | 347,221 2 ± 0,012 1 g/mol C 34,59 %, H 4,06 %, N 20,17 %, O 32,25 %, P 8,92 %, |
| pKa | pKa1 3,8[1] pKa2=6,2[1] |
| Propriétés physiques | |
| T° fusion | 195 °C[3] |
| Solubilité | 10 g·L-1 (eau, 20 °C)[3] |
| Précautions | |
| Directive 67/548/EEC | |
| Écotoxicologie | |
| DL50 | 4 mg·kg-1 (souris, i.p.)[4] |
| LogP | -1,680[3] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L’adénosine monophosphate (AMP), également appelée acide 5'-adénylique, est un ribonucléotide constitué de résidus d'adénine, une base nucléique, et de ribose estérifié par un groupe phosphate. Avec l'uridine monophosphate (UMP), la guanosine monophosphate (GMP) et la cytidine monophosphate (CMP), elle est l'un des monomères constituant l'ARN, où l'adénine peut se lier à l'uracile par deux liaisons hydrogène.
Production et dégradation[modifier | modifier le code]
L'AMP peut être produite lors de la synthèse de l'adénosine triphosphate (ATP) par l'enzyme adénylate kinase, par combinaison de deux molécules d'adénosine diphosphate (ADP) :
Une molécule d'AMP (adenosine monophosphate) peut aussi être produite par l'hydrolyse d'une liaison phosphate de haute énergie de l'ADP :
L'AMP peut aussi être produite par l'hydrolyse de l'ATP en AMP et pyrophosphate :
Quand l'ARN est dégradé dans les systèmes vivants, des nucléosides monophosphatés sont formés, et parmi eux l'adénosine monophosphate.
L'AMP peut être régénéré en ATP :
- AMP + ATP 2 ADP (catalysé par l'adénylate kinase)
- ADP + Pi → ATP (cette étape est plus souvent effectuée chez les aérobies par l'ATP synthase pendant la phosphorylation oxydative)
Contrairement aux autres dérivés phosphatés de l'adénosine, l'AMP ne peut se séparer d'un groupe phosphate pour la phosphorylation d'autres molécules dans la cellule; en effet, le groupe phosphate attaché au carbone 5' du ribose ne peut pas être utilisé pour la phosphorylation d'autres groupes dans la cellule, car le potentiel de transfert de groupe est trop faible (le phosphate n'a pas assez d'énergie pour réagir).
L'AMP peut être convertie en acide inosinique (IMP) par l'enzyme AMP désaminase, libérant un groupe amine.
Par voie catabolique, l'adénosine monophosphate peut être convertie en acide urique qui est alors excrété du corps.
AMPc[modifier | modifier le code]
L'AMP existe aussi sous la forme d'une structure cyclique appelée adénosine monophosphate cyclique (AMPc). Dans certaines cellules, l'enzyme adénylate cyclase fabrique l'AMPc à partir de l'ATP, réaction en général régulée par des hormones comme l'adrénaline ou le glucagon. L'AMPc joue un rôle important dans la signalisation intracellulaire.il joue le rôle de second messager.
Masqueur du goût amer[modifier | modifier le code]
L'AMP a été la première molécule identifiée à avoir la capacité de masquer le goût amer sur la langue, ce qui donne la sensation d'un goût plus « sucré ». En effet l'AMP bloquerait la protéine G responsable de la transmission du goût amer[5]. Cette propriété rend cette molécule intéressante pour d'éventuelles applications dans l'industrie-agroalimentaire. La Food and Drug Administration a par ailleurs autorisé l'AMP comme additif « Bitter Blocker » dans la nourriture[6].
Notes et références[modifier | modifier le code]
- Thieme Chemistry (Hrsg.): Römpp Online. Version 3.1. Georg Thieme Verlag, Stuttgart 2007.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Adénosine monophosphate », sur ChemIDplus
- Pharmaceutical Chemistry Journal Vol. 20, Pg. 160, 1986.
- drugresearcher.com
- Bitter Blocker Backed
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Adenosine monophosphate » (voir la liste des auteurs).

