« Fibromyalgie » : différence entre les versions
Aucun résumé des modifications |
|||
| Ligne 15 : | Ligne 15 : | ||
Dans les années 1970 et 1980, elle est considérée comme une maladie psychiatrique avec un versant dépressif. Celà a été subdoré par le fait que les douleurs résistent aux [[analgésique]]s musculaires usuels. |
Dans les années 1970 et 1980, elle est considérée comme une maladie psychiatrique avec un versant dépressif. Celà a été subdoré par le fait que les douleurs résistent aux [[analgésique]]s musculaires usuels. |
||
L'appellation « syndrome polyalgique idiopathique diffus » (SPID) a été créé par le |
L'appellation « syndrome polyalgique idiopathique diffus » (SPID) a été créé par le Professeur [[Kahn]] dans les années 1980, mais le terme anglo-saxon ''fibromyalgia'' a prévalu dans les congrès médicaux et a été francisé en « fibromyalgie ». |
||
Ce n'est qu'en [[1992]] que l'[[Organisation mondiale de la santé]] a reconnu cette maladie comme rhumatismale, alors qu'elle était auparavant considérée comme une maladie psychiatrique par les médecins, du fait de sa rareté, touchant principalement les femmes, pouvant donner une certaine atteinte comportementale et n'ayant aucune trace biologique, ce « syndrome » fut attribué à tort à l'[[hystérie]] féminine. Cette supposée cause [[psychosomatique]] est désormais abandonnée. |
Ce n'est qu'en [[1992]] que l'[[Organisation mondiale de la santé]] a reconnu cette maladie comme rhumatismale, alors qu'elle était auparavant considérée comme une maladie psychiatrique par les médecins, du fait de sa rareté, touchant principalement les femmes, pouvant donner une certaine atteinte comportementale et n'ayant aucune trace biologique, ce « syndrome » fut attribué à tort à l'[[hystérie]] féminine. Cette supposée cause [[psychosomatique]] est désormais abandonnée. |
||
En effet, dans les années 1990 et 2000, plusieurs études prouvent des déficiences en [[neurotransmetteur]]s chez les personnes atteintes de fibromyalgie. |
En effet, dans les années 1990 et 2000, plusieurs études prouvent des déficiences en [[neurotransmetteur]]s chez les personnes atteintes de fibromyalgie. Et en [[2006]], des études démontrent par l'[[Imagerie par résonance magnétique|IRM]] fonctionnel une activité anormale dans la partie du cerveau qui traite la douleur chez les fibromyalgiques, inexistante chez les personnes non atteintes. Une cause exclusivement [[psychiatrique]] et/ou [[psychologique]] est exclue. |
||
En 2006, une étude démontre par l'[[Imagerie par résonance magnétique|IRM]] fonctionnel une activité anormale dans la partie du cerveau qui traite la douleur chez les fibromyalgiques, inexistante chez les personnes non atteintes. Une cause exclusivement [[psychiatrique]] et/ou [[psychologique]] est exclue. |
|||
La fibromyalgie était codée {{nobr|M 70.0}} comme [[rhumatisme]] non spécifié dans la [[classification internationale des maladies]] (CIM). Depuis janvier 2006, elle est maintenant codée sous {{nobr|M 79.7}} sous son propre nom, indiquant qu'il s'agit d'une maladie reconnue à part entière. |
La fibromyalgie était codée {{nobr|M 70.0}} comme [[rhumatisme]] non spécifié dans la [[classification internationale des maladies]] (CIM). Depuis janvier 2006, elle est maintenant codée sous {{nobr|M 79.7}} sous son propre nom, indiquant qu'il s'agit d'une maladie reconnue à part entière. |
||
| Ligne 37 : | Ligne 35 : | ||
Au {{s-|XXI|e}}, les spécialistes préfèrent utiliser le terme multi-fibromyalgies, certains travaux de recherches biologiques faisant état de sous-catégories. |
Au {{s-|XXI|e}}, les spécialistes préfèrent utiliser le terme multi-fibromyalgies, certains travaux de recherches biologiques faisant état de sous-catégories. |
||
== |
== Diagnostic == |
||
[[Image:Tender points fibromyalgia.gif|thumb|Position des 18 points que reconnait l'[[American College of Rheumatology]] depuis 1990 comme critères pour la fibromyalgie.]] |
|||
À partir de 2000-2004, les scientifiques se penchent de plus en plus vers des désordres de natures immuno-chimiques et/ou environnementaux, compte tenu de la résurgence surprenante de cas. Une atteinte du [[système nerveux central]] et un dérèglement [[neurone|neuronal]] ont été largement constatés chez les fibromyalgiques. |
|||
La fibromyalgie est considérée parfois comme un diagnostic controversé, certains auteurs affirmant qu'il s'agit d'un non diagnostic. En effet il n'existe pas encore de test spécifique et fiable à 100% pour la validation de la fibromyalgie. La difficulté vient essentiellement du fait que des personnes atteintes peut voir l'ensemble de ses analyses en laboratoire revenir normales. et que beaucoup des symptômes se retrouvent dans d'autres maladies ([[rhumatisme]] articulaire, [[ostéoporose]], ...). Dans la plus part des cas, la conclusion du médecin est basée sur un [[diagnostic différentiel]], prenant en cause l'ensemble des autres possibilités, les symptômes, ainsi que le profil du patient. |
|||
Il semble exister une perception différente de la douleur chez le fibromyalgique, avec en particulier, un seuil de perception plus bas<ref>Abeles AM, Pillinger MH, Solitar BM, Abeles M, [http://www.annals.org/cgi/content/full/146/10/726 ''The pathophysiology of fibromyalgia''], Ann Int Med, 2007;146;726-734</ref>. Le mécanisme de ce fait est toujours débattu, mais lourdement supposé lié aux neurotransmetteurs responsables du traitement de la douleur. |
|||
Les critères de classification les plus couramment acceptés ont été élaborés en [[1990]] par le [[Collège américain de rhumatologie]][http://www.rheumatology.org/], souvent surnommés critères "ACR 1990". Ils définissent la fibromyalgie suivant la présence des points suivants : |
|||
Il est possible que les différentes variantes de fibromyalgie soient liés à une combinaise d'une ou plusieurs de ces causes suposées. |
|||
* Un historique de douleur répandue sur tout le corps, durant depuis plus de 3 mois, et affectant l'ensemble des quatre quadrants du corps (les deux côtés, et au dessous et en dessous de la ceinture). |
|||
=== Prédisposition génétique === |
|||
* Des points douloureux, au nombre de 18 (bien que le patient puisse avoir mal à d'autres endroits du corps). Durant le diagnostique, le médecin doit exercer une [[force (physique)|force]] de 39 [[Newton_(unité)|Newtons]] sur ces points. Le patient doit ressentir une douleur vive sur au moins 11 de ces points pour que la fibromyalgie puisse être confirmée<ref>{{cite web |author=National Institute of Arthritis and Musculoskeletal and Skin Diseases |titre=Questions and Answers About Fibromyalgia – How Is Fibromyalgia Diagnosed? |url=http://www.niams.nih.gov/hi/topics/fibromyalgia/fibrofs.htm#fib_d |month=June | year=2004 |publisher=National Institutes for Health}}</ref>. Il faut noter que la localisation et le nombre des points douloureux peut varier selon les périodes, les circonstances... |
|||
Outre le fait que cette maladie touche beaucoup plus de femmes que d'hommes, il existe de nombreuses preuves qu'un facteur génétique puisse jouer un rôle important dans le développement de la fibromyalgie.<ref>Yunus MB, Khan MA, Rawlings KK, Green JR, Olson JM, Shah S. Genetic linkage analysis of multicase families with fibromyalgia syndrome. J Rheumatol 1999 Feb;26(2):408-12 [http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=PubMed&list_uids=9972977&dopt=Abstract]</ref><ref>Buskila D, Neumann L Genetics of fibromyalgia. Curr Pain Headache Rep. 2005 Oct;9(5):313-5. [http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=PubMed&dopt=Abstract&list_uids=16157058]</ref><ref>Buskila D, Neumann L, Hazanov I, Carmi R. Familial aggregation in the fibromyalgia syndrome. Semin Arthritis Rheum 1996 Dec;26(3):605-11 [http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=PubMed&list_uids=8989805&dopt=Abstract]</ref> Par exemple, il existe beaucoup de familles présentants plusieurs personnes atteintes<ref>{{cite journal |author=Stormorken H |coauthors=Brosstad F |authorlink=Helge Stormorken |title=Fibromyalgia: family clustering and sensory urgency with early onset indicate genetic predisposition and thus a "true" disease |journal=Scand J Rheumatol. |volume=21 |issue=4 |pages=207 |year=1992 |pmid=1529291 |doi=10.3109/03009749209099225}}</ref><ref>{{cite journal |author=Arnold LM, Hudson JI, Hess EV, ''et al'' |title=Family study of fibromyalgia |journal=Arthritis Rheum. |volume=50 |issue=3 |pages=944–52 |year=2004 |month=March |pmid=15022338 |doi=10.1002/art.20042}}</ref> Le mode de transmission est encore inconnu mais est probablement [[polygénique]].<ref>{{cite journal |author=Buskila D, Sarzi-Puttini P |title=Biology and therapy of fibromyalgia. Genetic aspects of fibromyalgia syndrome |journal=Arthritis Res Ther. |volume=8 |issue=5 |pages=218 |year=2006 |pmid=16887010 |pmc=1779444 |doi=10.1186/ar2005}}</ref> Les recherches ont démontrés que la fibromyalgie est associée à des variation (ou [[polymorphisme]]) sur les [[gène]]s de production de la [[serotonine]],<ref>{{cite journal |author=Cohen H, Buskila D, Neumann L, Ebstein RP |title=Confirmation of an association between fibromyalgia and serotonin transporter promoter region (5- HTTLPR) polymorphism, and relationship to anxiety-related personality traits |journal=Arthritis Rheum. |volume=46 |issue=3 |pages=845–7 |year=2002 |month=March |pmid=11920428 |doi=10.1002/art.10103 }}</ref> [[dopamine]]<ref>{{cite journal |author=Buskila D, Dan B, Cohen H, ''et al'' |title=An association between fibromyalgia and the dopamine D4 receptor exon III repeat polymorphism and relationship to novelty seeking personality traits |journal=Mol. Psychiatry |volume=9 |issue=8 |pages=730–1 |year=2004 |month=August |pmid=15052273 |doi=10.1038/sj.mp.4001506 }}</ref> et [[catecholamine]].<ref>{{cite journal |author=Zubieta JK, Heitzeg MM, Smith YR, ''et al'' |title=COMT val158met genotype affects mu-opioid neurotransmitter responses to a pain stressor |journal=Science (journal) |volume=299 |issue=5610 |pages=1240–3 |year=2003 |month=February |pmid=12595695 |doi=10.1126/science.1078546 }}</ref> Cependant ces polymorphismes ne sont pas spécifiques à la fibromyalgie, et sont associés à une variétés d'autres maladies (comme le [[neurasthénie|syndrôme de fatigue chronique]],<ref>{{cite journal |author=Narita M, Nishigami N, Narita N, ''et al'' |title=Association between serotonin transporter gene polymorphism and chronic fatigue syndrome |journal=Biochem Biophys Res Commun. |volume=311 |issue=2 |pages=264–6 |year=2003 |month=November |pmid=14592408 |doi=10.1016/j.bbrc.2003.09.207 |url=http://linkinghub.elsevier.com/retrieve/pii/S0006291X03020497}} |
|||
</ref> syndrôme du [[côlon_irritable]]<ref>{{cite journal |author=Camilleri M, Atanasova E, Carlson PJ, ''et al'' |title=Serotonin-transporter polymorphism pharmacogenetics in diarrhea-predominant irritable bowel syndrome |journal=Gastroenterology |volume=123 |issue=2 |pages=425–32 |year=2002 |month=August |pmid=12145795 |doi=10.1053/gast.2002.34780 |url=http://linkinghub.elsevier.com/retrieve/pii/S0016508502001208}}</ref>) et certaines formes de dépression <ref> Hudson JI, Mangweth B, Pope HG JR, De COL C, Hausmann A, Gutweniger S, Laird NM, Biebl W, Tsuang MT. Family study of affective spectrum disorder. Arch Gene Psychiatry. 2003;60:170–177. doi: 10.1001/archpsyc.60.2.170.</ref> |
|||
Cet ensemble de critère a été créé dans le but de classifier les indifidus comme ayant la fibromyalgie, a des fins de [[recherche]]. Sa marge d'erreur considérée comme faible, ainsi que l'absence d'un autre test plus précis ont établi ce test ''de facto'' pour le milieu clinique. |
|||
=== Hypothèse d'un dérèglement des neurotransmetteurs === |
|||
=== Symptômes === |
|||
Une déficience dans certains [[neurotransmetteur]]s (excès de [[substance P]], manque de [[sérotonine]] et de [[noradrénaline]]) a été identifiée<ref>Evengard B, Nilsson CG, Lindh G, Lindquist L, Eneroth P, Fredrikson S et al. Chronic fatigue syndrome differs from fibromyalgia. No evidence for elevated substance P levels in cerebrospinal fluid of patients with chronic fatigue syndrome [In Process Citation]. Pain 1998; 78(2):153-155.</ref>{{,}}<ref>Russell IJ, Orr MD, Littman B, Vipraio GA, Alboukrek D, Michalek JE et al. Elevated cerebrospinal fluid levels of substance P in patients with the fibromyalgia syndrome. Arthritis Rheum 1994; 37(11):1593-1601.</ref>{{,}}<ref>Vaeroy H, Helle R, Forre O, Kass E, Terenius L. Elevated CSF levels of substance P and high incidence of Raynaud phenomenon in patients with fibromyalgia: new features for diagnosis. Pain 1988; 32(1):21-26. </ref>. L'excès de substance P est reconnu pour provoquer une [[hyperalgésie]]<ref>. Hua XY, Chen P, Marsala M, Yaksh TL. Intrathecal substance P-induced thermal hyperalgesia and spinal release of prostaglandin E2 and amino acids. Neurosci 1999; 89(2):525-534.</ref>{{,}}<ref>Dirig DM, Yaksh TL. Thermal hyperalgesia in rat evoked by intrathecal substance P at multiple stimulus intensities reflects an increase in the gain of nociceptive processing. Neurosci Lett 1996; 220(2):93-96. </ref>, une réduction de la [[sérotonine]] et/ou de la [[noradrénaline]] produit également une hyperalgésie par la réduction des [[système inhibiteur de la douleur|systèmes inhibiteurs de la douleur]]<ref>Lautenbacher S, Rollman GB. Possible deficiencies of pain modulation in fibromyalgia. Clin J Pain 1997; 13(3):189-196.</ref>{{,}}<ref>Kosek E, Hansson P. Modulatory influence on somatosensory perception from vibration and heterotopic noxious conditioning stimulation (HNCS) in fibromyalgia patients and healthy subjects. Pain 1997; 70(1):41-51</ref> . |
|||
Les fibromyalgies se présentent sous diverses formes de douleurs chroniques (douleurs franches, douleurs diffuses, sensations de brûlures, de coups, d'[[ecchymose]], d'écrasement, d'arrachage, etc.) des muscles du squelette, des tendons et moins fréquemment des articulations, pouvant toucher tout le corps ou partiellement ([[quadrant]]), plus fréquemment le dos, les jambes et les bras. Ces symptômes variant tout au long de la journée, de la semaine, du mois, de l'année. Le patient fibromyalgique a tout ou partie des symptômes suivants : |
|||
Les taux plus élevés d'anticorps anti-[[sérotonine]] dans le sang, de [[facteur de croissance|facteurs de croissance]]<ref>Giovengo SL, Russell IJ, Larson AA. Increased concentrations of nerve growth factor in cerebrospinal fluid of patients with fibromyalgia. J Rheumatol 1999; 26(7):1564-1569.</ref>{{,}}<ref>Fischer HP, Eich W, Russell IJ. A possible role for saliva as a diagnostic fluid in patients with chronic pain. Semin Arthritis Rheum 1998; 27(6):348-359.</ref> dans le [[liquide céphalo-rachidien]]<ref>Russell IJ. Neurochemical pathogenesis of fibromyalgia. Z Rheumatol 1998; 57 Suppl 2:63-66. </ref> et des variations du système de réponse [[inflammation|inflammatoire]] viennent corroborer cette hypothèse. Certains docteurs posent désormais clairement l'existance d'une composante [[auto-immune]] de la fibromyalgie<ref>http://www.cenaf.org/blogs/fibromyalgie/</ref>{{,}}<ref>Maes M, Libbrecht I, Van Hunsel F, Lin AH, De Clerck L, Stevens W et al. The immune-inflammatory pathophysiology of fibromyalgia: increased serum soluble gp130, the common signal transducer protein of various neurotrophic cytokines. Psychoneuroendocrinology 1999; 24(4):371-383. </ref>. |
|||
* douleurs musculaires, osseuses, des articulations, des tendons ; |
|||
Un lien a également été prouvé entre fabrication des monoamines et fibromyalgie<ref>2007: Su Shan-Yu; Chen Jonathan Jiunn-Horng; Lai Chien-Chen; Chen Chun-Ming; Tsai Fuu-Jen. The association between fibromyalgia and polymorphism of monoamine oxidase A and interleukin-4.Clinical rheumatology 2007;26(1):12-6.</ref>. Des [[génétique|gènes]], responsables de la fabriquation des [[monoamine]]s, ont été identifiés comme déficients. Ces monoamines comprennent la [[sérotonine]] et les [[catécholamine]]s, qui servent à fabrication de la [[dopamine]], de l'[[adrénaline]] et de la [[noradrénaline]]. Ces [[neuromédiateur]]s, substances ayant un rôle pour transmettre l'influx nerveux, et qui influent sur l'[[anxiété]], le [[stress]] et le moral seraient en nombre insuffisants chez les fibromyalgiques<ref>http://www.vulgaris-medical.com/actualites/fibromyalgie-du-nouveau-dans-la-comprehension-de-la-maladie-100.html</ref>. |
|||
* fatigue physique ; |
|||
* fatigue psychique, sensation de vide psychologique, regard vague ; |
|||
* irritabilité générale (au toucher, aux sollicitations, au bruit, à la lumière, à la présence d'autrui, à des odeurs inhabituelles, à l'odeur de nourriture, etc.) et impatience ; |
|||
* pensées suicidaires constantes, dépression nerveuse ; |
|||
* besoin de consommer des glucides (gâteaux, pain, pommes de terre, frites, etc.) ; |
|||
* troubles assez sévères de la mémoire (court ou long terme) ; |
|||
* sensations de brûlures, de coups, de bleus, d'écrasement, d'arrachage, etc. ; |
|||
* troubles du système digestif (diarrhées, ballonnements) ; |
|||
* dessèchement et brûlure des yeux ; |
|||
* insomnie, grande difficulté à dormir et à se régénérer lors du sommeil ; |
|||
* chaleur au niveau de la paume des mains et de la plante des pieds (jusqu'au besoin de passer ses mains et/ou ses pieds sous l'eau du robinet pour soulager la douleur) ; |
|||
* très grande difficulté à se concentrer, surtout pour lire, pour se concentrer sur ce que dit un interlocuteur ; |
|||
* aggravation des symptômes avec la consommation de sucre et de produits sucrés ou avec la faim ; |
|||
* Au moins onze points douloureux sur les 18 indiqués dans le test ACR |
|||
* tremblements, sensations de faiblesse ; |
|||
* sensation d'avoir le corps rouillé, rigide, courbattu. |
|||
Ces troubles sont souvent associés à des problèmes gastro-intestinaux ([[allergie au gluten]], [[syndrôme du côlon irritable]] ...) et à des maux de tête.<ref>Wolfe F, Snilders AMJ, Yunus MB, et al. The Amerian College of Rhumatology 1990 criteria for the classification of fibromylagia: report of the Multicenter Criteria Commitee. Arthritis Rheum 1990; 33:160-172.</ref>{{,}}<ref>Clauw DJ. The pathogenesis of chronic pain and fatigue syndromes, with special reference to fibromyalgia. Med Hypotheses 1995; 44(5):369-3</ref> Le quotidien d'un fibromyalgique peut être aisément comparé à celui d'une personne atteinte de [[polyarthrite rhumatoïde]]. |
|||
=== Hypothèse d'un dérèglement immunologique === |
|||
=== Pathophysiologie === |
|||
D'autres études tentent à démontrer que les [[cytokine]]s, impliquées dans le [[système immunitaire]] auraient une action perturbée chez les personnes atteintes de fibromyalgie.Il existerait donc une cause de survenue de la fibromyalgie mettant en cause un phénomène immunologique en relation étroite avec un phénomène neurologique<ref>http://www.fibromyalgiesos.com/fm/zFibromyalgievulgarismedicalMartzolff.pdf {{pdf}}</ref>{{,}}<ref>http://www.medscape.com/viewarticle/470556_8</ref>. Ces études, restantes à être confirmées, car portant sur un nombre réduits de patients, prouvent que ces personnes atteintes de fibromyalgie ont un excès en [[cytokine]], qui peut provoquer un excès en [[substance P]]. Le niveau de [[cytokine]] observé augmenterait avec la durée de la maladie. On remarque également des niveaux de cytokine élevés chez les personnes manquant de sommeil<ref>http://www.prohealth.com/library/showarticle.cfm?id=3748&t=CFIDS_FM</ref>. Il est actuellement impossible de déterminer si le manque de sommeil des fibromyalgiques est à l'origine de ce niveau de cytokine, ou si le taux de cytokine est à même de provoquer les maux, et donc l'absence de sommeil. |
|||
==== Anomalies du liquide cérébro-spinal ==== |
|||
=== Hypothèse d'un dysfonctionnement de l'irrigation du cerveau === |
|||
La découverte la plus systématiquement reproduite en laboratoire est une concentration haute, chez les sujets atteints, des niveaux en [[substance P]], un [[neurotransmetteur]] lié à la perception de la douleur.<ref>{{cite journal |author=Russell IJ, Orr MD, Littman B, ''et al.'' |title=Elevated cerebrospinal fluid levels of substance P in patients with the fibromyalgia syndrome |journal=Arthritis Rheum. |volume=37 |issue=11 |pages=1593–601 |year=1994 |month=November |pmid=7526868 |doi=10.1002/art.1780371106 }}</ref>{{,}}<ref> {{cite journal |author=Vaerøy H, Helle R, Førre O, Kåss E, Terenius L |title=Elevated CSF levels of substance P and high incidence of Raynaud phenomenon in patients with fibromyalgia: new features for diagnosis |journal=Pain |volume=32 |issue=1 |pages=21–6 |year=1988 |month=January |pmid=2448729 |url=http://linkinghub.elsevier.com/retrieve/pii/0304-3959(88)90019-X |doi=10.1016/0304-3959(88)90019-X}}</ref>{{,}}<ref>{{cite journal |author=Evengard B, Nilsson CG, Lindh G, ''et al.'' |title=Chronic fatigue syndrome differs from fibromyalgia. No evidence for elevated substance P levels in cerebrospinal fluid of patients with chronic fatigue syndrome |journal=Pain |volume=78 |issue=2 |pages=153–5 |year=1998 |month=November |pmid=9839828 |url=http://linkinghub.elsevier.com/retrieve/pii/S0304-3959(98)00134-1 |doi=10.1016/S0304-3959(98)00134-1}} |
|||
Fin 2008, une équipe de chercheurs du Centre hospitalo-universitaire de la Timone à Marseille, dirigée par le professeur Eric Guedj, a identifié une anomalie<ref>[http://www.webmd.com/fibromyalgia/news/20081103/fibromyalgia-a-real-disease-study-shows {{Citation étrangère|lang=en|Fibromyalgia a ‘Real Disease,’ Study Shows}}], sur les site ''webmd.com''.</ref> au niveau de la [[circulation sanguine]] dans le [[cerveau]] de patients atteints de fibromyalgie, grâce à une tomographie à émission de photons (SPECT). L'étude a permis de découvrir que chez les patients atteints de fibromyalgie, certaines régions du cerveau sont trop irriguées, alors que d'autres le sont insuffisamment. Cette irrégularité modifie la manière donc le patient ressent et traite la douleur. Les chercheurs ont en outre identifié des liens entre le flux sanguin de certaines zones du cerveau et l'anxiété, les douleur intempestives, le handicap et la dépression nerveuse. Les chercheurs ont identifié une augmentation de la circulation du sang dans certaines zones du cerveau qui servent à ressentir la douleur, alors qu'une diminution du flux sanguin a été identifié dans une autre zone chargée de la réponse émotionnelle à la douleur. |
|||
</ref> La présence des métabolites servant à la formations des neurotransmetteurs [[monoamine]]s [[serotonine]], [[norepinephrine}}, et [[dopamine]]— qui jouent tous un rôle dans l'[[analgésie]] naturelle du corps, ont été prouvé comme étant anormalement basses.<ref>{{cite journal |author=Russell IJ, Vaeroy H, Javors M, Nyberg F |title=Cerebrospinal fluid biogenic amine metabolites in fibromyalgia/fibrositis syndrome and rheumatoid arthritis |journal=Arthritis Rheum. |volume=35 |issue=5 |pages=550–6 |year=1992 |month=May |pmid=1374252 |doi=10.1002/art.1780350509 }} |
|||
</ref> alors que la concentratnion des [[opïacé]]s endogènes (comme l'[[endorphine]] et l'[[enképhaline]]) semblent être plus hautes que la normale.<ref> {{cite journal |author=Vaerøy H, Nyberg F, Terenius L |title=No evidence for endorphin deficiency in fibromyalgia following investigation of cerebrospinal fluid (CSF) dynorphin A and Met-enkephalin-Arg6-Phe7 |journal=Pain |volume=46 |issue=2 |pages=139–43 |year=1991 |month=August |pmid=1684241 |url=http://linkinghub.elsevier.com/retrieve/pii/0304-3959(91)90068-9 |doi=10.1016/0304-3959(91)90068-9}}</ref> Une concentration élevée visible en [[facteur de croissance nerveuse]] (Nerve Growth Factor) a été prouvée. Cette substance est connue pour participer à la structuration et à la plasticité des interconnexions entre le [[cerveau]] et la [[moelle épinière]].<ref>{{cite journal |author=Giovengo SL, Russell IJ, Larson AA |title=Increased concentrations of nerve growth factor in cerebrospinal fluid of patients with fibromyalgia |journal=J Rheumatol. |volume=26 |issue=7 |pages=1564–9 |year=1999 |month=July |pmid=10405946 }}</ref> Il y a également des preuves d'une stimulation accrue des [[acide aminé|acides aminés]] au sein du [[liquide cérébro-spinal]], avec une corrélation prouvée entre les niveaux des métabolites de [[glutamate]]s et d'[[oxyde nitrique]] et la sensation de douleur.<ref>{{cite journal |author=Larson AA, Giovengo SL, Russell IJ, Michalek JE |title=Changes in the concentrations of amino acids in the cerebrospinal fluid that correlate with pain in patients with fibromyalgia: implications for nitric oxide pathways |journal=Pain |volume=87 |issue=2 |pages=201–11 |year=2000 |month=August |pmid=10924813 |url=http://linkinghub.elsevier.com/retrieve/pii/S0304-3959(00)00284-0 |doi=10.1016/S0304-3959(00)00284-0}}</ref> |
|||
====Troubles du sommeil décelés par un encéphalogramme==== |
|||
=== Hypothèse de troubles du sommeil === |
|||
Les premières découvertes objectives associées à la maladie ont été rapportée en [[1975]] où ont été démontrées la présences d'[[onde alpha|ondes alpha]] (associées usuellement à des phases de [[sommeil léger]]) anormales en phase 4 ([[sommeil profond]]) durant l'[[encélaphogramme]] de patients fibromyalgiques.<ref name=p169541>{{cite journal |author=Moldofsky H, Scarisbrick P, England R, Smythe H |title=Musculosketal symptoms and non-REM sleep disturbance in patients with "fibrositis syndrome" and healthy subjects |journal=Psychosom Med |volume=37 |issue=4 |pages=341–51 |month=Jul-August |year=1975 |pmid=169541 |url=http://www.psychosomaticmedicine.org/cgi/pmidlookup?view=long&pmid=169541 |day=01}}</ref> |
|||
Des études d'[[électroencéphalogramme]]s du sommeil ont prouvé que les personnes atteintes de fibromyalgie manquent de la phase de [[sommeil]] profond, et que les circonstances influant le sommeil de phase 4 (douleur, dépression, manque de sérotonine, certains médicaments, anxiété...) peuvent causer ou aggraver la maladie.<ref>Fibromyalgia – An Information Booklet [http://www.arc.org.uk/arthinfo/patpubs/6013/6013.asp]</ref> Selon cette hypothèse d'une perturbation du sommeil, un évènement, tel un traumatisme, peut causer une perturbation du sommeil, causant la douleur initiale du processus. |
|||
En fait, en interrompant le sommeil de phase 4 constamment sur des sujets jeunes et en bonne santé, [[Moldofsky]] et son équipe ont été capable de reproduire une tension musculaire supposée comparable à celle des patients fibromyalgiques. Cependant ces sensations ont disparu lorsque les sujets ont pu retrouver un sommeil normal.<ref>{{cite journal |author=Moldofsky H, Scarisbrick P |title=Induction of neurasthenic musculoskeletal pain syndrome by selective sleep stage deprivation |journal=Psychosom Med |volume=38 |issue=1 |pages=35–44 |month=Jan-February |year=1976 |pmid=176677 |url=http://www.psychosomaticmedicine.org/cgi/pmidlookup?view=long&pmid=176677 |day=01}}</ref> |
|||
Cette hypothèse repose sur l'hypothèse que le sommeil de stage 4 est critique pour le fonctionnement du [[système nerveux]], sachant que certains processus neurochimiques redémarrent durant cette phase. En particulier, la douleur cause la sécrétion d'une [[neuropeptide]], la [[substance P]] dans la [[Moelle épinière]] qui a pour effet d'amplifier la douleur et rend les nerfs plus sensibles à la douleur. Dans des circonstances normales, les zones autour d'une blessure deviennent plus sensibles à la douleurs, mais si la douleur devient chronique, ce processus peut dérailler et s'étendre. |
|||
Depuis cette étude, de nombreuses études confirment des anomalies variées dans des sous-groupes de patients fibromyalgiques.<ref>{{cite journal |author=Drewes AM, Gade K, Nielsen KD, Bjerregård K, Taagholt SJ, Svendsen L |title=Clustering of sleep electroencephalographic patterns in patients with the fibromyalgia syndrome |journal=Br J Rheumatol. |volume=34 |issue=12 |pages=1151–6 |year=1995 |month=December |pmid=8608357 |url=http://rheumatology.oxfordjournals.org/cgi/pmidlookup?view=long&pmid=8608357 |doi=10.1093/rheumatology/34.12.1151}}</ref> |
|||
Cette hypothèse repose sur l'hypothèse que le sommeil profond permettrait de réinitialiser le mécanisme de la substance P, et qu'un manque de sommeil pourrait alors devenir une cause de la maladie. |
|||
====Imagerie du cerveau==== |
|||
=== Hypothèse d'une déficience en hormone de croissance humaine === |
|||
La preuve d'une réaction anormale du [[cerveau]] dans le cadre de la fibromyalgie a été prouvée par [[imagerie cérébrale]] fonctionnelle. Les premières découvertes font état d'une [[circulation sanguine]] diminuée dans le [[thalamus]], des [[ganglions de la base]] et de certaines zones médiannes du cerveau.<ref>{{cite journal |author=Mountz JM, Bradley LA, Modell JG, ''et al.'' |title=Fibromyalgia in women. Abnormalities of regional cerebral blood flow in the thalamus and the caudate nucleus are associated with low pain threshold levels |journal=Arthritis Rheum. |volume=38 |issue=7 |pages=926–38 |year=1995 |month=July |pmid=7612042 |doi=10.1002/art.1780380708 }}</ref><ref>{{cite journal |author=Kwiatek R, Barnden L, Tedman R, ''et al.'' |title=Regional cerebral blood flow in fibromyalgia: single-photon-emission computed tomography evidence of reduction in the pontine tegmentum and thalami |journal=Arthritis Rheum. |volume=43 |issue=12 |pages=2823–33 |year=2000 |month=December |pmid=11145042 |doi=10.1002/1529-0131(200012)43:12<2823::AID-ANR24>3.0.CO;2-E }}</ref> Une activation différée de ces zones dans la réaction à la douleur a également été prouvée.<ref name=p12115241>{{cite journal |author=Gracely RH, Petzke F, Wolf JM, Clauw DJ |title=Functional magnetic resonance imaging evidence of augmented pain processing in fibromyalgia |journal=Arthritis Rheum. |volume=46 |issue=5 |pages=1333–43 |year=2002 |month=May |pmid=12115241 |doi=10.1002/art.10225 }}</ref><ref name=p14760810 >{{cite journal |author=Cook DB, Lange G, Ciccone DS, Liu WC, Steffener J, Natelson BH |title=Functional imaging of pain in patients with primary fibromyalgia |journal=J Rheumatol. |volume=31 |issue=2 |pages=364–78 |year=2004 |month=February |pmid=14760810 |url=http://www.jrheum.com/subscribers/04/02/364.html |doi=10.1093/rheumatology/31.6.364}}</ref> |
|||
Une hypothèse alternative suggère que des problèmes induits par le stress, dans l'[[hypothalamus]] peuvent conduire à un sommeil réduit et réduit la production d'[[hormone de croissance]] humaine durant le [[sommeil]] profond. {{refnec|Les gens atteints de fibromalgies tendent à produire des niveaux inadéquats de cette hormone}}. Cette théorie est supportée par le fait que plusieurs substances, qui sont produites sous le contrôle direct ou indirect de cette hormone (comme [[IGF-1]], [[cortisol]], [[leptine]] et le [[neuropeptide]] Y) atteignent des niveaux anormaux avec les personnes atteintes de fibromyalgie.<ref>{{cite journal |author=Anderberg UM, Liu Z, Berglund L, Nyberg F |pmid=10700334 |title=Elevated plasma levels of neuropeptide Y in female fibromyalgia patients |journal=Eur J Pain |volume=3 |issue=1 |year=1999 |pages=19–30 |doi=10.1016/S1090-3801(99)90185-4}}</ref> De plus, des traitements avec injection d'[[hormone de croissance]] réduit la douleur induite par la maladie, et permettrait l'obtention de [[sommeil profond]]<ref> {{ cite journal |author=Jones KD, Deodhar P, Lorentzen A, Bennett RM, Deodhar AA |title=Growth hormone perturbations in fibromyalgia: a review |journal=Seminars in Arthritis and Rheumatism |year=2007 |volume=36 |issue=6 |pages=357–79 |pmid=17224178 |doi=10.1016/j.semarthrit.2006.09.006 }}</ref>{{,}}<ref>{{cite journal |last=Shuer |first=ML |title=Fibromyalgia: symptom constellation and potential therapeutic options |journal=Endocrine |volume=22 |issue=1 |pages=67–76 |pmid=14610300 |doi=10.1385/ENDO:22:1:67 |year=2003}}</ref><ref>{{cite journal |last=Yuen |first=KC |coauthors=Bennett RM, Hryciw CA, Cook MB, Rhoads SA, Cook DM |journal=Growth hormone & IGF research |title=Is further evaluation for growth hormone (GH) deficiency necessary in fibromyalgia patients with low serum insulin-like growth factor (IGF)-I levels? |volume=17 |issue=1 |year=2007 |pages=82–8 |pmid=17289417 |doi=10.1016/j.ghir.2006.12.006 }}</ref>{{,}}<ref>{{cite journal | last = Bennett | first = RM | coauthors = Cook DM, Clark SR, Burckhardt CS, Campbell SM. | pmid = 9228141 | title = Hypothalamic-pituitary-insulin-like growth factor-I axis dysfunction in patients with fibromyalgia | volume = 24 | issue = 7 | pages = 1384–9 | journal =J Rheumatology }}</ref>; l'influence de l'hormone de croissance fait encore débat, d'autres études ne faisant pas cas d'un manque de cette hormone chez d'autres patients<ref>{{cite journal | last = McCall-Hosenfeld | first = JS | coauthors = Goldenberg DL, Hurwitz S, Adler GK. | title = Growth hormone and insulin-like growth factor-1 concentrations in women with fibromyalgia | journal = Journal of Rheumatology | volume = 30 | issues = 4 | pages = 809–14 | pmid = 12672204 }}</ref>. |
|||
=== Hypothèse d'un dérèglement hormonal lié au stress=== |
|||
====Sensibilité polymodale==== |
|||
Des études montrent que le [[stress]] est un facteur aggravant significatif dans le développement de la fibromyalgie.<ref>{{cite journal |author = Anderberg UM, Marteinsdottir I, Theorell T, von Knorring L |title=The impact of life events in female patients with fibromyalgia and in female healthy controls |journal=Eur Psychiatry |month=August |year=2000 |pages=33–41 |volume=15 |issue=5 |pmid=10954873 |doi=10.1016/S0924-9338(00)00397-7}}</ref> |
|||
Plusieurs études résultant de stimulation expérimentale ont démontré que les patients fibromyalgiques démontrent une sensibilité accrue à la [[pression]], aux sensations de [[chaleur]] et de [[froid]], , à des stimulations électriques et chimiques.<ref>{{cite journal |author=Desmeules JA, Cedraschi C, Rapiti E, ''et al.'' |title=Neurophysiologic evidence for a central sensitization in patients with fibromyalgia |journal=Arthritis Rheum. |volume=48 |issue=5 |pages=1420–9 |year=2003 |month=May |pmid=12746916 |doi=10.1002/art.10893 }}</ref> Des expérimentation sur les [[système régulateur de la douleur|systèmes régulateurs de la douleur]] ont montré que les patients atteints de fibromyalgie montrent aussi une dérégulation de différents mécanismes [[inhibiteur]]s de la douleur.<ref>{{cite journal |author=Kosek E, Hansson P |title=Modulatory influence on somatosensory perception from vibration and heterotopic noxious conditioning stimulation (HNCS) in fibromyalgia patients and healthy subjects |journal=Pain |volume=70 |issue=1 |pages=41–51 |year=1997 |month=March |pmid=9106808 |url=http://linkinghub.elsevier.com/retrieve/pii/S0304395996032952 |doi=10.1016/S0304-3959(96)03295-2}}</ref> Elles démontrent également une réaction exagéré à un stimuli répété,<ref>{{cite journal |author=Staud R, Vierck CJ, Cannon RL, Mauderli AP, Price DD |title=Abnormal sensitization and temporal summation of second pain (wind-up) in patients with fibromyalgia syndrome |journal=Pain |volume=91 |issue=1-2 |pages=165–75 |year=2001 |month=March |pmid=11240089 |url=http://linkinghub.elsevier.com/retrieve/pii/S0304-3959(00)00432-2 |doi=10.1016/S0304-3959(00)00432-2}}</ref> et la diminution ou l'absence de la réaction [[analgésique]] induite par l'effort physique.<ref>{{cite journal |author=Staud R, Robinson ME, Price DD |title=Isometric exercise has opposite effects on central pain mechanisms in fibromyalgia patients compared to normal controls |journal=Pain |volume=118 |issue=1-2 |pages=176–84 |year=2005 |month=November |pmid=16154700 |doi=10.1016/j.pain.2005.08.007 }} |
|||
En conséquence il a été avancé que la fibromialgie puisse résulter d'un dysfonctionnement induit par le stress, notamment dans la fonction et l'intégrité de l'[[hippocampe]].<ref>{{cite journal |author = Wood PB |title=Fibromyalgia: A Central Role for the Hippocampus – A Theoretical Construct |journal=J usculoskeletal Pain |year=2004 |pages=19–26 |volume=12 |issue=1 |url=http://www.haworthpress.com/store/ArticleAbstract.asp?sid=02FUKHQ65W2U9PXDV722GK6D5GQWC5PE&ID=42619}}</ref> Cettre proposition est basée sur des études pré-cliniques sur des singes, qui ont montré que l'exposition à un stress psychosocial peut avoir des conséquences physiques sur les tissus du cerveau, incluant de l'[[atrophie]] et des changements métaboliques de [[hippocampe]].<ref name=p2723746 >{{cite journal |author=Uno H, Tarara R, Else JG, Suleman MA, Sapolsky RM.|title=Hippocampal damage associated with prolonged and fatal stress in primates.|journal=J Neurosci. |volume=9 |issue=5 |pages=1705–11 |year=1989|month=May|pmid=2723746}}</ref>{{,}}<ref name=p11488960 >{{cite journal |author=Lucassen PJ, Vollmann-Honsdorf GK, Gleisberg M, Czéh B, De Kloet ER, Fuchs E.|title=Chronic psychosocial stress differentially affects apoptosis in hippocampal subregions and cortex of the adult tree shrew.|journal=Eur J Neurosci. |volume=14 |issue=1 |pages=161–6 |year=2001|month=Ju1|pmid=11488960}}</ref> |
|||
</ref> Ensemble, ces résutlants pointent une dérégulation du [[système nerveux central]]. |
|||
====Perturbation neuroendocrinienne==== |
|||
Cette hypothèse est soutenue par deux études qui ont utilisé un [[spectroscope à résonance magnétique]] pour trouver des anomalies métaboliques dans l'[[hippocampe]] de patients atteints de fibromyalgie, avec une corrélation significative entre anomalies et sévérité des symptômes cliniques.<ref name=p18484688 >{{cite journal |author=Emad Y, Ragab Y, Zeinhom F, El-Khouly G, Abou-Zeid A, Rasker JJ.|title=Hippocampus dysfunction may explain symptoms of fibromyalgia syndrome. A study with single-voxel magnetic resonance spectroscopy. |journal=J Rheumatol. |volume=35 |issue=7 |pages=1371–7 |year=2008|month=July|pmid=18484688}}</ref><ref name=p18771960 >{{cite journal |author=Wood PB, Ledbetter CR, Glabus MF, Broadwell LK, Patterson JC 2nd|title=Hippocampal Metabolite Abnormalities in Fibromyalgia: Correlation With Clinical Features.|journal=J Pain. |doi=10.1016/j.jpain.2008.07.003|pmid=18771960}}</ref> Il est actuellement impossible de déduire si le stress a provoqué la malformation de l'hippocampe, ou si la maladie est la cause de la malformation. |
|||
Les études de patients atteints de fibromyalgie ont démontré des anomalies dans les fonctions neuroendocriniennes usuelles comme une [[hypocortisolemie]],<ref>{{cite journal |author=Gur A, Cevik R, Sarac AJ, Colpan L, Em S |title=Hypothalamic-pituitary-gonadal axis and cortisol in young women with primary fibromyalgia: the potential roles of depression, fatigue, and sleep disturbance in the occurrence of hypocortisolism |journal=Ann. Rheum. Dis. |volume=63 |issue=11 |pages=1504–6 |year=2004 |month=November |pmid=15479904 |pmc=1754816 |doi=10.1136/ard.2003.014969 }} |
|||
Un autre mécanisme reconnu est le dérèglement de l'[[axe hypothala-hypophysaire-surrénalien]]<ref>Demitrack MA, Crofford LJ. Evidence for and pathophysiologic implications of hypothalamic- pituitary-adrenal axis dysregulation in fibromyalgia and chronic fatigue syndrome. Ann N Y Acad Sci 1998; 840:684-697.</ref>{{,}}<ref>Crofford LJ, Demitrack MA. Evidence that abnormalities of central neurohormonal systems are key to understanding fibromyalgia and chronic fatigue syndrome. Rheum Dis Clin North Am 1996; 22(2):267-284.</ref> , qui influe sur le stress, et peut provoquer une variation cyclique des symptômes<ref>Moldofsky H. Sleep, neuroimmune and neuroendocrine functions in fibromyalgia and chronic fatigue syndrome. Adv Neuroimmunol 1995; 5(1):39-56. </ref>. |
|||
</ref> une sécrétion excessive de l'[[hormone]] [[adrenocorticotropine]] en réponse à une stimulation, et une résistance au feedback [[glucocorticoïde]].<ref>{{cite journal |author=Griep EN, Boersma JW, Lentjes EG, Prins AP, van der Korst JK, de Kloet ER |title=Function of the hypothalamic-pituitary-adrenal axis in patients with fibromyalgia and low back pain |journal=J. Rheumatol. |volume=25 |issue=7 |pages=1374–81 |year=1998 |month=July |pmid=9676772 }}</ref> Une réduction progressive de la présence d'[[hormone de croissance humaine]] a aussi été démontré sur certains groupes patients, alors que la plus part démontrent des sécrétions hormonales diminuées façe à des efforts physiques intentses, ou à des stimulations [[pharmacie|pharmaceutiques]].<ref>{{cite journal |author=Bennett RM |title=Adult growth hormone deficiency in patients with fibromyalgia |journal=Curr Rheumatol Rep |volume=4 |issue=4 |pages=306–12 |year=2002 |month=August |pmid=12126582 |doi=10.1007/s11926-002-0039-4 }} |
|||
</ref> D'autres anomalies incluent un temps de réponse réduit de la [[thyrotropine]] et des [[hormone]]s [[thyroïde|thyroïdiennes]] lors de stimulations hormonales,<ref>{{cite journal |author=Neeck G, Riedel W |title=Thyroid function in patients with fibromyalgia syndrome |journal=J. Rheumatol. |volume=19 |issue=7 |pages=1120–2 |year=1992 |month=July |pmid=1512769 }} |
|||
</ref>. Une hausse relativement élevée des niveaux de [[prolactine]], avec une déshinibition de la sécrétion de prolactine lors de stimulations hormonales <ref> {{cite journal |author=Riedel W, Layka H, Neeck G |title=Secretory pattern of GH, TSH, thyroid hormones, ACTH, cortisol, FSH, and LH in patients with fibromyalgia syndrome following systemic injection of the relevant hypothalamic-releasing hormones |journal=Z Rheumatol |volume=57 Suppl 2 |issue= |pages=81–7 |year=1998 |pmid=10025090 |url=http://link.springer.de/link/service/journals/00393/bibs/857%20Suppl%202000/857%20Suppl%2020081.htm |doi=10.1007/s003930050242}}</ref> et une sécrétion insuffisante des hormones produites par les [[glande surrénale|glandes surrénales]] ont également été constatés.<ref>{{cite journal |author=Dessein PH, Shipton EA, Joffe BI, Hadebe DP, Stanwix AE, Van der Merwe BA |title=Hyposecretion of adrenal androgens and the relation of serum adrenal steroids, serotonin and insulin-like growth factor-1 to clinical features in women with fibromyalgia |journal=Pain |volume=83 |issue=2 |pages=313–9 |year=1999 |month=November |pmid=10534604 |url=http://linkinghub.elsevier.com/retrieve/pii/S030439599900113X |doi=10.1016/S0304-3959(99)00113-X}} |
|||
</ref> |
|||
Ces changements pourraient être attribués aux effets du stress chronique que cause la maladie, qui après avoir été reçu et traité par le [[système nerveux central]], activent la sécrétion d'hormones [[neurone|neuronales]] [[corticotrophine]]s [[hypothalamus|hypotalamique]]s. Cela résulterait en une perturbation de la communication [[Hypophyse]]-[[Glande Surrénale]], et en un excès en [[somatostatine]] [[hypothalamus|hypothalamique]], qui en retour, inhibent la sécrétion d'un certain nombre d'autres hormones.<ref>{{cite journal |author=Neeck G, Crofford LJ |title=Neuroendocrine perturbations in fibromyalgia and chronic fatigue syndrome |journal=Rheum. Dis. Clin. North Am. |volume=26 |issue=4 |pages=989–1002 |year=2000 |month=November |pmid=11084955 |doi=10.1016/S0889-857X(05)70180-0 }}</ref> |
|||
===Autres hypothèses=== |
|||
====Hyperactivité du système nerveux sympathique==== |
|||
D'autres hypothèses ont été avancées, comme : |
|||
Une analyse a démontré une activité perturbée et excessive du [[système nerveux sympathique]].<ref> Martinez-Lavin M. Biology and therapy of fibromyalgia. Stress, the stress response system, and fibromyalgia. Arthritis Res Ther. 2007;9(4):216.</ref> with reduced sympathoadrenal reactivity in response to a variety of stressors including physical exertion and mental stress.<ref>{{cite journal |author=Giske L, Vøllestad NK, Mengshoel AM, Jensen J, Knardahl S, Røe C |title=Attenuated adrenergic responses to exercise in women with fibromyalgia--a controlled study |journal=Eur J Pain |volume=12 |issue=3 |pages=351–60 |year=2008 |month=April |pmid=17827042 |doi=10.1016/j.ejpain.2007.07.007 }} |
|||
* Certaines [[toxine]]s dans l'environnement du patient<ref>{{cite journal |author=Laylander JA |title=A Nutrient/Toxin Interaction Theory of the Etiology and Pathogenesis of Chronic Pain-Fatigue Syndromes: Part I |journal=Journal of Chronic Fatigue Syndrome |volume=5 |issue=1 |pages=67–91 |year=1999 | doi=10.1300/J092v05n01_08 }}</ref>{{,}}<ref>{{cite journal |author=Laylander JA |title=A Nutrient/Toxin Interaction Theory of the Etiology and Pathogenesis of Chronic Pain-Fatigue Syndromes: Part II |journal=Journal of Chronic Fatigue Syndrome |volume=5 |issue=1 |pages=93–126 |year=1999 | doi=10.1300/J092v05n01_08 }}</ref> |
|||
</ref><ref> Nilsen KB, Sand T, Westgaard RH, Stovner LJ, White LR, Bang Leistad R, Helde G, Rø M. Autonomic activation and pain in response to low-grade mental stress in fibromyalgia and shoulder/neck pain patients. Eur J Pain. 2007 Oct;11(7):743-55. </ref> Fibromyalgia patients demonstrate lower heart rate variability, an index of sympathetic/parasympathetic balance, indicating sustained sympathetic hyperactivity, especially at night.<ref> {{cite journal |author=Martínez-Lavín M, Hermosillo AG, Mendoza C, ''et al.'' |title=Orthostatic sympathetic derangement in subjects with fibromyalgia |journal=J. Rheumatol. |volume=24 |issue=4 |pages=714–8 |year=1997 |month=April |pmid=9101507 }} |
|||
</ref> De plus, les niveaux en [[neuropeptide Y]] dans le [[plasma (médecine)|plasma]] sont bas chez les malades; ce neuropetide localisé avec la [[norepinephrine]] dans le système nerveux sympathique.<ref>{{cite journal |author=Anderberg UM, Liu Z, Berglund L, Nyberg F |title=Elevated plasma levels of neuropeptide Y in female fibromyalgia patients |journal=Eur J Pain |volume=3 |issue=1 |pages=19–30 |year=1999 |month=March |pmid=10700334 |doi=10.1016/S1090-3801(99)90185-4 }}</ref>. A l'inverse les niveaux circulatoires d'[[epinephrine]] et de [[norepinephrine]] ont été parfois décris comme haut, bas et normaux.<ref>{{cite journal |author=van Denderen JC, Boersma JW, Zeinstra P, Hollander AP, van Neerbos BR |title=Physiological effects of exhaustive physical exercise in primary fibromyalgia syndrome (PFS): is PFS a disorder of neuroendocrine reactivity? |journal=Scand. J. Rheumatol. |volume=21 |issue=1 |pages=35–7 |year=1992 |pmid=1570485 |doi=10.3109/03009749209095060 }}</ref><ref>{{cite journal |author=Adler GK, Kinsley BT, Hurwitz S, Mossey CJ, Goldenberg DL |title=Reduced hypothalamic-pituitary and sympathoadrenal responses to hypoglycemia in women with fibromyalgia syndrome |journal=Am J Med. |volume=106 |issue=5 |pages=534–43 |year=1999 |month=May |pmid=10335725 |url=http://linkinghub.elsevier.com/retrieve/pii/S0002934399000741 |doi=10.1016/S0002-9343(99)00074-1}}</ref> |
|||
L'injection d'[[interleukine-6]] (une [[cytokine]] capable de stimuler la production d'hormone de sécrétion de [[corticotropine]] [[hypothalamus|hypotalamique]], qui à son tour stimule l'activité du système nerveux sympatique) provoque une hausse forte des niveaux circulatoire de [[norepinephrine]], et une hausse du [[rythme cardiaque]]. Ces hausses sont plus fortes chez les patients fybromyalgique que chez les personnes saines.<ref>{{cite journal |author=Torpy DJ, Papanicolaou DA, Lotsikas AJ, Wilder RL, Chrousos GP, Pillemer SR |title=Responses of the sympathetic nervous system and the hypothalamic-pituitary-adrenal axis to interleukin-6: a pilot study in fibromyalgia |journal=Arthritis Rheum. |volume=43 |issue=4 |pages=872–80 |year=2000 |month=April |pmid=10765933 |doi=10.1002/1529-0131(200004)43:4<872::AID-ANR19>3.0.CO;2-T }}</ref> |
|||
* une cause [[virus|virale]] comme le [[virus Epstein-Barr]]<ref>{{cite journal |author=Komaroff AL, Goldenberg D |title=The chronic fatigue syndrome: definition, current studies and lessons for fibromyalgia research |journal=Med. Hypotheses |volume=69 |issue=3 |pages=517–25 |year=2007 |pmid=17376601 |doi=10.1016/j.mehy.2005.10.037 }}</ref> |
|||
* une réaction immunitaire anormale à une [[bactérie]] [[intestin]]ale<ref name="AnnRheumDis2004-PimentalM">{{cite journal | author=Pimental M, Wallace D, Hallegua D et al. | title=A link between irritable bowel syndrome and fibromyalgia may be related to findings on lactulose breath testing | journal=J Rheumatol Suppl | month=November | year=1989 | pages=23–7 | volume=19 |pmid=2691680 }}</ref> |
|||
* Une érosion de la gaine chimique autour des nerfs sensoriels.<ref>{{cite journal |author=Szalavitz M |title=SAMe as it ever was? |journal=Notes Undergr |volume=39 |pages=14–5 |year=1999 |pmid=11366783 }}</ref> |
|||
* une dérégulation de la [[vasomotricité]] résultant en une [[ischémie]] des muscles ou une [[circulation sanguine]] anormale<ref>{{cite journal |author=Katz DL, Greene L, Ali A, Faridi Z |title=The pain of fibromyalgia syndrome is due to muscle hypoperfusion induced by regional vasomotor dysregulation |journal=Med. Hypotheses |volume=69 |issue=3 |pages=517–25 |year=2007 |pmid=17376601 |doi=10.1016/j.mehy.2005.10.037 }}</ref> |
|||
* une dégradation de la posture causée par la dysfonction de l'[[articulation temporo-mandibulaire]], elle-même due à une [[occlusion dentaire]] défectueuse. L'épuisement généré par les contractures musculaires résultant d'une posture vrillée contribuerait au syndrome de fatigue chronique rendant tout effort musculaire pénible, voire impossible. {{refnec|En outre, une partie des personnes atteintes ont une antériorité de traitements d'orthodontie, souvent avec extractions, ayant déséuilibré l'occlusion et la posture.}} |
|||
== Diagnostic == |
|||
[[Image:Tender points fibromyalgia.gif|thumb|Position des 18 points que reconnait l'[[American College of Rheumatology]] depuis 1990 comme critères pour la fibromyalgie.]] |
|||
La fibromyalgie est considérée parfois comme un diagnostic controversé, certains auteurs affirmant qu'il s'agit d'un non diagnostic. En effet il n'existe pas encore de test spécifique et fiable à 100% pour la validation de la fibromyalgie. La difficulté vient essentiellement du fait que des personnes atteintes peut voir l'ensemble de ses analyses en laboratoire revenir normales. et que beaucoup des symptômes se retrouvent dans d'autres maladies ([[rhumatisme]] articulaire, [[ostéoporose]], ...). Dans la plus part des cas, la conclusion du médecin est basée sur un [[diagnostic différentiel]], prenant en cause l'ensemble des autres possibilités, les symptômes, ainsi que le profil du patient. |
|||
Les critères de classification les plus couramment acceptés ont été élaborés en [[1990]] par le [[Collège américain de rhumatologie]][http://www.rheumatology.org/], souvent surnommés critères "ACR 1990". Ils définissent la fibromyalgie suivant la présence des points suivants : |
|||
* Un historique de douleur répandue sur tout le corps, durant depuis plus de 3 mois, et affectant l'ensemble des quatre quadrants du corps (les deux côtés, et au dessous et en dessous de la ceinture). |
|||
* Des points douloureux, au nombre de 18 (bien que le patient puisse avoir mal à d'autres endroits du corps). Durant le diagnostique, le médecin doit exercer une [[force (physique)|force]] de 39 [[Newton_(unité)|Newtons]] sur ces points. Le patient doit ressentir une douleur vive sur au moins 11 de ces points pour que la fibromyalgie puisse être confirmée<ref>{{cite web |author=National Institute of Arthritis and Musculoskeletal and Skin Diseases |titre=Questions and Answers About Fibromyalgia – How Is Fibromyalgia Diagnosed? |url=http://www.niams.nih.gov/hi/topics/fibromyalgia/fibrofs.htm#fib_d |month=June | year=2004 |publisher=National Institutes for Health}}</ref>. Il faut noter que la localisation et le nombre des points douloureux peut varier selon les périodes, les circonstances... |
|||
Cet ensemble de critère a été créé dans le but de classifier les indifidus comme ayant la fibromyalgie, a des fins de [[recherche]]. Sa marge d'erreur considérée comme faible, ainsi que l'absence d'un autre test plus précis ont établi ce test ''de facto'' pour le milieu clinique. |
|||
=== Liste de symptômes === |
|||
Les fibromyalgies se présentent sous diverses formes de douleurs chroniques (douleurs franches, douleurs diffuses, sensations de brûlures, de coups, d'[[ecchymose]], d'écrasement, d'arrachage, etc.) des muscles du squelette, des tendons et moins fréquemment des articulations, pouvant toucher tout le corps ou partiellement ([[quadrant]]), plus fréquemment le dos, les jambes et les bras. Ces symptômes variant tout au long de la journée, de la semaine, du mois, de l'année. Le patient fibromyalgique a tout ou partie des symptômes suivants : |
|||
* douleurs musculaires, osseuses, des articulations, des tendons ; |
|||
* fatigue physique extrême (difficultés à se tenir debout, à se lever) ; |
|||
* fatigue psychique, sensation de vide psychologique, regard vague ; |
|||
* irritabilité générale (au toucher, aux sollicitations, au bruit, à la lumière, à la présence d'autrui, à des odeurs inhabituelles, à l'odeur de nourriture, etc.) ; |
|||
* pensées suicidaires constantes, dépression nerveuse ; |
|||
* impatience ; |
|||
* besoin de consommer des glucides (gâteaux, pain, pommes de terre, frites, etc.) ; |
|||
* troubles assez sévères de la mémoire à court terme ; |
|||
* sensations de brûlures, de coups, de bleus, d'écrasement, d'arrachage, etc. ; |
|||
* trouble du système digestif (diarrhées, ballonnements) ; |
|||
* dessèchement et brûlure des yeux ; |
|||
* insomnie, grande difficulté à dormir et à se régénérer lors du sommeil ; |
|||
* chaleur extrême au niveau de la paume des mains et de la plante des pieds (besoin de passer ses mains et/ou ses pieds sous l'eau du robinet pour soulager la douleur) ; |
|||
* très grande difficulté à se concentrer, surtout pour lire, pour se concentrer sur ce que dit un interlocuteur ; |
|||
* aggravation des symptômes avec la consommation de sucre et de produits sucrés, avec la faim (avant les repas) ; |
|||
* onze points douloureux sur les 18 indiqués dans le test ACR |
|||
* tremblements, sensations de faiblesse ; |
|||
* sensation d'avoir le corps rouillé, rigide. |
|||
Ces troubles sont souvent associés à des problèmes gastro-intestinaux et à des maux de tête.<ref>Wolfe F, Snilders AMJ, Yunus MB, et al. The Amerian College of Rhumatology 1990 criteria for the classification of fibromylagia: report of the Multicenter Criteria Commitee. Arthritis Rheum 1990; 33:160-172.</ref>{{,}}<ref>Clauw DJ. The pathogenesis of chronic pain and fatigue syndromes, with special reference to fibromyalgia. Med Hypotheses 1995; 44(5):369-3</ref> Le quotidien d'un fibromyalgique peut être aisément comparé à celui d'une personne atteinte de [[polyarthrite rhumatoïde]]. |
|||
=== Facteurs aggravants === |
=== Facteurs aggravants === |
||
Les symptômes de la fibromyalgie seraient aggravés<ref>http://www.fibromyalgiesos.com/fm/zFibromyalgievulgarismedicalMartzolff.pdf</ref> notoirement dans les conditions suivantes, qui peuvent déclencher des réactions au niveau des neurotransmetteurs : |
Les symptômes de la fibromyalgie seraient aggravés<ref>http://www.fibromyalgiesos.com/fm/zFibromyalgievulgarismedicalMartzolff.pdf</ref> notoirement dans les conditions suivantes, liées au stress, et qui peuvent déclencher des réactions au niveau des neurotransmetteurs ou des hormones : |
||
* traumatisme, stress et choc émotionnel; |
* traumatisme, stress et choc émotionnel; |
||
* autre maladie ; |
* autre maladie ; |
||
| Ligne 204 : | Ligne 178 : | ||
À noter que certaines personnes affectées ont constaté une rémission partielle en suivant un régime strict sans [[gluten]]. Cela pourrait être lié à une inflammation spécifique de l'appareil digestif générant des toxines particulières, mais cela reste éminemment conditionnel. Cela pourrait également être lié au rôle de la sérotonine dans l'[[allergie au gluten]] aggravée <ref>Chiaravalloti G, et al. Platelet serotonin transporter in celiac disease. Acta Paediatr. 1997 Jul;86(7):696-9.</ref> (sa destruction par la réaction immunitaire de l'[[allergie]] peut causer des symptômes similaires à la fibromyalgie<ref>Cronin CC, et al. Celiac disease and epilepsy. QJM. 1998 Apr;91(4):303-8.</ref> <ref>Bernasconi A, et al. Celiac disease, bilateral occipital calcifications and intractable epilepsy: mechanisms of seizure origin. Epilepsia. 1998 Mar;39(3):300-6.</ref>), une autre étude prouvant la rémission de formes de maladies neuronales après une diète sans gluten pour des patients allergiques<ref> Hallert C, et al. Psychic disturbances in adult celiac disease. III. Reduced central monoamine metabolism and signs of depression. Scand J Gastroenterol. 1982 Jan;17(1):25-8.</ref>{{,}}<ref>De Santis A, et al. Schizophrenic symptoms and SPECT abnormalities in a celiac patient: regression after a gluten-free diet. J Intern Med. 1997 Nov;242(5):421-3.</ref> <ref>Hernandez MA, et al. Epilepsy, cerebral calcifications and clinical or subclinical celiac disease. Course and follow up with gluten-free diet. Seizure. 1998 Feb;7(1):49-54</ref>. Il existerait un nombre relativement visible de personnes à la fois fibromyalgiques et allergiques au gluten.<ref>Wallace DJ, Hallegua DS. Fibromyalgia: the gastrointestinal link. ; Curr Pain Headache Rep. 2004 Oct;8(5):364-8. [http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?db=pubmed&cmd=Retrieve&dopt=AbstractPlus&list_uids=15361320&query_hl=13&itool=pubmed_docsum]</ref> |
À noter que certaines personnes affectées ont constaté une rémission partielle en suivant un régime strict sans [[gluten]]. Cela pourrait être lié à une inflammation spécifique de l'appareil digestif générant des toxines particulières, mais cela reste éminemment conditionnel. Cela pourrait également être lié au rôle de la sérotonine dans l'[[allergie au gluten]] aggravée <ref>Chiaravalloti G, et al. Platelet serotonin transporter in celiac disease. Acta Paediatr. 1997 Jul;86(7):696-9.</ref> (sa destruction par la réaction immunitaire de l'[[allergie]] peut causer des symptômes similaires à la fibromyalgie<ref>Cronin CC, et al. Celiac disease and epilepsy. QJM. 1998 Apr;91(4):303-8.</ref> <ref>Bernasconi A, et al. Celiac disease, bilateral occipital calcifications and intractable epilepsy: mechanisms of seizure origin. Epilepsia. 1998 Mar;39(3):300-6.</ref>), une autre étude prouvant la rémission de formes de maladies neuronales après une diète sans gluten pour des patients allergiques<ref> Hallert C, et al. Psychic disturbances in adult celiac disease. III. Reduced central monoamine metabolism and signs of depression. Scand J Gastroenterol. 1982 Jan;17(1):25-8.</ref>{{,}}<ref>De Santis A, et al. Schizophrenic symptoms and SPECT abnormalities in a celiac patient: regression after a gluten-free diet. J Intern Med. 1997 Nov;242(5):421-3.</ref> <ref>Hernandez MA, et al. Epilepsy, cerebral calcifications and clinical or subclinical celiac disease. Course and follow up with gluten-free diet. Seizure. 1998 Feb;7(1):49-54</ref>. Il existerait un nombre relativement visible de personnes à la fois fibromyalgiques et allergiques au gluten.<ref>Wallace DJ, Hallegua DS. Fibromyalgia: the gastrointestinal link. ; Curr Pain Headache Rep. 2004 Oct;8(5):364-8. [http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?db=pubmed&cmd=Retrieve&dopt=AbstractPlus&list_uids=15361320&query_hl=13&itool=pubmed_docsum]</ref> |
||
== |
== Causes supposées == |
||
À partir de 2000-2004, les scientifiques se penchent de plus en plus vers des désordres de natures immuno-chimiques et/ou environnementaux, compte tenu de la résurgence surprenante de cas. Une atteinte du [[système nerveux central]] et un dérèglement [[neurone|neuronal]] ont été largement constatés chez les fibromyalgiques. |
|||
Il semble exister une perception différente de la douleur chez le fibromyalgique, avec en particulier, un seuil de perception plus bas<ref>Abeles AM, Pillinger MH, Solitar BM, Abeles M, [http://www.annals.org/cgi/content/full/146/10/726 ''The pathophysiology of fibromyalgia''], Ann Int Med, 2007;146;726-734</ref>. Le mécanisme de ce fait est toujours débattu, mais lourdement supposé lié aux neurotransmetteurs responsables du traitement de la douleur. |
|||
Il est possible que les différentes variantes de fibromyalgie soient liés à une combinaise d'une ou plusieurs de ces causes suposées. |
|||
=== Prédisposition génétique === |
|||
Outre le fait que cette maladie touche beaucoup plus de femmes que d'hommes, il existe de nombreuses preuves qu'un facteur génétique puisse jouer un rôle important dans le développement de la fibromyalgie.<ref>Yunus MB, Khan MA, Rawlings KK, Green JR, Olson JM, Shah S. Genetic linkage analysis of multicase families with fibromyalgia syndrome. J Rheumatol 1999 Feb;26(2):408-12 [http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=PubMed&list_uids=9972977&dopt=Abstract]</ref><ref>Buskila D, Neumann L Genetics of fibromyalgia. Curr Pain Headache Rep. 2005 Oct;9(5):313-5. [http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=PubMed&dopt=Abstract&list_uids=16157058]</ref><ref>Buskila D, Neumann L, Hazanov I, Carmi R. Familial aggregation in the fibromyalgia syndrome. Semin Arthritis Rheum 1996 Dec;26(3):605-11 [http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=PubMed&list_uids=8989805&dopt=Abstract]</ref> Par exemple, il existe beaucoup de familles présentants plusieurs personnes atteintes<ref>{{cite journal |author=Stormorken H |coauthors=Brosstad F |authorlink=Helge Stormorken |title=Fibromyalgia: family clustering and sensory urgency with early onset indicate genetic predisposition and thus a "true" disease |journal=Scand J Rheumatol. |volume=21 |issue=4 |pages=207 |year=1992 |pmid=1529291 |doi=10.3109/03009749209099225}}</ref><ref>{{cite journal |author=Arnold LM, Hudson JI, Hess EV, ''et al'' |title=Family study of fibromyalgia |journal=Arthritis Rheum. |volume=50 |issue=3 |pages=944–52 |year=2004 |month=March |pmid=15022338 |doi=10.1002/art.20042}}</ref> Le mode de transmission est encore inconnu mais est probablement [[polygénique]].<ref>{{cite journal |author=Buskila D, Sarzi-Puttini P |title=Biology and therapy of fibromyalgia. Genetic aspects of fibromyalgia syndrome |journal=Arthritis Res Ther. |volume=8 |issue=5 |pages=218 |year=2006 |pmid=16887010 |pmc=1779444 |doi=10.1186/ar2005}}</ref> Les recherches ont démontrés que la fibromyalgie est associée à des variation (ou [[polymorphisme]]) sur les [[gène]]s de production de la [[serotonine]],<ref>{{cite journal |author=Cohen H, Buskila D, Neumann L, Ebstein RP |title=Confirmation of an association between fibromyalgia and serotonin transporter promoter region (5- HTTLPR) polymorphism, and relationship to anxiety-related personality traits |journal=Arthritis Rheum. |volume=46 |issue=3 |pages=845–7 |year=2002 |month=March |pmid=11920428 |doi=10.1002/art.10103 }}</ref> [[dopamine]]<ref>{{cite journal |author=Buskila D, Dan B, Cohen H, ''et al'' |title=An association between fibromyalgia and the dopamine D4 receptor exon III repeat polymorphism and relationship to novelty seeking personality traits |journal=Mol. Psychiatry |volume=9 |issue=8 |pages=730–1 |year=2004 |month=August |pmid=15052273 |doi=10.1038/sj.mp.4001506 }}</ref> et [[catecholamine]].<ref>{{cite journal |author=Zubieta JK, Heitzeg MM, Smith YR, ''et al'' |title=COMT val158met genotype affects mu-opioid neurotransmitter responses to a pain stressor |journal=Science (journal) |volume=299 |issue=5610 |pages=1240–3 |year=2003 |month=February |pmid=12595695 |doi=10.1126/science.1078546 }}</ref> Cependant ces polymorphismes ne sont pas spécifiques à la fibromyalgie, et sont associés à une variétés d'autres maladies (comme le [[neurasthénie|syndrôme de fatigue chronique]],<ref>{{cite journal |author=Narita M, Nishigami N, Narita N, ''et al'' |title=Association between serotonin transporter gene polymorphism and chronic fatigue syndrome |journal=Biochem Biophys Res Commun. |volume=311 |issue=2 |pages=264–6 |year=2003 |month=November |pmid=14592408 |doi=10.1016/j.bbrc.2003.09.207 |url=http://linkinghub.elsevier.com/retrieve/pii/S0006291X03020497}} |
|||
</ref> syndrôme du [[côlon_irritable]]<ref>{{cite journal |author=Camilleri M, Atanasova E, Carlson PJ, ''et al'' |title=Serotonin-transporter polymorphism pharmacogenetics in diarrhea-predominant irritable bowel syndrome |journal=Gastroenterology |volume=123 |issue=2 |pages=425–32 |year=2002 |month=August |pmid=12145795 |doi=10.1053/gast.2002.34780 |url=http://linkinghub.elsevier.com/retrieve/pii/S0016508502001208}}</ref>) et certaines formes de dépression <ref> Hudson JI, Mangweth B, Pope HG JR, De COL C, Hausmann A, Gutweniger S, Laird NM, Biebl W, Tsuang MT. Family study of affective spectrum disorder. Arch Gene Psychiatry. 2003;60:170–177. doi: 10.1001/archpsyc.60.2.170.</ref> |
|||
=== Hypothèse d'un dérèglement des neurotransmetteurs === |
|||
Une déficience dans certains [[neurotransmetteur]]s (excès de [[substance P]], manque de [[sérotonine]] et de [[noradrénaline]]) a été identifiée<ref>Evengard B, Nilsson CG, Lindh G, Lindquist L, Eneroth P, Fredrikson S et al. Chronic fatigue syndrome differs from fibromyalgia. No evidence for elevated substance P levels in cerebrospinal fluid of patients with chronic fatigue syndrome [In Process Citation]. Pain 1998; 78(2):153-155.</ref>{{,}}<ref>Russell IJ, Orr MD, Littman B, Vipraio GA, Alboukrek D, Michalek JE et al. Elevated cerebrospinal fluid levels of substance P in patients with the fibromyalgia syndrome. Arthritis Rheum 1994; 37(11):1593-1601.</ref>{{,}}<ref>Vaeroy H, Helle R, Forre O, Kass E, Terenius L. Elevated CSF levels of substance P and high incidence of Raynaud phenomenon in patients with fibromyalgia: new features for diagnosis. Pain 1988; 32(1):21-26. </ref>. L'excès de substance P est reconnu pour provoquer une [[hyperalgésie]]<ref>. Hua XY, Chen P, Marsala M, Yaksh TL. Intrathecal substance P-induced thermal hyperalgesia and spinal release of prostaglandin E2 and amino acids. Neurosci 1999; 89(2):525-534.</ref>{{,}}<ref>Dirig DM, Yaksh TL. Thermal hyperalgesia in rat evoked by intrathecal substance P at multiple stimulus intensities reflects an increase in the gain of nociceptive processing. Neurosci Lett 1996; 220(2):93-96. </ref>, une réduction de la [[sérotonine]] et/ou de la [[noradrénaline]] produit également une hyperalgésie par la réduction des [[système inhibiteur de la douleur|systèmes inhibiteurs de la douleur]]<ref>Lautenbacher S, Rollman GB. Possible deficiencies of pain modulation in fibromyalgia. Clin J Pain 1997; 13(3):189-196.</ref>{{,}}<ref>Kosek E, Hansson P. Modulatory influence on somatosensory perception from vibration and heterotopic noxious conditioning stimulation (HNCS) in fibromyalgia patients and healthy subjects. Pain 1997; 70(1):41-51</ref> . |
|||
Les taux plus élevés d'anticorps anti-[[sérotonine]] dans le sang, de [[facteur de croissance|facteurs de croissance]]<ref>Giovengo SL, Russell IJ, Larson AA. Increased concentrations of nerve growth factor in cerebrospinal fluid of patients with fibromyalgia. J Rheumatol 1999; 26(7):1564-1569.</ref>{{,}}<ref>Fischer HP, Eich W, Russell IJ. A possible role for saliva as a diagnostic fluid in patients with chronic pain. Semin Arthritis Rheum 1998; 27(6):348-359.</ref> dans le [[liquide céphalo-rachidien]]<ref>Russell IJ. Neurochemical pathogenesis of fibromyalgia. Z Rheumatol 1998; 57 Suppl 2:63-66. </ref> et des variations du système de réponse [[inflammation|inflammatoire]] viennent corroborer cette hypothèse. Certains docteurs posent désormais clairement l'existance d'une composante [[auto-immune]] de la fibromyalgie<ref>http://www.cenaf.org/blogs/fibromyalgie/</ref>{{,}}<ref>Maes M, Libbrecht I, Van Hunsel F, Lin AH, De Clerck L, Stevens W et al. The immune-inflammatory pathophysiology of fibromyalgia: increased serum soluble gp130, the common signal transducer protein of various neurotrophic cytokines. Psychoneuroendocrinology 1999; 24(4):371-383. </ref>. |
|||
Un lien a également été prouvé entre fabrication des monoamines et fibromyalgie<ref>2007: Su Shan-Yu; Chen Jonathan Jiunn-Horng; Lai Chien-Chen; Chen Chun-Ming; Tsai Fuu-Jen. The association between fibromyalgia and polymorphism of monoamine oxidase A and interleukin-4.Clinical rheumatology 2007;26(1):12-6.</ref>. Des [[génétique|gènes]], responsables de la fabriquation des [[monoamine]]s, ont été identifiés comme déficients. Ces monoamines comprennent la [[sérotonine]] et les [[catécholamine]]s, qui servent à fabrication de la [[dopamine]], de l'[[adrénaline]] et de la [[noradrénaline]]. Ces [[neuromédiateur]]s, substances ayant un rôle pour transmettre l'influx nerveux, et qui influent sur l'[[anxiété]], le [[stress]] et le moral seraient en nombre insuffisants chez les fibromyalgiques<ref>http://www.vulgaris-medical.com/actualites/fibromyalgie-du-nouveau-dans-la-comprehension-de-la-maladie-100.html</ref>. |
|||
=== Hypothèse d'un dérèglement immunologique === |
|||
D'autres études tentent à démontrer que les [[cytokine]]s, impliquées dans le [[système immunitaire]] auraient une action perturbée chez les personnes atteintes de fibromyalgie.Il existerait donc une cause de survenue de la fibromyalgie mettant en cause un phénomène immunologique en relation étroite avec un phénomène neurologique<ref>http://www.fibromyalgiesos.com/fm/zFibromyalgievulgarismedicalMartzolff.pdf {{pdf}}</ref>{{,}}<ref>http://www.medscape.com/viewarticle/470556_8</ref>. Ces études, restantes à être confirmées, car portant sur un nombre réduits de patients, prouvent que ces personnes atteintes de fibromyalgie ont un excès en [[cytokine]], qui peut provoquer un excès en [[substance P]]. Le niveau de [[cytokine]] observé augmenterait avec la durée de la maladie. On remarque également des niveaux de cytokine élevés chez les personnes manquant de sommeil<ref>http://www.prohealth.com/library/showarticle.cfm?id=3748&t=CFIDS_FM</ref>. Il est actuellement impossible de déterminer si le manque de sommeil des fibromyalgiques est à l'origine de ce niveau de cytokine, ou si le taux de cytokine est à même de provoquer les maux, et donc l'absence de sommeil. |
|||
=== Hypothèse d'un dysfonctionnement de l'irrigation du cerveau === |
|||
Fin 2008, une équipe de chercheurs du Centre hospitalo-universitaire de la Timone à Marseille, dirigée par le professeur Eric Guedj, a identifié une anomalie<ref>[http://www.webmd.com/fibromyalgia/news/20081103/fibromyalgia-a-real-disease-study-shows {{Citation étrangère|lang=en|Fibromyalgia a ‘Real Disease,’ Study Shows}}], sur les site ''webmd.com''.</ref> au niveau de la [[circulation sanguine]] dans le [[cerveau]] de patients atteints de fibromyalgie, grâce à une tomographie à émission de photons (SPECT). L'étude a permis de découvrir que chez les patients atteints de fibromyalgie, certaines régions du cerveau sont trop irriguées, alors que d'autres le sont insuffisamment. Cette irrégularité modifie la manière donc le patient ressent et traite la douleur. Les chercheurs ont en outre identifié des liens entre le flux sanguin de certaines zones du cerveau et l'anxiété, les douleur intempestives, le handicap et la dépression nerveuse. Les chercheurs ont identifié une augmentation de la circulation du sang dans certaines zones du cerveau qui servent à ressentir la douleur, alors qu'une diminution du flux sanguin a été identifié dans une autre zone chargée de la réponse émotionnelle à la douleur. |
|||
=== Hypothèse de troubles du sommeil === |
|||
Des études d'[[électroencéphalogramme]]s du sommeil ont prouvé que les personnes atteintes de fibromyalgie manquent de la phase de [[sommeil]] profond, et que les circonstances influant le sommeil de phase 4 (douleur, dépression, manque de sérotonine, certains médicaments, anxiété...) peuvent causer ou aggraver la maladie.<ref>Fibromyalgia – An Information Booklet [http://www.arc.org.uk/arthinfo/patpubs/6013/6013.asp]</ref> Selon cette hypothèse d'une perturbation du sommeil, un évènement, tel un traumatisme, peut causer une perturbation du sommeil, causant la douleur initiale du processus. |
|||
Cette hypothèse repose sur l'hypothèse que le sommeil de stage 4 est critique pour le fonctionnement du [[système nerveux]], sachant que certains processus neurochimiques redémarrent durant cette phase. En particulier, la douleur cause la sécrétion d'une [[neuropeptide]], la [[substance P]] dans la [[Moelle épinière]] qui a pour effet d'amplifier la douleur et rend les nerfs plus sensibles à la douleur. Dans des circonstances normales, les zones autour d'une blessure deviennent plus sensibles à la douleurs, mais si la douleur devient chronique, ce processus peut dérailler et s'étendre. |
|||
Cette hypothèse repose sur l'hypothèse que le sommeil profond permettrait de réinitialiser le mécanisme de la substance P, et qu'un manque de sommeil pourrait alors devenir une cause de la maladie. |
|||
=== Hypothèse d'une déficience en hormone de croissance humaine === |
|||
Une hypothèse alternative suggère que des problèmes induits par le stress, dans l'[[hypothalamus]] peuvent conduire à un sommeil réduit et réduit la production d'[[hormone de croissance]] humaine durant le [[sommeil]] profond. {{refnec|Les gens atteints de fibromalgies tendent à produire des niveaux inadéquats de cette hormone}}. Cette théorie est supportée par le fait que plusieurs substances, qui sont produites sous le contrôle direct ou indirect de cette hormone (comme [[IGF-1]], [[cortisol]], [[leptine]] et le [[neuropeptide]] Y) atteignent des niveaux anormaux avec les personnes atteintes de fibromyalgie.<ref>{{cite journal |author=Anderberg UM, Liu Z, Berglund L, Nyberg F |pmid=10700334 |title=Elevated plasma levels of neuropeptide Y in female fibromyalgia patients |journal=Eur J Pain |volume=3 |issue=1 |year=1999 |pages=19–30 |doi=10.1016/S1090-3801(99)90185-4}}</ref> De plus, des traitements avec injection d'[[hormone de croissance]] réduit la douleur induite par la maladie, et permettrait l'obtention de [[sommeil profond]]<ref> {{ cite journal |author=Jones KD, Deodhar P, Lorentzen A, Bennett RM, Deodhar AA |title=Growth hormone perturbations in fibromyalgia: a review |journal=Seminars in Arthritis and Rheumatism |year=2007 |volume=36 |issue=6 |pages=357–79 |pmid=17224178 |doi=10.1016/j.semarthrit.2006.09.006 }}</ref>{{,}}<ref>{{cite journal |last=Shuer |first=ML |title=Fibromyalgia: symptom constellation and potential therapeutic options |journal=Endocrine |volume=22 |issue=1 |pages=67–76 |pmid=14610300 |doi=10.1385/ENDO:22:1:67 |year=2003}}</ref><ref>{{cite journal |last=Yuen |first=KC |coauthors=Bennett RM, Hryciw CA, Cook MB, Rhoads SA, Cook DM |journal=Growth hormone & IGF research |title=Is further evaluation for growth hormone (GH) deficiency necessary in fibromyalgia patients with low serum insulin-like growth factor (IGF)-I levels? |volume=17 |issue=1 |year=2007 |pages=82–8 |pmid=17289417 |doi=10.1016/j.ghir.2006.12.006 }}</ref>{{,}}<ref>{{cite journal | last = Bennett | first = RM | coauthors = Cook DM, Clark SR, Burckhardt CS, Campbell SM. | pmid = 9228141 | title = Hypothalamic-pituitary-insulin-like growth factor-I axis dysfunction in patients with fibromyalgia | volume = 24 | issue = 7 | pages = 1384–9 | journal =J Rheumatology }}</ref>; l'influence de l'hormone de croissance fait encore débat, d'autres études ne faisant pas cas d'un manque de cette hormone chez d'autres patients<ref>{{cite journal | last = McCall-Hosenfeld | first = JS | coauthors = Goldenberg DL, Hurwitz S, Adler GK. | title = Growth hormone and insulin-like growth factor-1 concentrations in women with fibromyalgia | journal = Journal of Rheumatology | volume = 30 | issues = 4 | pages = 809–14 | pmid = 12672204 }}</ref>. |
|||
=== Hypothèse d'un dérèglement hormonal lié au stress=== |
|||
Des études montrent que le [[stress]] est un facteur aggravant significatif dans le développement de la fibromyalgie.<ref>{{cite journal |author = Anderberg UM, Marteinsdottir I, Theorell T, von Knorring L |title=The impact of life events in female patients with fibromyalgia and in female healthy controls |journal=Eur Psychiatry |month=August |year=2000 |pages=33–41 |volume=15 |issue=5 |pmid=10954873 |doi=10.1016/S0924-9338(00)00397-7}}</ref> |
|||
En conséquence il a été avancé que la fibromialgie puisse résulter d'un dysfonctionnement induit par le stress, notamment dans la fonction et l'intégrité de l'[[hippocampe]].<ref>{{cite journal |author = Wood PB |title=Fibromyalgia: A Central Role for the Hippocampus – A Theoretical Construct |journal=J usculoskeletal Pain |year=2004 |pages=19–26 |volume=12 |issue=1 |url=http://www.haworthpress.com/store/ArticleAbstract.asp?sid=02FUKHQ65W2U9PXDV722GK6D5GQWC5PE&ID=42619}}</ref> Cettre proposition est basée sur des études pré-cliniques sur des singes, qui ont montré que l'exposition à un stress psychosocial peut avoir des conséquences physiques sur les tissus du cerveau, incluant de l'[[atrophie]] et des changements métaboliques de [[hippocampe]].<ref name=p2723746 >{{cite journal |author=Uno H, Tarara R, Else JG, Suleman MA, Sapolsky RM.|title=Hippocampal damage associated with prolonged and fatal stress in primates.|journal=J Neurosci. |volume=9 |issue=5 |pages=1705–11 |year=1989|month=May|pmid=2723746}}</ref>{{,}}<ref name=p11488960 >{{cite journal |author=Lucassen PJ, Vollmann-Honsdorf GK, Gleisberg M, Czéh B, De Kloet ER, Fuchs E.|title=Chronic psychosocial stress differentially affects apoptosis in hippocampal subregions and cortex of the adult tree shrew.|journal=Eur J Neurosci. |volume=14 |issue=1 |pages=161–6 |year=2001|month=Ju1|pmid=11488960}}</ref> |
|||
Cette hypothèse est soutenue par deux études qui ont utilisé un [[spectroscope à résonance magnétique]] pour trouver des anomalies métaboliques dans l'[[hippocampe]] de patients atteints de fibromyalgie, avec une corrélation significative entre anomalies et sévérité des symptômes cliniques.<ref name=p18484688 >{{cite journal |author=Emad Y, Ragab Y, Zeinhom F, El-Khouly G, Abou-Zeid A, Rasker JJ.|title=Hippocampus dysfunction may explain symptoms of fibromyalgia syndrome. A study with single-voxel magnetic resonance spectroscopy. |journal=J Rheumatol. |volume=35 |issue=7 |pages=1371–7 |year=2008|month=July|pmid=18484688}}</ref><ref name=p18771960 >{{cite journal |author=Wood PB, Ledbetter CR, Glabus MF, Broadwell LK, Patterson JC 2nd|title=Hippocampal Metabolite Abnormalities in Fibromyalgia: Correlation With Clinical Features.|journal=J Pain. |doi=10.1016/j.jpain.2008.07.003|pmid=18771960}}</ref> Il est actuellement impossible de déduire si le stress a provoqué la malformation de l'hippocampe, ou si la maladie est la cause de la malformation. |
|||
Un autre mécanisme reconnu est le dérèglement de l'[[axe hypothala-hypophysaire-surrénalien]]<ref>Demitrack MA, Crofford LJ. Evidence for and pathophysiologic implications of hypothalamic- pituitary-adrenal axis dysregulation in fibromyalgia and chronic fatigue syndrome. Ann N Y Acad Sci 1998; 840:684-697.</ref>{{,}}<ref>Crofford LJ, Demitrack MA. Evidence that abnormalities of central neurohormonal systems are key to understanding fibromyalgia and chronic fatigue syndrome. Rheum Dis Clin North Am 1996; 22(2):267-284.</ref> , qui influe sur le stress, et peut provoquer une variation cyclique des symptômes<ref>Moldofsky H. Sleep, neuroimmune and neuroendocrine functions in fibromyalgia and chronic fatigue syndrome. Adv Neuroimmunol 1995; 5(1):39-56. </ref>. |
|||
===Autres hypothèses=== |
|||
D'autres hypothèses ont été avancées, comme : |
|||
* Certaines [[toxine]]s dans l'environnement du patient<ref>{{cite journal |author=Laylander JA |title=A Nutrient/Toxin Interaction Theory of the Etiology and Pathogenesis of Chronic Pain-Fatigue Syndromes: Part I |journal=Journal of Chronic Fatigue Syndrome |volume=5 |issue=1 |pages=67–91 |year=1999 | doi=10.1300/J092v05n01_08 }}</ref>{{,}}<ref>{{cite journal |author=Laylander JA |title=A Nutrient/Toxin Interaction Theory of the Etiology and Pathogenesis of Chronic Pain-Fatigue Syndromes: Part II |journal=Journal of Chronic Fatigue Syndrome |volume=5 |issue=1 |pages=93–126 |year=1999 | doi=10.1300/J092v05n01_08 }}</ref> |
|||
* une cause [[virus|virale]] comme le [[virus Epstein-Barr]]<ref>{{cite journal |author=Komaroff AL, Goldenberg D |title=The chronic fatigue syndrome: definition, current studies and lessons for fibromyalgia research |journal=Med. Hypotheses |volume=69 |issue=3 |pages=517–25 |year=2007 |pmid=17376601 |doi=10.1016/j.mehy.2005.10.037 }}</ref> |
|||
* une réaction immunitaire anormale à une [[bactérie]] [[intestin]]ale<ref name="AnnRheumDis2004-PimentalM">{{cite journal | author=Pimental M, Wallace D, Hallegua D et al. | title=A link between irritable bowel syndrome and fibromyalgia may be related to findings on lactulose breath testing | journal=J Rheumatol Suppl | month=November | year=1989 | pages=23–7 | volume=19 |pmid=2691680 }}</ref> |
|||
* Une érosion de la gaine chimique autour des nerfs sensoriels.<ref>{{cite journal |author=Szalavitz M |title=SAMe as it ever was? |journal=Notes Undergr |volume=39 |pages=14–5 |year=1999 |pmid=11366783 }}</ref> |
|||
* une dérégulation de la [[vasomotricité]] résultant en une [[ischémie]] des muscles ou une [[circulation sanguine]] anormale<ref>{{cite journal |author=Katz DL, Greene L, Ali A, Faridi Z |title=The pain of fibromyalgia syndrome is due to muscle hypoperfusion induced by regional vasomotor dysregulation |journal=Med. Hypotheses |volume=69 |issue=3 |pages=517–25 |year=2007 |pmid=17376601 |doi=10.1016/j.mehy.2005.10.037 }}</ref> |
|||
* une dégradation de la posture causée par la dysfonction de l'[[articulation temporo-mandibulaire]], elle-même due à une [[occlusion dentaire]] défectueuse. L'épuisement généré par les contractures musculaires résultant d'une posture vrillée contribuerait au syndrome de fatigue chronique rendant tout effort musculaire pénible, voire impossible. {{refnec|En outre, une partie des personnes atteintes ont une antériorité de traitements d'orthodontie, souvent avec extractions, ayant déséuilibré l'occlusion et la posture.}} |
|||
== Reconnaissance de la maladie == |
|||
=== Organisation mondiale de la santé === |
|||
L'[[Organisation Mondiale de la Santé]] reconnait la fibromyalgie comme [[rhumatisme]], sous sous son propre nom {{nobr|M 79.7}}, indiquant qu'il s'agit d'une maladie reconnue à part entière. |
|||
=== En France === |
|||
Officiellement en 2005 le gouvernement estime à 3,9~4,5 %<ref>[http://www.senat.fr/basile/rechercheQuestion.do?unk=fibromyalgie&radio=dp&dp=3+ans&de=&au=&rch=qs&ok.x=0&ok.y=0 Site du Sénat]</ref> de la population Française atteinte de fibromyalgie, environ {{nobr|3 millions}} de français, {{nobr|1 personne}} sur 25.<br /> |
Officiellement en 2005 le gouvernement estime à 3,9~4,5 %<ref>[http://www.senat.fr/basile/rechercheQuestion.do?unk=fibromyalgie&radio=dp&dp=3+ans&de=&au=&rch=qs&ok.x=0&ok.y=0 Site du Sénat]</ref> de la population Française atteinte de fibromyalgie, environ {{nobr|3 millions}} de français, {{nobr|1 personne}} sur 25.<br /> |
||
Carole Robert, pour l'association Fibromyalgie France, estimait en [[avril 2007]] que plus de {{nobr|3 millions}} de Français seraient concernés<ref>[http://fibromyalgie.ufaf.free.fr/ Association Fibromyalgie France]</ref> (soit autant que l'ensemble des personnes atteintes de maladies rares en France, selon les chiffres transmis par le ministère de la Santé et des Solidarités en [[mai 2006]]. Des pistes environnementales et génétiques sont à creuser car, selon l'association, 64 % des personnes myalgiques présentent une intolérance à des produits chimiques. |
Carole Robert, pour l'association Fibromyalgie France, estimait en [[avril 2007]] que plus de {{nobr|3 millions}} de Français seraient concernés<ref>[http://fibromyalgie.ufaf.free.fr/ Association Fibromyalgie France]</ref> (soit autant que l'ensemble des personnes atteintes de maladies rares en France, selon les chiffres transmis par le ministère de la Santé et des Solidarités en [[mai 2006]]. Des pistes environnementales et génétiques sont à creuser car, selon l'association, 64 % des personnes myalgiques présentent une intolérance à des produits chimiques. |
||
| Ligne 215 : | Ligne 262 : | ||
== Notes et références == |
== Notes et références == |
||
{{Traduction/Référence|en|Fibromyalgia|type=note}} |
|||
{{Références|colonnes=2}} |
{{Références|colonnes=2}} |
||
== Bibliographie == |
== Bibliographie == |
||
Version du 2 juin 2009 à 05:40
Modèle:CIM-10 La fibromyalgie est le terme pour désigner un syndrome connu depuis longtemps sous le nom de syndrome polyalgique idiopathique diffus (SPID), ou FMS en anglais (pour Fibromyalgia Syndrome). Le mot « fibromyalgie » vient du latin fibra (« filament »), du grec ancien myos (« muscle ») et du grec ancien algos (« douleur »).
Cette affection est caractérisée par un état douloureux musculaire chronique (myalgies diffuses) étendu à des régions du corps diverses, notamment présente sous forme d'allodynie tactile, ainsi qu'une asthénie (fatigue) persistante.
Les troubles psychologiques (chronicité des symptômes, charge psychologique) qui lui sont associés ont donné lieu à maintes hypothèses au plan psycho-pathologique. L'importance des traits anxio-dépressifs a même pu conduire à se demander laquelle de ces deux disciplines, de la rhumatologie ou de la psychiatrie, était habilitée à la prendre en charge. Les dernières découvertes tentent à prouver son aspect neurologique, lié à des déficiences en neurotransmetteurs.
Historique
Graham fait une description de la maladie dès 1953[1]. L' American College of Rheumatology committee en définit les critères en 1990[2].
Dans les années 1970 et 1980, elle est considérée comme une maladie psychiatrique avec un versant dépressif. Celà a été subdoré par le fait que les douleurs résistent aux analgésiques musculaires usuels.
L'appellation « syndrome polyalgique idiopathique diffus » (SPID) a été créé par le Professeur Kahn dans les années 1980, mais le terme anglo-saxon fibromyalgia a prévalu dans les congrès médicaux et a été francisé en « fibromyalgie ».
Ce n'est qu'en 1992 que l'Organisation mondiale de la santé a reconnu cette maladie comme rhumatismale, alors qu'elle était auparavant considérée comme une maladie psychiatrique par les médecins, du fait de sa rareté, touchant principalement les femmes, pouvant donner une certaine atteinte comportementale et n'ayant aucune trace biologique, ce « syndrome » fut attribué à tort à l'hystérie féminine. Cette supposée cause psychosomatique est désormais abandonnée.
En effet, dans les années 1990 et 2000, plusieurs études prouvent des déficiences en neurotransmetteurs chez les personnes atteintes de fibromyalgie. Et en 2006, des études démontrent par l'IRM fonctionnel une activité anormale dans la partie du cerveau qui traite la douleur chez les fibromyalgiques, inexistante chez les personnes non atteintes. Une cause exclusivement psychiatrique et/ou psychologique est exclue.
La fibromyalgie était codée M 70.0 comme rhumatisme non spécifié dans la classification internationale des maladies (CIM). Depuis janvier 2006, elle est maintenant codée sous M 79.7 sous son propre nom, indiquant qu'il s'agit d'une maladie reconnue à part entière.
Depuis 1995, il y une résurgence importante (surtout depuis 2000) de ce syndrome, de plus en plus de jeunes (moins de 30 ans) en sont affectés. De plus en plus d'hommes seraient également atteints (jusqu'à un homme pour huit femmes, à l'origine un homme pour dix femmes).[réf. nécessaire]
Épidémiologie
Une moyenne (mondiale) de 2 à 10 % (selon les pays) de la population des « pays industrialisés » est touchée par cette maladie (2 % de la population américaine avec une prédominance féminine nette[3]).
En France un rapport gouvernemental de 2007[4] donne une prévalence française estimée à 3,4 % chez la femme et à 0,5 % chez l'homme,
La fibromyalgie constitue 10 à 20% des motifs de consultation dans certains services de rhumatologie[5].
Au XXIe siècle, les spécialistes préfèrent utiliser le terme multi-fibromyalgies, certains travaux de recherches biologiques faisant état de sous-catégories.
Diagnostic
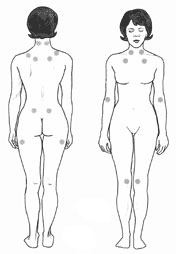
La fibromyalgie est considérée parfois comme un diagnostic controversé, certains auteurs affirmant qu'il s'agit d'un non diagnostic. En effet il n'existe pas encore de test spécifique et fiable à 100% pour la validation de la fibromyalgie. La difficulté vient essentiellement du fait que des personnes atteintes peut voir l'ensemble de ses analyses en laboratoire revenir normales. et que beaucoup des symptômes se retrouvent dans d'autres maladies (rhumatisme articulaire, ostéoporose, ...). Dans la plus part des cas, la conclusion du médecin est basée sur un diagnostic différentiel, prenant en cause l'ensemble des autres possibilités, les symptômes, ainsi que le profil du patient.
Les critères de classification les plus couramment acceptés ont été élaborés en 1990 par le Collège américain de rhumatologie[7], souvent surnommés critères "ACR 1990". Ils définissent la fibromyalgie suivant la présence des points suivants :
- Un historique de douleur répandue sur tout le corps, durant depuis plus de 3 mois, et affectant l'ensemble des quatre quadrants du corps (les deux côtés, et au dessous et en dessous de la ceinture).
- Des points douloureux, au nombre de 18 (bien que le patient puisse avoir mal à d'autres endroits du corps). Durant le diagnostique, le médecin doit exercer une force de 39 Newtons sur ces points. Le patient doit ressentir une douleur vive sur au moins 11 de ces points pour que la fibromyalgie puisse être confirmée[6]. Il faut noter que la localisation et le nombre des points douloureux peut varier selon les périodes, les circonstances...
Cet ensemble de critère a été créé dans le but de classifier les indifidus comme ayant la fibromyalgie, a des fins de recherche. Sa marge d'erreur considérée comme faible, ainsi que l'absence d'un autre test plus précis ont établi ce test de facto pour le milieu clinique.
Symptômes
Les fibromyalgies se présentent sous diverses formes de douleurs chroniques (douleurs franches, douleurs diffuses, sensations de brûlures, de coups, d'ecchymose, d'écrasement, d'arrachage, etc.) des muscles du squelette, des tendons et moins fréquemment des articulations, pouvant toucher tout le corps ou partiellement (quadrant), plus fréquemment le dos, les jambes et les bras. Ces symptômes variant tout au long de la journée, de la semaine, du mois, de l'année. Le patient fibromyalgique a tout ou partie des symptômes suivants :
- douleurs musculaires, osseuses, des articulations, des tendons ;
- fatigue physique ;
- fatigue psychique, sensation de vide psychologique, regard vague ;
- irritabilité générale (au toucher, aux sollicitations, au bruit, à la lumière, à la présence d'autrui, à des odeurs inhabituelles, à l'odeur de nourriture, etc.) et impatience ;
- pensées suicidaires constantes, dépression nerveuse ;
- besoin de consommer des glucides (gâteaux, pain, pommes de terre, frites, etc.) ;
- troubles assez sévères de la mémoire (court ou long terme) ;
- sensations de brûlures, de coups, de bleus, d'écrasement, d'arrachage, etc. ;
- troubles du système digestif (diarrhées, ballonnements) ;
- dessèchement et brûlure des yeux ;
- insomnie, grande difficulté à dormir et à se régénérer lors du sommeil ;
- chaleur au niveau de la paume des mains et de la plante des pieds (jusqu'au besoin de passer ses mains et/ou ses pieds sous l'eau du robinet pour soulager la douleur) ;
- très grande difficulté à se concentrer, surtout pour lire, pour se concentrer sur ce que dit un interlocuteur ;
- aggravation des symptômes avec la consommation de sucre et de produits sucrés ou avec la faim ;
- Au moins onze points douloureux sur les 18 indiqués dans le test ACR
- tremblements, sensations de faiblesse ;
- sensation d'avoir le corps rouillé, rigide, courbattu.
Ces troubles sont souvent associés à des problèmes gastro-intestinaux (allergie au gluten, syndrôme du côlon irritable ...) et à des maux de tête.[7],[8] Le quotidien d'un fibromyalgique peut être aisément comparé à celui d'une personne atteinte de polyarthrite rhumatoïde.
Pathophysiologie
Anomalies du liquide cérébro-spinal
La découverte la plus systématiquement reproduite en laboratoire est une concentration haute, chez les sujets atteints, des niveaux en substance P, un neurotransmetteur lié à la perception de la douleur.[9],[10],[11] La présence des métabolites servant à la formations des neurotransmetteurs monoamines serotonine, [[norepinephrine}}, et dopamine— qui jouent tous un rôle dans l'analgésie naturelle du corps, ont été prouvé comme étant anormalement basses.[12] alors que la concentratnion des opïacés endogènes (comme l'endorphine et l'enképhaline) semblent être plus hautes que la normale.[13] Une concentration élevée visible en facteur de croissance nerveuse (Nerve Growth Factor) a été prouvée. Cette substance est connue pour participer à la structuration et à la plasticité des interconnexions entre le cerveau et la moelle épinière.[14] Il y a également des preuves d'une stimulation accrue des acides aminés au sein du liquide cérébro-spinal, avec une corrélation prouvée entre les niveaux des métabolites de glutamates et d'oxyde nitrique et la sensation de douleur.[15]
Troubles du sommeil décelés par un encéphalogramme
Les premières découvertes objectives associées à la maladie ont été rapportée en 1975 où ont été démontrées la présences d'ondes alpha (associées usuellement à des phases de sommeil léger) anormales en phase 4 (sommeil profond) durant l'encélaphogramme de patients fibromyalgiques.[16]
En fait, en interrompant le sommeil de phase 4 constamment sur des sujets jeunes et en bonne santé, Moldofsky et son équipe ont été capable de reproduire une tension musculaire supposée comparable à celle des patients fibromyalgiques. Cependant ces sensations ont disparu lorsque les sujets ont pu retrouver un sommeil normal.[17]
Depuis cette étude, de nombreuses études confirment des anomalies variées dans des sous-groupes de patients fibromyalgiques.[18]
Imagerie du cerveau
La preuve d'une réaction anormale du cerveau dans le cadre de la fibromyalgie a été prouvée par imagerie cérébrale fonctionnelle. Les premières découvertes font état d'une circulation sanguine diminuée dans le thalamus, des ganglions de la base et de certaines zones médiannes du cerveau.[19][20] Une activation différée de ces zones dans la réaction à la douleur a également été prouvée.[21][22]
Sensibilité polymodale
Plusieurs études résultant de stimulation expérimentale ont démontré que les patients fibromyalgiques démontrent une sensibilité accrue à la pression, aux sensations de chaleur et de froid, , à des stimulations électriques et chimiques.[23] Des expérimentation sur les systèmes régulateurs de la douleur ont montré que les patients atteints de fibromyalgie montrent aussi une dérégulation de différents mécanismes inhibiteurs de la douleur.[24] Elles démontrent également une réaction exagéré à un stimuli répété,[25] et la diminution ou l'absence de la réaction analgésique induite par l'effort physique.[26] Ensemble, ces résutlants pointent une dérégulation du système nerveux central.
Perturbation neuroendocrinienne
Les études de patients atteints de fibromyalgie ont démontré des anomalies dans les fonctions neuroendocriniennes usuelles comme une hypocortisolemie,[27] une sécrétion excessive de l'hormone adrenocorticotropine en réponse à une stimulation, et une résistance au feedback glucocorticoïde.[28] Une réduction progressive de la présence d'hormone de croissance humaine a aussi été démontré sur certains groupes patients, alors que la plus part démontrent des sécrétions hormonales diminuées façe à des efforts physiques intentses, ou à des stimulations pharmaceutiques.[29] D'autres anomalies incluent un temps de réponse réduit de la thyrotropine et des hormones thyroïdiennes lors de stimulations hormonales,[30]. Une hausse relativement élevée des niveaux de prolactine, avec une déshinibition de la sécrétion de prolactine lors de stimulations hormonales [31] et une sécrétion insuffisante des hormones produites par les glandes surrénales ont également été constatés.[32]
Ces changements pourraient être attribués aux effets du stress chronique que cause la maladie, qui après avoir été reçu et traité par le système nerveux central, activent la sécrétion d'hormones neuronales corticotrophines hypotalamiques. Cela résulterait en une perturbation de la communication Hypophyse-Glande Surrénale, et en un excès en somatostatine hypothalamique, qui en retour, inhibent la sécrétion d'un certain nombre d'autres hormones.[33]
Hyperactivité du système nerveux sympathique
Une analyse a démontré une activité perturbée et excessive du système nerveux sympathique.[34] with reduced sympathoadrenal reactivity in response to a variety of stressors including physical exertion and mental stress.[35][36] Fibromyalgia patients demonstrate lower heart rate variability, an index of sympathetic/parasympathetic balance, indicating sustained sympathetic hyperactivity, especially at night.[37] De plus, les niveaux en neuropeptide Y dans le plasma sont bas chez les malades; ce neuropetide localisé avec la norepinephrine dans le système nerveux sympathique.[38]. A l'inverse les niveaux circulatoires d'epinephrine et de norepinephrine ont été parfois décris comme haut, bas et normaux.[39][40]
L'injection d'interleukine-6 (une cytokine capable de stimuler la production d'hormone de sécrétion de corticotropine hypotalamique, qui à son tour stimule l'activité du système nerveux sympatique) provoque une hausse forte des niveaux circulatoire de norepinephrine, et une hausse du rythme cardiaque. Ces hausses sont plus fortes chez les patients fybromyalgique que chez les personnes saines.[41]
Facteurs aggravants
Les symptômes de la fibromyalgie seraient aggravés[42] notoirement dans les conditions suivantes, liées au stress, et qui peuvent déclencher des réactions au niveau des neurotransmetteurs ou des hormones :
- traumatisme, stress et choc émotionnel;
- autre maladie ;
- bruit ;
- entourage de personnes ;
- manque de protéines dans l'alimentation ;
- quantité de nourriture insuffisante ;
- mauvaise gestion du sommeil (quantité insuffisante ou excessive);
- fatigue ou effort physique trop important ;
- Chaleur et canicule ;
- Froid ;
- Utilisation de produits influant sur les neurotransmetteurs (tabac...).
Pour certains patients les cycles correspondent à :
- une barosensibilité - réaction aux changements de la pression atmosphérique ;
- une hygrosensibilité - réaction au taux d'humidité ;
- une thermosensibilité - réaction à la température.
On parle globalement d'hypersensibilité.
Fatigue chronique
S'ajoute une fatigue dite « chronique » réactionnelle (à ne pas confondre avec le syndrome de fatigue chronique, que peuvent avoir en plus certains fibromyalgiques). Le syndrome de fatigue chronique n'est pas lié à un excès de substance P. Les mécanismes responsables de la douleur sont probablement différents pour ces deux conditions[43])
Un enchaînement dans le sens « fatigue de l'organisme » (attaques virales, infections répétitives, résistances), puis « syndrome de fatigue chronique », puis fibromyalgie est plus que probable pour certains.
Variabilité des symptômes
Il existe diverses formes de sévérités à la fibromyalgie, pouvant éventuellement correspondre à diverses causes, ou à différentes variantes de la maladie. La problématique étant de trouver une échelle (un marqueur) de sévérité fiable, inexistant du fait qu'aucun marqueur n'a encore été mis à jour. Cependant certains travaux de recherches tendent à prouver qu'il existe une corrélation entre substance P (un neurotransmetteur) et sévérité des symptômes.
Etant donné l'implication des neurotransmetteurs dans la maladie, chaque fibromyalgique a ses cycles, ses symptômes, d'intensités et de durées variables. Les variantes d'atteintes de fibromyalgies sont très larges, d'une fibromyalgie peu sévère permettant de garder une vie presque « normale » à la fibromyalgie sévère handicapante il y a un panache de variantes très difficilement classifiables.
La subjectivité, l'interprétation de ses symptômes, l'interprétation du médecin, la tolérance à la douleur, les aléas des symptômes, les rémissions, les intensités, les amplitudes, la gestion psychologique, la chronicité, les échecs thérapeutiques, les échecs de dialogue, de compréhension, ainsi de suite, amène une pathologie très complexe pour le patient, et encore plus complexe à transmettre.
On retrouve cependant quelques points communs comme une prédominance de raideurs et une grosse fatigue au réveil pouvant s'atténuer à plus ou moins long terme indépendamment de chaque symptôme (de quelques minutes à quelques heures, voires persistant la journée, plusieurs jours), une fatiguabilité exacerbée, des troubles du sommeil (pas de sommeil profond, points d'appuis gênants/douloureux, agitations), puis tout un ensemble d'autres symptômes satellites dont les plus courants sont des migraines, des troubles de la concentration (variable), des troubles de la mémoire (mémoire à court terme), des troubles de la vision (brouillard, décalage), une certaine irritabilité, des sauts d'humeur, des problèmes du comportement (attitude), d'élocution (concentration, mémoire, fatigue), des troubles digestifs, le syndrome des jambes sans repos, maladie de Raynaud, acouphènes, picotements, démangeaisons, impatience, etc.
Un tiers des fibromyalgiques présentent une dépression, voire un état névrotique de type hystérique, pour certains du type réactionnel (charge psychologique, atteinte neurologique sévère). La prévalence de la dépression est plus importante chez les patients souffrant de fibromyalgie que dans la population générale, mais elle reste comparable à celle qu’on observe dans d’autres contextes de douleurs chroniques[44]. Comme c'est le cas dans les autres pathologies chroniques, ces éléments d'anxiété et de dépression ne permettent pas, cependant, de préjuger d'une personnalité morbide pré-existante ; ils seraient bien être la conséquence de la chronicité de la douleur.
Ce syndrome, restant mal perçu et peu reconnu, tant par l'entourage, que par les administrations, voire certains médecins, il peut pousser les personnes malades à l'isolement, voire à la dépression et/ou à la culpabilité de souffrir et de devenir handicapé par cet état douloureux et épuisant.
Traitement
Bien qu'il n'y ait pas de traitement ayant démontré une efficacité globale, il existe des solutions ayant des effets cliniques prouvés, incluant certains médicament, de l'exercice, et une éducation du patient.[45]
Les traitements reposent au cas par cas sur des antidouleurs et/ou des antidépresseurs et/ou des antiépileptiques, ces deux derniers étant prescrits pour leurs effets antalgiques sur le système nerveux central (et non pas pour une dépression avec les antidépresseurs) et doivent être associé à une réadaptation fonctionnelle basée sur des exercices physiques permettant d'augmenter le seuil de la douleur.
Les antidépresseurs les plus efficaces sembles être ceux de la classe des tricycliques, avec une amélioration de la qualité de vie et la diminution des douleurs[46].
Chacun ayant son seuil de tolérance à l'effort et à la douleur, ainsi qu'une atteinte plus ou moins sévère incalculable, il n'est pas simple de généraliser. Pour certains la marche est juste supportable et variable, pour d'autres une activité « pleine et normale » est réalisable.
La prise en compte des conséquences psychiques peut comporter :
- écoute active par un psychiatre, psychanalyste, psychologue ou psychothérapeute ;
- une proposition d'exercices - différentes approches de la relaxation, détente en eau chaude, méthode Feldenkrais, etc. ;
- séjour en lieu calme avec repos.
En 2008 il n'existe pas de traitement curatif, aucun traitement n'est efficace sur le long terme et aucun régime n'a prouvé son efficacité. Le Lyrica[47], un antalgique, semble avoir une bonne efficacité sur la maladie[48].
À noter que certaines personnes affectées ont constaté une rémission partielle en suivant un régime strict sans gluten. Cela pourrait être lié à une inflammation spécifique de l'appareil digestif générant des toxines particulières, mais cela reste éminemment conditionnel. Cela pourrait également être lié au rôle de la sérotonine dans l'allergie au gluten aggravée [49] (sa destruction par la réaction immunitaire de l'allergie peut causer des symptômes similaires à la fibromyalgie[50] [51]), une autre étude prouvant la rémission de formes de maladies neuronales après une diète sans gluten pour des patients allergiques[52],[53] [54]. Il existerait un nombre relativement visible de personnes à la fois fibromyalgiques et allergiques au gluten.[55]
Causes supposées
À partir de 2000-2004, les scientifiques se penchent de plus en plus vers des désordres de natures immuno-chimiques et/ou environnementaux, compte tenu de la résurgence surprenante de cas. Une atteinte du système nerveux central et un dérèglement neuronal ont été largement constatés chez les fibromyalgiques.
Il semble exister une perception différente de la douleur chez le fibromyalgique, avec en particulier, un seuil de perception plus bas[56]. Le mécanisme de ce fait est toujours débattu, mais lourdement supposé lié aux neurotransmetteurs responsables du traitement de la douleur.
Il est possible que les différentes variantes de fibromyalgie soient liés à une combinaise d'une ou plusieurs de ces causes suposées.
Prédisposition génétique
Outre le fait que cette maladie touche beaucoup plus de femmes que d'hommes, il existe de nombreuses preuves qu'un facteur génétique puisse jouer un rôle important dans le développement de la fibromyalgie.[57][58][59] Par exemple, il existe beaucoup de familles présentants plusieurs personnes atteintes[60][61] Le mode de transmission est encore inconnu mais est probablement polygénique.[62] Les recherches ont démontrés que la fibromyalgie est associée à des variation (ou polymorphisme) sur les gènes de production de la serotonine,[63] dopamine[64] et catecholamine.[65] Cependant ces polymorphismes ne sont pas spécifiques à la fibromyalgie, et sont associés à une variétés d'autres maladies (comme le syndrôme de fatigue chronique,[66] syndrôme du côlon_irritable[67]) et certaines formes de dépression [68]
Hypothèse d'un dérèglement des neurotransmetteurs
Une déficience dans certains neurotransmetteurs (excès de substance P, manque de sérotonine et de noradrénaline) a été identifiée[69],[70],[71]. L'excès de substance P est reconnu pour provoquer une hyperalgésie[72],[73], une réduction de la sérotonine et/ou de la noradrénaline produit également une hyperalgésie par la réduction des systèmes inhibiteurs de la douleur[74],[75] .
Les taux plus élevés d'anticorps anti-sérotonine dans le sang, de facteurs de croissance[76],[77] dans le liquide céphalo-rachidien[78] et des variations du système de réponse inflammatoire viennent corroborer cette hypothèse. Certains docteurs posent désormais clairement l'existance d'une composante auto-immune de la fibromyalgie[79],[80].
Un lien a également été prouvé entre fabrication des monoamines et fibromyalgie[81]. Des gènes, responsables de la fabriquation des monoamines, ont été identifiés comme déficients. Ces monoamines comprennent la sérotonine et les catécholamines, qui servent à fabrication de la dopamine, de l'adrénaline et de la noradrénaline. Ces neuromédiateurs, substances ayant un rôle pour transmettre l'influx nerveux, et qui influent sur l'anxiété, le stress et le moral seraient en nombre insuffisants chez les fibromyalgiques[82].
Hypothèse d'un dérèglement immunologique
D'autres études tentent à démontrer que les cytokines, impliquées dans le système immunitaire auraient une action perturbée chez les personnes atteintes de fibromyalgie.Il existerait donc une cause de survenue de la fibromyalgie mettant en cause un phénomène immunologique en relation étroite avec un phénomène neurologique[83],[84]. Ces études, restantes à être confirmées, car portant sur un nombre réduits de patients, prouvent que ces personnes atteintes de fibromyalgie ont un excès en cytokine, qui peut provoquer un excès en substance P. Le niveau de cytokine observé augmenterait avec la durée de la maladie. On remarque également des niveaux de cytokine élevés chez les personnes manquant de sommeil[85]. Il est actuellement impossible de déterminer si le manque de sommeil des fibromyalgiques est à l'origine de ce niveau de cytokine, ou si le taux de cytokine est à même de provoquer les maux, et donc l'absence de sommeil.
Hypothèse d'un dysfonctionnement de l'irrigation du cerveau
Fin 2008, une équipe de chercheurs du Centre hospitalo-universitaire de la Timone à Marseille, dirigée par le professeur Eric Guedj, a identifié une anomalie[86] au niveau de la circulation sanguine dans le cerveau de patients atteints de fibromyalgie, grâce à une tomographie à émission de photons (SPECT). L'étude a permis de découvrir que chez les patients atteints de fibromyalgie, certaines régions du cerveau sont trop irriguées, alors que d'autres le sont insuffisamment. Cette irrégularité modifie la manière donc le patient ressent et traite la douleur. Les chercheurs ont en outre identifié des liens entre le flux sanguin de certaines zones du cerveau et l'anxiété, les douleur intempestives, le handicap et la dépression nerveuse. Les chercheurs ont identifié une augmentation de la circulation du sang dans certaines zones du cerveau qui servent à ressentir la douleur, alors qu'une diminution du flux sanguin a été identifié dans une autre zone chargée de la réponse émotionnelle à la douleur.
Hypothèse de troubles du sommeil
Des études d'électroencéphalogrammes du sommeil ont prouvé que les personnes atteintes de fibromyalgie manquent de la phase de sommeil profond, et que les circonstances influant le sommeil de phase 4 (douleur, dépression, manque de sérotonine, certains médicaments, anxiété...) peuvent causer ou aggraver la maladie.[87] Selon cette hypothèse d'une perturbation du sommeil, un évènement, tel un traumatisme, peut causer une perturbation du sommeil, causant la douleur initiale du processus.
Cette hypothèse repose sur l'hypothèse que le sommeil de stage 4 est critique pour le fonctionnement du système nerveux, sachant que certains processus neurochimiques redémarrent durant cette phase. En particulier, la douleur cause la sécrétion d'une neuropeptide, la substance P dans la Moelle épinière qui a pour effet d'amplifier la douleur et rend les nerfs plus sensibles à la douleur. Dans des circonstances normales, les zones autour d'une blessure deviennent plus sensibles à la douleurs, mais si la douleur devient chronique, ce processus peut dérailler et s'étendre.
Cette hypothèse repose sur l'hypothèse que le sommeil profond permettrait de réinitialiser le mécanisme de la substance P, et qu'un manque de sommeil pourrait alors devenir une cause de la maladie.
Hypothèse d'une déficience en hormone de croissance humaine
Une hypothèse alternative suggère que des problèmes induits par le stress, dans l'hypothalamus peuvent conduire à un sommeil réduit et réduit la production d'hormone de croissance humaine durant le sommeil profond. Les gens atteints de fibromalgies tendent à produire des niveaux inadéquats de cette hormone[réf. nécessaire]. Cette théorie est supportée par le fait que plusieurs substances, qui sont produites sous le contrôle direct ou indirect de cette hormone (comme IGF-1, cortisol, leptine et le neuropeptide Y) atteignent des niveaux anormaux avec les personnes atteintes de fibromyalgie.[88] De plus, des traitements avec injection d'hormone de croissance réduit la douleur induite par la maladie, et permettrait l'obtention de sommeil profond[89],[90][91],[92]; l'influence de l'hormone de croissance fait encore débat, d'autres études ne faisant pas cas d'un manque de cette hormone chez d'autres patients[93].
Hypothèse d'un dérèglement hormonal lié au stress
Des études montrent que le stress est un facteur aggravant significatif dans le développement de la fibromyalgie.[94]
En conséquence il a été avancé que la fibromialgie puisse résulter d'un dysfonctionnement induit par le stress, notamment dans la fonction et l'intégrité de l'hippocampe.[95] Cettre proposition est basée sur des études pré-cliniques sur des singes, qui ont montré que l'exposition à un stress psychosocial peut avoir des conséquences physiques sur les tissus du cerveau, incluant de l'atrophie et des changements métaboliques de hippocampe.[96],[97]
Cette hypothèse est soutenue par deux études qui ont utilisé un spectroscope à résonance magnétique pour trouver des anomalies métaboliques dans l'hippocampe de patients atteints de fibromyalgie, avec une corrélation significative entre anomalies et sévérité des symptômes cliniques.[98][99] Il est actuellement impossible de déduire si le stress a provoqué la malformation de l'hippocampe, ou si la maladie est la cause de la malformation.
Un autre mécanisme reconnu est le dérèglement de l'axe hypothala-hypophysaire-surrénalien[100],[101] , qui influe sur le stress, et peut provoquer une variation cyclique des symptômes[102].
Autres hypothèses
D'autres hypothèses ont été avancées, comme :
- une cause virale comme le virus Epstein-Barr[105]
- une réaction immunitaire anormale à une bactérie intestinale[106]
- Une érosion de la gaine chimique autour des nerfs sensoriels.[107]
- une dérégulation de la vasomotricité résultant en une ischémie des muscles ou une circulation sanguine anormale[108]
- une dégradation de la posture causée par la dysfonction de l'articulation temporo-mandibulaire, elle-même due à une occlusion dentaire défectueuse. L'épuisement généré par les contractures musculaires résultant d'une posture vrillée contribuerait au syndrome de fatigue chronique rendant tout effort musculaire pénible, voire impossible. En outre, une partie des personnes atteintes ont une antériorité de traitements d'orthodontie, souvent avec extractions, ayant déséuilibré l'occlusion et la posture.[réf. nécessaire]
Reconnaissance de la maladie
Organisation mondiale de la santé
L'Organisation Mondiale de la Santé reconnait la fibromyalgie comme rhumatisme, sous sous son propre nom M 79.7, indiquant qu'il s'agit d'une maladie reconnue à part entière.
En France
Officiellement en 2005 le gouvernement estime à 3,9~4,5 %[109] de la population Française atteinte de fibromyalgie, environ 3 millions de français, 1 personne sur 25.
Carole Robert, pour l'association Fibromyalgie France, estimait en avril 2007 que plus de 3 millions de Français seraient concernés[110] (soit autant que l'ensemble des personnes atteintes de maladies rares en France, selon les chiffres transmis par le ministère de la Santé et des Solidarités en mai 2006. Des pistes environnementales et génétiques sont à creuser car, selon l'association, 64 % des personnes myalgiques présentent une intolérance à des produits chimiques.
En 2006, le ministre de la Santé a commandé un rapport sur la fibromyalgie à un groupe de travail de l'Académie nationale de médecine, coordonné par Charles Joël Menkes (rhumatologue) et Pierre Godeau (interniste), rendu en janvier 2007. Ce rapport reconnait « la réalité de ce syndrome douloureux chronique et même sur sa fréquence », mais « tout en entretenant des doutes sur la légitimité d'en faire une maladie, avec les conséquences médico-sociales qui peuvent en résulter »». Le rapport note aussi la difficulté de mesure des symptômes en raison du « caractère subjectif des troubles invoqués (douleur, fatigue, mal-être, troubles du sommeil) [...] » ou encore le caractère « artificiel et abusif des critères de classification quand on les utilise à tort comme critères de diagnostic ».
Le ministère aurait aussi prévu[111] une enquête épidémiologique, mais l'Institut de Veille Sanitaire attendait toujours, en avril 2007, une définition du ministère pour cette maladie, étude demandée en 2002. La reconnaissance de l'OMS devrait accélérer la reconnaissance au niveau national et l'intensification nécessaire de la recherche.
Pour l'instant, l'évaluation est laissée à « l'appréciation » du médecin conseil, décidant le temps d'une consultation sur le motif de convocation « fibromyalgie », et se référant au « rapport de l'Académie de médecine », incomplet.
Notes et références
- Graham W., The fibrosits syndrome, Bull Rheum Dis. 1953;3:33-4
- Wolfe F, Smythe HA, Yunus MB, Bennett RM, Bombardier C, Goldenberg DL, et al, The American College of Rheumatology 1990 criteria for the classification of fibromyalgia. Report of the multicenter criteria committee, Arthritis Rheum, 1990;33:160-72
- Wolfe F, Ross K, Anderson J, Russell IJ, Hebert L., The prevalence and characteristics of fibromyalgia in the general population, Arthritis Rheum, 1995;38:19-28
- Ministère de la Santé et des Solidarités, publiée dans le JO Sénat du 3 mai 2007, p. 915
- Données du service Algologie/Clinique Catherine de Sienne/Nantes
- National Institute of Arthritis and Musculoskeletal and Skin Diseases, « Questions and Answers About Fibromyalgia – How Is Fibromyalgia Diagnosed? », National Institutes for Health,
- Wolfe F, Snilders AMJ, Yunus MB, et al. The Amerian College of Rhumatology 1990 criteria for the classification of fibromylagia: report of the Multicenter Criteria Commitee. Arthritis Rheum 1990; 33:160-172.
- Clauw DJ. The pathogenesis of chronic pain and fatigue syndromes, with special reference to fibromyalgia. Med Hypotheses 1995; 44(5):369-3
- Russell IJ, Orr MD, Littman B, et al., « Elevated cerebrospinal fluid levels of substance P in patients with the fibromyalgia syndrome », Arthritis Rheum., vol. 37, no 11, , p. 1593–601 (PMID 7526868, DOI 10.1002/art.1780371106)
- Vaerøy H, Helle R, Førre O, Kåss E, Terenius L, « Elevated CSF levels of substance P and high incidence of Raynaud phenomenon in patients with fibromyalgia: new features for diagnosis », Pain, vol. 32, no 1, , p. 21–6 (PMID 2448729, DOI 10.1016/0304-3959(88)90019-X, lire en ligne)
- Evengard B, Nilsson CG, Lindh G, et al., « Chronic fatigue syndrome differs from fibromyalgia. No evidence for elevated substance P levels in cerebrospinal fluid of patients with chronic fatigue syndrome », Pain, vol. 78, no 2, , p. 153–5 (PMID 9839828, DOI 10.1016/S0304-3959(98)00134-1, lire en ligne)
- Russell IJ, Vaeroy H, Javors M, Nyberg F, « Cerebrospinal fluid biogenic amine metabolites in fibromyalgia/fibrositis syndrome and rheumatoid arthritis », Arthritis Rheum., vol. 35, no 5, , p. 550–6 (PMID 1374252, DOI 10.1002/art.1780350509)
- Vaerøy H, Nyberg F, Terenius L, « No evidence for endorphin deficiency in fibromyalgia following investigation of cerebrospinal fluid (CSF) dynorphin A and Met-enkephalin-Arg6-Phe7 », Pain, vol. 46, no 2, , p. 139–43 (PMID 1684241, DOI 10.1016/0304-3959(91)90068-9, lire en ligne)
- Giovengo SL, Russell IJ, Larson AA, « Increased concentrations of nerve growth factor in cerebrospinal fluid of patients with fibromyalgia », J Rheumatol., vol. 26, no 7, , p. 1564–9 (PMID 10405946)
- Larson AA, Giovengo SL, Russell IJ, Michalek JE, « Changes in the concentrations of amino acids in the cerebrospinal fluid that correlate with pain in patients with fibromyalgia: implications for nitric oxide pathways », Pain, vol. 87, no 2, , p. 201–11 (PMID 10924813, DOI 10.1016/S0304-3959(00)00284-0, lire en ligne)
- Erreur Lua dans Module:Date à la ligne 387 : attempt to index field '?' (a nil value).
- Erreur Lua dans Module:Date à la ligne 387 : attempt to index field '?' (a nil value).
- Drewes AM, Gade K, Nielsen KD, Bjerregård K, Taagholt SJ, Svendsen L, « Clustering of sleep electroencephalographic patterns in patients with the fibromyalgia syndrome », Br J Rheumatol., vol. 34, no 12, , p. 1151–6 (PMID 8608357, DOI 10.1093/rheumatology/34.12.1151, lire en ligne)
- Mountz JM, Bradley LA, Modell JG, et al., « Fibromyalgia in women. Abnormalities of regional cerebral blood flow in the thalamus and the caudate nucleus are associated with low pain threshold levels », Arthritis Rheum., vol. 38, no 7, , p. 926–38 (PMID 7612042, DOI 10.1002/art.1780380708)
- Kwiatek R, Barnden L, Tedman R, et al., « Regional cerebral blood flow in fibromyalgia: single-photon-emission computed tomography evidence of reduction in the pontine tegmentum and thalami », Arthritis Rheum., vol. 43, no 12, , p. 2823–33 (PMID 11145042, DOI 10.1002/1529-0131(200012)43:12<2823::AID-ANR24>3.0.CO;2-E)
- Gracely RH, Petzke F, Wolf JM, Clauw DJ, « Functional magnetic resonance imaging evidence of augmented pain processing in fibromyalgia », Arthritis Rheum., vol. 46, no 5, , p. 1333–43 (PMID 12115241, DOI 10.1002/art.10225)
- Cook DB, Lange G, Ciccone DS, Liu WC, Steffener J, Natelson BH, « Functional imaging of pain in patients with primary fibromyalgia », J Rheumatol., vol. 31, no 2, , p. 364–78 (PMID 14760810, DOI 10.1093/rheumatology/31.6.364, lire en ligne)
- Desmeules JA, Cedraschi C, Rapiti E, et al., « Neurophysiologic evidence for a central sensitization in patients with fibromyalgia », Arthritis Rheum., vol. 48, no 5, , p. 1420–9 (PMID 12746916, DOI 10.1002/art.10893)
- Kosek E, Hansson P, « Modulatory influence on somatosensory perception from vibration and heterotopic noxious conditioning stimulation (HNCS) in fibromyalgia patients and healthy subjects », Pain, vol. 70, no 1, , p. 41–51 (PMID 9106808, DOI 10.1016/S0304-3959(96)03295-2, lire en ligne)
- Staud R, Vierck CJ, Cannon RL, Mauderli AP, Price DD, « Abnormal sensitization and temporal summation of second pain (wind-up) in patients with fibromyalgia syndrome », Pain, vol. 91, nos 1-2, , p. 165–75 (PMID 11240089, DOI 10.1016/S0304-3959(00)00432-2, lire en ligne)
- Staud R, Robinson ME, Price DD, « Isometric exercise has opposite effects on central pain mechanisms in fibromyalgia patients compared to normal controls », Pain, vol. 118, nos 1-2, , p. 176–84 (PMID 16154700, DOI 10.1016/j.pain.2005.08.007)
- Gur A, Cevik R, Sarac AJ, Colpan L, Em S, « Hypothalamic-pituitary-gonadal axis and cortisol in young women with primary fibromyalgia: the potential roles of depression, fatigue, and sleep disturbance in the occurrence of hypocortisolism », Ann. Rheum. Dis., vol. 63, no 11, , p. 1504–6 (PMID 15479904, PMCID 1754816, DOI 10.1136/ard.2003.014969)
- Griep EN, Boersma JW, Lentjes EG, Prins AP, van der Korst JK, de Kloet ER, « Function of the hypothalamic-pituitary-adrenal axis in patients with fibromyalgia and low back pain », J. Rheumatol., vol. 25, no 7, , p. 1374–81 (PMID 9676772)
- Bennett RM, « Adult growth hormone deficiency in patients with fibromyalgia », Curr Rheumatol Rep, vol. 4, no 4, , p. 306–12 (PMID 12126582, DOI 10.1007/s11926-002-0039-4)
- Neeck G, Riedel W, « Thyroid function in patients with fibromyalgia syndrome », J. Rheumatol., vol. 19, no 7, , p. 1120–2 (PMID 1512769)
- Riedel W, Layka H, Neeck G, « Secretory pattern of GH, TSH, thyroid hormones, ACTH, cortisol, FSH, and LH in patients with fibromyalgia syndrome following systemic injection of the relevant hypothalamic-releasing hormones », Z Rheumatol, vol. 57 Suppl 2, , p. 81–7 (PMID 10025090, DOI 10.1007/s003930050242, lire en ligne)
- Dessein PH, Shipton EA, Joffe BI, Hadebe DP, Stanwix AE, Van der Merwe BA, « Hyposecretion of adrenal androgens and the relation of serum adrenal steroids, serotonin and insulin-like growth factor-1 to clinical features in women with fibromyalgia », Pain, vol. 83, no 2, , p. 313–9 (PMID 10534604, DOI 10.1016/S0304-3959(99)00113-X, lire en ligne)
- Neeck G, Crofford LJ, « Neuroendocrine perturbations in fibromyalgia and chronic fatigue syndrome », Rheum. Dis. Clin. North Am., vol. 26, no 4, , p. 989–1002 (PMID 11084955, DOI 10.1016/S0889-857X(05)70180-0)
- Martinez-Lavin M. Biology and therapy of fibromyalgia. Stress, the stress response system, and fibromyalgia. Arthritis Res Ther. 2007;9(4):216.
- Giske L, Vøllestad NK, Mengshoel AM, Jensen J, Knardahl S, Røe C, « Attenuated adrenergic responses to exercise in women with fibromyalgia--a controlled study », Eur J Pain, vol. 12, no 3, , p. 351–60 (PMID 17827042, DOI 10.1016/j.ejpain.2007.07.007)
- Nilsen KB, Sand T, Westgaard RH, Stovner LJ, White LR, Bang Leistad R, Helde G, Rø M. Autonomic activation and pain in response to low-grade mental stress in fibromyalgia and shoulder/neck pain patients. Eur J Pain. 2007 Oct;11(7):743-55.
- Martínez-Lavín M, Hermosillo AG, Mendoza C, et al., « Orthostatic sympathetic derangement in subjects with fibromyalgia », J. Rheumatol., vol. 24, no 4, , p. 714–8 (PMID 9101507)
- Anderberg UM, Liu Z, Berglund L, Nyberg F, « Elevated plasma levels of neuropeptide Y in female fibromyalgia patients », Eur J Pain, vol. 3, no 1, , p. 19–30 (PMID 10700334, DOI 10.1016/S1090-3801(99)90185-4)
- van Denderen JC, Boersma JW, Zeinstra P, Hollander AP, van Neerbos BR, « Physiological effects of exhaustive physical exercise in primary fibromyalgia syndrome (PFS): is PFS a disorder of neuroendocrine reactivity? », Scand. J. Rheumatol., vol. 21, no 1, , p. 35–7 (PMID 1570485, DOI 10.3109/03009749209095060)
- Adler GK, Kinsley BT, Hurwitz S, Mossey CJ, Goldenberg DL, « Reduced hypothalamic-pituitary and sympathoadrenal responses to hypoglycemia in women with fibromyalgia syndrome », Am J Med., vol. 106, no 5, , p. 534–43 (PMID 10335725, DOI 10.1016/S0002-9343(99)00074-1, lire en ligne)
- Torpy DJ, Papanicolaou DA, Lotsikas AJ, Wilder RL, Chrousos GP, Pillemer SR, « Responses of the sympathetic nervous system and the hypothalamic-pituitary-adrenal axis to interleukin-6: a pilot study in fibromyalgia », Arthritis Rheum., vol. 43, no 4, , p. 872–80 (PMID 10765933, DOI 10.1002/1529-0131(200004)43:4<872::AID-ANR19>3.0.CO;2-T)
- http://www.fibromyalgiesos.com/fm/zFibromyalgievulgarismedicalMartzolff.pdf
- Evengard B, Nilsson CG, Lindh G, Lindquist L, Eneroth P, Fredrikson S et al. Chronic fatigue syndrome differs from fibromyalgia. No evidence for elevated substance P levels in cerebrospinal fluid of patients with chronic fatigue syndrome. Pain 1998; 78(2):153-155.
- Thieme K, Turk DC, Flor H. Comorbid depression and anxiety in fibromyalgia syndrome: relationship to somatic and psychosocial variables. Psychosom Med. 2004;66:837–44.
- Goldenberg DL (2008). "Multidisciplinary modalities in the treatment of fibromyalgia". J Clin Psychiatry 69: 30–4. PMID 18537461. [1]
- Häuser W, Bernardy K, Üçeyler N, Sommer C, Treatment of fibromyalgia syndrome with antidepressants, a meta-analysis, Jama, 2009;301:198-209
- Page sur le Lyrica sur le site des laboratoires Pfizer
- Communiqué de l'agence Reuters sur l'autorisation de commercialisation de Lyrica dans la fibromyalgie
- Chiaravalloti G, et al. Platelet serotonin transporter in celiac disease. Acta Paediatr. 1997 Jul;86(7):696-9.
- Cronin CC, et al. Celiac disease and epilepsy. QJM. 1998 Apr;91(4):303-8.
- Bernasconi A, et al. Celiac disease, bilateral occipital calcifications and intractable epilepsy: mechanisms of seizure origin. Epilepsia. 1998 Mar;39(3):300-6.
- Hallert C, et al. Psychic disturbances in adult celiac disease. III. Reduced central monoamine metabolism and signs of depression. Scand J Gastroenterol. 1982 Jan;17(1):25-8.
- De Santis A, et al. Schizophrenic symptoms and SPECT abnormalities in a celiac patient: regression after a gluten-free diet. J Intern Med. 1997 Nov;242(5):421-3.
- Hernandez MA, et al. Epilepsy, cerebral calcifications and clinical or subclinical celiac disease. Course and follow up with gluten-free diet. Seizure. 1998 Feb;7(1):49-54
- Wallace DJ, Hallegua DS. Fibromyalgia: the gastrointestinal link. ; Curr Pain Headache Rep. 2004 Oct;8(5):364-8. [2]
- Abeles AM, Pillinger MH, Solitar BM, Abeles M, The pathophysiology of fibromyalgia, Ann Int Med, 2007;146;726-734
- Yunus MB, Khan MA, Rawlings KK, Green JR, Olson JM, Shah S. Genetic linkage analysis of multicase families with fibromyalgia syndrome. J Rheumatol 1999 Feb;26(2):408-12 [3]
- Buskila D, Neumann L Genetics of fibromyalgia. Curr Pain Headache Rep. 2005 Oct;9(5):313-5. [4]
- Buskila D, Neumann L, Hazanov I, Carmi R. Familial aggregation in the fibromyalgia syndrome. Semin Arthritis Rheum 1996 Dec;26(3):605-11 [5]
- Stormorken H, « Fibromyalgia: family clustering and sensory urgency with early onset indicate genetic predisposition and thus a "true" disease », Scand J Rheumatol., vol. 21, no 4, , p. 207 (PMID 1529291, DOI 10.3109/03009749209099225)
- Arnold LM, Hudson JI, Hess EV, et al, « Family study of fibromyalgia », Arthritis Rheum., vol. 50, no 3, , p. 944–52 (PMID 15022338, DOI 10.1002/art.20042)
- Buskila D, Sarzi-Puttini P, « Biology and therapy of fibromyalgia. Genetic aspects of fibromyalgia syndrome », Arthritis Res Ther., vol. 8, no 5, , p. 218 (PMID 16887010, PMCID 1779444, DOI 10.1186/ar2005)
- Cohen H, Buskila D, Neumann L, Ebstein RP, « Confirmation of an association between fibromyalgia and serotonin transporter promoter region (5- HTTLPR) polymorphism, and relationship to anxiety-related personality traits », Arthritis Rheum., vol. 46, no 3, , p. 845–7 (PMID 11920428, DOI 10.1002/art.10103)
- Buskila D, Dan B, Cohen H, et al, « An association between fibromyalgia and the dopamine D4 receptor exon III repeat polymorphism and relationship to novelty seeking personality traits », Mol. Psychiatry, vol. 9, no 8, , p. 730–1 (PMID 15052273, DOI 10.1038/sj.mp.4001506)
- Zubieta JK, Heitzeg MM, Smith YR, et al, « COMT val158met genotype affects mu-opioid neurotransmitter responses to a pain stressor », Science (journal), vol. 299, no 5610, , p. 1240–3 (PMID 12595695, DOI 10.1126/science.1078546)
- Narita M, Nishigami N, Narita N, et al, « Association between serotonin transporter gene polymorphism and chronic fatigue syndrome », Biochem Biophys Res Commun., vol. 311, no 2, , p. 264–6 (PMID 14592408, DOI 10.1016/j.bbrc.2003.09.207, lire en ligne)
- Camilleri M, Atanasova E, Carlson PJ, et al, « Serotonin-transporter polymorphism pharmacogenetics in diarrhea-predominant irritable bowel syndrome », Gastroenterology, vol. 123, no 2, , p. 425–32 (PMID 12145795, DOI 10.1053/gast.2002.34780, lire en ligne)
- Hudson JI, Mangweth B, Pope HG JR, De COL C, Hausmann A, Gutweniger S, Laird NM, Biebl W, Tsuang MT. Family study of affective spectrum disorder. Arch Gene Psychiatry. 2003;60:170–177. doi: 10.1001/archpsyc.60.2.170.
- Evengard B, Nilsson CG, Lindh G, Lindquist L, Eneroth P, Fredrikson S et al. Chronic fatigue syndrome differs from fibromyalgia. No evidence for elevated substance P levels in cerebrospinal fluid of patients with chronic fatigue syndrome [In Process Citation]. Pain 1998; 78(2):153-155.
- Russell IJ, Orr MD, Littman B, Vipraio GA, Alboukrek D, Michalek JE et al. Elevated cerebrospinal fluid levels of substance P in patients with the fibromyalgia syndrome. Arthritis Rheum 1994; 37(11):1593-1601.
- Vaeroy H, Helle R, Forre O, Kass E, Terenius L. Elevated CSF levels of substance P and high incidence of Raynaud phenomenon in patients with fibromyalgia: new features for diagnosis. Pain 1988; 32(1):21-26.
- . Hua XY, Chen P, Marsala M, Yaksh TL. Intrathecal substance P-induced thermal hyperalgesia and spinal release of prostaglandin E2 and amino acids. Neurosci 1999; 89(2):525-534.
- Dirig DM, Yaksh TL. Thermal hyperalgesia in rat evoked by intrathecal substance P at multiple stimulus intensities reflects an increase in the gain of nociceptive processing. Neurosci Lett 1996; 220(2):93-96.
- Lautenbacher S, Rollman GB. Possible deficiencies of pain modulation in fibromyalgia. Clin J Pain 1997; 13(3):189-196.
- Kosek E, Hansson P. Modulatory influence on somatosensory perception from vibration and heterotopic noxious conditioning stimulation (HNCS) in fibromyalgia patients and healthy subjects. Pain 1997; 70(1):41-51
- Giovengo SL, Russell IJ, Larson AA. Increased concentrations of nerve growth factor in cerebrospinal fluid of patients with fibromyalgia. J Rheumatol 1999; 26(7):1564-1569.
- Fischer HP, Eich W, Russell IJ. A possible role for saliva as a diagnostic fluid in patients with chronic pain. Semin Arthritis Rheum 1998; 27(6):348-359.
- Russell IJ. Neurochemical pathogenesis of fibromyalgia. Z Rheumatol 1998; 57 Suppl 2:63-66.
- http://www.cenaf.org/blogs/fibromyalgie/
- Maes M, Libbrecht I, Van Hunsel F, Lin AH, De Clerck L, Stevens W et al. The immune-inflammatory pathophysiology of fibromyalgia: increased serum soluble gp130, the common signal transducer protein of various neurotrophic cytokines. Psychoneuroendocrinology 1999; 24(4):371-383.
- 2007: Su Shan-Yu; Chen Jonathan Jiunn-Horng; Lai Chien-Chen; Chen Chun-Ming; Tsai Fuu-Jen. The association between fibromyalgia and polymorphism of monoamine oxidase A and interleukin-4.Clinical rheumatology 2007;26(1):12-6.
- http://www.vulgaris-medical.com/actualites/fibromyalgie-du-nouveau-dans-la-comprehension-de-la-maladie-100.html
- http://www.fibromyalgiesos.com/fm/zFibromyalgievulgarismedicalMartzolff.pdf [PDF]
- http://www.medscape.com/viewarticle/470556_8
- http://www.prohealth.com/library/showarticle.cfm?id=3748&t=CFIDS_FM
- « Fibromyalgia a ‘Real Disease,’ Study Shows », sur les site webmd.com.
- Fibromyalgia – An Information Booklet [6]
- Anderberg UM, Liu Z, Berglund L, Nyberg F, « Elevated plasma levels of neuropeptide Y in female fibromyalgia patients », Eur J Pain, vol. 3, no 1, , p. 19–30 (PMID 10700334, DOI 10.1016/S1090-3801(99)90185-4)
- Jones KD, Deodhar P, Lorentzen A, Bennett RM, Deodhar AA, « Growth hormone perturbations in fibromyalgia: a review », Seminars in Arthritis and Rheumatism, vol. 36, no 6, , p. 357–79 (PMID 17224178, DOI 10.1016/j.semarthrit.2006.09.006)
- ML Shuer, « Fibromyalgia: symptom constellation and potential therapeutic options », Endocrine, vol. 22, no 1, , p. 67–76 (PMID 14610300, DOI 10.1385/ENDO:22:1:67)
- KC Yuen, « Is further evaluation for growth hormone (GH) deficiency necessary in fibromyalgia patients with low serum insulin-like growth factor (IGF)-I levels? », Growth hormone & IGF research, vol. 17, no 1, , p. 82–8 (PMID 17289417, DOI 10.1016/j.ghir.2006.12.006)
- RM Bennett, « Hypothalamic-pituitary-insulin-like growth factor-I axis dysfunction in patients with fibromyalgia », J Rheumatology, vol. 24, no 7, {{Article}} : paramètre «
date» manquant, p. 1384–9 (PMID 9228141) - JS McCall-Hosenfeld, « Growth hormone and insulin-like growth factor-1 concentrations in women with fibromyalgia », Journal of Rheumatology, vol. 30, {{Article}} : paramètre «
date» manquant, p. 809–14 (PMID 12672204) - Anderberg UM, Marteinsdottir I, Theorell T, von Knorring L, « The impact of life events in female patients with fibromyalgia and in female healthy controls », Eur Psychiatry, vol. 15, no 5, , p. 33–41 (PMID 10954873, DOI 10.1016/S0924-9338(00)00397-7)
- Wood PB, « Fibromyalgia: A Central Role for the Hippocampus – A Theoretical Construct », J usculoskeletal Pain, vol. 12, no 1, , p. 19–26 (lire en ligne)
- Uno H, Tarara R, Else JG, Suleman MA, Sapolsky RM., « Hippocampal damage associated with prolonged and fatal stress in primates. », J Neurosci., vol. 9, no 5, , p. 1705–11 (PMID 2723746)
- Lucassen PJ, Vollmann-Honsdorf GK, Gleisberg M, Czéh B, De Kloet ER, Fuchs E., « Chronic psychosocial stress differentially affects apoptosis in hippocampal subregions and cortex of the adult tree shrew. », Eur J Neurosci., vol. 14, no 1, , p. 161–6 (PMID 11488960)
- Emad Y, Ragab Y, Zeinhom F, El-Khouly G, Abou-Zeid A, Rasker JJ., « Hippocampus dysfunction may explain symptoms of fibromyalgia syndrome. A study with single-voxel magnetic resonance spectroscopy. », J Rheumatol., vol. 35, no 7, , p. 1371–7 (PMID 18484688)
- Wood PB, Ledbetter CR, Glabus MF, Broadwell LK, Patterson JC 2nd, « Hippocampal Metabolite Abnormalities in Fibromyalgia: Correlation With Clinical Features. », J Pain., {{Article}} : paramètre «
date» manquant (PMID 18771960, DOI 10.1016/j.jpain.2008.07.003) - Demitrack MA, Crofford LJ. Evidence for and pathophysiologic implications of hypothalamic- pituitary-adrenal axis dysregulation in fibromyalgia and chronic fatigue syndrome. Ann N Y Acad Sci 1998; 840:684-697.
- Crofford LJ, Demitrack MA. Evidence that abnormalities of central neurohormonal systems are key to understanding fibromyalgia and chronic fatigue syndrome. Rheum Dis Clin North Am 1996; 22(2):267-284.
- Moldofsky H. Sleep, neuroimmune and neuroendocrine functions in fibromyalgia and chronic fatigue syndrome. Adv Neuroimmunol 1995; 5(1):39-56.
- Laylander JA, « A Nutrient/Toxin Interaction Theory of the Etiology and Pathogenesis of Chronic Pain-Fatigue Syndromes: Part I », Journal of Chronic Fatigue Syndrome, vol. 5, no 1, , p. 67–91 (DOI 10.1300/J092v05n01_08)
- Laylander JA, « A Nutrient/Toxin Interaction Theory of the Etiology and Pathogenesis of Chronic Pain-Fatigue Syndromes: Part II », Journal of Chronic Fatigue Syndrome, vol. 5, no 1, , p. 93–126 (DOI 10.1300/J092v05n01_08)
- Komaroff AL, Goldenberg D, « The chronic fatigue syndrome: definition, current studies and lessons for fibromyalgia research », Med. Hypotheses, vol. 69, no 3, , p. 517–25 (PMID 17376601, DOI 10.1016/j.mehy.2005.10.037)
- Pimental M, Wallace D, Hallegua D et al., « A link between irritable bowel syndrome and fibromyalgia may be related to findings on lactulose breath testing », J Rheumatol Suppl, vol. 19, , p. 23–7 (PMID 2691680)
- Szalavitz M, « SAMe as it ever was? », Notes Undergr, vol. 39, , p. 14–5 (PMID 11366783)
- Katz DL, Greene L, Ali A, Faridi Z, « The pain of fibromyalgia syndrome is due to muscle hypoperfusion induced by regional vasomotor dysregulation », Med. Hypotheses, vol. 69, no 3, , p. 517–25 (PMID 17376601, DOI 10.1016/j.mehy.2005.10.037)
- Site du Sénat
- Association Fibromyalgie France
- « La fibromyalgie enfin reconnue », Le Monde, 24 avril 2007
Bibliographie
- Patricia Le Garf, Fibromyalgique – Une souffrance en pleine lumière , éd. Le Garf Éditions, 2006, 266 p. (ISBN 2952126127 et 978-2952126120)
- Alison Fraser, Guide pratique du fibromyalgique, éditions Publibook, 2009 [présentation en ligne]
