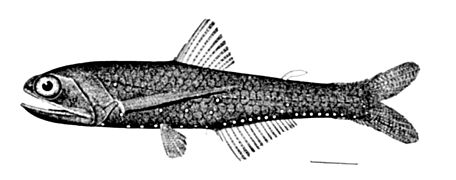
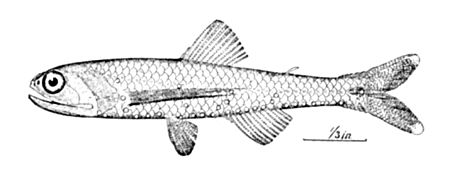
Myctophidae
Les Myctophidés (Myctophidae, du grec mykter, « nez » et ophis, « serpent »), également connus sous le nom de poissons-lanternes dû à leur bioluminescence, sont une famille de poissons téléostéens d’une taille allant de quelques centimètres à environ 30 centimètres de longueur. Ceux-ci appartenant à l'ordre des Myctophiformes qui sont représentés par environ 250 espèces dans 33 genres. Cette famille est répandue dans la zone aphotique, de tous les océans du monde, des eaux tempérées aux eaux tropicales et polaires habitant ces zones déjà depuis des millions d’années. Certains genres existent déjà depuis 145 millions d’années, tel que les genres Diaphus et Ceratoscopelus qui sont originaires du Crétacé[1].
Les poissons-lanternes sont parmi les vertébrés les plus largement distribués, les plus diversifiés et les plus peuplés, certaines estimations suggérant qu'ils pourraient avoir une biomasse mondiale totale de 1,8 à 16 gigatonnes, représentant jusqu'à 65% de toute la biomasse des poissons des profondeurs abyssales[2]. Des pêcheries commerciales existent au large de l'Afrique du Sud, dans la région subantarctique et dans le golfe d'Oman.
Histoire
[modifier | modifier le code]Les myctophidés sont dans ce monde depuis des millions d'années. Ils ont vécu, évolué et se sont adaptés à l'environnement en constante évolution de la Terre. Des reliques de ces poissons fossilisées ou en fossilisation sont trouvables, ce qui a donné une indication de leur présence au cours de l'évolution de la vie sur terre. Des restes sous forme d'otolithes isolés, de dents et d'écailles de roches sédimentaires ont été trouvés. Certains fossiles appartenant aux genres Diaphus et Ceratoscopelus dateraient de la période crétacée d'il y environ a 145 millions d'années[3]. Des myctophidés fossilisés, Eomyctophum koraense et Oligophus moravicus ont été trouvés dans les gisements datant Paléocène, de l'Éocène et de l'Oligocène de la Russie et des régions adjacentes des bassins de Thetys et Parathetys[4]. Le genre Eomyctophum a ensuite été séparé dans la sous-famille des Eomyctophinae, différant des autres poissons myctophiformes par l'absence d'épaississements des photophores en forme de lentille. Des archives fossiles sont également signalées à l'époque du Miocène de la période tertiaire supérieure il y a environ 23 millions d'années. Les découvertes de fossiles peuvent ainsi aider à comprendre le type de climat, d'hydrographie et d'habitats dans lesquels ces poissons vivaient, ainsi que leur évolution et leurs adaptations au cours du temps.
Morphologie
[modifier | modifier le code]
Les poissons-lanternes ont un corps mince et compressé recouvert d'écailles caduques, cycloïdes ou cténoïdes, qui recouvrent également les glandes luminescentes chez la plupart des espèces. La taille des poissons varie de 2 à 30 cm, ce qui est une longueur standard, la majorité étant inférieure à 15 cm et pesant entre 2 et 6 g[5]. Les myctophidés sont caractérisées par une tête proéminente et arrondie avec de grands yeux elliptiques. Ils présentent également plusieurs nageoires ; une nageoire dorsale haute, une nageoire adipeuse, une nageoire pelvienne et une nageoire anale soutenues par une plaque cartilagineuse à sa base, prenant naissance sous ou légèrement en arrière de l'extrémité postérieure de la nageoire dorsale.
Les nageoires pectorales ont généralement huit rayons et peuvent être petits ou réduits chez certaines espèces et bien développés chez d’autres espèces. La nageoire caudale est fourchue à son amorce. La couleur des myctophidés varie du bleu-vert à l'argent chez les espèces peu profondes, par ex. Diaphus sp., tandis que les espèces d'eau profonde sont brun foncé à noir, par ex. Lampanyctus sp. et Taaningichthys sp.
Les branchies portent des branchiospines agrandies en forme de lame bien développées le long du premier arc branchial, sauf chez Centrobranchus sp[6]. Qui ont des branchiospines moins développées, néanmoins le nombre de branchiospines que possède cette espèce est utilisé comme caractère taxonomique pour différencier les espèces[7].
Les myctophidés montrent la présence d'organes bioluminescents non bactériens appelés photophores, disposés ventralement et spécifiques à l'espèce. Ce sont des structures complexes constituées d'écailles modifiées en forme de coupe (lentille), contenant du tissu photogénique. Une fonction qui peut être nécessaire pour voir dans le noir en plus de leurs grands yeux photosensibles et aussi pour attirer les partenaires et tromper les prédateurs[8].

Des glandes lumineuses accessoires sont également observées chez certains myctophidés. Par exemple, chez le poisson phare, Diaphus sp. les glandes sont à proximité des yeux ou sont supracaudales (dorsales) chez les mâles et infracaudales (ventrales) chez les femelles de Lobianchia gemellari, suggérant leur nature sexuellement dimorphe[7]. Certaines autres espèces présentant ces glandes sont Stenobrachius leucopsarus et Lampanyctus ritteri, à l'exception de Symbolophorus californiensis où elles sont absentes. Toutes les espèces de Myctophidés présentent des photophores à l'exception d'une, à savoir Taaningichthys paurolychnus (trouvé dans l'Atlantique Est: Madère et Cap-Vert; Atlantique Ouest: près des Bermudes et de la Jamaïque; Océan Indien occidental) alors que toutes les autres espèces de ce genre sont bioluminescentes[9].
Les vessies natatoires facilitent la flottabilité pendant les stades juvéniles, qui se remplissent ensuite de lipides ou dégénèrent pendant la maturation chez la plupart des espèces. L'intestin est légèrement sigmoïde, s'étend jusqu'au milieu du corps et présente des plis muqueux transversaux, qui vont d'extrêmement courts chez Lampanyctus sp. allongée et dégagée du corps chez Myctophum aurolaternatum[10]. Une autre situation de dimorphisme est observable chez certaines espèces telles que Ceratoscopelus warmingii et Electrona Antarctica dans lequel les mâles sont nettement plus petits que les femelles à la taille adulte[11].
Physiologie
[modifier | modifier le code]
Biochimie
[modifier | modifier le code]Les poissons mésopélagiques contiennent de grandes quantités d'esters de cire qui, lorsqu'ils sont consommés en grandes quantités, provoquent la diarrhée et la séborrhée chez les animaux. Des études sur le myctophidé a montré la présence de 86,2 à 90,5 % d'esters de cire dans les lipides totaux[2]. Les myctophidés ont également une teneur élevée en protéines et en minéraux, une teneur très variable en lipides et une teneur uniformément faible en glucides indiquant son importance nutritionnelle. Un certain nombre d'études ont évalué la teneur en lipides des myctophidés migrant verticalement et ont découvert qu'ils comprenaient des triglycérides, censés servir principalement de réserve d'énergie et des cérides (esters de cire), principalement utilisés pour la flottabilité[12]. D’autres études ont signalé que les poissons-lanternes sont une bonne source de potassium, de sodium et de calcium. Ils n'ont également trouvé aucune bactérie nocive comme les coliformes, les streptocoques fécaux et les staphylocoques à coagulase positive[13]. Ils ont conclu à partir des découvertes biochimiques et pathologiques ci-dessus que les poissons-lanternes sont suffisamment bons comme aliment agréable au goût pour la consommation humaine et animale après un traitement approprié[14].
Bioluminescence et réponse à une stimulation photique
[modifier | modifier le code]
Les poissons-lanternes sont connus pour leur bioluminescence, qui leur permet de produire et de contrôler leur propre lumière par la présence de photophores luminescents disposés systématiquement sur leur corps. Les photophores sont des organes lumineux complexes, situés sur différents endroits de leur corps, qui leur permettent de communiquer, de se camoufler ou d'attirer des proies. Ces organes lumineux peuvent être disposés en bandes, en taches, en croissants ou en cercles autour de leur corps, créant une variété de motifs et de couleurs[15].
Ces organes émettent une lumière bleu-vert-jaune faible à vive, qui est le résultat d'une réaction chimique d'oxydation, déclenchée et régulée par le système nerveux. Le composé luciférine est responsable de l'effet de luminescence et de la couleur et qui est catalysé par l'enzyme luciférase. Ce composé est présent dans de nombreux autres groupes bioluminescents marins et terrestres avec des structures chimiques différentes[16].Cette adaptation aurait pu évoluer lorsque ces poissons ont commencé à habiter les eaux plus sombres de l'océan[17]. La distribution ventrale caractéristique des photophores de poissons suggère que leur luminescence réduit la silhouette lorsqu'elle est vue sur un fond de lumière devenant de plus en plus sombre. Ces poissons font correspondre leur luminescence à l'éclairage de fond des océans en manipulant l'intensité des photophore à la suite d’une stimulation visuelle dite stimulation photique. Des expériences ont démontré la capacité de contrôle neuronal direct des photophores chez plusieurs espèces de myctophidés qui dépendent également des caractéristiques morphologiques et comportementales selon l’espèce de myctophidés[15].
La bioluminescence est donc surtout utile pour la réduction de la silhouette pour permettre à ces organismes de se fondre avec le décor. Ceci a pour but pour soit se camoufler, soit contre l’illumination ou soit pour distraire ou leurrer prédateur et proie. Dans les profondeurs de l'océan, où la lumière est très faible, la bioluminescence peut être utilisée pour se fondre dans l'environnement. Ces poissons peuvent contrôler l'intensité et la couleur de la lumière émise par leurs photophores pour correspondre à la faible lumière ambiante, ce qui les rend moins visibles pour les prédateurs ou les proies potentielles[18]. Lorsqu'un myctophidé est vu de dessous, sa silhouette apparaît plus sombre par rapport à la luminosité de la surface de l'eau s'il n'ajuste pas sa bioluminescence. Pour contrer cela le contrôle des photophores permet d'émettre de la lumière vers le bas, ce qui réduit le contraste entre l'animal et la lumière provenant de la surface et rend la détection de ces animaux plus difficiles pour les prédateurs et les proies. Cette bioluminescence peut également être utilisée pour attirer ou distraire d'autres créatures. Les myctophidés peuvent créer des éclairs lumineux rapides ou des motifs lumineux complexes pour désorienter les prédateurs ou attirer des proies. Cette bioluminescence peut être utilisée pour aussi attirer des partenaires. Autrement cette bioluminescence peut améliorer la vision dans le profondeurs abyssales lorsque couplé à leurs grands yeux photosensibles[9].
Alimentation
[modifier | modifier le code]
Les myctophidés sont connus pour être des prédateurs opportunistes sur les copépodes, les ostracodes, les euphausiacés, les amphipodes hyperiidés, les chaetognathes, les ptéropodes, ainsi que les œufs de poisson et les larves de poisson[19]. Ils présentent une alimentation nocturne prédominante durant de 8 à 10 h. Néanmoins les myctophidés post-métamorphiques et adultes sont principalement des nourrisseurs nocturnes contrairement aux larves qui se nourrissent pendant la journée chez la plupart des espèces[19]. Les myctophidés occupent également un statut trophique important en tant que consommateurs de zooplancton[20]. Les myctophidés des régions tempérées et les régions de haute latitude semblent présenter un degré élevé de chevauchement dans leur spectre alimentaire. Toutefois il a été établi qu’il y a une faible concurrence inter-espèce alimentaire en raison de la forte disponibilité alimentaire régionale[21].
Comportement
[modifier | modifier le code]Comportement migratoire
[modifier | modifier le code]
Les poissons-lanterne effectuent une migration verticale journalière et occupent la région bathypélagique qui s’étend de 200 à 2 000 m pendant la journée et durant la nuit dans la région épipélagique qui se prolonge de 10 à 100 m. Ils sont adaptés pour survivre dans des couches à faible teneur en oxygène ambiant (à environ 1 ml/l ou 4,5 μM), une caractéristique du nord de la mer d'Oman[22], y compris le golfe du Bengale et les marges continentales le long de l'est de l'océan Pacifique et au large de l'Afrique de l'Ouest. Le Diaphus arabicus et Benthosema pterotum par exemple sont adaptés aux conditions de faible teneur en oxygène dans le nord de la mer d'Oman[23].
Il existe une grande variabilité observée dans les schémas de migration océanique verticale au sein de la famille. Certaines espèces vivant en profondeur peuvent ne pas migrer du tout tandis que d'autres ne le font qu'à intervalles irréguliers. La migration verticale nocturne commence généralement environ 1 h avant le coucher du soleil et se termine essentiellement entre une demi-heure et une heure après le coucher du soleil. Les schémas migratoires peuvent également dépendre du stade du cycle vital, du sexe, de la latitude, de l'hydrographie, de la topographie et de la saison. Les myctophidés présentent quatre types de modèles de migration qui sont:
- Les migrants,montrant une nette séparation de l'habitat jour-nuit avec une abondance maximale au-dessus de 200 m la nuit, tel que: Symbolophorus californiensis, Tarletonbeania taylori, Notoscopelus japonicus, Diaphus theta, Ceratoscopelus warmingi et Diaphus gigas.
- Les Semi-migrants, dans lesquels une partie de la population reste souvent dans l'habitat diurne la nuit. Les profondeurs de distribution des individus migrateurs et non migrateurs ne se chevauchent pas: Stenobrachius leucopsarus.
- Les Migrateurs passifs, dans lesquels il n'y a pas de séparation des habitats jour-nuit, mais la limite supérieure de la population diurne se déplace vers une couche moins profonde la nuit, probablement lorsque les poissons suivent des proies migratrices : Lampanyctus jordani.
- Les Non-migrants comme Stenobrachius nannochir, Lampanyctus regalis et Protomyctophum thompsoni[24].
Les formes plus petites parcourent une distance de 10 à 170 m/h tandis que les taxons plus gros parcourent une distance de 100 à 200 m/h dans un sens. Les larves de myctophidés restent dans la zone épipélagique (à 200 m de profondeur) puis se déplacent vers des profondeurs pour s'adapter à leur vie adulte ultérieure dans les zones mésopélagiques, après quoi la plupart des espèces commencent une migration verticale quotidienne[25]. Ils sont également capables de traverser des gradients de densité tels que la thermocline et l'halocline qui sont difficiles à pénétrer pour la plupart des espèces dû à des processus physiques. Le comportement de nage observé chez les myctophidés prend deux formes selon le type de corps. Les espèces au corps robuste nagent en courtes rafales, propulsées par une fermeture rapide des rayons de la nageoire caudale et un mouvement de la queue.
En général, ce sont les migrateurs les plus forts, avec la plus grande différence de distribution verticale diurne et nocturne. Les individus au corps flasque ont tendance à se déplacer avec un lent frétillement de tout le corps, semblable à une anguille. La zone épipélagique est la zone responsable du développement des myctophidés ; c'est dans cette zone que ces poissons réalisent la plupart de leurs activités comme l'alimentation, la reproduction et le développement. La migration verticale quotidienne du poisson-lanterne adulte est liée à la nutrition et à l'échange d'énergie entre les niveaux trophiques inférieurs et supérieurs[26]. Par conséquent, il est important de comprendre leurs proies comme les copépodes, les euphausiacés grâce à des analyses du contenu intestinal qui, à leur tour, mettront en évidence leur écologie alimentaire et leur structure communautaire. En outre, la migration verticale est également contrôlée par l'intensité lumineuse. Cela pourrait être dû au fait qu'ils sont adaptés aux conditions de faible luminosité dans les eaux profondes et pourrait être une autre raison de leur migration vers la surface après le crépuscule.
Reproduction
[modifier | modifier le code]Les myctophidés se caractérisent par une croissance rapide, une maturité sexuelle précoce, une durée de vie de 1 à 5 ans et un fort taux de mortalité. Les femelles sont ovipares et les deux sexes sont des géniteurs pélagiques non-gardien. Ils libèrent des œufs et du liquide séminal dans l'eau, où la fécondation a lieu. Les œufs minuscules ont une taille de 0,70 à 0,90 mm, avec un jaune segmenté, un espace modérément périvitellin, un seul globule d'huile et un chorion délicat. Ceux-ci sont rendus flottants par des gouttelettes lipidiques[7]. Les œufs fécondés (embryons) puis les larves écloses (~2,0 mm) dérivent au gré des courants jusqu'à leur développement. Les femelles produisent environ 100 à 2 000 œufs non fécondés par ponte, selon l'espèce et l'âge du poisson[27].
Le frai peut se poursuivre toute l'année chez certaines espèces, mais a le plus été signalé entre l'hiver et le début du printemps. Tous les poissons-lanternes ont un faible taux de fécondité. Benthosema pterotum, l'une des espèces dominantes, est connue pour frayer une seule fois dans sa durée de vie et ceci se produisant généralement à l'âge de 7 mois[21].
Les espèces plus grandes telles que Benthosema glaciale peuvent vivre jusqu'à 8 ans, atteignant la maturité à 2–3 ans, tandis que les myctophidés plus petits comme le Diogenichthys lateratus ont tendance à avoir une plus grande résilience, doublant leurs populations en 15 mois[28].
Écologie
[modifier | modifier le code]
L'important contenu calorique des lipides chez les Myctophidés constitue une source d'énergie importante pour les prédateurs supérieurs, en particulier pendant la saison de reproduction[29]. Des études menées sur des poissons mésopélagiques dans la mer d'Oman suggèrent que les Myctophidés constituent une part importante du régime alimentaire des poissons prédateurs comme Chauliodus pamelas, Chauliodus sloani, Stomias affinis et Scinax nebulosus[30]. Un certain nombre d'espèces de cétacés et de manchots se nourrissent de myctophidés et font partie des animaux non mésopélagiques susceptibles d'être affectés par la pêche commerciale des myctophidés.
Dans le golfe d'Oman, les régions du nord de la mer d'Oman, l'est de l'océan Pacifique, au large de l'Afrique de l'Ouest et du golfe du Bengale, où la teneur en oxygène de l'eau a limité ou éliminé la présence d'autres petites espèces de poissons, les poissons-lanternes peuvent être une composante plus importante du régime alimentaire pour au moins les poissons scombridés comme les thons, les maquereaux.
D’autres études mettent en évidence les liens trophiques entre les poissons des hautes latitudes et leurs proies et soulignent l'importance des Myctophidés en tant que source d'énergie importante pour les prédateurs marins qui se nourrissent dans la zone frontale polaire[30]. Récemment, des analyses d'acides gras ont été utilisées pour résoudre les interactions trophiques des Myctophidés dans les réseaux trophiques marins de l'Antarctique[31]. Les Myctophidés ne sont généralement pas accessibles aux oiseaux de mer volants comme les mouettes car les poissons ne se trouvent pas près de la surface (0–5 m) et ces oiseaux ne plongent généralement pas. La biomasse des myctophidés ne peut les atteindre que lorsque ces oiseaux consomment leurs principales proies comme les calmars, les notothéniides des poissons endémiques de la région antarctique, également appelés « poissons des glaces » ou aussi les poissons channichthyidés aussi connus sous le nom « poissons des glaces crocodiles ou poissons à sang blanc », qui se nourrissent de Myctophidés[32]. Lorsqu'elle n'est pas consommée par les prédateurs (mortalité des non-prédateurs), la biomasse en décomposition des poissons-lanteres finit par contribuer à la nutrition benthique. Les myctophidés apportent à la fois des nutriments et du dioxyde de carbone aux couches plus profondes (500 à 1 000 m) dans ou à proximité des régions à faible teneur d'oxygène[12].
Ces poissons effectuent des migrations verticales journalières entre les régions méso-(200–2 000 m) et épipélagiques (10–100 m) et montre des adaptations aux eaux à faible teneur en oxygène[33]. Ils sont abondants dans les eaux profondes et jouent un rôle important dans l'écosystème océanique et dans la dynamique de l'énergie océanique, en formant un maillon important du réseau trophique. Ils remplissent le rôle prédateur et des proies pour de nombreuses autres espèces, comme les poissons plus gros, les mammifères marins et les oiseaux marins. En tant que proies, ils sont une source importante de nourriture pour les prédateurs des eaux profondes et pour les espèces qui se nourrissent dans les eaux de surface, comme les thons et les requins. En tant que prédateurs, ils sont importants pour réguler les populations d'autres espèces de poissons et de plancton[7].
Distribution mondiale
[modifier | modifier le code]La distributions des poissons-lanternes est circumglobales donc ceux-ci se trouvent dans tous les océans à l'exception de l'Arctique Ils sont très diversifiés, ce qui pourrait être utilisé comme indicateur de la distinction biogéographique d'une zone spécifique. Benthosema pterotum est l'espèce la plus commune et la plus nombreuse dans l'ouest dans la région du golfe d'Oman en Somalie et dans l'est le long de la côte ouest de l'Inde la mer d'Oman. Cette espèce est également le plus grand stock de poissons au monde escomposé uniquement d'une seule espèce[34]. D'autres espèces telles que Benthosema fibulatum, Diaphus spp., Myctophum spinosum et Symbolophorus evermanni étaient occasionnelles en nombre dans le golfe d’Aden. Le long de la côte sud d'Oman et du nord-est de la Somalie, B. fibulatum a dominé les collectes au chalut et des relevés acoustiques[5]. Dans l'est de la mer d'Oman, Diaphus arabicus et Hygophum proximum sont des formes communes. Le long de la côte du Pakistan, les concentrations de myctophidés sont presque exclusivement constituées de B. pterotum avec des densités décroissantes vers l'ouest. Une enquête dans l'ouest de l'océan Indien a estimé la présence de 97 espèces de myctophidés appartenant à 23 genres[35]. Stenobrachius leucopsarus est l'un des poissons-lanternes sans vessie abondants et dominants dans le Pacifique subarctique, y compris la mer de Béring et la mer d’Okhotsk. Environ 43 espèces appartenant à 16 genres ont été enregistrées potentiellement dans l'océan Austral, dont 7 espèces : Electrona antarctica, Gymnoscopelus braueri, G. ophisthopetrus, G. nicholski, Krefftichthys anderssoni, Protomyctophum bolini et P. tensioni étaient considérées comme de véritables représentants des régions du sud du front polaire antarctique[36].
Liste de certaines espèces et leur région géographique spécifique
[modifier | modifier le code]| Espèce rencontrés | Région géographique[7] |
| Benthosema fibulatum | Golfe d'Aden, sud d'Oman et côtes nord-est de la Somalie |
| Benthosema glaciale | Atlantique Nord-Ouest Norvège, Groenland et Canada, mer Méditerranée, Baie de Baffin |
| Centrobranchus spp. | Atlantique Est : Maroc au Sénégal et du Gabon à l'Angola
Atlantique Ouest : USA et du Brésil à l'Argentine, Atlantique Nord-Ouest : Canada, Océan Indien Pacifique sud-est : USA et au large du Chili, d'Hawaï et du Japon et de la mer de Chine |
| Ceratoscopelus warmingii | Océan Atlantique, Océan Pacifique, Océan Indien
Signalé comme commun en Afrique australe, au sud et à l'est de la mer de Chine |
| Diaphus arabicus | Mer d'Arabie septentrionale et orientale |
| Diaphus coeruleus | Océan Indien sud-ouest et Atlantique sud |
| Diaphus theta | Subarctique et Pacifique nord-ouest |
| Diogenichthys laternatus | Pacifique oriental : Californie, USA et Mexique jusqu'au Chili, océans Atlantique et Indien et mer de Chine méridionale |
| Eomyctophum koraense | Formes fossilisées en Russie |
| Gymnoscopelus bolini et G. nicholski | Sud-ouest de l'océan Indien, sud de l'Atlantique et front polaire de l'Antarctique |
| Gymnoscopelus braueri et G. ophisthopterus | Front polaire de l'Antarctique |
| Hygophum proximum | Mer d'Arabie septentrionale et orientale |
| Krefftichthys anderssoni | Front polaire de l'Antarctique |
| Lampanyctodes hectoris | Eaux sud-africaines et Atlantique sud |
| Lampanyctus ritteri | Océan Pacifique oriental |
| Lobianchia gemellari | Océan Pacifique, Méditerranée et Mer Noire, Océan Indien et Océan Atlantique aux Îles de Madère et Afrique du Sud |
| Myctophum aurolaternatum | Pacifique et océan Indien |
| Myctophum spinosum | Golfe d'Aden |
| Oligophus moravicus | Formes fossilisées en Russie |
| Protomyctophum bolini and P. tensioni | Front polaire de l'Antarctique |
| Stenobrachius leucopsarus | Pacifique subarctique
Pacifique nord-ouest : mer de Béring et mer d'Okhotsk |
| Symbolophorus californiensis | Pacifique Nord près Japon et de l'Alaska à la Basse-Californie et au Mexique |
| Taaningichthys paurolychnus | Atlantique Est près des îles de Madère et du Cap-Vert, Atlantique Ouest près de la Jamaïque et Océan Indien occidental |
| Tarletonbeania crenularis | Pacifique oriental du sud-est de l'Alaska jusqu'au large du Mexique, y compris le golfe d'Alaska et la mer de Béring |
Relations avec l'homme
[modifier | modifier le code]
Certains poissons-lanternes, tels que les espèces du genre Electrona, sont exploités commercialement dans certaines régions du monde. Ils sont généralement utilisés pour la production d'huile de poisson, de farine de poisson et de produits de consommation humaine comme les compléments alimentaires[7].
Les pêcheries commerciales de poissons-lanternes comprennent des opérations limitées au large de l'Afrique du Sud, dans la région subantarctique et dans le golfe. Mais la majorité des myctophidés ne sont pas utilisés pour la consommation humaine directe en raison de leur teneur élevée en lipides ou en esters de cire, ils sont donc utilisés comme aliments pour poissons prédateurs, aliments pour volailles, aliments pour animaux et engrais pour les cultures[8].
Les exceptions à cette règle sont Diaphus coeruleus, Gymnoscopelus nicholski et G. bolini qui étaient considérés comme comestibles dans le sud-ouest de l'océan Indien et le sud de l'Atlantique à la fin des années 1970. Néanmoins, il n'y a plus aucun rapport de consommation humaine de myctophidés en Inde aujourd'hui.En 1973 cette espèce particulière représentait environ 42 560 tonnes (10,45 %) des prises pélagiques[37]. Ensuite au milieu des années 1980 une pêcherie industrielle de Lampanyctodes hectoris dans les eaux sud-africaines a dû fermer en raison de difficultés de traitement causées par la forte teneur en huile du poisson. Il est donc intéressant, compte tenu de leur importante biomasse, des efforts sont nécessaires pour concevoir des idées et proposer une technologie de traitement rentable[38].
Les poissons-lanternes sont donc souvent étudiés par les scientifiques pour mieux comprendre leur écologie, leur comportement, leur bioluminescence et leur rôle dans les écosystèmes marins. Ces études contribuent à notre compréhension générale de la vie marine et des interactions entre les espèces[34].
Vulnérabilité
[modifier | modifier le code]
Comme les myctophidés ont un faible taux de fécondité, ils sont sujets à des menaces de survie. L'exploitation sous la forme d'une pêche conventionnelle extensive peut réduire les stocks des poissons-lanternes dans des zones facilement accessibles, sans leur donner une chance de se régénérer et de se reconstituer. Des études dans la mer d'Oman ont déjà montré que le taux de capture de la biomasse a considérablement diminué d’environ 100 millions de tonnes métriques des estimations récentes d'environ 1,7 à 20 millions[39].
Des recherches pour comprendre le cycle de vie des myctophidés et leurs adaptations aux différents stress entre autres sont recherchées afin de raviver les stocks en déclin dans les milieux naturels grâce à des habitats artificiels. Ces stocks élevés artificiellement peuvent répondre à la production de farine de poisson, d'huile de poisson plutôt que de stresser les réserves des océans[40].
Les dommages ou la perte de populations de myctophidés pourraient avoir de graves répercussions sur de nombreux autres organismes, en particulier les prédateurs supérieurs et d'autres poissons d'importance commerciale dans les réseaux trophiques océaniques ouverts. La biodiversité de cette communauté de poissons doit être conservée en protégeant leurs habitats, ce qui comprend également une étude détaillée et un inventaire des bioressources[41]. Il est possible que les populations de poissons-lanternes puissent soutenir des pêcheries d'importance mondiale. De nombreuses espèces de myctophidés et de gonostomatidés représentent ensemble environ 75% du total des captures mondiales potentielles de petits poissons océaniques mésopélagiques dans l'océan Indien, en particulier la mer d'Oman. Sans oublier que les poissons myctophidés, en particulier Benthosema pterotum, sont parmi les espèces cibles les plus disponibles dans le monde pour la recherche en biologie pélagique à de nombreux niveaux différents. En somme, leur statut de sensibilité est considéré comme intermédiaire avec une préoccupation mineure donc c’est une espèce pour laquelle le risque de disparition est faible[42].
Liste des genres
[modifier | modifier le code]Selon le World Register of Marine Species (19 février 2016)[43] :
- genre Benthosema Goode & Bean, 1896
- genre Bolinichthys Paxton, 1972
- genre Centrobranchus Fowler, 1904
- genre Ceratoscopelus Günther, 1864
- genre Diaphus Eigenmann & Eigenmann, 1890
- genre Diogenichthys Bolin, 1939
- genre Electrona Goode & Bean, 1896
- genre Gonichthys Gistel, 1850
- genre Gymnoscopelus Günther, 1873
- genre Hintonia Fraser-Brunner, 1949
- genre Hygophum Bolin, 1939
- genre Idiolychnus Nafpaktitis & Paxton, 1978
- genre Krefftichthys Hulley, 1981
- genre Lampadena Goode & Bean, 1893
- genre Lampanyctodes Fraser-Brunner, 1949
- genre Lampanyctus Bonaparte, 1840
- genre Lampichthys Fraser-Brunner, 1949
- genre Lepidophanes Fraser-Brunner, 1949
- genre Lobianchia Gatti, 1904
- genre Loweina Fowler, 1925
- genre Macrostoma Risso, 1827
- genre Metelectrona Wisner, 1963
- genre Myctophum Rafinesque, 1810
- genre Nannobrachium Günther, 1887
- genre Nanobrachium Günther, 1887
- genre Notolychnus Fraser-Brunner, 1949
- genre Notoscopelus Günther, 1864
- genre Parvilux Hubbs & Wisner, 1964
- genre Protomyctophum Fraser-Brunner, 1949
- genre Scopelopsis Brauer, 1906
- genre Stenobrachius Eigenmann & Eigenmann, 1890
- genre Symbolophorus Bolin & Wisner, 1959
- genre Taaningichthys Bolin, 1959
- genre Tarletonbeania Eigenmann & Eigenmann, 1890
- genre Triphoturus Fraser-Brunner, 1949
Voir aussi
[modifier | modifier le code]Articles connexes
[modifier | modifier le code]Liens externes
[modifier | modifier le code]- (en) Référence WoRMS : Myctophiformes (+ liste familles + liste genres)
- (en) Référence Paleobiology Database : Myctophiformes Regan 1911
- (en + fr) Référence FishBase : ()
- (fr + en) Référence ITIS : Myctophiformes
- (en) Référence Animal Diversity Web : Myctophiformes
- (en) Référence Catalogue of Life : Myctophiformes (consulté le )
- (en) Référence NCBI : Myctophiformes (taxons inclus)
Notes et références
[modifier | modifier le code]- (en) C. Giles Miller, Martha Richter et Dermeval A. Do Carmo, « Fish and ostracod remains from the Santos Basin (Cretaceous to Recent), Brazil », Geological Journal, vol. 37, no 4, , p. 297–316 (ISSN 0072-1050 et 1099-1034, DOI 10.1002/gj.917, lire en ligne, consulté le )
- Hulley, P. Alexander, Encyclopedia of Fishes, San Diego, Academic Press, , 127–128 p. (ISBN 0-12-547665-5)
- (en) C. Giles Miller, Martha Richter et Dermeval A. Do Carmo, « Fish and ostracod remains from the Santos Basin (Cretaceous to Recent), Brazil », Geological Journal, vol. 37, no 4, , p. 297–316 (ISSN 0072-1050 et 1099-1034, DOI 10.1002/gj.917, lire en ligne, consulté le )
- A. M. Prokofiev, « Fossil myctophoid fishes (Myctophiformes: Myctophoidei) from Russia and adjacent regions », Journal of Ichthyology, vol. 46, no S1, , S38–S83 (ISSN 0032-9452 et 1555-6425, DOI 10.1134/s0032945206100043, lire en ligne, consulté le )
- (en) Kouichi Kawaguchi et Keiko Aioi, « Myctophid fishes of the genusMyctophum (myctophidae) in the pacific and Indian oceans », Journal of Oceanography, vol. 28, no 4, , p. 161–175 (ISSN 0916-8370 et 1573-868X, DOI 10.1007/BF02108760, lire en ligne, consulté le )
- F. Javier Gago et Robert J. Lavenberg, « Systematics of the Lanternfish Genus Centrobranchus (Pisces: Myctophidae) », Copeia, vol. 1992, no 1, , p. 154 (DOI 10.2307/1446547, lire en ligne, consulté le )
- (en) Venecia Catul, Manguesh Gauns et P. K. Karuppasamy, « A review on mesopelagic fishes belonging to family Myctophidae », Reviews in Fish Biology and Fisheries, vol. 21, no 3, , p. 339–354 (ISSN 0960-3166 et 1573-5184, DOI 10.1007/s11160-010-9176-4, lire en ligne, consulté le )
- (en) Daniel Pauly, Chiara Piroddi, Lincoln Hood et Nicolas Bailly, « The Biology of Mesopelagic Fishes and Their Catches (1950–2018) by Commercial and Experimental Fisheries », Journal of Marine Science and Engineering, vol. 9, no 10, , p. 1057 (ISSN 2077-1312, DOI 10.3390/jmse9101057, lire en ligne, consulté le )
- (en) J. F. Case, J. Warner, A. T. Barnes et M. Lowenstine, « Bioluminescence of lantern fish (Myctophidae) in response to changes in light intensity », Nature, vol. 265, no 5590, , p. 179–181 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/265179a0, lire en ligne, consulté le )
- (en) P. Alexander Hulley et Guy Duhamel, « A review of the lanternfish genus �Bolinichthys� Paxton, 1972 (Myctophidae) », Cybium, vol. 33, no 4, , p. 259-304 (lire en ligne, consulté le ).
- Syed Makhhdoom Hussain et Jafar Ali-Khan, « Fecundity of Benthosema fibulatum and Benhosema pterotum from the northern Arabian sea », Deep Sea Research Part A. Oceanographic Research Papers, vol. 34, no 7, , p. 1293–1299 (ISSN 0198-0149, DOI 10.1016/0198-0149(87)90077-x, lire en ligne, consulté le )
- Marzieh Moosavi-Nasab, Rezvan Mohammadi et Najme Oliyaei, « Physicochemical evaluation of sausages prepared by lantern fish (Benthosema pterotum) protein isolate », Food Science & Nutrition, vol. 6, no 3, , p. 617–626 (ISSN 2048-7177, DOI 10.1002/fsn3.583, lire en ligne, consulté le )
- (en) Viktor P. Voronin, Dmitrii V. Artemenkov, Alexei M. Orlov et Svetlana A. Murzina, « Fatty Acid Spectra in Mesopelagic Fishes of the Myctophidae and Stomiidae Families Collected in the North East Atlantic », Diversity, vol. 15, no 2, , p. 166 (ISSN 1424-2818, DOI 10.3390/d15020166, lire en ligne, consulté le )
- (en) Charles F. Phleger, Matthew M. Nelson, Ben D. Mooney et Peter D. Nichols, « Wax esters versus triacylglycerols in myctophid fishes from the Southern Ocean », Antarctic Science, vol. 11, no 4, , p. 436–444 (ISSN 0954-1020 et 1365-2079, DOI 10.1017/S0954102099000565, lire en ligne, consulté le )
- (en) Frederick I. Tsuji et Yata Haneda, « Luminescent System in a Myctophid Fish, Diaphus elucens Brauer », Nature, vol. 233, no 5322, , p. 623–624 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/233623a0, lire en ligne, consulté le )
- (en) A.T. Barnes et J.F. Case, « The luminescence of lanternfish (myctophidae): Spontaneous activity and responses to mechanical, electrical, and chemical stimulation », Journal of Experimental Marine Biology and Ecology, vol. 15, no 2, , p. 203–221 (DOI 10.1016/0022-0981(74)90046-X, lire en ligne, consulté le )
- (en) Jean-François Rees, Bertrand De Wergifosse, Olivier Noiset et Marlene Dubuisson, « The Origins of Marine Bioluminescence: Turning Oxygen Defence Mechanisms Into Deep-Sea Communication Tools », Journal of Experimental Biology, vol. 201, no 8, , p. 1211–1221 (ISSN 0022-0949 et 1477-9145, DOI 10.1242/jeb.201.8.1211, lire en ligne, consulté le )
- (en) J.R. Turner, E.M. White, M.A. Collins et J.C. Partridge, « Vision in lanternfish (Myctophidae): Adaptations for viewing bioluminescence in the deep-sea », Deep Sea Research Part I: Oceanographic Research Papers, vol. 56, no 6, , p. 1003–1017 (DOI 10.1016/j.dsr.2009.01.007, lire en ligne, consulté le )
- (en) Ea Pakhomov, R Perissinotto et Cd McQuaid, « Prey composition and daily rations of myctophid fishes in the Southern Ocean », Marine Ecology Progress Series, vol. 134, , p. 1–14 (ISSN 0171-8630 et 1616-1599, DOI 10.3354/meps134001, lire en ligne, consulté le )
- Ryan A. Saunders, Simeon L. Hill, Geraint A. Tarling et Eugene J. Murphy, « Myctophid Fish (Family Myctophidae) Are Central Consumers in the Food Web of the Scotia Sea (Southern Ocean) », Frontiers in Marine Science, vol. 6, (ISSN 2296-7745, DOI 10.3389/fmars.2019.00530, lire en ligne, consulté le )
- (en) P. Dalpadado et J. Gj�s�ter, « Feeding ecology of the lanternfish Benthosema pterotum from the Indian Ocean », Marine Biology, vol. 99, no 4, , p. 555–567 (ISSN 0025-3162 et 1432-1793, DOI 10.1007/BF00392563, lire en ligne, consulté le )
- (en) S. Wajih A. Naqvi, Hermann W. Bange, Stuart W. Gibb et Catherine Goyet, « Biogeochemical ocean-atmosphere transfers in the Arabian Sea », Progress in Oceanography, vol. 65, nos 2-4, , p. 116–144 (DOI 10.1016/j.pocean.2005.03.005, lire en ligne, consulté le )
- (en) Johannes Kinzer, Ruth Böttger-Schnack et Knud Schulz, « Aspects of horizontal distribution and diet of myctophid fish in the Arabian Sea with reference to the deep water oxygen deficiency », Deep Sea Research Part II: Topical Studies in Oceanography, vol. 40, no 3, , p. 783–800 (DOI 10.1016/0967-0645(93)90058-U, lire en ligne, consulté le )
- (en) Hikaru Watanabe, Masatoshi Moku, Kouichi Kawaguchi et Kimie Ishimaru, « Diel vertical migration of myctophid fishes (Family Myctophidae) in the transitional waters of the western North Pacific », Fisheries Oceanography, vol. 8, no 2, , p. 115–127 (ISSN 1054-6006 et 1365-2419, DOI 10.1046/j.1365-2419.1999.00103.x, lire en ligne, consulté le )
- (en) Chiyuki Sassa, Kouichi Kawaguchi, Yuichi Hirota et Minoru Ishida, « Distribution depth of the transforming stage larvae of myctophid fishes in the subtropical–tropical waters of the western North Pacific », Deep Sea Research Part I: Oceanographic Research Papers, vol. 54, no 12, , p. 2181–2193 (DOI 10.1016/j.dsr.2007.09.006, lire en ligne, consulté le )
- T. B. Linkowski, « Lunar rhythms of vertical migrations coded in otolith microstructure of North Atlantic lanternfishes, genus Hygophum (Myctophidae) », Marine Biology, vol. 124, no 4, , p. 495–508 (ISSN 0025-3162 et 1432-1793, DOI 10.1007/bf00351031, lire en ligne, consulté le )
- (en) Adrian J. Flynn et John R. Paxton, « Spawning aggregation of the lanternfish Diaphus danae (family Myctophidae) in the north-western Coral Sea and associations with tuna aggregations », Marine and Freshwater Research, vol. 63, no 12, , p. 1255 (ISSN 1323-1650, DOI 10.1071/MF12185, lire en ligne, consulté le )
- (en) Chiyuki Sassa et Motomitsu Takahashi, « Diurnal maturation rhythm, spawning frequency and fecundity of Diaphus fulgens (Teleostei: Myctophidae) in the Kuroshio waters of the East China Sea », Deep Sea Research Part I: Oceanographic Research Papers, vol. 184, , p. 103768 (DOI 10.1016/j.dsr.2022.103768, lire en ligne, consulté le )
- (en) Mary-Anne Lea, Peter D. Nichols et Gareth Wilson, « Fatty acid composition of lipid-rich myctophids and mackerel icefish (Champsocephalus gunnari) – Southern Ocean food-web implications », Polar Biology, vol. 25, no 11, , p. 843–854 (ISSN 0722-4060 et 1432-2056, DOI 10.1007/s00300-002-0428-1, lire en ligne, consulté le )
- (en) Mari Butler, Stephen M Bollens, Brenda Burkhalter et Laurence P Madin, « Mesopelagic fishes of the Arabian Sea: distribution, abundance and diet of Chauliodus pammelas, Chauliodus sloani, Stomias affinis, and Stomias nebulosus », Deep Sea Research Part II: Topical Studies in Oceanography, vol. 48, nos 6-7, , p. 1369–1383 (DOI 10.1016/S0967-0645(00)00143-0, lire en ligne, consulté le )
- (en) Gabriele Stowasser, David W. Pond et Martin A. Collins, « Using fatty acid analysis to elucidate the feeding habits of Southern Ocean mesopelagic fish », Marine Biology, vol. 156, no 11, , p. 2289–2302 (ISSN 0025-3162 et 1432-1793, DOI 10.1007/s00227-009-1256-4, lire en ligne, consulté le )
- Ainhoa Bernal, Víctor Manuel Tuset et María Pilar Olivar, « Multiple Approaches to the Trophic Role of Mesopelagic Fish around the Iberian Peninsula », Animals, vol. 13, no 5, , p. 886 (ISSN 2076-2615, DOI 10.3390/ani13050886, lire en ligne, consulté le )
- « IUEM – Institut Universitaire Européen de la Mer », (consulté le )
- (en) Mari Butler, Stephen M Bollens, Brenda Burkhalter et Laurence P Madin, « Mesopelagic fishes of the Arabian Sea: distribution, abundance and diet of Chauliodus pammelas, Chauliodus sloani, Stomias affinis, and Stomias nebulosus », Deep Sea Research Part II: Topical Studies in Oceanography, vol. 48, nos 6-7, , p. 1369–1383 (DOI 10.1016/S0967-0645(00)00143-0, lire en ligne, consulté le )
- (en) Kouichi Kawaguchi et Keiko Aioi, « Myctophid fishes of the genusMyctophum (myctophidae) in the pacific and Indian oceans », Journal of Oceanography, vol. 28, no 4, , p. 161–175 (ISSN 0916-8370 et 1573-868X, DOI 10.1007/BF02108760, lire en ligne, consulté le )
- (en) Hiroki Yasuma, Yoshimi Takao, Kouichi Sawada et Kazushi Miyashita, « Target strength of the lanternfish, Stenobrachius leucopsarus (family Myctophidae), a fish without an airbladder, measured in the Bering Sea », ICES Journal of Marine Science, vol. 63, no 4, , p. 683–692 (ISSN 1095-9289 et 1054-3139, DOI 10.1016/j.icesjms.2005.02.016, lire en ligne, consulté le )
- Ryan A. Saunders, Simeon L. Hill, Geraint A. Tarling et Eugene J. Murphy, « Myctophid Fish (Family Myctophidae) Are Central Consumers in the Food Web of the Scotia Sea (Southern Ocean) », Frontiers in Marine Science, vol. 6, (ISSN 2296-7745, DOI 10.3389/fmars.2019.00530, lire en ligne, consulté le )
- (en) Amane Hayashi, Hikaru Watanabe, Minoru Ishida et Kouichi Kawaguchi, « Growth of Myctophum asperum (Pisces: Myctophidae) in the Kuroshio and transitional waters », Fisheries Science, vol. 67, no 5, , p. 983–984 (ISSN 0919-9268 et 1444-2906, DOI 10.1046/j.1444-2906.2001.00350.x, lire en ligne, consulté le )
- (en) T. Valinassab, G. J. Pierce et K. Johannesson, « Lantern fish (Benthosema pterotum) resources as a target for commercial exploitation in the Oman Sea », Journal of Applied Ichthyology, vol. 23, no 5, , p. 573–577 (ISSN 0175-8659 et 1439-0426, DOI 10.1111/j.1439-0426.2007.01034.x, lire en ligne, consulté le )
- « FAO Fisheries Department - FAO Fisheries Circular No. 920 FIRM/C920 », sur www.fao.org (consulté le )
- « Aquaculture and capture fisheries », OECD-FAO Agricultural Outlook 2019-2028, (ISSN 1999-1142, DOI 10.1787/01e1d7e5-en, lire en ligne, consulté le )
- (en) Jennifer J. Freer, Geraint A. Tarling, Martin A. Collins et Julian C. Partridge, « Predicting future distributions of lanternfish, a significant ecological resource within the Southern Ocean », Diversity and Distributions, (ISSN 1366-9516 et 1472-4642, DOI 10.1111/ddi.12934, lire en ligne, consulté le )
- World Register of Marine Species, consulté le 19 février 2016