Pémétrexed
| Pémétrexed | ||

| ||
 | ||
| Identification | ||
|---|---|---|
| DCI | pémétrexed | |
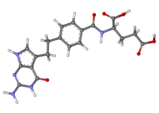
| Nom UICPA | acide (2S)-2-[[4-[2-(2-amino-4-oxo-1,7-dihydropyrrolo[2,3-d]pyrimidin-5-yl)éthyl]benzoyl]amino]pentanedioïque | |
| No CAS | (sel disodique) |
|
| No ECHA | 100.205.735 | |
| Code ATC | « BA04 » | |
| DrugBank | DB00642 | |
| PubChem | 446556 | |
| ChEBI | 63616 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C20H21N5O6 [Isomères] |
|
| Masse molaire[1] | 427,410 6 ± 0,020 3 g/mol C 56,2 %, H 4,95 %, N 16,39 %, O 22,46 %, |
|
| Considérations thérapeutiques | ||
| Classe thérapeutique | Antimétabolites | |
| Voie d’administration | Intraveineuse | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Le pémétrexed (LY231514 ; Alimta) est un médicament anticancéreux utilisé dans le traitement du mésothéliome pleural malin et du cancer bronchique non à petites cellules, commercialisé par le laboratoire américain Eli Lilly.
Le pémétrexed est un analogue de l'acide folique inhibant préférentiellement la réplication des cellules cancéreuses.
Historique de découverte[modifier | modifier le code]
Depuis le milieu des années 1970, l'équipe du Dr Edward C. Taylor, chimiste à l'université de Princeton et ancien consultant pour la firme pharmaceutique Eli Lilly basée à Indianapolis, s’intéressait aux inhibiteurs de l'acide folique (aminoptérine, méthotrexate, etc.) avec pour objectif de synthétiser de nouveaux dérivés moins toxiques[2],[3].
Dans les années 1980, en collaboration avec le Dr Chuan Shih, responsable du développement de médicaments anticancéreux d'Eli Lilly[4],[5], des dérivés de l'acide folique (5,10-didéaza-5,6,7,8 tétrahydrofolate ; Lometrexol[6]) ont été testés in vitro sur des modèles animaux et de xénogreffes humaines, montrant une activité plus importante que le méthotrexate[7]. Cependant, ce composé nécessitait pour sa synthèse 23 étapes dont le produit final était un diastéréo-isomère du carbone 6, dont seule l'une des deux formes devait être utilisée dans les essais cliniques conformément aux instructions de la FDA, mais le rendement de récupération était très faible[8]. Afin de contourner le problème, l'échange du noyau ptéridine pour une pyrrolo pyrimidine a abouti au composé LY231514 (pémétrexed) synthétisé en 1989[9],[2],[10]. Le premier brevet a été publié en 1991 et le développement de la molécule en médicament a été réalisé par la firme.
Synthèse chimique[modifier | modifier le code]
Synthèse industrielle[modifier | modifier le code]
La synthèse industrielle développée par les chimistes d'Eli Lilly fait intervenir la réaction entre le 2-bromo-4-arylbutanal et la 2,4-diamino-6-hydroxypyrimidine conduisant à la pyrrolo[2,3-d]pyrimidine. L'addition finale de l'acide glutamique aboutit au pémétrexed[11].
Mécanisme d'action et devenir dans l'organisme[modifier | modifier le code]
Mécanisme d'action[modifier | modifier le code]
Le pémétrexed est un membre de la classe des antimétabolites analogues de l'acide folique. Le pémétrexed bloque des processus métaboliques folate-dépendants essentiels à la réplication cellulaire par le biais de l'inhibition de la thymidylate synthétase (TS), la dihydrofolate réductase (DHFR) et la glycinamide ribonucléotide formyltransférase (GARFT). Ces enzymes folate-dépendantes jouent un rôle clé pour la biosynthèse de novo de la thymidine et des nucléotides puriques nécessaires pour la réplication cellulaire.
Pharmacogénomique[modifier | modifier le code]
Pharmacocinétique[modifier | modifier le code]
Distribution[modifier | modifier le code]
La liaison aux protéines plasmatiques est de 81 %. Le volume de distribution à l'état d'équilibre est de 16,1 litres.
Métabolisation et excrétion[modifier | modifier le code]
Le pémétrexed est peu métabolisé. Il est excrété par voie rénale, sa clairance systémique totale est de 91,8 ml/min et sa demi-vie est de 3,5 heures pour une fonction rénale normale (90 ml/min)[12]. Après administration, 90 % de la dose est retrouvée sous forme inchangée dans les urines en 24 heures[13].
Co-administrations médicamenteuses[modifier | modifier le code]
L'administration de cisplatine et des vitamines B9 et B12 concomitamment ne modifie pas la pharmacocinétique du pémétrexed.
Indications, posologies et modalités d'administration[modifier | modifier le code]
Indications AMM[modifier | modifier le code]
Le pémétrexed peut être administré seul ou en association avec le cisplatine fréquemment utilisé dans les indications pulmonaires.
Mésothéliome pleural malin [modifier | modifier le code]
Le mésothéliome est un cancer lié dans 80 % des cas à une exposition à l'amiante[14].
En première ligne[modifier | modifier le code]
- Dans le mésothéliome pleural malin non résécable en association avec le cisplatine.
Cancer bronchique non à petites cellules [modifier | modifier le code]
En monothérapie[modifier | modifier le code]
En seconde ligne[modifier | modifier le code]
- Cancer bronchique non à petites cellules, localement avancé ou métastatique dès lors que l'histologie n'est pas à prédominance épidermoïde.
- Dans le traitement de maintenance du cancer bronchique non à petites cellules, localement avancé ou métastatique immédiatement à la suite d'une chimiothérapie à base de sel de platine (cisplatine ou carboplatine).
En association[modifier | modifier le code]
En première ligne[modifier | modifier le code]
- Cancer bronchique non à petites cellules localement avancé ou métastatique avec le cisplatine.
Posologie et adaptation[modifier | modifier le code]
Posologie[modifier | modifier le code]
Le pémétrexed à la posologie de 500 mg·m-2 (de surface corporelle) sera administré par voie intraveineuse sur dix minutes, tous les 21 jours.
Adaptation de posologie[modifier | modifier le code]
Le pémétrexed est contre-indiqué chez le patient ayant un DFG < 45 ml/min. Au-delà de 45 ml/min, il peut être utilisé à dose normale.
Modalités de reconstitution et d'administration[modifier | modifier le code]
- L'Alimta existe en deux dosages : 100 mg et 500 mg. Il se présente en poudre lyophilisée de couleur blanche à jaune pâle ou jaune verdâtre.
- Le flacon de 100 mg est à reconstituer à l'aide de 4,2 ml de chlorure de sodium à 0,9 %. Le flacon à 500 mg est lui à reconstituer avec 20 ml de chlorure de sodium à 0,9 %. Après homogénéisation, il est à diluer en poche pour perfusion de 100 ml, également avec du chlorure de sodium 0,9 %.
- Après reconstitution dans du chlorure de sodium 0,9 %, le pémétrexed est stable 24 heures à température ambiante[15].
- En cas d'association avec le cisplatine, la perfusion de cisplatine commencera au minimum 30 minutes après la fin de la perfusion de pémétrexed.
- Le pémétrexed est incompatible avec les diluants contenant du calcium, comme les solutions de Ringer et Ringer lactate.
- En l'absence d'étude de stabilité, le pémétrexed ne doit pas être injecté en même temps que d'autres médicaments.
Utilisation[modifier | modifier le code]
Précautions d'emploi[modifier | modifier le code]
Prémédication[modifier | modifier le code]
Dans les études de phase I, des rash cutanés sont apparus chez certains patients, prévenus dans la suite des études par une prémédication par corticoïdes la veille, le jour de l'administration de pémétrexed et le lendemain matin[3],[16],[17].
Par ailleurs, afin de réduire la toxicité du pémétrexed, une prémédication par acide folique et vitamine B12 sera effectuée :
- la prise d'acide folique dosé à 0,4 mg se fera dans la semaine précédant l'injection du pémétrexed, pendant toute la durée du traitement et jusqu'à 3 semaines après la dernière administration ;
- l'injection de vitamine B12 en intramusculaire se fera dans la semaine précédant l'administration de pémétrexed puis une fois tous les 3 cycles, dans ce dernier cas, l'injection pourra avoir lieu le jour de l'administration de la chimiothérapie.
Surveillance biologique[modifier | modifier le code]
Avant toute administration de pémétrexed :
- une numération de formule sanguine doit être réalisée incluant la mesure du taux de plaquettes ;
- un bilan biochimique évaluant la fonction rénale (créatininémie) et hépatique (ASAT/ALAT, PAL, bilirubine totale) sera également effectué.
Effets indésirables[modifier | modifier le code]
- Myélosuppression : Neutropénie, anémie, thrombopénie
- Raison majeure d'arrêt du traitement, le nadir est atteint vers J10.
- Toxicités gastro-intestinales : nausées, vomissements, anorexie, mucite, stomatite/pharyngite, diarrhée, constipation, dyspepsies[18]
- Déshydratation avec hyponatrémie pouvant entraîner des affections oculaires telles que des conjonctivites
- L'intensité de l'hyponatrémie semble corrélée à l'exposition au pémétrexed (AUC) et inversement corrélée avec la clairance de la créatinine[19].
- Éruption cutanée et desquamation
- Caractérisée par des œdèmes faciaux, périorbitaires ou touchant les membres, avec parfois des œdèmes à type de sclérodermie réversible à l'arrêt du traitement[20].
- Alopécie
- Elle intervient dans environ 6 % des cas lors de l'administration de pémétrexed seul et dans environ 11 % des cas lorsque celui-ci est donné en association avec le cisplatine[21].
- Fatigue
- Elle intervient dans environ 1/3 des cas lors de l'administration de pémétrexed seul et dans environ 1 cas sur 2 lorsque celui-ci est donné en association avec le cisplatine[21].
- Toxicité hépatique (élévation des ASAT/ALAT)
- Très fréquente (environ 80 % des cas) et transitoire.
- Toxicité rénale
- Celle-ci est progressive et cumulative[22].
Contre-indications[modifier | modifier le code]
- Hypersensibilité à la substance active ou à l'un des excipients (principalement le mannitol utilisé pour assurer une iso-osmolarité du médicament). Cette hypersensibilité reste exceptionnelle au vu de la dose utilisée.
- Grossesse et allaitement (passage de pémétrexed au fœtus et à l'enfant).
- Association concomitante avec le vaccin contre la fièvre jaune (vaccin vivant atténué avec risque de fièvre jaune induite de par la neutropénie fréquente provoquée par le pémétrexed).
Interactions médicamenteuses[modifier | modifier le code]
Études pré-cliniques[modifier | modifier le code]
La combinaison pémétrexed + cisplatine a montré une activité anticancéreuse in vitro sur les lignées de cellules humaines de cancer bronchique non à petites cellules (H460) et sur un modèle animal de souris après xénogreffe de cellules cancéreuses Calu-6[23].
Études cliniques[modifier | modifier le code]
Phases I et II[modifier | modifier le code]
Trois études de phase 1 ont été réalisées afin de déterminer la dose appropriée de pémétrexed. Dans ces 3 études, la durée de perfusion était de 10 minutes[24].
Dans la première étude a été administrée de manière hebdomadaire une dose de 10 à 40 mg/m2 pendant 4 semaines toutes les 6 semaines. La dose maximale tolérée était de 40 mg/m2. Dans la deuxième étude, le pémétrexed a été administré entre 0,2 et 5,2 mg/m2 chaque jour pendant 5 jours toutes les 3 semaines. La dose journalière maximale tolérée était de 4 mg/m2. Dans la troisième étude, le pémétrexed a été administré entre 50 et 700 mg/m2 une fois toutes les 3 semaines. La dose maximale tolérée était alors de 600 mg/m2 avec une dose limitante causée par la toxicité hématologique et la fatigue. Sur la base de la plus haute dose-intensité possible, le 3e schéma d'administration a finalement été retenu.
La dose initialement retenue pour la phase 2 était de 600 mg/m2, réduite par la suite à 500 mg/m2 en raison des toxicités induites. Il a par ailleurs été observé que la toxicité hématologique était corrélée à la fonction rénale. Une nouvelle étude de phase 1 a alors été menée stratifiant les patients en fonction de leur fonction rénale. La clairance rénale étant corrélée au taux de filtration glomérulaire.
Le pémétrexed a par la suite été testé en monothérapie et en association avec l'irinotécan, la gemcitabine, les taxanes, la vinorelbine, les sels de platine, la doxorubicine et le fluorouracil, et présente une activité dans les mésothéliomes, le cancer du poumon non à petites cellules, le cancer du sein, de l'utérus, de la vessie, de la tête et du cou, le cancer colorectal et pancréatique[24]. Une concentration sanguine élevée en acide méthylmalonique, signe d'un déficit en vitamine B12 ou vitamine B9 (folates), a été associée au cours d'une étude à des diarrhées et des mucites plus fréquentes. Une supplémentation en folates (350 à 1 000 μg) et vitamine B12 (1 000 μg en IM) toutes les 9 semaines a donc été lancée.
Phase III[modifier | modifier le code]
Mésothéliome (1re ligne)[modifier | modifier le code]
Étude EMPACIS : étude de phase 3 multicentrique, randomisée, en simple aveugle, comparant pémétrexed + cisplatine vs cisplatine seul. La survie globale médiane est de 12,1 mois dans le groupe pémétrexed et de 9,3 mois dans le groupe cisplatine seul.
Cancer bronchique non à petites cellules (CBNPC)[modifier | modifier le code]
1re ligne :
Étude clinique de phase 3 multicentrique, randomisée, en ouvert comparant pémétrexed + cisplatine vs gemcitabine + cisplatine. L'analyse statistique a montré la non-infériorité du pémétrexed + cisplatine.
2e ligne :
Étude clinique de phase 3 multicentrique, randomisée, en ouvert comparant pémétrexed vs docétaxel. La médiane de survie globale est de 8,3 mois pour le groupe pémétrexed (population en intention de traiter : n = 283) et de 7,9 mois pour le groupe docétaxel (population en intention de traiter : n = 288). Une analyse de l'influence de l'histologie du CBNPC sur l'effet du traitement sur la survie globale a été réalisée. Les résultats sont en faveur du pémétrexed lorsque l'histologie n'est pas à prédominance épidermoïde (n = 399, 9,3 vs 8,0 mois), et en faveur du docétaxel lorsque l'histologie est de type carcinome à cellules épidermoïdes (n = 172, 6,2 vs 7,4 mois).
Traitement de maintenance
Étude JMEN[25] : étude de phase 3 multicentrique, randomisée, en double aveugle, contrôlée versus placebo. La survie sans progression était meilleure dans le groupe pémétrexed par rapport au groupe placebo (médiane de 4,0 vs 2,0 mois). La survie globale médiane pour la population globale (n = 663) était de 13,4 mois pour le bras pémétrexed et 10,6 mois pour le bras placebo.
Étude PARAMOUNT[26]: étude de phase 3 multicentrique, randomisée, en double aveugle, contrôlée versus placebo. L'étude a atteint son objectif principal et a montré une amélioration statistiquement significative de la survie sans progression dans le groupe pémétrexed par rapport au groupe placebo (médianes de 3,9 vs 2,6 mois). À la suite d'un traitement d'induction avec pémétrexed + cisplatine (4 cycles), le traitement par pémétrexed était statistiquement supérieur au placebo pour la survie globale (médiane de 13,9 mois versus 11,0 mois). Lors de l'analyse finale de la survie, 28,7 % des patients étaient en vie ou perdus de vue dans le bras pémétrexed vs 21,7 % dans le bras placebo. Les taux de survie à 1 an et à 2 ans des patients sous pémétrexed étaient de 58 % et 32 % respectivement, comparés à 45 % et 21 % pour les patients sous placebo.
Phase IV[modifier | modifier le code]
La toxicité rénale des antimétabolites est connue. Celle-ci a également été rapportée avec le pémétrexed dans des études cliniques et dans des cas rapportés dans la littérature avec une insuffisance rénale aiguë apparaissant de J2 à J54. Ainsi, 5 à 10 % des patients recevant plus de 4 cycles de chimiothérapie par le pémétrexed développent une toxicité rénale progressive et cumulative[27].
Autres études cliniques[modifier | modifier le code]
Le pémétrexed a été testé dans les cancers du côlon, du sein, du pancréas, de l'estomac, de la vessie, du col de l'utérus et de la tête et du cou[27].
Renseignements administratifs[modifier | modifier le code]
Autorisation de mise sur le marché (AMM)[modifier | modifier le code]
Le traitement par le pémétrexed du mésothéliome pleural malin, indication de niche, a été approuvé par la FDA et l'Agence européenne des médicaments (AEM) en 2004, prélude à d'autres demandes dans des indications plus larges telles que le traitement de première ligne du cancer bronchique non à petites cellules autorisé par la FDA en 2008 et en traitement de maintenance en 2009.
Avis des autorités de santé[modifier | modifier le code]
Haute Autorité de santé (France)[modifier | modifier le code]
La Haute Autorité de santé (HAS) considère que le service médical rendu par l’Alimta est important. Par ailleurs, dans le traitement du CBNPC, si l’histologie n’est pas à prédominance épidermoïde, en 1re ligne de traitement et en association avec le cisplatine, l’Alimta n’apporte pas d’amélioration du service médical rendu (ASMR V) par rapport à la gemcitabine[28].
NICE (Royaume-Uni)[modifier | modifier le code]
Prise en charge[modifier | modifier le code]
Le coût de l'Alimta à 100 mg est de 215,681 € HT et de 1 026 € HT pour celui à 500 mg (données du )[29].
L'Alimta est un médicament qui peut être rétrocédé aux particuliers et facturé dans le cadre d'une hospitalisation en sus du GHS. Il est alors remboursé à 100 %.
Marché[modifier | modifier le code]
Les ventes d'Alimta ont rapporté à l'entreprise Eli Lilly 142,6 millions de dollars US en 2004, et plus de 2,79 milliards de dollars en 2014, ce qui en fait le médicament le plus vendu du groupe[30],[31].
Le brevet principal d'exploitation de l'Alimta prévoyait la fin du monopole en .
Le brevet d'exploitation du pémétrexed expirant en 2015, la société Actavis a attaqué le brevet d'Eli Lilly et remporté en Allemagne son procès.
Les royalties reversées à l'université de Princeton ont permis de financer la construction d'un bâtiment consacré à la chimie sur le campus de l'université[32].
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « dailyprincetonian.com/news/200… »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?).
- « Chemistry International -- Newsmagazine for IUPAC », sur iupac.org (consulté le ).
- Brevet US 4871743 A
- « reuters.com/article/2010/03/12… »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?).
- E. C. Taylor, P. J. Harrington, S. R. Fletcher et G. P. Beardsley, « Synthesis of the antileukemic agents 5,10-dideazaaminopterin and 5,10-dideaza-5,6,7,8-tetrahydroaminopterin », Journal of Medicinal Chemistry, vol. 28, , p. 914-921 (ISSN 0022-2623, PMID 4009615, lire en ligne, consulté le )
- Discovery and Synthesis of Alimta, A New and Broadly Effective Antitumor Agent, présentation PowerPoint de Edward C. Taylor.
- (en) R. G. Moran, S. W. Baldwin, E. C. Taylor et C. Shih, « The 6S- and 6R-diastereomers of 5, 10-dideaza-5, 6, 7, 8-tetrahydrofolate are equiactive inhibitors of de novo purine synthesis. », Journal of Biological Chemistry, vol. 264, 12/15/1989, p. 21047-21051 (ISSN 0021-9258 et 1083-351X, PMID 2592365, lire en ligne, consulté le )
- (en) « Synthesis of pyrazolo[3,4-d]pyrimidine analogues of the potent antitumor agent N-{4-[2-(2-amino-4(3H)-oxo-7H-pyrrolo[2,3-d]pyrimidin-5-yl)ethyl]benzoyl}-L-glutamic acid (LY231514) », Tetrahedron,
- (en) Shrikanta Chattopadhyay, Richard G. Moran et I. David Goldman, « Pemetrexed: biochemical and cellular pharmacology, mechanisms, and clinical applications », Molecular Cancer Therapeutics, vol. 6, , p. 404-417 (ISSN 1535-7163 et 1538-8514, PMID 17308042, DOI 10.1158/1535-7163.MCT-06-0343, lire en ligne, consulté le )
- Charles J. Barnett, Thomas M. Wilson et Michael E. Kobierski, « A Practical Synthesis of Multitargeted Antifolate LY231514 », Organic Process Research & Development, vol. 3, , p. 184-188 (ISSN 1083-6160, DOI 10.1021/op9802172, lire en ligne, consulté le )
- (en) « Pemetrexed in malignant pleural mesothelioma. », Clin. Cancer Res.,
- (en) « FDA drug approval summaries: pemetrexed (Alimta) », Oncologist,
- (en) « Malignant mesothelioma », The Lancet,
- Ann. Pharmacother., 40, 6 : 1082-1085, 2006
- http://www.ema.europa.eu/docs/fr_FR/document_library/EPAR_-_Product_Information/human/000564/WC500025611.pdf
- (ja) Michihiro Shino, « [Effectiveness of Steroids for the Rash Side Effect of Pemetrexed] - PubMed », Gan to kagaku ryoho. Cancer & chemotherapy, vol. 40, no 1, , p. 75–78 (ISSN 0385-0684, PMID 23306922, lire en ligne, consulté le ).
- Site E-Vidal
- (en) Kumar Prabhash, « High Plasma Exposure to Pemetrexed Leads to Severe Hyponatremia in Patients With Advanced Non Small Cell Lung Cancer Receiving Pemetrexed-Platinum Doublet Chemotherapy - PubMed », Cancer management and research, vol. 6, , p. 261–265 (ISSN 1179-1322, PMID 24940080, DOI 10.2147/CMAR.S60177, lire en ligne, consulté le ).
- « Widespread use of pemetrexed in oncology: has it turned it into a new drug? - Cidon - Chinese Clinical Oncology », sur www.thecco.net (consulté le )
- « Résumé des caractéristiques du produit », sur www.ema.europa.eu (consulté le )
- Hassan Izzedine, « [Pemetrexed nephrotoxicity] », Bulletin du Cancer, vol. 102, , p. 190-197 (ISSN 1769-6917, PMID 25641712, DOI 10.1016/j.bulcan.2014.12.012, lire en ligne, consulté le )
- (en) « Treatment regimens including the multitargeted antifolate LY231514 in human tumor xenografts. », Clinical Cancer Research,
- (en) Stephen Neidle, Cancer Drug Design and Discovery
- (en) « Maintenance pemetrexed plus best supportive care versus placebo plus best supportive care for non-small-cell lung cancer: a randomised, double-blind, phase 3 study », The Lancet,
- (en) Luis G. Paz-Ares, « PARAMOUNT: Final Overall Survival Results of the Phase III Study of Maintenance Pemetrexed Versus Placebo Immediately After Induction Treatment With Pemetrexed Plus Cisplatin for Advanced Nonsquamous Non–Small-Cell Lung Cancer », Journal of clinical oncology,
- Hassan Izzedine, « Pemetrexed nephrotoxicity », Bulletin du Cancer, vol. 102, , p. 190-197 (ISSN 1769-6917, PMID 25641712, DOI 10.1016/j.bulcan.2014.12.012, lire en ligne, consulté le )
- « Haute Autorité de Santé - Alimta », sur www.has-sante.fr (consulté le )
- Site thériaque
- David VoreacosSusan Decker, « Princeton Drug Royalties Spark Suit Over Tax Exemption », sur Bloomberg.com (consulté le )
- « Eli Lilly loses Alimta drug patent case in Germany to Actavis », Reuters, (lire en ligne, consulté le )
- « Eli Lilly's Alimta gains may cause Princeton pain », sur FiercePharma (consulté le )
