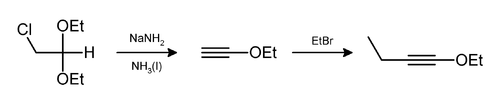Amidure de sodium
| Amidure de sodium | |
| |
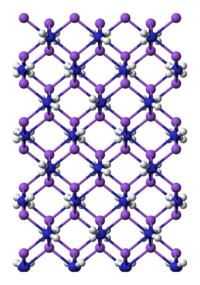
| Amidure de sodium : en bleu, les atomes d'azote, en violet, les sodium et en blanc, les hydrogène | |
| Identification | |
|---|---|
| Nom UICPA | sodium amide |
| No CAS | |
| No ECHA | 100.029.064 |
| No CE | 231-971-0 |
| PubChem | 24533 |
| Apparence | poudre grisâtre, incolore quand elle est pure |
| Propriétés chimiques | |
| Formule | H2NNa |
| Masse molaire[2] | 39,012 3 ± 0,000 3 g/mol H 5,17 %, N 35,9 %, Na 58,93 %, |
| pKa | 38 [1] |
| Propriétés physiques | |
| T° fusion | 210 °C |
| T° ébullition | 400 °C |
| Solubilité | soluble dans l'ammoniac, réagit avec l'eau |
| Masse volumique | 1,39 g·cm-3 |
| T° d'auto-inflammation | 450 °C |
| Point d’éclair | 4,44 °C |
| Cristallographie | |
| Structure type | orthogonal |
| Précautions | |
| NFPA 704 | |
| Directive 67/548/EEC | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'amidure de sodium est le composé chimique de formule brute NaNH2. Ce composé qui réagit violemment avec l'eau, est blanc quand il est pur ; dans le commerce il est typiquement gris, ce qui est dû à la présence d'une petite quantité de fer métallique issue du processus de préparation. De telles impuretés n'affectent généralement pas la réactivité de l'amidure de sodium. NaNH2 est très largement employé en synthèse organique comme base forte.
Préparation et structure[modifier | modifier le code]
L'amidure de sodium peut être préparé par la réaction du sodium sur l'ammoniac gazeux (NH3)[3] mais généralement la réaction dans l'ammoniac liquide en utilisant du nitrate de fer(III) comme catalyseur est préférée. En effet, cette réaction est plus rapide au point d'ébullition de l'ammoniac, c'est-à-dire −33 °C[4] :
- 2 Na + 2 NH3 → 2 NaNH2 + H2
NaNH2 est un composé plutôt ionique et comme tel cristallise en un polymère tridimensionnel et infini[5]. La géométrie autour des atomes de sodium est tétraédrique[6]. Dans l'ammoniac, l'amide de sodium forme des solutions conductrices, ce qui s'explique par la présence des ions Na(NH3)6+ et des anions NH2−.
Emplois[modifier | modifier le code]
L'amidure de sodium est utilisé dans les productions industrielles d'indigo, d'hydrazine et de cyanure de sodium[7]. C'est un réactif de choix pour l'assèchement de l'ammoniac (liquide ou gazeux) mais son emploi principal est celui d'une base forte en chimie organique, souvent en solution dans l'ammoniac liquide. L'un des principaux avantages de l'utilisation de l'amidure de sodium est qu'il est une excellente base et un mauvais nucléophile. Cependant, du fait de sa faible solubilité, il est souvent remplacé par des réactifs comme l'hydrure de sodium, le bis(triméthylsilyl)amidure de sodium (NaHMDS) ou le diisopropylamidure de lithium (LDA).
Synthèse des alcynes[modifier | modifier le code]
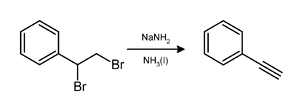
L'amidure de sodium induit la perte de deux molécules de bromure d'hydrogène (HBr) sur les dibromoalcanes vicinaux pour donner une triple liaison carbone-carbone, comme dans la synthèse du phényléthyne[8]:
Normalement deux équivalents d'amidure de sodium produisent l'alcyne désiré. Cependant, trois équivalents sont nécessaires pour la préparation d'un alcyne terminal parce que dans ce type d'alcyne, l'atome d'hydrogène terminal est acide et est immédiatement déprotoné par un équivalent de la base.
Du chlorure d'hydrogène (HCl) et/ou de l'éthanol (C2H5OH) peuvent aussi être éliminés de la même façon[9] comme dans la préparation du 1-éthoxy-but-1-yne[10]:
Réactions de cyclisation[modifier | modifier le code]
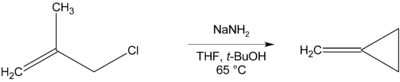
S'il n'y a pas d'atome d'hydrogène en β pouvant être éliminé, des composés cycliques peuvent être formés, comme dans la préparation du méthylènecyclopropane[11]:
Des cyclopropènes[12], des aziridines[13] et des cyclobutanes[14] peuvent être formés de cette manière.
déprotonation de carbone et d'azote acides[modifier | modifier le code]
Les atomes de carbone acides qui peuvent être déprotonés par l'amidure de sodium dans l'ammoniac liquide sont, entre autres, les alcynes terminaux[15], les méthyl cétones[16], les cyclohexanones[17], l'acide phénylacétique et ses dérivés[18] et les diphénylméthanes[19]. L'acétylacétone perd deux protons et forme un dianion[20]:
L'amidure de sodium déprotone aussi les indoles[21] et les pipéridines[22].
Autres réactions[modifier | modifier le code]
- Réarrangement avec ortho-déprotonation[23].
- Synthèse d'oxiranes (via carbène?)[24]
- synthèse d'indoles[25]
- Réaction de Chichibabin
Sécurité[modifier | modifier le code]
L'amidure de sodium réagit violemment avec l'eau pour produire de l'ammoniac et de l'hydroxyde de sodium et brûle dans l'air en donnant des oxydes de sodium et d'azote :
Dans le cas d'une quantité limitée d'air et d'humidité, par exemple dans un conteneur mal fermé, un mélange explosif de produits d'oxydation, caractérisé par un jaunissement ou un brunissement du solide, peut se former. Ainsi l'amidure de sodium doit toujours être conservé dans des conteneurs scrupuleusement fermés et si possible, sous azote. Les parts d'amidure de sodium qui sont de couleur jaune à marron doivent être détruits immédiatement. Une méthode de destruction est d'additionner précautionneusement de l'éthanol à une suspension de cet amidure de sodium dans un solvant hydrocarbure.
L'amidure de sodium est soupçonné d'être corrosif sur la peau, les yeux et les muqueuses. Des précautions doivent être prises pour empêcher la dispersion de poussière d'amidure de sodium.
Notes[modifier | modifier le code]
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Sodium amide » (voir la liste des auteurs).
- Buncel, Menon; J. Organomet. Chem., 1977, 141, 1
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Sodium amide, Bergstrom, F. W.; Org. Synth., 1955, vol. 3, p. 778.
- Sodium Amide, Greenlee, K. W.; Henne, A. L.; Inorganic Syntheses, 1946, vol. 2, p. 128-35.
- The Crystal Structure of Sodium Amide, Zalkin, A.; Templeton, D. H.; Journal of Physical Chemistry, 1956, vol. 60, p. 82-823. DOI 10.1021/j150540a042.
- Structural Inorganic Chemistry, Wells, A.F.; 1984, Oxford: Clarendon Press. (ISBN 0-19-855370-6).
- Merck Index (12th Edn.)
- Phenylacetylene, Campbell, Kenneth N.; Campbell, Barbara K.; Org. Synth., 1950, vol. 4, p. 72.
- Ethoxyacetylene, Jones, E. R. H.; Eglinton, Geoffrey; Whiting, M. C.; Shaw, B. L.; Org. Synth., 1954, vol. 4, p. 404.
Dialkoxyacetylenes: di-tert-butoxyethyne, a valuable synthetic intermediate, Bou, Anna; Pericàs, Miquel A.; Riera, Antoni; Serratosa, Fèlix; Org. Synth., 1987, vol.8, p. 161.
Phenylthioacetylene, Magriotis, Plato A.; Brown, John T.; Org. Synth., 1995, vol. 9, p. 656.
2-Butyn-1-ol, Ashworth, P. J.; Mansfield, G. H.; Whiting, M. C.; Org.Synth., 1955, Vol. 4, p. 128. - 1-Ethoxy-1-butyne, Newman, Melvin S.; Stalick, W. M., Org. Synth., 1977, vol. 6, p. 564.
- Cyclobutanone from methylenecyclopropane via oxaspiropentane, Salaun, J. R.; Champion, J.; Conia, J. M., Org. Synth., 1977, vol. 6, p. 320.
- Synthesis and (3+2)-cycloaddition of a 2,2-dialkoxy-1-methylenecyclopropane: 6,6-dimethyl-1-methylene-4,8-dioxaspiro(2.5)octane and cis-5-(5,5-dimethyl-1,3-dioxan-2-ylidene)hexahydro-1(2H)-pentalen-2-one, Nakamura, Masuharu; Wang, Xio Qun; Isaka, Masahiko; Yamago, Shigeru; Nakamura, Eiichi ; Org. Synth., 2003, vol. 80, p. 144.
- N-Ethylallenimine, Bottini, Albert T.; Olsen, Robert E.; Org. synth., 1964, vol. 5, p. 541.
- 1-Cyanobenzocyclobutene, Skorcz, J. A.; Kaminski, F. E.; Org. synth., 1968, vol. 5, p. 263.
- 1-Ethynylcyclohexanol, Saunders, J. H.; Org. Synth., 1949, vol. 3, p. 416.
(Z)-4-Chloro-4-hexenyl trifluoroacetate, Peterson, P. E.; Dunham, M.; Org. Synth., 1977, vol. 6, p. 273.
Tetrolic acid, Kauer, J. C.; Brown, M.; Org. synth., 1962, vol. 5, p. 1043. - Dimethylethynylcarbinol, Coffman, Donald D.; Org. synth., 1940, vol. 3, p. 320.
Diisovalerylmethane, Hauser, C. R.; Adams, J. T.; Levine, R.; Org. Synth., 1948, vol. 3, p. 291. - 2-Allylcyclohexanone, Vanderwerf, Calvin A.; Lemmerman, Leo V.; Org. Synth., 1948, vol. 3, p. 44.
- α,β-Diphenylpropionic acid, Hauser, Charles R.; Dunnavant, W. R.; Org. Synth., 1960, vol.5, p. 526.
Ethyl 2,4-diphenylbutanoate, Kaiser, Edwin M.; Kenyon, William G.; Hauser, Charles R.; Org. Synth., 1967, vol. 5, p. 559.
α,β-Diphenylcinnamonitrile, Wawzonek, Stanley; Smolin, Edwin M.; Org. Synth., 1957, vol. 4, p. 387. - 1,1-Diphenylpentane, Murphy, William S.; Hamrick, Phillip J.; Hauser, Charles R.; Org. Synth., 1968, vo. 5, p. 523.
- Phenylation of diphenyliodonium chloride: 1-phenyl-2,4-pentanedione, Hampton, K. Gerald; Harris, Thomas M.; Hauser, Charles R.; Org. Synth., 1971, vol. 6, p. 928.
- 1-Methylindole, Potts, K. T.; Saxton, J. E; Org. Synth., 1960, vol. 5, p. 769.
- N-β-Naphthylpiperidine, Bunnett, J. F.; Brotherton, T. K.; Williamson, S. M.; Org. Synth., 1960, vol. 5, p. 816.
- 2-Methylbenzyldimethylamine, Brazen, W. R.; Hauser, C. R.; Org. Synth., 1954, vol. 4, p. 585.
- Phenylmethylglycidic ester, Allen, C. F. H.; VanAllen, J.; Org. Synth., 1944, vol. 3, p. 727.
- 2-Methylindole, Allen, C. F. H.; VanAllen, James; Org. Synth., 1942, vol. 3, p. 597.