Perchlorate de sodium
| Perchlorate de sodium | |
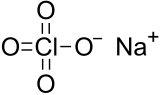
| |
| Identification | |
|---|---|
| Nom UICPA | Perchlorate de sodium |
| No CAS | |
| No ECHA | 100.028.647 |
| No CE | 231-511-9 |
| SMILES | |
| InChI | |
| Apparence | blanc cristallin. |
| Propriétés chimiques | |
| Formule | NaClO4 |
| Masse molaire[1] | 122,44 ± 0,003 g/mol Cl 28,96 %, Na 18,78 %, O 52,27 %, |
| Propriétés physiques | |
| T° fusion | 130 °C monohydrate |
| T° ébullition | 482 °C decomposition |
| Solubilité | solide hygroscopique, soluble dans l'eau et dans l'alcool. |
| Précautions | |
| SGH | |
| H271, H302, H319, H373, P210, P220, P260, P301+P312 et P305+P351+P338 |
|
| Directive 67/548/EEC | |
| Transport | |
| Composés apparentés | |
| Autres cations | Perchlorate de lithium Perchlorate de potassium Perchlorate de rubidium Perchlorate de césium Perchlorate d'ammonium |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le perchlorate de sodium est le sel produit par l'action de l'acide perchlorique sur le cation sodium.
Il contient donc un atome de chlore de valence maximale, +7 et a pour formule NaClO4.
Le perchlorate de sodium (NaClO4) est particulièrement soluble dans l'eau : 209,6 g se solubilisent spontanément dans seulement 100 mL à 25 °C[2], il est ainsi environ 100 fois plus soluble que le KClO4, très soluble dans l'eau (1,5 g se dissolvent dans 100 mL d'eau à 25 °C[3]), et plus soluble que d'autres perchlorates de métaux alcalins, ce qui lui confère des propriétés chimiques mais aussi toxicologiques et écotoxicologiques particulières, notamment pour les organismes aquatiques.
Procédé de fabrication[modifier | modifier le code]
Le perchlorate de sodium est fabriqué par oxydation électrolytique du chlorure de sodium ou du chlorate de sodium à haute densité de courant, avec une anode en platine ou, dans certains cas, le dioxyde de plomb, le dioxyde de manganèse, ou, éventuellement, la magnétite et l'oxyde de cobalt, et une cathode en graphite, acier, nickel ou titane.
ClO3−+ H2O → ClO4−+ 2 H+ + 2 e -
Utilisations[modifier | modifier le code]
De manière générale, l'utilisation principale actuelle des sels de perchlorate est la fabrication d'oxydants de propergols solides tels qu'utilisés dans les propulseurs à poudre de la NASA ou d'Ariane ou d'autres propulseurs (avec ou sans boosters).[réf. nécessaire]
Le perchlorate d'ammonium tend à remplacer le sel de potassium autrefois utilisé (perchlorate de potassium, qui était un peu moins performant et plus hygroscopique) ; le perchlorate de lithium serait théoriquement plus puissant pour cet usage, car ayant le plus haut pourcentage en poids d'oxygène parmi tous les perchlorates, mais il a le défaut d'être très hygroscopique, ce qui nuit à sa conservation.
Le perchlorate de sodium est assez peu utilisé en pyrotechnie, également car trop hygroscopique ; les artificiers et fabricants lui préfèrent les perchlorates d'ammonium et de potassium.
Le perchlorate de sodium est aussi utilisé dans l'extraction de l'ADN standard et dans certaines réactions d'hybridation dans le domaine de la biologie moléculaire.
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Helmut Vogt, Jan Balej, John E. Bennett, Peter Wintzer, Saeed Akbar Sheikh, Patrizio Gallone “Chlorine Oxides and Chlorine Oxygen Acids” in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH. DOI 10.1002/14356007.a06_483
- (en) « Material Safety Data Sheet - Sodium perchlorate MSDS », sur sciencelab.com (consulté le )







