Matériau à changement de phase (thermique)
Un matériau à changement de phase, ou MCP, est un matériau capable de changer d'état physique dans une plage de température située entre 10 °C et 80 °C environ. Dans cet intervalle de température, le changement de phase prépondérant reste la fusion/solidification. Ces températures sont accessibles naturellement et sont omniprésentes dans la vie quotidienne (température d'ambiance d'une maison, température d'un corps humain, de l'eau chaude sanitaire, etc.).
Cet article n'aborde que les MCP dont le changement d'état se situe entre les phases liquides et solides.
Principe du changement de phase : chaleur sensible et chaleur latente[modifier | modifier le code]
Tout matériau, solide, liquide ou gazeux possède une capacité à absorber, stocker ou céder de l'énergie sous forme de chaleur. On distingue deux types de transfert de chaleur (ou transfert thermique) :
- le [transfert thermique par chaleur sensible (CS) : dans ce cas, le matériau en question peut absorber ou céder de l'énergie en voyant varier sa propre température, sans pour autant changer d'état. La grandeur utilisée pour quantifier la chaleur ainsi échangée par un matériau est la capacité thermique massique, notée Cp et exprimée en J kg−1 K−1. Par exemple, pour l'eau, signifie qu'il faut 4 186 J pour élever 1 kg d'eau de 1 °C (valable aux températures proches de 20 °C) ;
- le transfert thermique par chaleur latente (CL) : dans ce cas, le matériau peut absorber ou céder de l'énergie par changement d'état, tout en conservant une température constante qui lui est propre. La grandeur utilisée pour quantifier la chaleur ainsi échangée par un matériau est la chaleur latente de changement d'état, notée Lf (f pour fusion) pour un changement de phase liquide/solide, c'est-à-dire une fonte, et Lv (v pour vaporisation) pour un changement de phase liquide/vapeur. Celle-ci est exprimée en J/kg. Par exemple, pour l'eau, signifie que la fusion de 1 kg de glace à la température (constante) de 0 °C nécessite une énergie de 330 000 joules soit 330 kJ.
Intérêts des matériaux à changement de phase[modifier | modifier le code]
Compacité ou densité énergétique[modifier | modifier le code]
Les quantités d'énergie mises en jeu dans le processus de changement de phase sont bien plus importantes que celles qui interviennent lors de transferts sensibles (dans la mesure où l'on travaille sur des intervalles restreints de températures). Cette caractéristique permet de réduire considérablement le volume d'un élément de stockage d'énergie (donc d'augmenter sa compacité) ou d'augmenter très fortement la quantité d'énergie contenue dans un même volume de stockage (donc d'augmenter sa densité énergétique).
D'autre part, un MCP peut cumuler les deux types de transferts thermiques décrits précédemment.
Exemple :
| Nom | Acétate de sodium trihydraté |
|---|---|
| Tfusion | 55 à 58 °C |
| Lf | 242,85 × 103 J/kg |
| Cpsolide | 3,31 × 103 J kg−1 K−1 à 30 °C |
| Cpliquide | 3,06 × 103 J kg−1 K−1 à 70 °C |
| ρliquide | 1 279 kg/m3 à 70 °C |
| ρsolide | 1 392 kg/m3 à 30 °C |
Densité énergétique[modifier | modifier le code]
L'énergie E30-70 accumulée par 1 m3 de ce MCP entre 30 °C et 70 °C vaut :
Sur le même intervalle de température, le même volume d'eau (1 m3) accumulerait une quantité Eeau30-70 :
Le MCP considéré a donc permis de stocker plus de trois fois plus d'énergie pour un même volume. Il possède donc une plus grande densité énergétique.
Compacité[modifier | modifier le code]
De la même manière, pour stocker 100 kWh de 55 à 58 °C, on a besoin des volumes Veau et VMCP suivants :
Le volume du MCP utilisé pour stocker 100 kWh entre 55 °C et 58 °C est donc plus de 26 fois plus petit que celui de l'eau. Il possède donc une plus grande compacité.
Matériaux thermorégulants (régulation passive, rôle tampon)[modifier | modifier le code]
Le caractère isotherme ou quasi isotherme de la charge et de la décharge énergétique d'un MCP permet son utilisation en tant que régulateur de température dans un matériau thermorégulant. En effet, si l'on intègre ce MCP dans un enduit, par exemple à l'enveloppe (murs extérieurs, plancher, plafond, etc.) d'un bâtiment, il peut stocker de la chaleur quand elle est surabondante (été) ou présente au mauvais moment (dans la journée l'hiver).
- Cycle saisonnier : en été, une partie de l'énergie solaire peut être stockée au fur et à mesure par les parois (sans fluctuation excessive de la température dans le bâtiment). Selon le Centre scientifique et technique du bâtiment (CSTB), il est alors possible d'écrêter de 3 à 5 °C les pics de température d'une pièce[1].
- Cycle journalier : en hiver, on peut de la même manière stocker la chaleur apportée par le soleil dans des MCP incorporés aux parois (enduit ou matériau originel) ; ceux-ci restitueront cette chaleur en fin de journée, la nuit ou au moment d'un refroidissement.
Par ailleurs, tout MCP peut servir de « déphaseur thermique »? Tout apport ou perte énergétique (variation de température, rayonnement solaire, etc.) en provenance du milieu peut provoquer la fusion ou la cristallisation du matériau à température quasi constante. Dès lors, le milieu situé de l'autre côté du MCP ne ressent pas aussitôt l'effet de cet apport ou de cette perte, mais ne commencera à le ressentir qu'après la fusion ou la cristallisation totale du matériau.
Éventail de températures[modifier | modifier le code]
Les MCP, grâce à leur grande variété possèdent des températures de fusion différentes. Ces dernières balayent la totalité de la zone de température restrictive dans laquelle nous nous sommes placés initialement. Cela permet, par exemple, de choisir des températures de fusion proches de 19 °C et 27 °C, respectivement températures limites de confort hivernal et estival. Le paragraphe suivant présente un tableau non exhaustif de différents matériaux à changement de phase, accompagnés de leur température de fusion et autres données techniques.
Exemples et types de matériaux à changement de phase[modifier | modifier le code]
Il existe de nombreux types de matériaux à changement de phase, de nature physico-chimique très différente les uns des autres. Ce sont leurs caractéristiques de fusion-cristallisation qui les rendent intéressants pour le stockage de chaleur latente. Parmi ces matériaux, on distingue les trois grandes familles suivantes :
- les composés minéraux (ou inorganiques). Parmi ces composés, seuls les sels hydratés présentent un intérêt pour leur utilisation en tant que MCP. Ils sont issus d'un alliage de sels organiques et d'eau. Ils ont l'avantage de posséder des grandes chaleurs latentes et des prix bas. En revanche, leur principal défaut concerne leur tendance à la surfusion ;
- les composés organiques. De propriétés thermiques (chaleur latente et conductivité thermique en particulier) moindre que les sels hydratés, ceux-ci présentent l'avantage de n'être pas ou très peu concernés par la surfusion. On utilise en particulier, pour le stockage de chaleur latente, les paraffines et les acides gras qui appartiennent à cette famille ;
- les eutectiques. Un eutectique est un mélange de corps purs possédant une température de fusion constante pour une valeur particulière de concentration. Il peut être inorganique et/ou organique.
| Nom | Tfusion (°C) |
Lf (kJ/kg) |
Cpsolide (kJ kg−1 K−1) |
Cpliquide (kJ kg−1 K−1) |
ρ solide (kg/m3) |
ρ liquide (kg/m3) |
|---|---|---|---|---|---|---|
| Composés organiques | ||||||
| Acide formique | 8,3 | 247 | ? | 0,099 | ? | 1 220 |
| Acide acétique | 16,7 | 194 | ? | ? | 1 266 | 1 049 |
| Phénol | 40,8 | 120 | ? | ? | 1 070 | ? |
| Acide dodécanoïque | 41-43 | 211,6 | 1,76 | 2,27 | 1 007 | 862 |
| Acétate de sodium trihydraté | 55-58 | 242,85 | 3,31 à 30 °C | 3,06 à 70 °C | 1 392 à 30 °C | 1 279 à 70 °C |
| Composés inorganiques | ||||||
| Eau (H2O) | 0 | 330 | 2,06 à 0 °C | 4,186 à 20 °C | 917 à 0 °C | 998 à 20 °C |
| Hydroxyde de sodium (NaOH) | 318 | 272,15 | 1,88 à 30 °C | 2,18 à 70 °C | 1 720 à 30 °C | 1 670 à 70 °C |
| Acide sulfurique (H2SO4) | 10,4 | 100 | ? | ? | ? | 1 838 |
| Trioxyde de soufre (SO3) | 16,9 | 108 | ? | 0,024 | ? | 1 920 |
| Acide phosphorique (H3PO4) | 26,0 | 147 | ? | ? | 1 834 | 1 685 |
| Gallium (Ga) | 29,8 | 80 | 0,370 | ? | 5 904 | 6 095 |
On peut néanmoins noter la dangerosité de certaines de ces substances.
Par exemple, le trioxyde de soufre réagit, entre autres, violemment avec l'eau pour former de l'acide sulfurique (un acide fort et un polluant majeur) tout en dégageant une chaleur importante.
Applications[modifier | modifier le code]
Amélioration de la stratification d'un ballon d'eau chaude sanitaire (ECS) solaire[modifier | modifier le code]
Stockage solaire thermique classique[modifier | modifier le code]

Le principal problème lié à l'utilisation de l'énergie solaire thermique concerne son stockage : la production d'eau chaude sanitaire (ECS) via la circulation d'eau au-travers de panneaux solaires est directement dépendante de l'ensoleillement. Cet apport énergétique a lieu que l'on en ait besoin (bénéfique) ou non (perte énergétique par surabondance). L'utilisation de MCP pour le stockage de cette énergie par chaleur latente permettrait de résoudre en partie ce problème :
- d'une part, la quantité d'énergie stockée dans un ballon de même volume sera plus grande avec un MCP qu'avec de l'eau seule (cf. paragraphe Compacité ou Densité énergétique) : il sera donc possible d'accumuler une plus grande quantité de chaleur que celle nécessaire à une seule journée d'occupation ;
- par ailleurs, ne pouvant élever indéfiniment la température du volume de stockage (risque de vaporisation du fluide néfaste aux pompes de circulation), il est en revanche possible de stocker cette chaleur sous forme latente sans pour autant élever la température du matériau (en utilisant par exemple un MCP dont la température de fusion se situe aux environs de 60 °C ou 70 °C). Cette chaleur supplémentaire accumulée sera cédée par la suite au réseau d'eau chaude sanitaire.
Stockage solaire thermique avec utilisation de MCP[modifier | modifier le code]

Le principal problème de stockage de l'énergie au sein d'un ballon d'ECS solaire est l'absence de stratification (l'intégralité du volume d'eau chaude contenue dans le ballon n'est que rarement prélevée en une seule fois) : le volume d'eau à l'intérieur du ballon a tendance à homogénéiser sa température lors de son retour et de son départ vers les panneaux. Une fois une température trop basse atteinte (par exemple 40 °C), il n'est plus possible d'utiliser cette eau pour le circuit d'ECS. Pourtant, il suffit que cette chaleur soit « mieux répartie » pour que l'on puisse encore puiser de l'eau à une température convenable (un ballon de 100 L à 40 °C contient la même quantité d'énergie que deux ballons de 50 L aux températures respectives de 30 °C et 50 °C).
L'utilisation de MCP permet alors la création de « couches stratifiées » dont les températures se situeront aux environs des températures de fusion des différents matériaux utilisés. Ainsi, un puisage intermittent ou ponctuel d'ECS entraîne la baisse de température de la partie haute du ballon (cf. schéma) dépourvue de nodules (=capsules) de MCP. En revanche, un puisage plus long entraîne l'utilisation de l'énergie contenue dans les couches inférieures du ballon, c'est-à-dire de la chaleur latente contenue dans les nodules. Ceux-ci se solidifient si nécessaire et cèdent ainsi leur énergie à l'eau de ville en la réchauffant.
Climatisation passive[modifier | modifier le code]
Certaines entreprises comme Dupont de Nemours proposent des panneaux d'inertie thermique incorporant un mélange MCP-polymère. Ces panneaux sont généralement recouverts d'une feuille d'aluminium qui leur apporte de la rigidité structurelle et joue éventuellement le rôle de pare-vapeur métallisé dans le cas où ces panneaux seraient utilisés dans l'enveloppe du bâtiment.
L'utilisation de tels matériaux présente un double intérêt :
- du fait de leur grande compacité, les MCP permettent au bâtiment d'acquérir une grande inertie thermique et donc d'être moins sensible aux variations quotidiennes de température. Selon les études[2],[3], il serait possible de réduire de 7 à 8 °C maximum les pics de température dans un bâtiment en utilisant de tels isolants ;
- le phénomène de changement de phase permet, quant à lui, d'absorber une partie de la chaleur de la pièce dès que la température ambiante dépasse la température de fusion du matériau. Cet écart de température entre le matériau et la pièce (réserve énergétique) va être réduit et la température de la pièce va tendre vers celle du matériau : dans la mesure où l'échange énergétique qui a lieu entre les deux systèmes se fait de manière quasi isotherme pour le MCP, c'est l'environnement qui va voir baisser sa température afin de permettre la fusion du MCP.
Ainsi, en choisissant un MCP dont la température de fusion est de 20 °C ou 21 °C, et en précisant que la température de consigne de chauffage pour un logement individuel est de 19 °C maximum, nous pourrons accumuler de la chaleur dans les panneaux de MCP grâce au rayonnement solaire traversant les ouvertures (fenêtres, baies vitrées), sans pour autant consommer davantage de chauffage ni élever la température de la pièce. Cette chaleur pourra ainsi être restituée durant la nuit, dès que la température du bâtiment descendra en dessous de la température de solidification du MCP.
Intégration aux textiles : régulation thermique corporelle[modifier | modifier le code]
Développés depuis maintenant plusieurs années par la recherche spatiale aux États-Unis, les MCP font depuis peu leur apparition dans l'industrie textile. Le but recherché est de réguler de manière passive la température corporelle en fonction de la température du milieu. Il devient alors particulièrement important de trouver des matériaux dont les températures de fusion et de cristallisation sont très proches de la température superficielle du corps humain.
Les matériaux utilisés pour ce genre d'applications sont généralement des paraffines, un matériau organique à chaîne carbonée linéaire, contenant une combinaison d'eicosane, d'octadécane, de nonadécane, d'heptadécane et d'hexadécane. Ces différents composés possèdent tous des températures de changement de phase différentes mais, une fois mélangés et encapsulés, ils se maintiennent à une température moyenne de 30 à 34 °C, ce qui devient très confortable pour le corps humain.
L'utilisation de ces textiles peut se faire dans des domaines tels que :
- l'industrie automobile, dans laquelle le problème de la climatisation reste majeur : une intégration correcte de MCP à l'intérieur de l'habitacle permettrait une meilleure régulation des pics de chaleur, et donc une diminution de l'utilisation d'une climatisation nuisible à l'environnement ;
- les vêtements techniques : ceux-ci ne permettent généralement pas d'atteindre un équilibre entre la chaleur produite par le corps et celle transmise à l'environnement lors de la pratique d'un sport. Cet excès de chaleur non évacuée provoque généralement des situations de stress thermique néfastes à l'activité pratiquée.
L'utilisation de vêtements régulateurs de chaleur pourrait alors permettre de diminuer cet inconfort et d'augmenter ainsi les capacités et l'efficacité des personnes lors d'activités physiques ou lors de situations de stress ; - l'aérospatial : certains produits aujourd'hui dans le commerce ont été à l'origine développés pour la création de combinaisons d'astronautes. Ils avaient pour but de les protéger des variations extrêmes de température présentes à l'extérieur des navettes lors des sorties.
Inconvénients[modifier | modifier le code]
Prix[modifier | modifier le code]
Bien que présents dans le commerce depuis quelques années maintenant, les MCP restent des technologies moins abordables que les isolants classiques, notamment en ce qui concerne leur utilisation dans l'habitat. Néanmoins, le surcoût généré à l'investissement peut se retrouver rapidement amorti grâce aux économies d'énergie réalisées, comme le démontre une étude de l'INSA de Lyon[4] sur un produit déjà commercialisé, dont le temps de retour sur investissement est d'environ huit ans.
Surfusion[modifier | modifier le code]
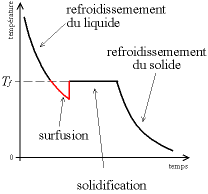
La surfusion correspond à l'état liquide d'un corps alors que sa température est inférieure à la température de cristallisation. Elle n'apparaît que pour certains types de MCP comme les matériaux inorganiques. Les solutions pour remédier à ce problème sont multiples :
- incorporation d'additifs tensio-actifs ;
- faciliter la nucléation au moyen de cristaux solides stables autour de la température de cristallisation : ceux-ci servent de points d'accroche pour la cristallisation du matériau ;
- garder une zone froide à l'intérieur du matériau.
La surfusion empêche l'utilisation de la chaleur latente de changement de phase à la température voulue.
Cinétique de cristallisation[modifier | modifier le code]
Les vitesses de cristallisation des MCP sont relativement faibles. S'il faut trop de temps au matériau pour accumuler ou libérer de l'énergie, celui-ci perd alors en efficacité dans les applications pratiques (incapacité à « lisser » les pics de températures par exemple).
Mais cette cinétique peut être améliorée par l'introduction de solvants à forte polarité et à forte constante diélectrique au sein du MCP. Ces solvants permettent d'abaisser les tensions superficielles au niveau des interfaces liquide/solide.
Résistance au transfert thermique[modifier | modifier le code]
Lors du changement de phase du MCP, l'échange thermique a lieu à l'interface solide/liquide. Lorsque le front de solidification ou de fusion se déplace, il laisse derrière lui une nouvelle phase (solide ou liquide) que le flux thermique doit traverser avant d'atteindre le front en question. Plus l'épaisseur de cette phase est importante et plus la résistance thermique qu'elle engendre est grande.
Malheureusement, les MCP ont une conductivité thermique assez faible (de l'ordre de 0,15 W m−1 K−1) ce qui empêche d'ores et déjà un bon transfert thermique. Ce phénomène est alors amplifié par l'épaisseur de la phase à traverser. Il faut donc, si l'on souhaite limiter ces phénomènes de résistance dus au déplacement du front thermique, faire en sorte que l'épaisseur à traverser soit la plus petite possible. C'est pour cela que l'on utilise souvent des micro-capsules sphériques qui changent facilement de phase sur l'ensemble de leur volume.
Confinement[modifier | modifier le code]
L'encapsulation semble être une bonne solution au confinement des MCP. En effet, lorsque ce dernier est à l'état liquide, il n'a plus de tenue physique et nécessite un contenant. La difficulté technologique consiste à maximiser les échanges thermiques par tous les moyens (en choisissant de bons conducteurs thermiques pour la fabrication des capsules par exemple).
Durée de vie[modifier | modifier le code]
Selon le Centre scientifique et technique du bâtiment[5], les MCP utilisés dans l'habitat auraient une durée de vie égale ou supérieure à celle des bâtiments actuels.
Aspects sanitaires et sécuritaires[modifier | modifier le code]
Les MCP étant très diversifiés et peu utilisés à l'heure actuelle, on comprend que peu d'études systématiques aient été faites au sujet de leur impact sanitaire et des risques qu'ils représentent.
Références[modifier | modifier le code]
- CSTB, « Matériaux à changement de phase : vers une 'climatisation' douce », .
- (en) Dupont, « Dupont Energain Product Information Sheet » [PDF],
- CSTB, « Utilisation des MCP en climatisation passive et chauffage d'intersaison » [PDF],
- Joseph Virgone, « Intégration des Matériaux à Changement de Phase dans le BATiment » [PDF],
- CSTB, « Liquides ou solides - Les matériaux à changement de phase »,
Bibliographie[modifier | modifier le code]
- Christophe Plantier, Étude numérique et expérimentale d'un prototype de chauffe-eau solaire équipé d'un stockage à chaleur latente, .
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- (en) Page personnelle d'un doctorant en MCP
- D. Quénard, H. Sallée, K. Johannes, A. Husaunnde, « Utilisation des Matériaux à Changement de Phase (MCP) en climatisation passive et chauffage d’intersaison ».
- J. Noël, S. Lepers, J. Virgone, « Amélioration du confort d'été sur des bâtiments à ossature légère par des matériaux à changement de phase ».




![{\displaystyle =[{1}\times {1\;392}\times {C_{p_{~{\text{MCP}}~{\text{solide}}}}}\times {(55-30)}]~+~[{1}\times {1\;392}\times {L_{\text{f}}}]~+~[{1}\times {1\;279}\times {C_{p_{~{\text{MCP}}~{\text{liquide}}}}}\times {(70-58)}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b26c2d22293f7047d99445d49d2b331e9ae477b3)




