Sulfate de cuivre
| Sulfate de cuivre | ||

| ||
 | ||
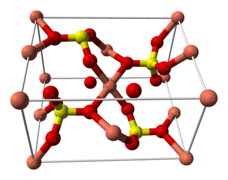
| Structure du sulfate de cuivre (anhydre) et sulfate de cuivre anhydre dans un bocal. | ||
| Identification | ||
|---|---|---|
| Nom UICPA | Sulfate de cuivre(II) | |
| Synonymes |
Couperose (blanche) |
|
| No CAS | anhydre pentahydrate | |
| No ECHA | 100.028.952 | |
| No CE | 231-847-6 | |
| Code ATC | V03 | |
| PubChem | anhydre 24462 pentahydrate 24463 |
|
| No E | E519 | |
| SMILES | ||
| InChI | ||
| Apparence | cristaux blancs hygroscopiques (anhydre)[1], solide bleu de forme variable (pentahydrate)[2] |
|
| Propriétés chimiques | ||
| Formule | CuSO4 CuSO4 · 5 H2O (hydraté) |
|
| Masse molaire[3] | 159,609 ± 0,009 g/mol Cu 39,81 %, O 40,1 %, S 20,09 %, 249,6 g/mol (pentahydrate) |
|
| Propriétés physiques | ||
| T° fusion | (décomposition) : 110 °C (pentahydrate)[2] | |
| T° ébullition | Se décompose au-dessous du point d'ébullition à 650 °C (anhydre)[1] | |
| Solubilité | dans l'eau à 0 °C : 317 g·l-1 ; (pentahydrate)[2] dans l'eau à 100 °C : 2 033 g·l-1[réf. nécessaire] |
|
| Masse volumique | 3,6 g·cm-3 (anhydre)[1], 2,3 g·cm-3 (pentahydrate)[2] |
|
| Thermochimie | ||
| S0solide | 109,05 J·K-1·mol-1 | |
| ΔfH0solide | -769,98 kJ/mol | |
| Cp | 67 cal/K/mol | |
| Propriétés optiques | ||
| Spectre d’absorption | λmax = 800 nm | |
| Précautions | ||
| SGH[4] | ||
| H302, H315, H319 et H410 |
||
| SIMDUT[5] | ||
 D2B, |
||
| Transport | ||
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Le sulfate de cuivre(II), couramment désigné sous le simple nom de sulfate de cuivre, est le composé chimique ionique ou sel anhydre blanc formé par le cation cuivre(II) (Cu2+) et l'anion sulfate (SO42− ), caractérisé par la formule chimique CuSO4.
Il est commercialisé sous forme anhydre ou encore sous formes hydratées. Dans ce dernier cas, il s'agit rigoureusement d'autres composés chimiques diversement hydratés de la même famille, soit le plus souvent le sulfate de cuivre pentahydraté de formule CuSO4,5H2O, autrefois nommé vitriol bleu, mais aussi les sulfates de cuivre mono- ou trihydraté.
Noms vernaculaires[modifier | modifier le code]
Le Sulfate de cuivre est affublé de nombreux noms : sulfate de deutoxyde de cuivre, couperose bleue, cuivre vitriolé, vitriol bleu, vitriol de cuivre, vitriol de Chypre[6].
Propriétés[modifier | modifier le code]

Le sulfate de cuivre anhydre CuSO4 est blanc (grisâtre par ses impuretés). Il est hygroscopique et bleuit au contact de l'eau ou de la vapeur d'eau en formant le pentahydrate CuSO4.5H2O. Cette propriété d'hydratation où la transformation du corps chimique anhydre en composé hydraté est corrélative d'un changement de coloration caractéristique explique son usage comme test de la présence d'eau dans un liquide, un milieu aérosol ou l'air ambiant.
Le sulfate de cuivre est facilement soluble dans l'eau.
Les solutions concentrées ou diluées des sulfates de cuivre anhydre ou hydratés ont une coloration bleu du fait de la présence d'ions Cu2+ hydratés, dispersés dans l'eau.
Pour retrouver le sulfate de cuivre, il faut chauffer doucement les différents sulfates de cuivre hydratés.
Chauffé fortement, le sulfate de cuivre anhydre se décompose en anhydride sulfurique (trioxyde de soufre) et en oxyde de cuivre ou en des sels cuivreux blancs.
Fabrication industrielle[modifier | modifier le code]

Le sulfate de cuivre est obtenu industriellement comme sous-produit du décapage chimique du cuivre par l'acide sulfurique. Cet acide n'attaquant pas le cuivre métallique, seule sa forme oxydée présente en surface sous forme d'oxydes, de carbonates (vert de gris) et autres, passe en solution. Dans ces conditions, seul le degré d'oxydation II (forme cuivrique) est stable.
La solution bleue de décapage est ensuite cristallisée dans des bacs (en cuivre) dans lesquels plongent des barres (en cuivre également). Les cristaux de sulfate de cuivre hydraté se forment en quelques heures à la surface du récipient et des barres. La couche de cristaux peut atteindre plusieurs centimètres d'épaisseur (de 5 à 15 ou plus). Ces cristaux sont récupérés et broyés. Lorsqu'ils sont broyés assez fin (1 à 3 mm de diamètre environ), leur couleur passe au bleu pâle terne, indiquant que la surface des cristaux ne possède plus la qualité optique initiale. Ils sont vendus sous cette forme sous l'appellation « sulfate de cuivre neige ».
Utilisation[modifier | modifier le code]

Une des principales utilisations actuelles du sulfate de cuivre est la préparation (industrielle ou non) de fongicides pour l'agriculture y compris biologique (toutefois l’Union européenne a fixé à 150 mg·kg-1 la teneur maximale des sols en cuivre en agriculture biologique). Les formes les plus courantes sont la bouillie bordelaise constituée de sulfate de cuivre et de chaux et la bouillie bourguignonne constituée de sulfate de cuivre et de bicarbonate de soude. Chaux et bicarbonate neutralisent l'acidité créée par la mise en solution du sulfate de cuivre. Les végétaux traités par une préparation à base de sulfate de cuivre présentent des taches bleu-pâle constituées de sels mixtes d'hydroxyde et de sulfate de cuivre.
Le sulfate de cuivre a été préconisé dès le début du XIXe siècle en traitement des semences, puis utilisé vers le milieu du siècle, sous une forme proche de la bouillie bordelaise, pour décourager les voleurs de raisin, puis comme fongicide anti-mildiou, sur vigne, à partir de 1880.
Le sulfate de cuivre hydraté, jadis appelé « vitriol bleu », a été longtemps utilisé comme désherbant chimique (en particulier des pommes de terre). Il entre dans la composition des algicides, vendus dans le commerce pour l'entretien des piscines alors que certains sites spécialisés recommandent aux particuliers de ne pas l'utiliser directement pour leur piscine.
Le sulfate de cuivre est aussi employé comme apport d'oligo-élément (cuivre), aussi bien en cas de carence en cuivre des végétaux, que des animaux (maladie du tour de l'œil blanc des bovins par exemple). Dans les élevages de porcs, il est régulièrement employé en complément minéral dans la nourriture, pour favoriser la prise de poids. C'est un complément alimentaire autorisé dans les denrées alimentaires[7].
Dangers, pollution[modifier | modifier le code]
Le sulfate de cuivre est un produit toxique :
- nocif en cas d'ingestion ;
- irritant pour les yeux et pour la peau ;
- très toxique pour les organismes aquatiques (marins tout particulièrement) ;
- le cuivre qu'il contient peut s'accumuler dans les sols, notamment au pied des pentes. L'érosion hydrique ou éolienne des sols peut alors devenir une source significative de transfert de pollution[8].
Utilisé de manière chronique (annuellement), il peut entraîner des effets néfastes à moyen et long terme pour l'environnement aquatique[9].
Il est également suspecté de favoriser l'apparition de la maladie de Parkinson[10].
Ce produit est donc à manipuler avec attention, en utilisant gants, masque et lunettes de protection à chaque utilisation.
- Différentes formes du sulfate de cuivre
-
Maille élémentaire.
-
Poudre de sulfate de cuivre hydraté.
-
Cristaux de sulfate de cuivre (II) produit par cristallisation lente d'une solution saturée.
-
Autres cristaux de sulfate de cuivre.
-
Évolution de la solubilité dans l'eau du sulfate de cuivre en fonction de la température, caractéristique d'une dissolution endothermique.
-
Sulfate de cuivre anhydre (blanc) devenant bleu au contact de l'eau.
-
Solution aqueuse de sulfate de cuivre.
Notes et références[modifier | modifier le code]
- SULFATE DE CUIVRE, ANHYDRE, Fiches internationales de sécurité chimique
- SULFATE DE CUIVRE (II) PENTAHYDRATE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Sulfate de cuivre (II) pentahydraté » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Littre-Réverso : vitriol
- (en)[PDF] Règlement (CE) no 1170/2009, sur eur-lex.europa.eu
- Quantification des flux de pesticides associés à l’érosion hydrique en contexte viticole (Cours en ligne), Université de Strasbourg, PDF, 2 pages
- Non trouvé le 14 septembre 2018, sur ac-nancy-metz.fr
- Nicolas Gutierrez C, « Parkinson : un lien de cause à effet avec plusieurs pesticides ? », sur Sciences et Avenir, (consulté le )