Encéphalite japonaise
| Groupe | Groupe IV |
|---|---|
| Famille | Flaviviridae |
| Genre | Flavivirus |
| Causes | Virus de l'encéphalite japonaise |
|---|---|
| Transmission | Transmission par les moustiques (d) |
| Incubation min | 5 j |
| Incubation max | 15 j |
| Symptômes | Fièvre, frissonnement (en), arthralgie, fatigue, céphalée, vomissement, raideur de la nuque (en), confusion (en) et coma |
| Traitement | Soins de support (d), diurétique, nootropique et antioxydant |
|---|---|
| Médicament | Furosémide, torasemide, néostigmine, piracetam et D-(-)-mannitol |
| Spécialité | Infectiologie |
| CIM-10 | A83.0 |
|---|---|
| CIM-9 | 062.0 |
| DiseasesDB | 7036 |
| eMedicine | 233802 |
| MeSH | D004672 |
L'encéphalite japonaise (日本脳炎, Nihon-nōen, auparavant appelée encéphalite japonaise de type B pour la différencier de l'encéphalite A de von Economo) est une maladie virale transmise par les piqûres de moustique. Le virus de l'encéphalite japonaise appartient à la famille des Flaviviridae. Un des plus importants vecteurs de cette maladie est le moustique Culex tritaeniorhynchus. Le porc et les oiseaux sauvages sont des réservoirs de ce virus à ARN dont la transmission à l'Homme peut entraîner l'apparition de graves symptômes.
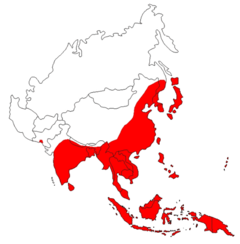
Cette maladie est très fréquente en Extrême-Orient et en Asie du Sud-Est (68.000 cas graves par an selon l'OMS[1]) ; c'est la 1re cause d'encéphalite infantile en Asie[1].
En zone équatoriale et tropicale chaude, les moustiques sont présents toute l'année, mais de manière intrigante, la maladie persiste toute l'année aussi en zone plus tempérée, y compris en hiver alors que les populations de moustiques adultes sont très diminuées voire absentes (comme au nord du Japon)[1]. Ceci a été récemment expliqué par le fait que ce virus peut aussi passer directement d'un porc à l'autre durant l'hiver (le porc joue donc bien un rôle de réservoir hivernal et d'amplificateur des populations virales), sans transmission via un moustique. Cette découverte faite par des chercheurs suisses est récente (Science, février 2016)[1]. Un vaccin existe pour le porc, mais est peu utilisé pour protéger le cheptel là où les porcs sont rapidement reproduits, engraissés et envoyés à l'abattoir. Si la transmission interporc se fait aussi facilement à la ferme ou dans la nature qu'en condition de laboratoire, selon les auteurs de l'étude, le contact porc à porc ne serait néanmoins probablement pas le principal mode de transmission du virus, et donc pas le risque[1]. Rem on avait déjà montré une transmission d'oiseau à oiseau, sans passage par un moustique pour un virus proche (le virus du Nil occidental) et le virus zika semble aussi pouvoir être propagé par voie sexuelle chez l'Homme[1].
Épidémiologie
L'encéphalite japonaise est la principale cause d'encéphalite virale en Asie, avec entre 30 000 et 50 000 nouveaux cas par an. Le taux de mortalité varie de 0,3 % à 60 % selon l'âge et la population touchée.
En moyenne, parmi ceux qui déclarent des symptômes d'encéphalite grave, 20 % à 30 % meurent[1]; et 30 % à 50 % des survivants conserveront des séquelles neurologiques ou psychiatriques à vie[1].
En zone d'endémie, les populations rurales sont particulièrement à risque, notamment là où les rizières marécageuses ou zones d'eaux stagnantes riches en fientes d'échassiers et larves de moustiques se trouvent à proximité d'élevages porcins ; alors que la maladie est très rare en zone urbaine.
Les pays qui ont connu dans le passé des épidémies majeures, mais qui ont contrôlé cette maladie grâce à la vaccination sont la République populaire de Chine, la Corée, le Japon, Taïwan et la Thaïlande. Les autres pays subissant régulièrement des épidémies ; ce sont notamment le Viêt Nam, le Cambodge, la Birmanie, l'Inde, le Népal et la Malaisie.
Des cas d'encéphalite japonaise ont été signalés dans les îles du détroit de Torres et deux cas mortels ont été rapportés au Nord de l'Australie en 1998. La diffusion du virus y est un problème de santé publique car elle est due à l'introduction involontaire du Culex gelidus, un vecteur potentiel du virus, venu tout droit d'Asie.
L'Homme, le bétail et les chevaux sont des « culs-de-sac épidémiologiques » (« impasses virologiques ») chez qui la maladie se manifeste par une encéphalite éventuellement mortelle, mais il n'y a pas assez de virus dans leur sang pour que les moustiques propagent l'infection à d'autres. Le porc joue le rôle d'hôte amplificateur et joue un rôle important dans l'épidémiologie de cette maladie. L'infection est asymptomatique chez le porc, hormis chez les truies pleines chez lesquelles elle provoque des avortements et des malformations fœtales.
Le vecteur principal est le moustique Cx. tritaeniorhynchus qui pique le bétail plutôt que l'Homme (il a été proposé d'éloigner les porcs des habitations et de se servir du bétail pour éloigner ce moustique des porcs et des humains[2].
L'hôte naturel du virus étant l'oiseau et non l'humain ou le porc, le virus ne sera jamais éradiqué.
Clinique
La période d'incubation de l'encéphalite japonaise est de 5 à 15 jours[réf. nécessaire]. La grande majorité des infections sont asymptomatiques ; seule une infection sur 250 se transformera en encéphalite[3].
Les prodromes marquant le début de la maladie chez l'humain sont des frissons, de la fièvre, des céphalées et des malaises. Ces symptômes non spécifiques peuvent durer de 1 à 6 jours. Durant la période d'état ou période aiguë de la maladie le malade peut présenter une rigidité de la nuque, une cachexie, une hémiparésie, des convulsions et une augmentation de la température corporelle entre 38 et 41 °C. Le coma s'il survient, peut laisser des séquelles neurologiques et un retard mental.
La mortalité varie, mais est habituellement plus importante chez les enfants. Des séquelles neurologiques définitives comme une surdité, une instabilité émotionnelle et une hémiparésie peuvent survenir chez des malades dont le système nerveux central a été atteint.
Virologie
Le virus de l'encéphalite japonaise est un virus enveloppé, du genre Flavivirus ; il est relativement proche du virus du Nil occidental et du virus de l'encéphalite de Saint Louis.
Le génome viral, représenté par un ARN positif monocaténaire, est enfermé dans une capside protéique.
L'enveloppe externe est formée par une protéine d'enveloppe (E) qui constitue l'antigène protecteur. Elle aide le virus à pénétrer dans la cellule-cible.
Le génome viral code aussi pour des protéines non structurelles (NS1, NS2a, NS2b, NS3, N4a, NS4b, NS5). La protéine NS1 est aussi produite sous forme sécrétoire. NS3 est probablement une hélicase et NS5 est une polymérase virale.
Diagnostic
Il repose sur la détection des anticorps dans le sérum et le LCS par méthode ELISA.
Prévention, vaccination
L'infection par le virus de l'encéphalite japonaise confère une immunité durable. Tous les vaccins actuels sont basés sur le génotype III du virus. Un vaccin dérivé de cerveaux de souris et inactivé par le formaldéhyde a été produit pour la première fois au Japon dans les années 1930 ; son utilisation a été approuvée à Taïwan dans les années 1960 et en Thaïlande dans les années 1980. Le large recours à ce vaccin et l'urbanisation ont permis de contrôler la maladie au Japon, en Corée, à Taïwan et à Singapour.
Le coût très élevé du vaccin (qui est produit à partir de souris vivantes) explique que les pays les plus pauvres ne peuvent pas se permettre de l'inclure dans leur programme de vaccination systématique.
Au Royaume-Uni, les deux vaccins utilisés (mais non licenciés) sont JE-Vax® et Green Cross. Trois injections sont réalisées à 0, 7–14 et 28–30 jours. Les doses sont de 1 ml pour les enfants et les adultes, et de 0,5 ml pour les nourrissons de moins de 36 mois.
Les effets indésirables les plus courants sont une rougeur et une douleur au point d'injection. Plus rarement, une réaction cutanée à type d’urticaire peut apparaître 4 jours après l'injection. Dans la mesure où le vaccin est produit à partir de cerveaux de souris, il existe un risque de complications neurologiques auto-immunes dans environ 1 vaccination sur 1 million.
Les anticorps neutralisants persistent dans la circulation pendant au moins 2 à 3 ans, peut-être davantage[4],[5]. La durée totale de protection est inconnue, mais dans la mesure où il n'y a pas de preuve de sa persistance au-delà de 3 ans, des rappels sont recommandés tous les deux ans pour les personnes à risque.
Il existe plusieurs nouveaux vaccins en cours de développement. Le vaccin dérivé de cerveaux de souris est en passe d'être remplacé par un vaccin issu de cultures cellulaires qui est à la fois plus sûr et moins onéreux. La République populaire de Chine a mis sur le marché un vaccin vivant atténué en 1988 et plus de 200 millions de doses ont déjà été délivrées ; il est également disponible au Népal, au Sri Lanka, en Corée du Sud et en Inde. Il existe enfin un vaccin chimérique basé sur le vaccin 17D contre la fièvre jaune en cours de développement.
Traitement
Il n'existe pas de traitement spécifique de l'encéphalite japonaise, mais seulement un traitement symptomatique. Dans la mesure où il n'y a pas de transmission inter-humaine du virus, aucune mesure d'isolement des malades n'est nécessaire.
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Japanese Encephalitis » (voir la liste des auteurs).
- Hamers L (2016) Japanese encephalitis could have a new transmission route in pigs, 26 février 2016 ; DOI: 10.1126/science.aaf4119
- (en) Tom Solomon, « Control of Japanese Encephalitis—within our grasp? », The new England Journal of Medecine, vol. 355, no 9, , p. 869-871 (résumé)
- (fr) OMS | Encéphalite japonaise
- (en) Gambel JM, DeFraites R, Hoke C, et al., « Japanese encephalitis vaccine: persistence of antibody up to 3 years after a three-dose primary series (letter) », J Infect Dis, vol. 171, , p. 1074
- (en) Kurane I, Takashi T, « Immunogenicity and protective efficacy of the current inactivated Japanese encephalitis vaccine against different Japanese encephalitis virus strains », Vaccine, vol. 18 Suppl, , p. 33–5
Voir aussi
Articles connexes
Liens externes
- Clinical medicine, fifth edition by Kumar and Clark, 2002 published by W.B Saunders
- Centers for Disease Control and Prevention Questions and Answers About Japanese Encephalitis
- Australian government Department of Health and Aging, Japanese Encephalitis, 2004
- Monath, TP, Pathobiology of the flaviviruses. In: The Togaviridae and flaviviridae (Eds Schlesinger, S. and Schlesinger, M.J.) Plenum Press, New York/London, pp. 375-440, 1986
- UK Department of Health. (2006) Immunisation against Infectious Disease Chapter 20: Japanese Encephalitis
Bibliographie
- Mathur, A., Tandon, H. O., Mathur, K. R., Sarkari, N. B. S., Singh, U. K., & Chaturvedi, U. C. (1985). Japanese encephalitis virus infection during pregnancy. Indian journal of medical research, 81, 9-12.
- Rodhain, F., GUENIOT, M., BLANCHER, G., LAVERDANT, C., PICHOT, P., SOURNIA, J. C., & BASTIN, R. (1996). Données récentes sur l'épidémiologie de l'encéphalite japonaise. Discussion. Bulletin de l'Académie nationale de médecine, 180(6), 1325-1340.

