Silice
| Silice | |

| |
| Identification | |
|---|---|
| Nom UICPA | dioxyde de silicium |
| No CAS | silice amorphe fondue quartz
|
| No CE | silice amorphe 262-373-8; 231-545-4 |
| PubChem | |
| SMILES | |
| InChI | |
| Apparence | poudre de couleur blanche |
| Propriétés chimiques | |
| Formule | SiO2 |
| Masse molaire[1] | 60,084 3 ± 0,000 9 g/mol O 53,26 %, Si 46,74 %, |
| Propriétés physiques | |
| T° fusion | 1 713 °C[réf. nécessaire] |
| T° ébullition | 2 700 °C[réf. nécessaire] |
| Solubilité | 0,14 g·L-1 (eau)[réf. nécessaire] |
| Masse volumique | 2,2 g·cm-3 solide[2] |
| Précautions | |
| SIMDUT[5],[6],[7] | |
| Silice amorphe : Produit non contrôlé Silice précipitée : Produit non contrôlé Silice fondue : Produit non contrôlé |
|
| Directive 67/548/EEC | |
| Classification du CIRC | |
| Groupe 1 : Cancérogène pour l'homme[3] (Silice cristalline inhalée sous forme de quartz ou de cristobalite de source professionnelle) Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[4] (Silice amorphe) |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La silice est la forme naturelle du dioxyde de silicium (SiO2) qui entre dans la composition de nombreux minéraux.
La silice existe à l'état libre sous différentes formes cristallines ou amorphes, et combiné à d'autres oxydes (Al2O3, FeO, MgO, CaO, Na2O, K2O, etc.) dans les silicates.
Les silicates sont les constituants principaux du manteau et de l'écorce terrestre. La silice libre est également très abondante dans la nature, sous forme de quartz, de calcédoine et de terre de diatomée. La silice représente 60,6 % de la masse de la croûte terrestre continentale[8]. Après l’oxygène le silicium est l’élément le plus abondant dans la lithosphère (27 % en masse[9]).
Au-delà de certains seuils, l'inhalation de toutes les formes de poussières, nanoparticules, particules fines de silice est dangereuse. Elle est notamment cause de silicose et de plusieurs autres maladies (dont des maladies auto-immunes). Dans l’Union européenne, la directive (UE) 2017/2398 classe en 2017 les poussières de silice comme agent cancérigène, tout en révisant les valeurs limites d'exposition (VLE) aux agents cancérigènes ou mutagènes pour rendre ces expositions plus contraignantes. Elle doit être progressivement appliquée par tous les États membres de l'Union européenne[10].
Propriétés[modifier | modifier le code]
La silice pure est un minéral dur. Elle existe sous des formes variées dans la nature :
- principal constituant des roches sédimentaires détritiques (sables, grès), elle représente 27 % de la masse de la croûte terrestre ;
- fréquente dans les roches métamorphiques ;
- fréquente dans les roches magmatiques : quartz dans les roches magmatiques acides, cristallisée ou amorphe dans les roches volcaniques.
Pure, elle est transparente dans tout le domaine visible. Ceci lui donne des applications intéressantes en optique. Ses propriétés de transparence se perdent dans les domaines UV et infrarouge, ce qui impose l'usage d'autres matériaux pour travailler dans ces longueurs d'onde, par exemple en spectrométrie infrarouge. Cet effet est mis à profit en agriculture ou dans l'Habitat (solaire thermique... maison passive) où l'on exploite l'effet de serre : la lumière pénètre les vitres, mais ces dernières piègent une partie des infrarouges, d'où un échauffement ou, tout au moins, le maintien d'une température plus élevée à l'intérieur qu'à l'extérieur du volume vitré.
La silice est un oxyde acide qui réagit avec les oxydes basiques pour donner des silicates (ions SiO32−, analogue à l'ion carbonate, et SiO44− entre autres). La présence majoritaire de silicates fait du silicium le deuxième élément en masse dans la croûte terrestre derrière l'oxygène.
La silice se présente soit sous forme de cristaux non-moléculaires formés de motifs tétraédriques SiO4 liés entre eux par les atomes d'oxygène de façon régulière, comme dans le quartz, soit sous forme amorphe, comme dans le verre.
La silice sert de matière première à l'obtention du silicium. Elle est réduite par réaction carbothermique dans des fours à arc à plus de 2 000 °C suivant la réaction :
La silice sert également de support isolant en électronique.
Applications[modifier | modifier le code]

| Minéral | Densité | Indice de réfraction |
|---|---|---|
| silice fibreuse | 1,96 | 1,40 |
| mélanophlogite | 2,05 | 1,42 |
| verre de silice | 2,20 | 1,46 |
| tridymite | 2,26 | 1,47 |
| cristobalite | 2,33 | 1,48 |
| kéatite | 2,50 | 1,52 |
| quartz | 2,65 | 1,55 |
| coésite | 3,0 | 1,59 |
| stishovite | 4,35 | 1,78 |
Le verre de silice est de la silice non cristallisée utilisée dans la fabrication des instruments d'optique, d'appareils de laboratoire et de fibre de verre.
La silice est chimiquement stable et n'est guère attaquée que par l'acide fluorhydrique, réaction utilisée dans la gravure sur verre. Cette réaction empêche d'utiliser du verre de silice pour manipuler le fluor.
La silice se dissout très partiellement dans l'eau pure sous la forme de Si(OH)4 l'acide silicique (acide faible). La limite de solubilité étant de 0,140 g·L-1 à 25 °C. Cette solubilité augmente très fortement avec le pH (formation d'ion silicate, par la présence d'alcali dans une eau en bouteille), la température et la pression ; ainsi cette solubilité atteint 20 % dans l'eau supercritique à 500 °C et 1 000 bar.
Dans l'eau, l'acide silicique forme des suspensions colloïdales qui sont responsables de l'apparente opacité de l'eau lorsqu'elles sont présentes. C'est le cas dans l'eau des geysers comme celui de Geysir en Islande. Pour une concentration donnée en silice colloïdale, la couleur bleue est d'autant plus intense que l'eau est plus froide (la solubilité de Si(OH)4 est alors plus faible).
La silice est aussi l'un des meilleurs isolants électriques qui existe. Pour cette raison, elle est souvent utilisée sur des circuits électriques de silicium, simplement en oxydant les couches voulues.
Dans l'industrie alimentaire, la silice est parfois utilisée comme agent anti-agglomérant ou anti-mottant dans des denrées en poudre (sucre, sucre glace, épices, etc.).
En minéralogie[modifier | modifier le code]
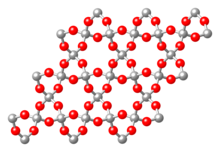
(atomes O en rouge, atomes Si en gris)
La silice cristallise sous plusieurs formes minérales en fonction de la température et de la pression de cristallisation. Par température de fusion, voici les polymorphes de la silice :
- stishovite (pf = 1 200 °C) ;
- quartz (α ou β) (pf = 1 650 °C) ;
- tridymite (pf = 1 670 °C) ;
- calcédoine (pf = 1 700 °C) ;
- cristobalite (pf = 1 713 °C) ;
- coésite.
Silice hydratée[modifier | modifier le code]
- L'opale
Il ne s’agit pas d’une espèce au sens strict du terme mais cette famille a une reconnaissance officielle par l’Association internationale de minéralogie (IMA)[11]
Elle se compose de trois espèces minérales bien distinctes, la cristobalite, la tridymite et la silice amorphe hydratée.
Elle se décompose en quatre variétés :

Opal-CT (la lussatite des francophones) composé de cristobalite-tridymite (d’où les deux lettre « C » et « T »).
Opal-C est une forme qui est encore à l’étude. Il semble que la base soit une cristobalite, présentant d’importantes anomalies de structures cristalline. Les différences sont assez franches pour la distinguer de la cristobalite ; de même le terme cristobalite-microcristalline n’est pas encore prouvé.
Opal-AG est l’opale la plus connue ; formée de microsphères de silice amorphe, associées à des molécules d’eau dans des proportions variable. La lettre « A » désigne le caractère amorphe, la lettre « G » suggère que nous sommes en présence d’un gel.
Opal-AN (la hyalite des francophones). Forme amorphe (Lettre A) comme la précédente mais cette opale apparait dans les formations volcaniques, où les pegmatites déposent la silice à des températures élevées. La lettre « N » (normal) rappelle que la structure en réseau est plus proche de la silice mais il reste tout de même des molécules d’eau dans des proportions significatives.
Dans le vivant[modifier | modifier le code]
Des organismes comme les éponges siliceuses, le phytoplancton et les plantes jouent un rôle important dans le cycle biogéochimique de la silice[12]. Le Si joue souvent un rôle important de rigidification de structure ou de parois cellulaire améliorant la résistance et la rigidité des organismes capables de l'utiliser.
Pour des raisons notamment génétiques, l'accumulation de silicium (Si) varie toutefois beaucoup selon les espèces végétales, plus ou moins apte à capter le Si via leur rhizosphère[12]. Un gène code un transporteur d'absorption de Si, a été découvert dans le riz[12].
Le Si semble aussi jouer un rôle actif de défense des plantes contre certaines maladies, en stimulant les mécanismes de réaction de défense[12].
OGM ? Au Japon, en 2006, des biotechnologistes ont proposé de doper des espèces incapables d'accumuler assez de Si pour qu'il leur soit bénéfique, par manipulation génétique pour accroître la capacité d'absorption du Si via les racines[12].
Silice et santé[modifier | modifier le code]

La silice colloïdale est très utilisée dans l'industrie du médicament comme excipient pour stabiliser les principes actifs.. C'est d'ailleurs l'excipient le plus utilisé[15].
La silice colloïdale ionisée (obtenue par électrolyse) stabilisée par de l'éthanol et de l'acide chlorhydrique en flacon opaque, est un médicament en soi avec une indication de modificateur de terrain, en particulier au cours d’affections rhumatismales inflammatoires (Laboratoire du Dissolvurol)[16]. Ce médicament était même remboursé autrefois par la Sécurité Sociale. Ce Dissolvurol silicium est aussi très utilisé pour des usages détournés, en particulier pour la perte de poids et par des naturopathes oligothérapeutes, Les patients ainsi traités rapporteraient un mieux-être général[17].
La silice cristalline est le matériau le plus présent de la croute terrestre. Il est donc logique de la retrouver dans la majorité des matériaux naturels d'origine minérale (presque toujours plus de 0,1 % du matériau et jusqu’à près de 100 % pour les sables, silex, etc.). Via les granulats qui contiennent tous de la silice cristalline, on la retrouve dans les routes, les bâtiments et de nombreux ouvrages de travaux publics. L’usure de ces matériaux et plus encore leur sciage, ponçage ou meulage à sec sont des sources d’exposition directe ou indirecte, immédiate ou différée à la silice cristalline.
Exposition à la silice et pathologies induites[modifier | modifier le code]
En 2019, dans le monde la silice n'est pas considérée comme toxique en tant que telle (on en trouve par exemple dans des dentifrices). Mais l'inhalation de particules de silice libre ou de poussière riche en silice cristalline (dans les mines, ateliers de sculpteurs ou dans certains métiers (meulage sur les chantiers de travaux publics ou de construction/déconstruction/démolition par exemple) est reconnue comme exposant à au moins deux maladies graves (généralement mortelles) affectant respectivement le système respiratoire et la peau et d'autres organes :
- silicose (typiquement chez les mineurs de fond ou ouvriers exposés aux fines particules de granit, grès, quartz, béton, briques ou silex notamment lors d'opérations à sec de tronçonnage, concassage, meulage, ponçage, burinage, explosion… ) ;
- sclérodermie généralisée[18]. La silice pourrait aussi dans ce cas être un facteur iatrogène[19] ; la silice est désormais classée cancérigène.
La silice cristalline peut aussi :
- entrainer une maladie auto-immune comme la sclérodermie systémique (syndrome d'Erasmus), la polyarthrite rhumatoïde ou le lupus érythémateux systémique ou disséminé (LED)[20],[21],[22]. Selon Miguel Hie, spécialiste en médecine interne : L’exposition à la silice cristalline est un des risques environnementaux associés au lupus les mieux documentés, bien que largement méconnu des cliniciens.[22]. Dans une étude effectuée en 2016 sur des souris femelles génétiquement prédisposées à être atteintes du lupus, 96 % des lésions des poumons provoquées par exposition à la silice ont été stoppées par la prise de DHA (ou acide docosahexaénoïque), un acide gras oméga-3[23] ;
- un syndrome de Sjögren[21].
- une probabilité augmentée de pathologie rénale (association statistique démontrée, mais avec un lien causal encore mal compris)[14] ;
- une pneumopathie infiltrante diffuse (PID) de type FPI, c'est-à-dire "fibrose pulmonaire idiopathique" (pour ces maladies, l'association statistique est en 2019 démontrée, mais avec un lien causal encore mal compris)[14] ;
En 2019, la silice cristalline est encore uniquement classée agent chimique dangereux (car cause de silicose), mais non reconnue comme cancérigène (en dépit de nombreuses études concluant à une cancérogénicité)[24].
En , les procédés dégageant des poussières de silice sont classés cancérigènes par une directive européenne devant être transposée dans le droit de tous les États membres[24]
En France, après 4 ans d’auto-saisine de la question des risques sanitaires induits par l’exposition à la silice, un nouveau rapport[25] de l’ANSES confirme aussi le risque de cancer, et conclut au besoin de renforcer la réglementation. Le risque sanitaire est jugé « particulièrement élevé (supérieur à 1 pour 1.000) pour les professionnels exposés à la silice cristalline » et « la valeur actuelle de la valeur limite d'exposition professionnelle (VLEP-8h) de 0,1 mg.m3 en France n'est pas suffisamment protectrice »[24]. Selon l’Anses, la silice présente « un risque sanitaire particulièrement élevé » pour les salariés. En France, selon le Réseau national de vigilance et de prévention des pathologies professionnelles (RNV3P) : de 2001 à 2017, 4 506 « problèmes de santé en relation avec le travail associé à la silice » ont été répertoriés (dont 40 % de cancers broncho-pulmonaires, 26 % de silicose et 8 % de broncho-pneumopathie chronique obstructive, sachant qu'un tiers des salariés concernés sont employés dans le BTP note le RNV3P[24]. En France toujours, près de 365 000 ouvriers, notamment dans les secteurs de la construction, de la métallurgie et des industries extractives (4 200 carrières d'extraction de minéraux et matériaux de construction en France[24]), y sont exposés[26], chiffre réévalué : 170 414 salariés du BTP ont été exposés à ce risque en 2017, rien qu'en France, selon l'enquête nationale Surveillance médicale des expositions des salariés aux risques professionnels (Sumer)[24]. Ce nombre correspond à 12,3 % de l'ensemble des travailleurs du secteur[24]. Les nombres de salariés exposés à un dépassement de la VLEP auraient été (en 2017) compris entre 14 600 et 22 400 personnes selon l'ANSES. L’Anses estime que pour l'exposition aux particules de quartz, 23 000 à 30 000 travailleurs y seraient en 2019 encore exposés à des niveaux excédant la valeur limite d’exposition professionnelle (VLEP) de 0,1 mg/m3 actuellement en vigueur en France. Ce nombre passe à 60 000 si l'on considère les dépassements de seuils pour la VLEP la plus basse existant au niveau international, qui est de 0,025 mg/m3 d'air (et plus des 2/3 des travailleurs exposés sont ceux de la construction ; devant ceux de la fabrication des produits minéraux non métalliques, puis de la métallurgie et des industries extractives[14]. Mi-, l'Anses invite donc le gouvernement à[14] :
- réviser la VLEP, quelle que soit le type de silice "polymorphe" (quartz, cristobalite et tridymite) ;
- augmenter la sensibilisation et la prévention, dont vers les professionnels exposés à la silice cristalline ou exposant leur entourage aux particules de silice cristalline ;
- mettre à jour le tableau des maladies professionnelles, en considérant l'inhalation des poussières de silice comme potentiellement déclencheur de cancers broncho-pulmonaires ;
et, pour la silice cristalline[14] :
- appliquer les mesures de prévention définies par la directive de 2004 (récemment modifiée pour mieux protéger les travailleurs contre les risques liés à l'exposition à des agents cancérogènes ou mutagènes au travail) et la Directive UE2017/2398 de 2017 qui classe les poussières de silice comme agent cancérigène, et révise les valeurs limites d'exposition (VLE) aux agents cancérigènes ou mutagènes pour rendre ces expositions plus contraignantes[10].) ;
- faire évoluer le diagnostic et le dépistage de pathologies telles que la silicose, tuberculose, pathologies rénales… pour des sujets exposés ou ayant été exposés professionnellement à la silice cristalline ;
- améliorer la connaissance de la prévalence des expositions, et concernant la métrologie et les effets sanitaires.
Valeurs limites d'exposition[modifier | modifier le code]
Elles varient selon les pays et devraient se durcir dans les années 2010-2020, dont en France car les avis de l'Anses, généralement très argumentés, sont souvent pris en compte (la réglementation et les manières de travailler dans le BTP devraient changer). Une directive européenne impose aussi une meilleure protection des individus exposés à la silice ;
En France où la valeur limite d'exposition (fixée à 0,1 mg/m3 de poussières de silice alvéolaire inhalé en 8 heures) semble souvent dépassée, un guide pédagogique a été publié en 2019 pour les entreprises encadrant des terrassiers, canalisateurs, maçons ou ouvriers des chantiers de BTP, en partenariat avec des Carsat régionales et experts en santé au travail dans le BTP[13]. Le guide recommande notamment d'utiliser des pièces préfabriquées ou pré-sciés et de "Privilégier la déconstruction par éléments plutôt que la démolition destructive". De même utiliser l'eau (carter de coupe, aspiratrice avec arrosage) et jamais le balayage et le soufflage, au profit de la brumisation, du rinçage et de l'aspiration avec filtres appropriés. Dans les chantiers à risques, les conducteurs d'engins doivent travailler cabine fermée, avec atmosphère filtrée et pressurisée[13]. Le personnel exposé doit porter des masques et appareils de protection respiratoire appropriés (ex : cagoule à adduction d'air… ) et des vêtements de protection jetables (classe 5 ou 6) pourraient même devenir obligatoire[13].
Prévention[modifier | modifier le code]
Elle consiste à éviter d'inhaler de l'air pollué, notamment par le tabac ou des particules.
En 2019 l'ANSES demande que soit généralisées des mesures telles que le travail à l'humide (immersion, arrosage ou brumisation des zones de perçage, meulage, broyage, sciage...) et/ou le captage des poussières à la source, en vérifiant systématiquement et préalablement leur efficacité selon l'outil et la techniques utilisées, dont lors de chantiers mobiles". Mais l'ANSES précise que ces deux techniques, mêmes associées, ne suffisent pas toujours : les niveaux résiduels peuvent dans certaines conditions conduire au dépassement des VLEP actuelles." Ceci questionne les moyens de protéger l'environnement et les salariés quand la VLEP n'est pas respectée, et/ou si elle est diminuée, ce qui sera le cas si l'on suit les recommandations des toxicologues et les prescriptions de l'Anses[14].
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Densities of Solids : Densities of common solids », sur engineeringtoolbox.com (consulté le ).
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 1 : Cancérogènes pour l'homme »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur monographs.iarc.fr, CIRC, (consulté le ).
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur monographs.iarc.fr, CIRC, (consulté le ).
- « Silice amorphe » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « Silice précipitée » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « Silice fondue » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- (en) R. L. Rudnick (dir.) et S. Gao, Treatise on Geochemistry, vol. 3 : The Crust, Elsevier, , 702 p. (ISBN 978-0-08-044847-3, présentation en ligne), « Composition of the Continental Crust », p. 48,53
- Meunier J.D (2003). Le rôle des plantes dans le transfert du silicium à la surface des continents. Comptes Rendus Geoscience, 335(16), 1199-1206.
- « DIRECTIVE (UE) 2017/2398 DU PARLEMENT EUROPÉEN ET DU CONSEIL » [PDF], sur eur-lex.europa.eu, (consulté le ).
- American Mineralogist 92, 2007, 1325.
- (en) Jian Feng Ma et Naoki Yamaji, « Silicon uptake and accumulation in higher plants », Trends in Plant Science, vol. 11, no 8, , p. 392–397 (DOI 10.1016/j.tplants.2006.06.007, lire en ligne, consulté le )
- BatuActu (2019) [ https://www.batiactu.com/edito/poussieres-silice-dans-tp-a-vos-masques-prets-coupez-55879.php Poussières de silice dans les TP : à vos masques, prêts, coupez !] Publié le 22/03/2019
- Exposition à la silice cristalline : des risques élevés pour la santé des travailleurs , Communiqué ANSES, mai 2019
- (en-US) « Anhydrous Colloidal Silica Excipient | Uses, Suppliers, and Specifications », sur PharmaCentral | Materials and Knowledge Platform (consulté le ).
- « Nos produits Bonne santé et Bien-être - Laboratoire Dissolvurol », sur dissolvurol.org (consulté le ).
- « Silicium - Bibliographie », sur sili.cium.free.fr (consulté le ).
- Amoudru C (1991) Sclérodermie généralisée et inhalation de poussières mixtes contenant de la silice libre Documents pour le médecin du travail, 46, 101-106.
- Hallé, O., Schaeverbeke, T., Bannwarth, B. et Dehais, J. (1997), Les facteurs d'environnement et les éléments iatrogènes dans la sclérodermie systémique et les syndromes apparentés. Revue de la littérature. La Revue de médecine interne, 18(3), 219-229.
- Lilian Tereza Lavras Costallat et Eduardo Mello De Capitani, « Silicose pulmonaire et lupus érythémateux disséminé chez l'homme. À propos de deux observations », sur em-consulte.com (consulté le ).
- Isabelle Marie, « Lupus, polymyosites, dermatomyosites et syndrome de Sjögren d’origine médicamenteuse et toxique », Médecine thérapeutique, vol. 14, no 4, (ISSN 1264-6520, DOI 10.1684/met.2008.0169, lire en ligne, consulté le )
- Miguel Hie, Lupus systémique induit par la silice cristalline : analyse détaillée de la littérature illustrée de deux observations cliniques, (lire en ligne).
- (en) Melissa A. Bates, Christina Brandenberger, Ingeborg I. Langohr et Kazuyoshi Kumagai, « Silica-Triggered Autoimmunity in Lupus-Prone Mice Blocked by Docosahexaenoic Acid Consumption », PLOS ONE, vol. 11, no 8, , e0160622 (ISSN 1932-6203, PMID 27513935, PMCID PMC4981380, DOI 10.1371/journal.pone.0160622, lire en ligne, consulté le )
- Florent Lacas (2019) « Silice cristalline : un "risque sanitaire particulièrement élevé" RAPPORT. Une étude alarmante de l'Agence nationale de sécurité sanitaire (Anses) vient confirmer la dangerosité et le caractère cancérigène des poussières de silice cristalline, omniprésentes dans les secteurs du BTP et de l'industrie extractive. Et formule un certain nombre de recommandations qui impacteront les manières de travailler », BatiActu, article publié le 22/05/2019
- ANSES (2019) Dangers, expositions et risques relatifs à la silice cristalline Rapport d’expertise collective - Saisine « n° 2015-SA-0236 - Silice cristalline » | mars
- « La silice, ce minéral qui présente « un risque sanitaire particulièrement élevé » pour les salariés », Le Monde, (lire en ligne, consulté le )
Voir aussi[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- IARC, Monographie, vol. 68, 1997, Silica, Some Silicates, Coal Dust and para-Aramid Fibrils
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- Dossier Futura-Sciences sur la silice : Au cœur de la silice… du silex au wafer
