Nickel de Raney
| Nickel de Raney | |||

| |||
| Nickel de Raney activé dans un verre de montre. | |||
| Identification | |||
|---|---|---|---|
| No CAS | (inactif) (activé) |
||
| Apparence | solide gris foncé[1] | ||
| Précautions | |||
| SGH[1] | |||
| (inactif)H261, H317, H334, H351, H372, P201, P280, P285, P231+P232, P302+P352, P304+P341, P308+P313 et P342+P311 |
|||
| NFPA 704[1] | |||
| Transport[1] | |||
(inactif)
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Le nickel de Raney est un catalyseur solide utilisé dans de nombreux procédés industriels. Constitué d'une fine poudre grise d'un alliage de nickel et d'aluminium, il a été développé en 1926 par l'ingénieur américain Murray Raney[2] comme solution de remplacement aux catalyseurs utilisés à cette époque dans l'industrie pour l'hydrogénation des huiles végétales. Plus récemment, il est utilisé comme catalyseur hétérogène pour une grande variété de réactions de la chimie organique, le plus souvent pour des hydrogénations.
Le nickel de Raney est produit en traitant un morceau d'alliage nickel-aluminium par la soude concentrée. Au cours de ce traitement appelé « activation » ou « lixiviation », la majeure partie de l'aluminium de l'alliage est dissous. La structure poreuse qui en résulte possède une surface spécifique très importante, ce qui contribue à son efficacité en catalyse. Le catalyseur est généralement constitué de 85 % de nickel (en masse), ce qui correspond approximativement à deux atomes de nickel pour un atome d'aluminium. L'aluminium qui n'est pas dissous aide à conserver la structure poreuse du catalyseur à l'échelle macroscopique. Sous sa forme activée, c'est un matériau pyrophorique qui doit être manipulé sous atmosphère inerte sous peine de subir des blessures.
Même si l’appellation « Raney » est la plus courante, c’est une marque déposée de W. R. Grace and Company, et seul celui produit par la division Grace Davison peut porter ce nom. Pour les catalyseurs possédant des propriétés physiques et chimiques similaires à celles du nickel de Raney, les termes les plus couramment utilisés sont des noms imagés tels que « spongy nickel » (« nickel spongieux ») ou « skeletal nickel » (« squelette de nickel » ) qui illustrent la structure de ce solide.
Développement[modifier | modifier le code]
Murray Raney a obtenu son diplôme d'ingénieur en mécanique de l'université du Kentucky en 1909. En 1915, il est embauché par la société Lookout Oil and Refining Company au Tennessee, société dans laquelle il est responsable de l'installation des cellules d'électrolyse destinées à la production de dihydrogène pour l'hydrogénation des huiles végétales. À cette époque, le catalyseur utilisé dans l'industrie pour cette hydrogénation est à base d'oxyde de nickel(II). Raney, croyant qu'il est possible de créer un catalyseur plus efficace, commence à mener des recherches indépendantes à partir de 1921 tout en continuant à travailler pour Lookout Oil. En 1924, il produit un alliage nickel-silicium en proportions égales, qui s'avère après traitement à l'hydroxyde de sodium cinq fois plus efficace que le meilleur catalyseur utilisé alors pour l'hydrogénation de l'huile de graines de coton. En , il dépose un brevet pour cette découverte[3].
Juste après cette première découverte, Raney fabrique un alliage nickel-aluminium en proportions égales, en suivant la même procédure que celle utilisée pour l'alliage nickel-silicium, notamment le traitement à la soude. Les essais effectués montrent alors que ce nouveau catalyseur est plus efficace, et Raney remplit une demande de dépôt de brevet en 1926[2]. Le choix de proportions égales pour le nickel/aluminium ne repose sur aucune base scientifique. Cette composition est toujours, en 2008, la plus utilisée pour la production de nickel de Raney.
À la suite du développement du nickel de Raney, d'autres alliages contenant de l'aluminium ont été étudiés, les plus importants contenant du cuivre, du ruthénium ou du cobalt. Des recherches ont montré par ailleurs que l'ajout d'un troisième métal (promoteur) au binaire permet d'augmenter le pouvoir du catalyseur. Les promoteurs les plus couramment utilisés sont le zinc, le molybdène et le chrome. Plus récemment, un nickel de Raney énantiosélectif a pu être préparé en utilisant de l'acide tartrique qui s'adsorbe en surface du catalyseur[4].
Fabrication[modifier | modifier le code]
Fabrication de l'alliage[modifier | modifier le code]

L'alliage est préparé industriellement par fusion du nickel (dans le cas du nickel de Raney, mais il est possible de préparer également des catalyseurs de type Raney à partir d’autres métaux comme le fer ou le cuivre) et de l'aluminium dans un creuset. L’alliage encore en fusion subit une trempe. Le mélange solide obtenu est alors finement broyé[5]. La poudre peut alors être tamisée pour obtenir une gamme de tailles de particules contrôlée, en fonction de l'application pour laquelle le catalyseur est fabriqué.
La composition initiale de l'alliage est un facteur important parce que la trempe produit de nombreuses phases nickel-aluminium différentes qui ont des propriétés de lixiviation distinctes, ce qui a une influence importante sur la porosité du catalyseur en fin de procédé. Les alliages les plus couramment utilisés dans l'industrie contiennent au départ la même quantité de nickel que d'aluminium (en masse), ce qui correspond d'ailleurs au ratio utilisé par Murray Raney lors du développement du catalyseur.
Au cours de l'étape de trempe, de petites quantités d'un troisième métal, comme le zinc ou le zirconium, peuvent être ajoutées. Cet ajout permet d'augmenter le pouvoir catalytique, si bien que le troisième métal est généralement appelé « promoteur »[5]. L'ajout d'un promoteur change la nature de l'alliage et son diagramme de phase (l'alliage devient un ternaire), ce qui induit des propriétés de trempe et de lixiviation différentes.
Activation[modifier | modifier le code]
La structure poreuse du catalyseur est obtenue par dissolution sélective de l'aluminium de l'alliage en utilisant une solution aqueuse de soude. La réaction de lixiviation correspond de manière simplifiée à l'équation suivante :
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
La formation d'aluminate de sodium (Na[Al(OH)4]) nécessite l'utilisation d'une solution de soude fortement concentrée pour éviter la formation d'hydroxyde d'aluminium qui précipiterait sous forme de bayérite[5]. Les solutions utilisées ont donc des concentrations qui peuvent atteindre 5 moles par litre. La précipitation de bayérite entraînerait un remplissage des pores formés au cours de la lixiviation et donc une perte de surface spécifique avec pour conséquence une diminution de l'efficacité du catalyseur.
La température à laquelle a lieu la lixiviation de l'alliage a une influence importante sur les propriétés de surface du catalyseur. Les températures couramment utilisées vont entre 70 °C et 100 °C. La surface spécifique du nickel de Raney (et des catalyseurs de type Raney en général) tend à décroître lorsque la température de lixiviation augmente[6]. Cette décroissance est due à des réarrangements structuraux au sein de l'alliage, analogues aux effets d'un frittage : les différentes particules constituant l'alliage commencent à adhérer les unes aux autres lorsque la température augmente, et il en résulte une diminution de la porosité de la structure.
Avant son stockage, le catalyseur peut être lavé avec de l'eau distillée à la température ambiante de manière à éliminer les traces éventuelles d'aluminate de sodium. Il est préférable d'utiliser de l'eau désoxygénée pour le stockage de manière à éviter l'oxydation du catalyseur. Celle-ci accélère en effet son vieillissement et tend à diminuer son pouvoir catalytique[5].
Propriétés[modifier | modifier le code]

Le nickel de Raney ressemble à une très fine poudre grise. À l'échelle microscopique, chaque particule de poudre ressemble à un réseau tridimensionnel, avec des pores de formes et de tailles irrégulières dont la plus grande partie est formée au cours de l'étape de lixiviation. Les principales particularités du nickel de Raney sont sa stabilité thermique et structurale, et sa très grande surface spécifique active pour l'adsorption des gaz. Ces propriétés sont directement liées au procédé d'activation, et contribuent à son pouvoir catalytique élevé.
Au cours de l'étape d'activation, l'aluminium est éliminé des phases NiAl3 et Ni2Al3 présentes dans l'alliage, la majeure partie de l'aluminium qui n'est pas éliminé étant contenu sous forme NiAl. La dissolution de l'aluminium contenu dans certaines phases et pas dans d'autres est connue sous le nom de « lixiviation sélective ». Il a été montré que c'est la phase NiAl qui contribue à la stabilité thermique et structurale du catalyseur. Du fait de la présence de cette phase, le nickel de Raney est assez résistant vis-à-vis de la décomposition (rupture ou vieillissement)[6]. Cette résistance permet au nickel de Raney d'être stocké et réutilisé durant de longues périodes, même si un catalyseur fraîchement préparé est généralement préféré en laboratoire. Pour cette raison, le nickel de Raney est disponible commercialement sous forme « active » (avec hydrogène adsorbé) et « inactive » (sans hydrogène adsorbé).
La surface spécifique est généralement déterminée par des mesures d'adsorption d'un gaz, qui s'adsorbe de manière préférentielle sur les surfaces métalliques comme l'hydrogène. Il a été montré en utilisant ce type de mesures que pratiquement toute la surface des particules du catalyseur est constituée d'atomes de nickel[5]. Le nickel étant le métal actif du catalyseur, une surface constituée préférentiellement de nickel implique une surface importante de disponible permettant à de nombreuses réactions de se produire de manière simultanée (ce qui correspond donc à un pouvoir catalytique élevé). Le nickel de Raney disponible commercialement possède une surface spécifique de nickel moyenne de l'ordre de 100 m2 par gramme de catalyseur[5].
Le nickel de Raney possédant un pouvoir catalytique élevé et l'hydrogène s'adsorbant dans ses pores, c'est un catalyseur très utile pour de nombreuses réactions d'hydrogénation. Sa stabilité structurale et thermique (par exemple le fait qu'il ne se décompose pas aux températures élevées) permet de l'utiliser dans une grande gamme de conditions opératoires. Par ailleurs, la solubilité du nickel de Raney est négligeable dans la plupart des solvants couramment utilisés en laboratoire, à l'exception des acides minéraux comme l'acide chlorhydrique, et sa densité relativement élevée (entre 6 et 7 g/cm3) rend plus facile sa séparation de la phase liquide en fin de réaction. Enfin, les propriétés magnétiques de ce solide permettent de le séparer facilement d'une phase aqueuse par simple utilisation d'un aimant.
Il existe une grande variétés de nickel de Raney, qui dépendent de la composition de son alliage Ni-Al, en général 50% en masse de chaque métal, mais d'autres compositions peuvent exister, qui sont des mélanges des différentes phases métalliques : NiAl3, Ni2Al3, voire la phase eutectique Al-NiAl3, le produit final étant aussi dépendant du traitement thermique utilisé lors de la préparation de l'alliage. La plupart des alliages commerciaux ont une teneur comprise entre 40 et 50% en masse de nickel, et peuvent donc être constitués de phases différentes, dont les ratios peuvent varier considérablement. Ces différentes phases sont attaquées plus ou moins rapidement par l'hydroxyde de sodium et libèrent donc l'hydroxyde d'aluminium avec plus ou moins de facilité. Du fait de la très grande variété des produits possibles, on les classe en huit catégories, nommé W1 à W8, selon divers facteurs, comme la température d'addition de l'hydroxyde de sodium (de −20 à 50 °C), le ratio NaOH/Alliage (1 ou 4/3), la température (50 à 120 °C), la durée du traitement (1 à 12 heures) et le mode de lavage choisi[7]. Les variété W1 et W8 sont les moins réactives, utilisées pour des hydrogénations sélectives, et la variété W2 est la plus courante est contient la plupart des produits commerciaux disponibles.
Applications[modifier | modifier le code]
Du fait de sa stabilité et de son pouvoir catalytique élevé à la température ambiante, le nickel de Raney est utilisé dans un grand nombre de procédés industriels et de réaction de chimie organique[5],[8]. Il est entre autres utilisé pour la réduction de composés organiques à liaisons multiples comme les alcynes, les alcènes[9], les nitriles[10], les diènes, les composés aromatiques[11] ou les carbonyles. Par ailleurs, le nickel de Raney permet de réduire des liaisons hétéroatome-hétéroatome comme dans le groupement nitro et les nitrosamines[12]. Il est également utilisable pour l'alkylation réductrice des amines[13] ou l'amination des alcools.
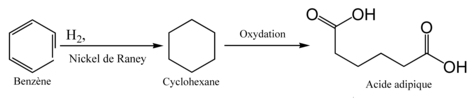
Un exemple pratique de l'utilisation du nickel de Raney dans l'industrie est montré dans la réaction suivante, au cours de laquelle le benzène est réduit en cyclohexane. La réduction de la structure aromatique du benzène est extrêmement difficile à mettre en œuvre sans catalyseur, mais peut être réalisée sans difficulté majeure en utilisant le nickel de Raney. D'autres catalyseurs hétérogènes peuvent être également utilisés pour cette réaction, comme notamment ceux utilisant des éléments du groupe du platine, mais ils sont beaucoup plus chers à produire. Après cette réaction de réduction, le cyclohexane peut être utilisé par exemple pour la synthèse d'acide adipique, un précurseur utilisé dans la fabrication des polyamides comme le nylon[14].
Lors de la réduction d'une double liaison carbone-carbone avec utilisation de nickel de Raney, l'addition des deux atomes d'hydrogène se fait dans une géométrie syn[14].
En plus de son action de catalyseur, le nickel de Raney peut être utilisé comme réactif pour la désulfurisation des composés organiques[15]. Il permet par exemple de réduire les thioacétals en hydrocarbures[14] :
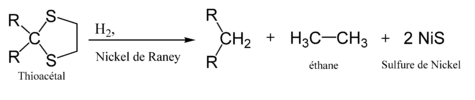
Au cours de cette réaction, le sulfure de nickel précipite sous forme de millérite, alors que l'éthane peut être aisément séparé du mélange réactionnel par distillation. Parmi les autres réactions similaires permettant l'obtention des alcanes à partir des cétones, on peut notamment citer les réactions de Clemmensen et de Wolff-Kishner.
En 1939, Leopold Ruzicka et Adolph Butenandt obtiennent le prix Nobel de chimie pour avoir synthétisé des hormones mâles à partir de cholestérol en utilisant le nickel de Raney comme catalyseur.
Sécurité[modifier | modifier le code]
Préparation[modifier | modifier le code]
Le nickel est soupçonné d'être une substance potentiellement cancérigène pour l'homme par le (CIRC Groupe 2B, EU category 3) et tératogène. L'inhalation de particules fines d'oxyde d'aluminium est directement associée quant à elle à la maladie de Shaver. Ces matériaux doivent donc être manipulés avec précaution lors de la préparation du nickel de Raney. Par ailleurs, l'un des sous-produits de la réaction d'activation du catalyseur est l'hydrogène, qui est un gaz hautement inflammable[16].
Manipulation[modifier | modifier le code]


Du fait de sa très grande surface spécifique et du volume très important d'hydrogène adsorbé, le nickel de Raney activé est un matériau pyrophorique qui doit être manipulé sous atmosphère inerte. Il est généralement fourni sous forme dispersée dans de l'eau (à 50 % en masse). Il ne doit jamais être exposé à l'air. Même après une réaction d'hydrogénation, le nickel de Raney contient toujours une quantité importante d'hydrogène et s'enflamme spontanément à l'air.
Lors de sa combustion, le nickel de Raney produit des fumées dangereuses, et il est recommandé de porter un masque à gaz pour éteindre un incendie éventuel. Par ailleurs, l'exposition aiguë au nickel de Raney peut entraîner une irritation des voies respiratoires, de la cavité nasale, ou des poumons en cas d'inhalation. L'ingestion peut occasionner des convulsions et des troubles intestinaux. Le nickel de Raney peut également entraîner une irritation des yeux et de la peau en cas de contact. L'exposition chronique peut occasionner des symptômes de pneumonies allergiques dues à une sensibilisation au nickel ainsi que des irritations allergiques de la peau[16].
Notes et références[modifier | modifier le code]
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Raney nickel » (voir la liste des auteurs).
- « Fiche du composé Nickel Aluminum, Raney® type non-activated », sur Alfa Aesar (consulté le ).
- (en) Brevet US 1628190 "Method of producing Finely Divided Nickel", Murray Raney, publié le 10 mai 1927
- (en) Brevet US 1563587 "Method of Preparing Catalytic Material", Murray Raney, publié le 1er décembre 1925
- (en) M. L. Bakker, D. J. Young et al., « Selective leaching of NiAl3 and Ni2Al3 intermetallics to form Raney nickels », J. Mat. Sci., vol. 23 « 23 », no 11, , p. 3921-3926 (ISSN 0022-2461 et 1573-4803, DOI 10.1007/BF01106814)
- (en) G. Ertl et H. Knözinger, Preparation of Solid Catalysts, Weinheim/New York/Chichester etc., Wiley-VCH, , 622 p. (ISBN 3-527-29826-6 et 9783527298266, présentation en ligne, lire en ligne)
- (en) A. J. Smith et D. L. Trimm, « The Preparation of Skeletal Catalysts », Ann. Rev. Mat. Res., vol. 35, , p. 127-142 (DOI 10.1146/annurev.matsci.35.102303.140758)
- (en) Robert L. Augustine, Heterogeneous Catalysis for the Synthetic Chemist, CRC Press, (ISBN 9781003067122)
- (en) Organic Syntheses, « Raney nickel usage in Organic Syntheses », sur www.orgsyn.org (consulté le )
- (en) G. A. Page et D. S. Tarbell, « β-(o-Carboxyphenyl)propionic acid », Org. Synth., vol. 34, , p. 8 (ISSN 0078-6209, lire en ligne)
- (en) H. C. Robinson, Jr. et H. R. Snyder, « β-Phenylethylamine », Org. Synth., vol. 23, , p. 71 (ISSN 0078-6209, lire en ligne)
- (en) E. Schwenk, D. Papa et al., « γ-n-Propylbutyrolactone and β-(Tetrahydrofuryl)propionic acid », Org. Synth., vol. 27, , p. 68 (ISSN 0078-6209, lire en ligne)
- (en) D. Enders, R. Pieter et al., « Nucleophilic α-sec-aminoalkylation: 2-(diphenylhydroxymethyl)pyrrolidene », Org. Synth., vol. 58, , p. 113 (ISSN 0078-6209, lire en ligne)
- (en) R. G. Rice et E. J. Kohn, « N,N'-Diethylbenzidene », Org. Synth., vol. 36, , p. 21 (ISSN 0078-6209, lire en ligne)
- (en) T. W. G. Solomons et C. B. Fryhle, Organic Chemistry, John Wiley & Sons, , 8e éd., 1344 p. (ISBN 0-471-41799-8 et 9780471417996, présentation en ligne)
- (en) P. G. Gassman et T. J. van Bergen, « Indoles from anilines: Ethyl 2-methylindole-5-carboxylate », Org. Synth., vol. 56, , p. 72 (ISSN 0078-6209, lire en ligne)
- (en) Electronic Space Products International (1994). Nickel aluminide MSDS. Last retrieved January 25, 2006.
Annexes[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- Préparation du nickel de Raney
- (en) R. Monzingo, « Catalyst, Raney-Nickel, W-2 », Org. Synth., vol. 21, , p. 15 (ISSN 0078-6209, lire en ligne)
- (en) H. R. Billica et H. Adkins, « Catalyst, Raney-Nickel, W-6 », Org. Synth., vol. 29, , p. 24 (ISSN 0078-6209, lire en ligne)
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- Notices dans des dictionnaires ou encyclopédies généralistes :
- (en) IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, vol. 49 : Chromium, Nickel and Welding, IARC, , 677 p. (lire en ligne), « Nickel and Nickel Compounds », p. 257-455
- (en) « Grace Davison - Nickel de Raney », sur www.graceraney.com




