Aldéhyde cinnamique
| Aldéhyde cinnamique | ||
| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | (E)-3-phénylprop-2-ènal | |
| Synonymes |
Aldéhyde cinnamique |
|
| No CAS | ||
| No ECHA | 100.111.079 | |
| No CE | 203-213-9 | |
| No RTECS | GD6475000 | |
| FEMA | 2286 | |
| SMILES | ||
| Apparence | liquide visqueux jaunâtre | |
| Propriétés chimiques | ||
| Formule | C9H8O [Isomères] |
|
| Masse molaire[2] | 132,159 2 ± 0,008 1 g/mol C 81,79 %, H 6,1 %, O 12,11 %, |
|
| pKa | 0,3 | |
| Moment dipolaire | 3,62 D [1] | |
| Diamètre moléculaire | 0,629 nm [1] | |
| Propriétés physiques | ||
| T° fusion | −7,5 °C sous 1 bar | |
| T° ébullition | 248 °C[3],[4] | |
| Solubilité | légèrement soluble dans l'eau: 1,1 g·l−1 (20 °C) soluble dans l'éthanol, l'éther et le chloroforme |
|
| Paramètre de solubilité δ | 24,1 J1/2·cm-3/2 (25 °C)[1] | |
| Masse volumique | 1,05 (20 °C) | |
| Point d’éclair | −3,15 °C | |
| Pression de vapeur saturante | 141 hPa (20 °C) | |
| Précautions | ||
| SGH[5] | ||
| H312, H315, H317 et H319 |
||
| SIMDUT[6] | ||
Produit non classé |
||
| NFPA 704 | ||
| Composés apparentés | ||
| Autres anions | CH3COOH CCl3COOH |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
L'aldéhyde cinnamique, cinnamaldéhyde (plus précisément trans-cinnamaldéhyde) ou 3-phénylpropénal est un composé organique de la famille des phénylpropanoïdes, de formule C9H8O. C’est un exemple d’aldéhyde parfumé.
Il est le composant principal (90 %) de l'essence de cannelle et se trouve à l'état naturel dans le tronc du cannelier de Ceylan, du camphrier et du cannelier de Chine (Casse).
Il est obtenu par synthèse à partir du benzaldéhyde C6H5CHO et d'acétaldéhyde CH3CHO ou par réduction de l'acide cinnamique.
Propriétés physiques et chimiques[modifier | modifier le code]
C'est un liquide jaune, plus visqueux que l'eau, à forte odeur de cannelle[7]. Lorsqu'il est concentré, il irrite la peau et peut s'avérer toxique s'il est présent en grandes quantités, mais il ne semble pas cancérogène. La plus grande partie du cinnamaldéhyde est excrété par les urines comme acide cinnamique, une forme oxydée du cinnamaldéhyde. De plus, il ne peut pas être extrait directement.
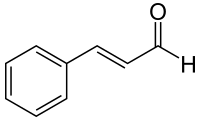
Comme il se présente à la fois comme hydrocarbure aromatique et aldéhyde, le cinnamaldéhyde possède un cycle benzènique monosubstitué. Il a une structure plane en raison d'une double liaison conjuguée (alcène). Comme le groupe carbonyle qui se situe à l'extrémité est de l'autre côté du cycle aromatique au-dessus de la double liaison rigide, le cinnamaldéhyde est en fait en position trans.
En 1884, Jean-Baptiste Dumas et Eugène Péligot publiaient un document sur la synthèse du cinnamaldéhyde. On connait de nos jours plusieurs méthodes de synthèse, mais la moins onéreuse pour produire ce produit est la distillation sous vapeur de l'essence d'écorce de cannelle. Le produit est obtenu à partir de l'alcool de cinnamaldéhyde, les premières synthèses étant faites à partir de la condensation aldolique de benzaldéhyde et d'acétaldéhyde.
Par l'action du permanganate de potassium ou de l'ozone, le cinnamaldéhyde s'oxyde en acide benzoïque.
Utilisations[modifier | modifier le code]
Le cinnamaldéhyde est utilisé dans les domaines suivants :
- Alimentation : antimicrobien[8], arôme pour chewing-gum, crèmes glacées, bonbons et boissons diverses ;
- Parfumerie : principal odorant des parfums à senteur fruitée ou orientale : amandes, abricot, caramel au beurre ;
- Agriculture : appliqué à la racine des plantes, le cinnamaldéhyde s'est montré un fongicide efficace et d'un emploi sans danger dans les récoltes agricoles. Il est aussi utilisé comme insecticide et son odeur éloigne les animaux comme chats et chiens ;
- Industrie : le cinnamaldéhyde empêche la corrosion de l'acier et d'autres alliages à base de fer soumis à l'action des fluides corrosifs.
Dérivés[modifier | modifier le code]
- Bien que n'entrant pas dans la composition de la substance naturelle, l'α-amyl-cinnamaldéhyde a une bonne odeur de jasmin[9] ;
- L'hydrocinnamaldéhyde a une lourde odeur de jacinthe[9].
Liens externes[modifier | modifier le code]
- (en) video sur la condensation aldol du cinnamaldéhyde: http://jchemed.chem.wisc.edu/JCEsoft/CCA/CCA5/MAIN/1ORGANIC/ORG12/TRAM12/F/0410121/MOVIE.HTM
- (en) emploi cinnamaldéhyde comme pesticide: http://www.epa.gov/pesticides/biopesticides/ingredients/factsheets/factsheet_040506.htm
- Fiche sécurité Baker Fischer
Références[modifier | modifier le code]
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, , 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Cinnamaldehyde », sur NIST
- (en) « Cinnamaldehyde », sur NCBI
- Fiche de sécurité établie par Sigma-Aldrich, consultée le 27 octobre 2020
- « Cinnamaldéhyde » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- « aldéhyde cinnamique », sur vitrinelinguistique.oqlf.gouv.qc.ca (consulté le )
- « Cinnamique — acadpharm », sur dictionnaire.acadpharm.org (consulté le )
- John Emsley, Guide des produits chimiques à l'usage du particulier, Paris, Odile Jacob, , 336 p. (ISBN 2-7381-0384-7), p. 17
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « cinnamaldehyde » (voir la liste des auteurs).


