Limonène
| Limonène | |
  |
|
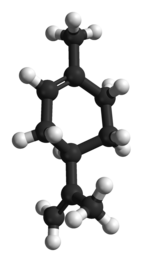
| Structure du R-limonène. | |
| Identification | |
|---|---|
| Nom UICPA | 1-méthyl-4-prop-1-èn-2-yl-cyclohexène |
| No CAS | (R) (S)(–) (RS) |
| No ECHA | 100.004.856 |
| No CE | 227-813-5 (R) 227-815-6 (–) |
| PubChem | |
| FEMA | 2633 |
| Apparence | liquide incolore, d'odeur caractéristique (d-limonène)[1] |
| Propriétés chimiques | |
| Formule | C10H16 [Isomères] |
| Masse molaire[2] | 136,234 ± 0,009 1 g/mol C 88,16 %, H 11,84 %, |
| Propriétés physiques | |
| T° fusion | −75 °C (d-limonène)[1] |
| T° ébullition | 176 °C (d-limonène)[1] |
| Solubilité | dans l'eau : nulle (d-limonène)[1] |
| Masse volumique | 0,84 g cm−3 (d-limonène)[1] |
| T° d'auto-inflammation | 255 °C[réf. souhaitée] |
| Point d’éclair | 48 °C (d-limonène)[1] |
| Limites d’explosivité dans l’air | 0,7–6,1 %vol[réf. souhaitée] |
| Pression de vapeur saturante | à 14,4 °C : 0,4 kPa (d-limonène)[1] |
| Thermochimie | |
| Cp | |
| Propriétés optiques | |
| Pouvoir rotatoire |
+106° dm−1 ml g−1
−106° dm−1 ml g−1 (dans l'éthanol)[réf. souhaitée] |
| Précautions | |
| SGH[5] | |
| H226, H315, H317, H410, P210, P233, P241, P242, P243, P264, P272, P273, P280, P331, P362, P391, P301+P310, P303+P361+P353, P333+P313, P370+P378, P405, P403+P235 et P501 |
|
| SIMDUT[6],[7],[8] | |
Limonène  B3, D2B, Limonène (d-)   B3, D2B, Limonène (l-)   B3, D2B, |
|
| NFPA 704 | |
| Classification du CIRC | |
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[4] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le limonène, LIM, de formule brute C10H16, est un hydrocarbure terpénique présent dans de nombreuses huiles essentielles à partir desquelles il peut être obtenu par distillation. À température ambiante, c'est un liquide incolore à odeur brillante, fraîche et propre d'orange, caractéristique des agrumes.
Le limonène est utilisé comme solvant dans les produits de nettoyage, la fabrication de produits alimentaires, la parfumerie et les produits d'hygiène, ainsi que comme insecticide.
Le limonène tire son nom du citron qui, comme les autres agrumes, contient des quantités considérables de ce composé chimique, responsable en grande partie de leur parfum.
Le limonène est une molécule chirale, et, comme pour de nombreuses molécules chirales, les sources biologiques produisent un énantiomère spécifique. La principale source industrielle, l'orange, contient du d-limonène ((+)-limonène), qui est l'énantiomère R dextrogyre[9]. L'eucalyptus et la menthe poivrée, quant à eux, contiennent du l-limonène ((–)-limonène), qui est l'énantiomère S lévogyre[10],[11]. Le limonène racémique est connu en tant que « dipentène »[12].
Le limonène peut favoriser la cicatrisation des plaies et l'anabolisme, tout en améliorant le stress, la dépression, l'inflammation, le stress oxydatif, les spasmes et les infections virales.
En outre, il présente une variété de propriétés anticancéreuses[13],[14],[15].
Utilisations[modifier | modifier le code]
Comme l'odeur principale qui constitue les agrumes (famille des Rutaceae), le D-limonène est utilisé dans l'industrie agroalimentaire ainsi que dans l'industrie pharmaceutique pour parfumer les médicaments, notamment les alcaloïdes amers. Il est également utilisé dans les produits nettoyants pour son odeur rafraîchissante orange-citron et son effet dissolvant.
Ainsi, le limonène est également de plus en plus utilisé comme solvant, notamment le dégraissage des machines, puisqu'il est produit depuis une source renouvelable, l'huile de citrus, comme un sous-produit de la fabrication de jus d'orange.
Le limonène fonctionne comme solvant à peinture lorsqu'elle est appliquée sur du bois.
L'énantiomère R est également utilisé comme insecticide et a des propriétés répulsive sur de nombreux insectes comme les aleurodes[16],[17].
L'énantiomère S (ou L-limonène) a une odeur plus proche du pin et de la térébenthine.
L'utilisation du limonène est très fréquente dans les produits cosmétiques.
Chimie[modifier | modifier le code]
Le limonène est un terpène relativement stable, qui peut être distillé sans décomposition, et forme de l'isoprène lorsqu'on le fait passer sur un filament de métal chaud. Il est facilement oxydé en environnement humide en carvéol et en carvone[18]. L'oxydation à l'aide du soufre produit du p-cymène et un sulfure.
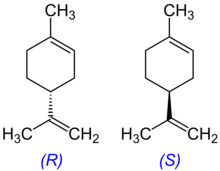
Le limonène existe naturellement comme (R)-énantiomère, mais peut être racémisé en dipentène, en le chauffant simplement à 300 °C. Lorsqu'il est chauffé avec un acide minéral, le limonène forme un diène conjugué, l'α-terpinène, qui s'oxyde facilement en p-cymène, un hydrocarbure aromatique. La preuve est en la formation d'α-terpinène résultant d'une réaction de Diels-Alder lorsque le limonène est chauffé avec de l'anhydride maléique.
Il est possible d'effectuer la réaction sur l'une des deux liaisons sélectivement. Le chlorure d'hydrogène anhydre réagit préférentiellement sur l'alcène disubstitué, alors que l'époxydation avec l'acide métachloroperbenzoïque (MCPBA) se fait sur l'alcène trisubstitué. Dans les deux cas, il est également possible de faire réagir l'autre double liaison.
Dans une autre méthode synthétique, l'addition Markovnikov d'acide trifluoroacétique suivie de l'hydrolyse de l'acétate donne du terpinéol.
Biosynthèse[modifier | modifier le code]
Le limonène est formé à partir de géranyl-pyrophosphate, via une cyclisation d'un néryle carbocation ou son équivalent, comme montré ci-dessous[19]. L'ultime étape inclut la perte d'un proton par le cation pour former l'alcène.

Sécurité / Santé[modifier | modifier le code]
Le limonène et ses produits d'oxydation en grande concentration sont irritants pour la peau. Le 1,2-dihydroxylimonène (formé par simple oxydation à l'air) est connu comme sensibilisant cutané.
La plupart des cas d'irritation ont été signalés chez des personnes exposées à long terme en milieu industriel au composé pur (par exemple, lors d'opération de dégraissage avant mise en peinture).
Toutefois une étude de patients présentant des dermatites a montré que 3 % d'entre eux avaient été sensibilisés par du limonène[20].
Bien qu'on ait un moment pensé qu'il pouvait être la cause de cancers du rein chez le rat, le limonène est aujourd'hui connu comme étant un agent anticancéreux[21] avec une valeur potentielle comme outil anticancéreux diététique chez les humains[22].
Il n'a pas été prouvé que ce produit soit cancérigène ou génotoxique pour l'être humain.
Le Centre international de recherche sur le cancer (CIRC) a classé le d-limonène au niveau 3 : « non classable comme cancérigène chez l'homme »[20].
Notes et références[modifier | modifier le code]
- D - LIMONENE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 3, Huston, Texas, Gulf Publishing Company, , 396 p. (ISBN 0-88415-859-4).
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Évaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur monographs.iarc.fr, CIRC, (consulté le ).
- Fiche Sigma-Aldrich du composé (R)-(+)-Limonene, consultée le 10 août 2020.
- « Limonène » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- « Limonène (d-) » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009.
- « Limonène (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- Numéro CAS , numéro EINECS 227-813-5.
- CAS et EINECS 227-815-6.
- (en) Günther Ohloff, Wilhelm Pickenhagen et Philip Kraft, Scent and chemistry : the molecular world of odors, Verlag Helvetica Chimica Acta, , 418 p. (ISBN 978-3-906390-66-6, OCLC 941919577, lire en ligne), p. 222.
- (en) J. L. Simonsen, The Terpenes, vol. I, 2e éd., Cambridge University Press, 1947.
- Joy J. Chebet, John E. Ehiri, Deborah Jean McClelland et Douglas Taren, « Effect of d-limonene and its derivatives on breast cancer in human trials: a scoping review and narrative synthesis », BMC Cancer, vol. 21, no 1, , p. 902 (ISSN 1471-2407, PMID 34362338, PMCID 8349000, DOI 10.1186/s12885-021-08639-1, lire en ligne, consulté le )
- Juliana de Vasconcelos C Braz, Fernanda O. de Carvalho, Daniele de Vasconcelos C Meneses et Fernanda A. F. Calixto, « Mechanism of Action of Limonene in Tumor Cells: A Systematic Review and Meta-Analysis », Current Pharmaceutical Design, vol. 27, no 26, , p. 2956–2965 (ISSN 1873-4286, PMID 33106139, DOI 10.2174/1381612826666201026152902, lire en ligne, consulté le )
- Heitor Gomes de Araújo-Filho, Jucilene F. Dos Santos, Mikaella T. B. Carvalho et Laurent Picot, « Anticancer activity of limonene: A systematic review of target signaling pathways », Phytotherapy Research: PTR, vol. 35, no 9, , p. 4957–4970 (ISSN 1099-1573, PMID 33864293, DOI 10.1002/ptr.7125, lire en ligne, consulté le )
- Deletre, « Naturally occurring bioactive compounds from four repellent essential oils against Bemisia tabaci whiteflies », Pest Management Science, , p. 72 (1), 179-189.
- Tu, H. et Qin, Y., « Repellent effects of different celery varieties in Bemisia tabaci (Hemiptera: Aleyrodidae) biotype Q. », Journal of Economic Entomology, , p. 110 (3), 1307-1316.
- European Chemicals Bureau.[source insuffisante]
- J. Mann, R. S. Davidson, J. B. Hobbs, D. V. Banthorpe et J. B. Harborne, Natural Products, p. 308-309, Addison Wesley Longman, Harlow, UK, 1994 (ISBN 0-582-06009-5).
- IARC Monographs on the evaluation of carcinogenic risks to humans [PDF], 1999, 73, 307-27.
- Crowell Pl., Prevention and therapy of cancer by dietary monoterpenes, J. Nutr., mars 1999, 129(3):775S-778S, .
- Tsuda H., Ohshima Y., Nomoto H., Fujita K., Matsuda E., Iigo M., Takasuka N. et Moore M.A., Cancer prevention by natural compounds, Drug Metab. Pharmacokinet, aout 2004, 19 (4), 245-63, .
Sources[modifier | modifier le code]
- E. E. Turner et M. M. Harris, Organic Chemistry, Longmans, Green & Co., Londres, 1952.
- Wallach, Annalen der Chemie, 246, 221, 1888.
- Blumann et Zeitschel, Berichte, 47, 2623, 1914.
- CSST Workplace Hazardous Materials Information System.
- M. Matura et al., J. Am. Acad. Dermatol., 2002, 33, 126-27.
Annexes[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- (en) Description sur le site de Biochem Corp.
- Fiche sécurité internationale CDC.








