Ostéogenèse imparfaite
| Spécialité | Génétique médicale |
|---|
| CIM-10 | Q78.0 |
|---|---|
| CIM-9 | 756.51 |
| OMIM | 166200 |
| DiseasesDB | 9342 |
| MedlinePlus | 001573 |
| eMedicine | ped/1674 |
| MeSH | D010013 |
| Patient UK | Osteogenesis-imperfecta |
L’ostéogenèse imparfaite, appelée aussi « maladie des os de verre », est un groupe de maladies caractérisées par une fragilité osseuse excessive, due à un défaut congénital d’élaboration des fibres collagènes du tissu conjonctif qui forme la trame de l’os. Tous les types se caractérisent par une extrême fragilité des os, signe le plus typique de la maladie. Cependant, tous les tissus contenant du collagène sont aussi touchés (os, peau, tendon). La plupart du temps cette maladie est due à une mutation génétique spontanée de novo mais elle peut aussi être familiale et transmise par seulement l’un des deux parents (transmission autosomique dominante).
Il existe six types d’ostéogenèse imparfaite.
Cause de la fragilité des os, le collagène, qui compose 25 % de la matrice osseuse (le reste est composé surtout de calcium et de phosphore), est soit synthétisé en moindre quantité (type 1) ou bien il s'agit d'un collagène anormal qui est synthétisé (les autres types). Le tissu osseux devient alors plus fragile. La matrice osseuse est synthétisée par des cellules appelées « ostéoblastes ».
Le collagène est aussi présent dans la peau, les ligaments, la sclérotique de l’œil (blanc de l’œil) et la dentine ce qui donne des manifestations cliniques très variées. Ces manifestations peuvent aller d’une simple coloration bleue de la sclérotique jusqu’à une forme létale à la naissance en passant par des formes sévères entrainant un handicap profond chez la personne atteinte. La conséquence la plus connue de l'ostéogenèse imparfaite est la survenue de fractures multiples sans traumatisme majeur. Chez certaines personnes (type III, IVB) les dents deviennent translucides et fragiles. Des troubles de l’audition (otospongiose) sont aussi possibles. La plupart du temps, la personne atteinte est de très petite taille et sa vie est constamment émaillée d’hospitalisations et de rééducation.
Autres termes de la maladie[modifier | modifier le code]
En gras les termes les plus employés mais le terme « ostéogenèse imparfaite » devrait être le seul utilisé[réf. souhaitée] :
- maladie des yeux bleus ;
- maladie des os de verre ;
- fragilité osseuse congénitale (1959) ;
- fragilité osseuse héréditaire (1959) ;
- hommes de verre (1928) ;
- triade de van der Hoeve (1918) ;
- dysplasie périostale de Durante (1905) ;
- maladie Porak et Durante (1894) ;
- pseudorachitismus (1891) ;
- maladie de Vrölik (1849) ;
- osteogenesis imperfecta (1849) ;
- maladie de Lobstein (1833) ;
- ostéopsathyrose idiopathique (1829) ;
- Rachitis congenita (1822).
Causes[modifier | modifier le code]
La plupart du temps il s’agit d’anomalies du gène COL1A1 du chromosome 17 ou du gène COL1A2 du chromosome 7. Ces gènes codent les chaînes alpha 1 et alpha 2 du collagène de type I et la maladie est de transmission autosomique dominante[1]. Ces anomalies sont très nombreuses et varient d’une famille à l’autre. Il existe certains cas où l’anomalie ne se trouve pas sur le COL1A1 ni sur le COL1A2. La transmission est alors de type autosomique récessive[2].
Physiopathologie[modifier | modifier le code]
Il existe une fragilité osseuse, avec déformation et déficit de croissance. Des anomalies de la microstructure osseuses sont retrouvées avec une densité minérale abaissée, une augmentation de l'espace inter-trabéculaire[3] et un amincissement de la corticale[4].
Incidence[modifier | modifier le code]
L’incidence est entre 1 pour 10 000 et 1 pour 20 000 naissances[5]. Cette maladie touche indifféremment les deux sexes, sans distribution géographique particulière observée. La maladie se révèle à un âge variable selon la gravité (durant la vie intra-utérine pour les formes sévères, à l’âge adulte pour les formes les moins graves). Le plus souvent on voit apparaître les premières fractures lors de l’apprentissage de la marche.
Manifestations cliniques[modifier | modifier le code]
Ancienne classification[modifier | modifier le code]
On classe l'ostéogenèse imparfaite en 4 types selon la gravité de la maladie :
Type 1[modifier | modifier le code]
- Forme dite modérée
- Sclérotique bleue
- Perte de l’audition dans 40 % des cas
- Fractures fréquentes des membres supérieurs et inférieurs, mains et pieds et déformation limite qui apparaissent après la naissance
- Taille proche de la normale
- Dentinogénèse imparfaite dans le type IA
- Dominant autosomique
Type 2[modifier | modifier le code]
- Forme grave, létale (mortelle)
- Par mutation de novo
- Sclérotique bleue
- Fracture de côtes responsable du décès par insuffisance respiratoire très rapidement après la naissance.
Type 3[modifier | modifier le code]
- La forme la plus sévère non létale
- Transmission dominante ou récessive autosomique
- Visage triangulaire
- Sclérotiques de couleurs variables
- Dentinogenèse imparfaite possible
- Fractures importantes qui surviennent assez souvent avant la naissance avec déformation de la colonne vertébrale et réduction de taille (ces fractures ne sont visibles que lors d'échographies pratiquées avant la naissance)
Type 4[modifier | modifier le code]
- Gravité intermédiaire entre le type I et le type III.
- Groupe hétérogène rassemblant les cas non classés dans les trois premiers cas
- Transmission dominante autosomique
- Dentinogenèse imparfaite possible.
- Déformations des os longs du crâne et des vertèbres.
- Sclérotique blanche
Nouvelle classification[modifier | modifier le code]
| Nom | Transmission | Sévérité | Fractures | Déformation | Taille | Trouble de la dentition | Sclérotique | Surdité |
|---|---|---|---|---|---|---|---|---|
| I | Dominante | Moyenne | De quelques à 100 | Rare | Normale à peu réduite | Rare | Bleue | 1 fois sur 2 |
| II | Dominante | Létale à la naissance | Multiples | Sévère | Réduite | Oui | Bleu foncé | Non |
| III | Dominante Rarement récessive |
Grave | Très fréquentes | Petite taille | Réduite | Oui | Bleue | Fréquente |
| IV | Dominante | Légère à moyenne | Multiples | Fréquent mais léger | Normale ou réduite | Plus ou moins | Normale ou grise | Rare |
| V | Dominante | Moyenne | Multiples avec cal hypertrophique | Modérées | Variable | Non | Normale | Non |
| VI | Incertaine | Modérée | Multiples | Nanisme rhizomélique | Moyenne | Non | Normale | Non |
| VII | Récessive | Modérée | Multiples | Oui | Moyenne | Non | Normale | Non |
Diagnostic[modifier | modifier le code]
Lorsque le diagnostic n’est pas effectué avant la naissance au moyen d’une échographie pour les types les plus graves (II et III), il repose surtout sur l’observation de manifestations cliniques décrites ci-dessus et de données radiologiques (ostéoporose et présence d’os wormiens sur les os du crâne).
Enfin l’ostéodensitométrie peut permettre de quantifier la perte de masse osseuse mais n'est pas indispensable au diagnostic. Elle ne modifiera pas la prise en charge du malade. La réalisation de cet examen n'est donc que facultative.
Les aspects radiographiques de l'os contribuent au diagnostic.
Diagnostic échographique anténatal[modifier | modifier le code]
L’échographie prescrite est une échographie de « seconde intention » c'est-à-dire qui va permettre de diagnostiquer les éventuelles malformations. Elle fait suite à la découverte, à la suite de la reconstitution de l’anamnèse, d’un risque élevé d’anomalie morphologique fœtale. L’objectif majeur de l’échographie est alors d’infirmer ou de confirmer la réalité d’une pathologie fœtale. Les signes échographiques de cette maladie sont[6] :
- un retard de croissance intra-utérin (évalué par la longueur fémorale) ;
- une hydramnios (quantité trop importante de liquide amniotique) ;
- des anomalies du pôle céphalique :
- hydrocéphalie (augmentation du volume de la tête),
- macrocéphalie (augmentation par 3 du périmètre crânien par rapport à la normale),
- déformation céphalique spontanée ou provoquée par la pression de la sonde,
- amincissement et faible échogénicité de la voûte osseuse,
- déflexion céphalique maximale,
- des anomalies thoraciques :
- thorax petit et étroit,
- hypoéchogénicité osseuse (diminution de l’ombre acoustique des côtes),
- fractures et cals osseux,
- des anomalies des membres :
- nanisme,
- fractures et cals osseux,
- déformation marquée des membres sans aucune symétrie,
- hypoéchogénicité osseuse (diminution de l’ombre acoustique des os longs).
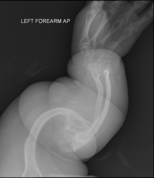
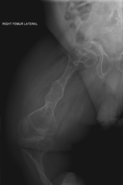
Diagnostic radiologique[modifier | modifier le code]
On observe une transparence excessive des os ainsi que des déformations sur les clichés radiologiques[7]. Ces déformations sont principalement constatées au niveau de :
- la partie diaphysaire de l’os : une corticale diaphysaire mince, une crosse au niveau des os longs ainsi que la présence de plusieurs cals osseux ;
- la hanche avec une protrusion acétabulaire c'est-à-dire une malformation associant une hanche trop profonde et des amplitudes articulaires diminuées ;
- des pieds avec des pieds plats et en valgus c'est-à-dire les membres qui s’écartent vers l’extérieur par rapport à l’axe du corps ;
- des membres supérieurs avec une déformation supérieur à 30° ;
- du crâne avec des os wormiens c'est-à-dire des petits os situés à l'intérieur de divers os constituant le crâne (occiput, pariétal, temporal…) présents en nombre plus important que la normale ;
- du rachis et du thorax avec un thorax plus bombé que la normal et des modifications au niveau des vertèbres telles que des tassements de certaines vertèbres, des vertèbres biconcaves, des scolioses… Lors de fractures, le siège se situe principalement au niveau des membres inférieurs et des vertèbres.
Diagnostic clinique[modifier | modifier le code]
Sclérotiques bleutées[modifier | modifier le code]
La sclérotique est l'enveloppe blanche et opaque de l’œil. Elle est constituée d'un tissu fibreux solide qui entoure le globe oculaire. Elle contient des vaisseaux sanguins fins. Lorsque l'œil est irrité, les vaisseaux sanguins vont se dilater : c’est ce qui est responsable de la couleur rosée ou rouge de l’œil. Les patients atteints de la maladie des os de verre présentent des sclérotiques bleutées.
Dentinogénèse imparfaite[modifier | modifier le code]
La dentinogénèse imparfaite est une pathologie qui se caractérise par une anomalie de la structure dentaire. Elle peut être présente sur les deux dentures, de façon simplement temporaire ou définitive. Les patients atteints de la maladie des os de verre souffrent souvent (entre 50 et 80 % des malades) de dentinogénèse imparfaite de type I[8], c'est-à-dire que les deux dentures sont touchées mais à différents degrés. En effet, on remarque que la denture temporaire est, dans de nombreux cas, plus touchée que la denture permanente. Cette situation pourrait s’expliquer par une édification plus rapide des dents de lait et une expression du défaut moléculaire plus importante pendant la période fœtale. De plus, on observe entre autres une anomalie au niveau de l’émail des dents : celui-ci s’écaille. Les dents sont également translucides et la coloration va varier du bleu gris au brun foncé. De plus, on peut remarquer l’usure prématurée des dents, la diminution de leurs hauteurs… Les patients doivent donc effectuer un panoramique dentaire à l’âge de 6 ans, puis de faire un bilan orthodontique tous les ans. Il faut ajouter à ceci, la bonne hygiène dentaire en passant par le port de gouttières ou de laque fluorée systématiquement.
Surdité[modifier | modifier le code]
Elle touche plus de la moitié des malades. Ces derniers ont des problèmes de surdité de perception mais aussi de transmission ou encore les deux. Ainsi, les patients doivent effectuer obligatoirement un audiogramme à l’âge de 10 ans et ensuite tous les 3 à 5 ans.
Diagnostic génétique[modifier | modifier le code]
La grande majorité des patients souffrant de la maladie des os de verre présentent une mutation affectant le collagène 1. Comme la séquence des acides nucléiques des exons du COL1A1 et du COL1A2 est connue, il est possible d’effectuer un diagnostic prénatal. Cependant, ce dernier n’est pas réalisé systématiquement. En effet, il est indiqué pour des personnes présentant un risque plus élevé de contracter la maladie et qui souhaitent vérifier au plus vite si leur enfant sera atteint de cette pathologie ou non. Les personnes qui peuvent présenter des risques de transmission de la maladie des os de verre sont :
- un couple dont l’un des deux (voire les deux) membres du couple est (sont) atteint(s) de cette maladie ;
- un couple, sans antécédent familial recensé, ayant déjà eu un enfant atteint d’ostéogenèse imparfaite et souhaitant avoir d’autres enfants ;
- un des ascendants ou membre de la famille de l’un des membres du couple est atteint.
Concernant l’éducation thérapeutique du couple, les médecins doivent l’informer de la possibilité d’un diagnostic précoce pour laisser la possibilité aux futurs parents de décider. Il n’est pas possible d’imposer cet examen à la famille.
Différentiel[modifier | modifier le code]
Il s’agit ici d’une maladie rare qui peut donc être facilement confondue avec d’autres.
Le principal problème du diagnostic différentiel est de distinguer l'ostéogenèse imparfaite du syndrome des enfants battus (ou syndrome de Silverman) beaucoup plus fréquent que l’ostéogenèse imparfaite. Ce problème se pose dans l’enfance pour des enfants présentant des fractures des os longs, de la colonne vertébrale et des hématomes. Malheureusement il n’est pas possible de compter sur la présence ou non de sclérotiques bleues car ce symptôme n’est pas présent dans tous les cas. Il est nécessaire pour le praticien d’être très prudent car un mauvais diagnostic peut engendrer des conséquences psychologiques catastrophiques pour l’enfant et la famille. En cas de doute, il est conseillé d’avoir recours à des examens complémentaires et de faire appel à un spécialiste.
Au cours de la grossesse si l’on observe des fémurs incurvés sans fractures il faut faire la différence avec d’autres maladies osseuses telles que la dysplasie campomélique, syndrome de Stüve et Wiedemann…
À la naissance, on peut confondre l’ostéogenèse imparfaite avec l’hyperparathyroïdie, l’I-cell disease (en) (mucolipidose de type II) et la dysplasie avec gracilité des os.
À l’âge adolescent ou adulte jeune l’ostéogénèse imparfaite peut être confondue avec des leucémies ou maladies de système (qui touchent plusieurs organes vitaux).
Aspects génétiques : dépistage et transmission[modifier | modifier le code]
Dans la majorité des cas la transmission est de type autosomique dominante ce qui signifie qu’un parent atteint de cette maladie a une chance sur deux d’avoir des enfants atteints à leur tour avec à peu près la même sévérité. C’est pourquoi il est important pour les personnes concernées de rencontrer un médecin généticien qui pourra leur donner les informations adaptées à leur cas et éventuellement procéder à des tests génétiques. Il est important de noter ici que les tests génétiques ne sont pas toujours concluants au vu du nombre d’anomalies possibles conduisant à l’ostéogénèse imparfaite.
Traitement et prise en charge[modifier | modifier le code]
Traitement médicamenteux[modifier | modifier le code]
Les biphosphonates permettent une amélioration de la solidité osseuse et un meilleur contrôle de la douleur[9]. Les premiers résultats utilisent la voie intraveineuse et montrent que ce traitement est plutôt bien toléré, en dehors de la fièvre lors de la première cure et du risque d’hypocalcémie qui peut être prévenu par l’administration de vitamine D et de calcium. L'arrivée des biphosphonates par voie orale facilite leur prise, mais avec une efficacité moindre du moins pour l'alendronate (taux de fractures équivalents)[10]. Le risédronate, autre biphosphonate per os, diminue le nombre de fractures[11]. Cependant il est important ici de bien évaluer la balance bénéfice/risque lors de la prescription d’une telle thérapeutique car il a également été constaté qu’en cas de mauvaise surveillance du traitement et de mauvais dosage il existe également un risque d’ostéosclérose (densification de l’os) et de déformations osseuses toutes aussi importantes que la maladie elle-même. Enfin, les biphosphonates semblent être à l’origine d’une surcharge pondérale nuisant à la réadaptation des enfants. Toutes ces incertitudes conduisent à ne traiter que les enfants atteints des formes les plus graves par voie veineuse.
Le traitement de la douleur peut être fait par la prescription d’analgésiques.
Une étude de phase I menée par Amgen est en cours aux États-Unis depuis le dans le traitement de la maladie par le romosozumab (evenity), un inhibiteur de sclérotine, pour les enfants et adolescents [12].
Traitement chirurgical[modifier | modifier le code]
Le traitement de la surdité peut se faire via une opération chirurgicale délicate ou un appareillage et doit donc être mûrement réfléchi et bien adapté au cas par cas. En ce qui concerne la dentinogenèse imparfaite, le traitement le plus utilisé est la pose de couronnes sur les dents de laits et d’implants à l’âge adulte. Un traitement chirurgical consistant à enclouer les os longs (fémur, tibia) peut également être proposé pour prévenir les grandes déformations osseuses. Le traitement de cette pathologie est multidisciplinaire puisqu’il est à la fois médical et rééducatif mais il peut être aussi chirurgical. Les fibres de collagène sont en partie responsables de la solidité et de la résistance des os. Dans la majorité des cas de l’ostéogenèse imparfaite, il s’agit d’un problème génétique qui va concerner la fabrication du collagène et donc diminuer la solidité et la résistance des os. De plus, dans cette maladie, l’équilibre entre les cellules qui détruisent l’os (ostéoclastes) et celles qui le fabriquent (ostéoblastes) est rompu. En effet, ce qui est détruit n’est pas remplacé, on a donc une diminution du volume osseux et donc l’apparition de nombreuses fractures. Les os les plus touchés sont en général les os longs comme le fémur et le tibia mais les côtes et les vertèbres sont aussi touchées.
Rééducation et réadaptation[modifier | modifier le code]
Le développement musculaire contribue au développement osseux ; il est donc primordial de s’intéresser à cet aspect. Il faut donc encourager la motricité globale, faciliter toutes les formes de mouvements actifs et encourager l’indépendance[13]. En effet, il est important de toujours mettre en charge le sujet malade c’est-à-dire de le faire bouger de manière à augmenter la charge musculaire et osseuse. Il est donc important de suivre un entraînement à l’effort afin d’éviter le déconditionnement et de pratiquer une activité sportive.
Prise en charge complémentaire[modifier | modifier le code]
Un suivi psychologique de l’enfant et de la famille est conseillé. La prise en charge rééducative est indispensable et permet à la fois aux parents de manipuler sans crainte leur enfant et à celui-ci, d’améliorer sa mobilité articulaire, sa force musculaire et de lutter contre l’immobilité, facteur aggravant de la maladie. La réadaptation fonctionnelle et l’ergothérapie ont pour but de donner à l’enfant une autonomie maximale en fournissant à l’enfant des aides techniques si nécessaire : aides au déplacement, aides à l’écriture.
Conséquences sociales[modifier | modifier le code]
La réadaptation fonctionnelle et l’ergothérapie[modifier | modifier le code]
Des dispositifs peuvent permettre d’augmenter l’autonomie des personnes atteintes gravement par cette maladie comme des dispositifs d’aide aux déplacements tels que les déambulateurs, les cannes, fauteuil roulant. Mais aussi des supports réglables qui permettent une adaptation pour l’écriture comme des tables à hauteur réglable, etc. (en raison de la faiblesse des membres supérieurs qui peuvent apparaître dans la maladie et donc d’une difficulté à écrire). Un point important en termes d’ergothérapie est à viser dans cette maladie.
Scolarisation[modifier | modifier le code]
En France, la plupart des enfants atteints d'ostéogenèse imparfaite peuvent être accueillis dans les structures habituelles de l'Éducation nationale où ils suivent une scolarité normale. Certains enfants atteints d'ostéogenèse imparfaite peuvent présenter une faiblesse des membres supérieurs ce qui affecte leur habilité à écrire ou à dactylographier. D'autres peuvent avoir une endurance limitée en position assise ou encore des douleurs chroniques dans le dos ce qui rend une journée complète à l'école difficile. Certains enfants peuvent avoir besoin d’être accompagnés par un auxiliaire de vie scolaire, d’autres en revanche seront autonomes si certaines petites précautions sont prises. En effet, cette maladie engendre beaucoup de fractures, le point essentiel à prendre en compte est donc d’éviter toutes bousculades. Il est préférable d’intégrer une classe au rez-de-chaussée s'il y a un fauteuil roulant ; d’avoir deux jeux de livres scolaires, un pour l’école, un pour la maison avec l’aménagement d’un coin de récréation avec des jeux calmes et posés afin d’éviter que l’enfant ne tombe et ne se cause des fractures. Afin d’éviter les bousculades, il faudrait prévoir un temps de sortie décalé par rapport aux autres élèves (soit avant, soit après). On peut trouver d’autres conseils sur l’adaptation à l’école de l'enfant sur un site Internet permettant d’aider les enseignants et les établissements sujets à accueillir des enfants handicapés et envisage les adaptations qui peuvent être mises en place pour améliorer au mieux l’accueil d’un enfant atteint de cette pathologie[14].
Les parents peuvent également demander l’établissement d’un PAI (projet d’accueil individualisé) avec l’Éducation nationale qui définira les modalités d’accueil et d’aide dont pourra bénéficier l’enfant.
Vie professionnelle[modifier | modifier le code]
À l’âge adulte, si l’affection empêche la personne atteinte de travailler, celle-ci pourra faire appel à la MDPH (Maison départementale des personnes handicapées) pour obtenir un statut de travailleur handicapé ou des allocations.
Vie familiale[modifier | modifier le code]
Les personnes atteintes peuvent mener une vie familiale et avoir des enfants si elles le désirent. Une femme peut mener une grossesse à terme mais celle-ci peut s’avérer douloureuse et nécessite un suivi particulier.
Évolution vers les nouvelles technologies[modifier | modifier le code]
Surveillance à domicile[modifier | modifier le code]
La surveillance à domicile pourrait être réalisée pour une caméra d’altimétrie qui permettrait d’identifier et de prévenir l’alerte en cas de chute de la personne afin de pouvoir prévenir les secours et de respecter la procédure d’urgence en cas de chute.
Télémédecine[modifier | modifier le code]
À l'heure actuelle, la télémédecine n'est pas très développée dans la prise en charge de l'ostéogénèse imparfaite. Cependant, le 2e plan national pour les maladies rares a vocation d'améliorer et de renforcer la qualité de la prise en charge du patient. En effet, « Le plan prévoit aussi la mise en place d'une Banque nationale de maladies rares ou encore le développement de la télémédecine[15]. » De plus, un dispositif de communication pourrait être mis en place avec le médecin spécialiste dans le but de communiquer avec lui sur la douleur des fractures par exemple afin de pouvoir poser des questions sur le traitement, son augmentation. Mais également sur le suivi de son traitement aux bisphosphonates par exemple, ou les données à risques pourraient être transmise en temps réel au médecin afin qu’il puisse vérifier si les constantes sont correctes ou non.
Évolutions, recherche[modifier | modifier le code]
Des recherches sont actuellement en cours et deux pistes sont notamment explorées :
- la greffe de cellules souches de moelle osseuse ;
- les thérapies géniques mais celles-ci sont rendues complexes car la maladie peut être due à beaucoup d’anomalies différentes.
L'utilisation de la parathormone (teriparatide) pourrait être intéressante chez l'adulte[16].
Grossesse chez une femme porteuse d'une ostéogenèse imparfaite de type 1[modifier | modifier le code]
- Risque de rupture utérine au cours d’un accouchement par voie basse
- Augmentation du risque d’hémorragie de la délivrance
- Augmentation du risque d’hyperthermie maligne au cours d’une anesthésie générale
Culture populaire[modifier | modifier le code]
Personnalités atteintes[modifier | modifier le code]
- Michel Petrucciani (1962-1999), pianiste et compositeur de jazz[17]
- Guillaume Bats (1987-2023), humoriste français[18].
- Leo Beuerman, sujet du documentaire Leo Beuerman, nommé aux Academy Awards du meilleur documentaire.
- McKenzie Coan, nageuse handisport américaine[19]
- Loïc « Toucouille » Dubois, joueur professionnel de League Of Legends[20]
- Elisa Rojas, avocate franco-chilienne au barreau de Paris et militante pour les droits des femmes.
- Rick Howland, acteur canadien
- Gaelynn Lea, chanteuse et violoniste americaine[21]
Films[modifier | modifier le code]
- Dans le film Le Fabuleux Destin d'Amélie Poulain, Raymond Dufayel, voisin d'Amélie, peintre, est atteint de cette maladie.
- Dans les films Incassable et Glass, Elijah Price, le personnage incarné par Samuel L. Jackson, souffre lui aussi de cette maladie.
- Dans la série télévisée Grey's Anatomy, le fœtus du docteur April Kepner est atteint d'ostéogénèse imparfaite de type 2 dans l'épisode 11x08.
- Dans la série télévisée Vikings, Ivar « le Désossé » est atteint de cette maladie.
- L'acteur Américain Atticus Shaffer, qui joue Brick Heck dans la série télévisée The Middle, est atteint d'ostéogénèse imparfaite de type 4. référence
Jeux vidéo[modifier | modifier le code]
- Dans la série Mass Effect, Jeff Moreau, surnommé « Joker », est victime de cette maladie.
Littérature[modifier | modifier le code]
- Tatau, le héros de la bande dessinée Burning Tattoo d'Emmanuel Nhieu, est atteint d'ostéogenèse imparfaite[22].
Notes et références[modifier | modifier le code]
- (en) Cundy T, « Recent advances in osteogenesis imperfecta » Calcif Tissue Int. 2012;90:439–449
- (en) Marini JC, Blissett AR, « New genes in bone development: what’s new in osteogenesis imperfecta » J Clin Endocrinol Metab. 2013;98:3095–3103
- (en) Folkestad L, Hald JD, Hansen S. et al. « Bone geometry, density, and microarchitecture in the distal radius and tibia in adults with osteogenesis imperfecta type I assessed by high-resolution pQCT » J Bone Miner Res. 2012;27:1405–1412
- (en) Gatti D, Colapietro F, Fracassi E. et al. « The volumetric bone density and cortical thickness in adult patients affected by osteogenesis imperfecta » J Clin Densitom. 2003;6:173–177
- (en) Andersen PE, Hauge M, « Osteogenesis imperfecta: a genetic, radiological, and epidemiological study » Clin Genet. 1989;36:250-255
- CNGOF, « Cours (Membres) », sur univ-paris5.fr via Internet Archive (consulté le ).
- « chu-lyon.fr/web/attached_file/… »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?).
- http://dumas.ccsd.cnrs.fr/docs/00/84/45/55/PDF/These-Odontologie-2013-CALVEZ_Marielle-version_expurgee.pdf
- (en) Glorieux FH, Bishop NJ, Plotkin H, Chabot G, Lanoue G, Travers R, « Cyclic administration of pamidronate in children with severe osteogenesis imperfecta » N Engl J Med. 1998;339:947-952
- (en) Ward LM, Rauch F, Whyte MP. et al. « Alendronate for the treatment of pediatric osteogenesis imperfecta: a randomized placebo-controlled study » J Clin Endocrinol Metab. 2011;96:355-364
- (en) Bishop N, Adami S, Ahmed SF. et al. « Risedronate in children with osteogenesis imperfecta: a randomised, double-blind, placebo-controlled trial » Lancet 2013;382:1424-1432
- « Étude pour évaluer le romosozumab chez les enfants et les adolescents atteints d'ostéogenèse imparfaite », sur ichgcp.net,
- http://www.cofemer.fr/UserFiles/File/4%20OI%20format%20cofemer%202012.pdf
- « Integrascol.fr - Pour une meilleure éducation des enfants malades et/ou handicapés », sur Integrascol.fr (consulté le ).
- http://ars.iledefrance.sante.fr/2eme-Plan-National-Maladies-Ra.106043.0.html
- (en) Orwoll ES, Shapiro J, Veith S, « Evaluation of teriparatide treatment in adults with osteogenesis imperfecta » J Clin Invest. 2014;124:491–498
- Michel Petrucciani sur l’encyclopédie universalis
- Yoann Mattei, « L'humour hand'vidéo », sur handimarseille.fr (consulté le )
- (en) « McKenzie Coan », sur IPC (consulté le )
- Paul Arrivé, « Toucouille, os de verre, diamant brut »
 , sur L'Équipe, (consulté le )
, sur L'Équipe, (consulté le )
- Handicap.fr, « G. Lea : son violon, une arme de sensibilisation massive ? », sur Handicap.fr, (consulté le )
- Dumbo, « Chronique BD : Burning Tattoo # 1 », sur Génération BD, (consulté le ).
Voir aussi[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- Ressources relatives à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :
- Association de l'ostéogenèse imparfaite (France)
- Association francophone belge de l'ostéogenèse imparfaite
- Association suisse Osteogenesis Imperfecta (français/allemand)
- OI Foundation (anglais)
- OIFE (Europe) (divers)