Tétroxyde de ruthénium
| Tétroxyde de ruthénium | |
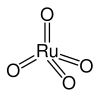 Structure du tétroxyde de ruthénium |
|
| Identification | |
|---|---|
| Nom UICPA | tétraoxoruthénium |
| Synonymes |
tétraoxyde de ruthénium, |
| No CAS | |
| No ECHA | 100.039.815 |
| No CE | 243-813-8 |
| PubChem | 119079 |
| SMILES | |
| InChI | |
| Apparence | aiguilles jaune-orangé à l'odeur piquante |
| Propriétés chimiques | |
| Formule | RuO4 |
| Masse molaire[1] | 165,07 ± 0,02 g/mol O 38,77 %, Ru 61,23 %, |
| Propriétés physiques | |
| T° fusion | 25,4 °C[2] |
| T° ébullition | décomposition à partir de 40 °C[2], totale à 108 °C |
| Solubilité | environ dans l'eau20,3 g·l-1 à 20 °C, 22,4 g·l-1 à 74 °C |
| Masse volumique | 3,29 g·cm-3[3] à 20 °C |
| Cristallographie | |
| Système cristallin | Orthorhombique |
| Précautions | |
| Directive 67/548/EEC[3] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le tétroxyde de ruthénium, ou tétraoxyde de ruthénium, est un (tétra)oxyde de ruthénium, composé chimique moléculaire de formule RuO4. Il se présente sous la forme d'aiguilles solides de couleur jaune-orangé, à l'odeur piquante, qui fondent vers 25,4 °C pour donner un liquide incolore, assez volatile à température et pression ambiante, qui se décompose dès 40 °C en libérant son oxygène et disparaît vers 108 °C pour laisser le dioxyde de ruthénium.
Il s'agit d'un agent oxydant, communément utilisé en chimie. L'un des rares solvants avec lesquels le RuO4 forme une solution stable, est le tétrachlorométhane CCl4. D'où l'association du réactif et du milieu solvant souvent systématique, notée RuO4/CCl4 pour signaler un processus d'oxydation en chimie organique.
Description de la molécule
[modifier | modifier le code]Il s'agit d'une molécule tétraédrique diamagnétique dont les liaisons Ru=O ont une longueur de 169 pm à 170 pm[4]. Le tétroxyde d'osmium OsO4, qui lui est analogue, est mieux connu et davantage utilisé.
Le tétraoxyde de ruthénium est soluble dans l'eau à hauteur de 2,03 g pour 100 g d'eau à 20 °C et de 2,24 g pour 100 g d'eau à 74 °C, mais aussi les acides et les alcalis, l'éthanol et surtout le tétrachlorure de carbone.
Préparation
[modifier | modifier le code]On prépare le tétroxyde de ruthénium par oxydation du chlorure de ruthénium(III) RuCl3 par le periodate de sodium NaIO4 :
Usages en chimie
[modifier | modifier le code]Les réactions qui font intervenir RuO4 comme oxydant utilisent typiquement diverses formes de ruthénium (tels que des hydrates d'oxyde ou de chlorures) comme précurseur du RuO4.
Le tétroxyde de ruthénium oxyde pratiquement n'importe quel hydrocarbure. Il oxyde par exemple l'adamantane en 1-adamantanol. On l'utilise en synthèse organique pour oxyder les alcynes terminaux en 1,2-dicétones et les alcools primaires en acides carboxyliques. Lorsqu'on l'utilise de cette façon, le tétroxyde de ruthénium est employé en quantité catalytique et régénéré par addition de periodate de sodium NaIO4 au chlorure de ruthénium(III) RuCl3 et un mélange de solvants d'acétonitrile CH3CN, d'eau H2O et de tétrachlorométhane CCl4.
RuO4 est un oxydant particulièrement énergique : il faut veiller à ce que les conditions opératoires soient douces, généralement à température ambiante. Les centres stéréogènes qui ne sont pas oxydés sont cependant préservés, comme l'illustre l'oxydation ci-dessous d'un diol en acide carboxylique :

L'oxydation d'alcools époxy conduit également à des acides carboxyliques sans altération du cycle époxy :

Des conditions opératoires plus douces conduisent à des aldéhydes au lieu d'acides carboxyliques. Le RuO4 convertit rapidement les alcools secondaires en cétones. On obtient bien entendu des résultats semblables avec des oxydants meilleur marché à base de PCC ou de DMSO, mais le tétroxyde de ruthénium s'impose dès lors qu'il s'agit d'utiliser un oxydant énergique avec des conditions opératoires douces.
RuO4 clive facilement des doubles liaisons pour donner des produits carbonylés, de façon semblable à une ozonolyse. Le tétroxyde d'osmium, d'emploi plus courant que RuO4, ne clive pas les doubles liaisons mais conduit plutôt à des diols vicinaux.
D'un point de vue pratique, le substrat à oxyder est généralement dissous dans un solvant tel que le tétrachlorométhane CCl4, et de l'acétonitrile CH3CN est ajouté comme ligand pour aider le cycle catalytique. De l'éther éthylique CH3CH2OCH2CH3 peut ensuite être ajouté pour faire précipiter et récupérer le catalyseur au ruthénium.
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- David R. Lide, dans « CRC Handbook of Chemistry and Physics », Taylor & Francis, 90e édition, 2009, Chap. 4, p. 86. (ISBN 978-1-4200-9084-0).
- Entrée « Ruthenium tetraoxide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 8 février 2013 (JavaScript nécessaire)
- (en) Martin Pley et Mathias S. Wickleder, « Two crystalline modifications of RuO4 », Journal of Solid State Chemistry, vol. 178, no 10, , p. 3206-3209 (lire en ligne) DOI 10.1016/j.jssc.2005.07.021


