Butane
| n-butane | |
  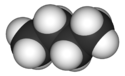 Structure et représentations du n-butane. |
|
| Identification | |
|---|---|
| Nom UICPA | butane |
| Synonymes |
n-butane |
| No CAS | |
| No ECHA | 100.003.136 |
| No CE | 203-448-7 |
| No RTECS | EJ4200000 |
| PubChem | 7843 |
| SMILES | |
| InChI | |
| Apparence | gaz comprimé liquéfié, inodore, incolore[1]. |
| Propriétés chimiques | |
| Formule | C4H10 [Isomères] |
| Masse molaire[2] | 58,122 2 ± 0,003 9 g/mol C 82,66 %, H 17,34 %, |
| Propriétés physiques | |
| T° fusion | −138,29 °C[3] |
| T° ébullition | −0,5 °C[3] |
| Solubilité | 61,2 mg l−1 (eau, 25 °C)[4] |
| Paramètre de solubilité δ | 13,9 MPa1/2 (25 °C)[5] |
| Masse volumique | 601,1 g l−1 (liquide, −0,5 °C) 2,709 g l−1 (gaz, 0 °C, 1 013 mbar)[3] |
| T° d'auto-inflammation | 287 °C[1] |
| Point d’éclair | −60 °C[1] |
| Limites d’explosivité dans l’air | 1,8–8,4 %vol[1] |
| Pression de vapeur saturante | 2,081 bar à 20 °C 2,8 bar à 30 °C 4,9 bar à 50 °C[3] |
| Point critique | 151,85 °C 38,0 bar 0,255 l mol−1[7] |
| Point triple | −138,55 °C 0,007 mbar[7] |
| Vitesse du son | 1 034 m s−1 (liquide, −0,5 °C)[8] |
| Thermochimie | |
| S0liquide, 1 bar | 231 J mol−1 K−1[9] |
| ΔfH0gaz | −125,6 kJ mol−1[10] |
| ΔvapH° | 22,389 kJ mol−1 à −1,1 °C[7] |
| Cp | 132,42 J mol−1 K−1 (liquide,−3,15 °C) 98,49 J mol−1 K−1 (gaz, 25 °C)[7] |
| PCS | 49,4 MJ kg−1[12] |
| PCI | 45,6 MJ kg−1[réf. souhaitée] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 10,53 ± 0,10 eV (gaz)[13] |
| Précautions | |
| SGH[14],[15] | |
| H220 Avec > 0,1 % de butadiène : H220, H340 et H350 |
|
| SIMDUT[16] | |
  A, B1, |
|
| NFPA 704 | |
| Transport[3] | |
| Écotoxicologie | |
| LogP | 2,89[1] |
| Seuil de l’odorat | bas : 1 262 ppm haut : 5 048 ppm[17] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le butane est un hydrocarbure saturé de la famille des alcanes et de formule brute C4H10. Il existe sous deux formes isomères, le n-butane et l'isobutane ou 2-méthylpropane.
Utilisation[modifier | modifier le code]

Le butane est un gaz principalement utilisé comme combustible à usage domestique (gazinière, chauffe-eau) et également d'appoint, notamment pour le chauffage (radiateur à gaz pour l'intérieur des locaux d'habitation, commerces et ateliers ainsi que pour le plein air). Il est généralement conditionné en bouteille de 13 kg[pas clair].
Il est également utilisé comme carburant dans les briquets à gaz.
Pour un usage en extérieur, le propane est plus indiqué en raison de sa température d'ébullition plus basse.
Au niveau industriel, le butane est un réactif pour la synthèse de l'éthylène et du propylène via le vapocraquage, du butadiène au moyen de la déshydrogénation catalytique et de l'anhydride maléique par le procédé de DuPont. L'oxydation non-catalytique du butane est utilisée pour la synthèse de l'acide acétique et l'isomérisation par catalyse acide permet de convertir le n-butane en isobutane[18].
Comme de nombreux hydrocarbures, le butane réagit avec le dichlore pour former du 1-chloro- et du 2-chlorobutane, mais aussi d'autres composés plus substitués. Les taux de chloration peuvent partiellement s'expliquer par les différentes énergies de dissociation des liaisons C-H, respectivement 425 et 411 kJ/mol pour celles des deux carbones termninaux et des deux carbones centraux (qui ont des liaisons C-H plus faibles).
Propriétés physico-chimiques[modifier | modifier le code]
Le butane est soluble dans l'alcool et l'éther, mais peu dans l'eau. Peu réactif, il nécessite un catalyseur pour participer à des réactions chimiques, sauf pour la réaction de combustion avec le dioxygène.
| Température | Pression (kPa) | Température | Pression (kPa) |
|---|---|---|---|
| −103,15 °C | 0,1 | −33,15 °C | 24,1 |
| −98,15 °C | 0,2 | −28,15 °C | 30,9 |
| −93,15 °C | 0,3 | −23,15 °C | 39,1 |
| −88,15 °C | 0,5 | −18,15 °C | 49,1 |
| −83,15 °C | 0,8 | −13,15 °C | 61,0 |
| −78,15 °C | 1,3 | −8,15 °C | 75,0 |
| −73,15 °C | 1,9 | −3,15 °C | 91,5 |
| −68,15 °C | 2,8 | 1,85 °C | 111 |
| −63,15 °C | 4,0 | 6,85 °C | 133 |
| −58,15 °C | 5,7 | 11,85 °C | 159 |
| −53,15 °C | 7,8 | 16,85 °C | 188 |
| −48,15 °C | 10,6 | 21,85 °C | 221 |
| −43,15 °C | 14,1 | 26,85 °C | 258 |
| −38,15 °C | 18,5 | 50 °C | 490[3] |
Son comportement dans la plage de température et de pression usuelles explique son usage commode dans des applications domestiques : à la pression atmosphérique (vers 100 kPa), la phase liquide apparait vers 0 °C, et réciproquement pour le maintenir sous état liquide à 25 °C, il suffit d'une pression d'environ 2,5 atm (aisé à obtenir même avec un réservoir en plastique comme celui d'un briquet).
Ses propriétés en font un fluide frigorigène, dont le code est R600.
Production et synthèse[modifier | modifier le code]
Le n-butane est obtenu par distillation sous pression du gaz de pétrole liquéfié (GPL) ainsi que par la purification du gaz naturel[18].
Notes et références[modifier | modifier le code]
- BUTANE (GAZ LIQUEFIE), Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « n-Butane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 5 octobre 2009 (JavaScript nécessaire).
- « Butane », sur Hazardous Substances Data Bank (consulté le ).
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, présentation en ligne), p. 294.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, États-Unis, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50.
- (en) « Butane », sur NIST/WebBook (consulté le 11 février 2010).
- (en) William M. Haynes, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 91e éd., 2610 p. (ISBN 9781439820773, présentation en ligne), p. 14-40.
- Aston, J.G. et Messerly, G.H., The heat capacity and entropy, heats of fusion and vaporization and the vapor pressure of n-butane, J. Am. Chem. Soc., 1940, 62, 1917-1923.
- Pittam, D.A. et Pilcher, G., Measurements of heats of combustion by flame calorimetry. Part 8.-Methane, ethane, propane, n-butane and 2-methylpropane, J. Chem. Soc. Faraday Trans. 1, 1972, 68, 2224-2229.
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub., (ISBN 0-88415-857-8).
- Les gaz Butane Propane, sur cfbp.fr.
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 10-205.
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE no 1272/2008 (16 décembre 2008).
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE no 1272/2008 (16 décembre 2008).
- « Butane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009.
- « n-Butane », sur hazmap.nlm.nih.gov (consulté le ).
- Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer et Hartmut Höke, Ullmann's Encyclopedia of Industrial Chemistry, Hydrocarbons, Wiley-VCH Verlag, .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 90e éd., 2804 p. (ISBN 9781420090840, présentation en ligne), p. 6-109.












