Dodécane
| Dodécane | ||
 | ||
| Structure 2D et 3D du dodécane | ||
| Identification | ||
|---|---|---|
| Nom UICPA | dodécane | |
| Synonymes |
n-dodécane |
|
| No CAS | ||
| No ECHA | 100.003.607 | |
| No CE | 203-967-9 | |
| DrugBank | DB02771 | |
| PubChem | 8182 | |
| SMILES | ||
| InChI | ||
| Apparence | liquide incolore | |
| Propriétés chimiques | ||
| Formule | C12H26 [Isomères] |
|
| Masse molaire[2] | 170,334 8 ± 0,011 4 g/mol C 84,62 %, H 15,39 %, |
|
| Diamètre moléculaire | 0,761 nm [1] | |
| Propriétés physiques | ||
| T° fusion | −9,65 °C [3] | |
| T° ébullition | 216,32 °C [4] | |
| Paramètre de solubilité δ | 16,0 J1/2·cm-3/2 (25 °C)[1] | |
| Masse volumique | 0,745 5 g·cm-3 à 24,95 °C [5] |
|
| T° d'auto-inflammation | 200 °C [7] | |
| Point d’éclair | 74 °C [7] | |
| Limites d’explosivité dans l’air | 0,6 - ? Vol.% [7] | |
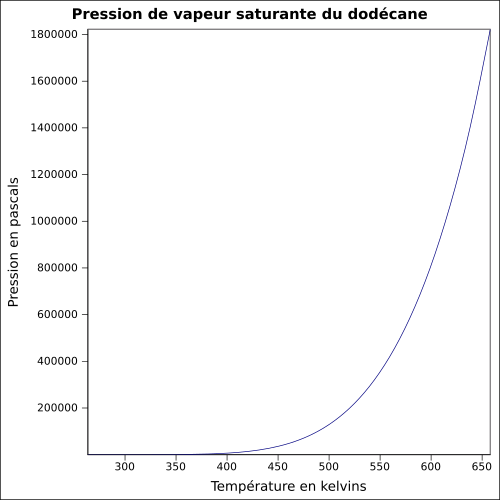
| Pression de vapeur saturante | 0,12 mbar à 20 °C 1 mbar à 50 °C [7] |
|
| Viscosité dynamique | 1,324 mPa·s à 24,95 °C 0,891 mPa·s à 49,95 °C [5] |
|
| Point critique | 1 820 kPa [8], 385,1 °C [4] | |
| Thermochimie | ||
| S0liquide, 1 bar | 490,66 J·mol-1·K-1 [3] | |
| ΔfH0liquide | −352,1 kJ·mol-1 [3] | |
| ΔfusH° | 36,836 kJ·mol-1 à −9,56 °C [3] | |
| ΔvapH° | 61,51 kJ·mol-1 à 25 °C [3] | |
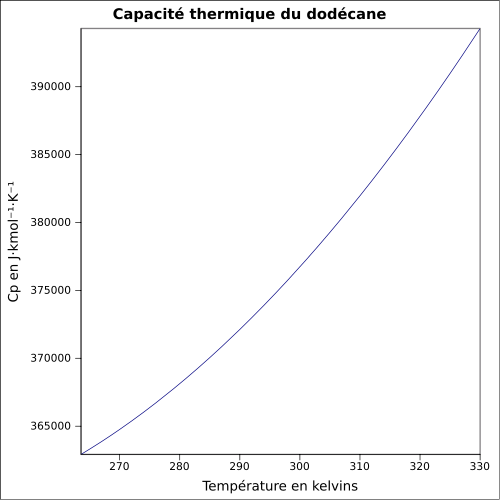
| Cp | 376 J·mol-1·K-1 (25 °C, liquide) [3]
|
|
| Propriétés optiques | ||
| Indice de réfraction | 1,4195 [1] | |
| Précautions | ||
| SIMDUT[10] | ||
 B3, |
||
| NFPA 704 | ||
| Directive 67/548/EEC | ||
| Écotoxicologie | ||
| Seuil de l’odorat | bas : 5,31 ppm[11] | |
| Composés apparentés | ||
| Isomère(s) | Isododécane | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Le dodécane est un alcane linéaire de formule brute C12H26. C'est un liquide huileux de la série des paraffines. Il possède 355 isomères structuraux.
Le dodécane est utilisé comme solvant, de solvant d'entraînement en distillation et de composé scintillateur. Il est aussi utilisé comme diluant du phosphate de tributyle utilisé pour l'extraction de l'uranium, du plutonium et du thorium depuis du combustible nucléaire usagé[12].
Réaction de combustion
[modifier | modifier le code]La réaction de combustion du dodécane est :
- 2 C12H26 (l) + 37 O2 (g) → 24 CO2 (g) + 26 H2O (g)
et son enthalpie de réaction ∆H˚ = −7 513 kJ.
Dans les conditions normales de température et de pression un litre de carburant nécessite environ 15 kg d'air pour brûler et produit 2,3 kg (ou 1,2 m3) de CO2 par combustion complète.
Carburant aviation de substitution
[modifier | modifier le code]Ces dernières années, le dodécane a retenu l'attention comme possible substitut au carburants à base de kérosène tels que le Jet-A, le S-8, et d'autres carburants aviation conventionnels. Il est considéré comme un substitut de carburant de deuxième génération, conçu pour émuler le vitesse de flamme laminaire, supplantant largement le n-décane, principalement en raison de sa masse moléculaire plus élevée et de son ratio hydrogène/carbone qui correspond mieux à ceux des n-alcanes de carburéacteurs.[réf. nécessaire]
Notes et références
[modifier | modifier le code]- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, , 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « n-Dodecane », sur NIST/WebBook, consulté le 21 avril 2009
- (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Temperatures. Part I. Aliphatic Hydrocarbons », J. Phys. Chem. Ref. Data, vol. 32, no 4, , p. 1411 (DOI 10.1063/1.1556431)
- (en) Makio Iwahashi, Yoshimi Yamaguchi, Yoshio Ogura et Masao Suzuki, « Dynamical Structures of Normal Alkanes, Alcohols, and Fatty Acids in the Liquid State as Determined by Viscosity, Self-Diffusion Coefficient, Infrared Spectra, and 13CNMR Spin-Lattice Relaxation Time Measurements », Bulletin of the Chemical Society of Japan, vol. 8, , p. 2154-2158 (DOI 10.1246/bcsj.63.2154)
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- Entrée « n-Dodecane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 21 avril 2009 (JavaScript nécessaire)
- (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Pressures. Part I. Aliphatic Hydrocarbons », J. Phys. Chem. Ref. Data, vol. 35, no 4, , p. 1461 (DOI 10.1063/1.2201061)
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 3, Huston, Texas, Gulf Pub. Co., (ISBN 0-88415-859-4)
- « Dodécane normal » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « Dodecane », sur hazmap.nlm.nih.gov (consulté le )
- (en) Jan Rydberg, Solvent Extraction Principles and Practice, New York, Marcel Dekker, , 2e éd., 480 p. (ISBN 978-0-8247-5063-3), p. 524