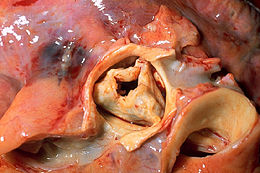
Rétrécissement aortique
| CIM-10 | I35.0, I06.0, Q23.0 |
|---|---|
| CIM-9 | 395.0, 424.1, 746.3 |
| DiseasesDB | 844 |
| MedlinePlus | 000178 |
| eMedicine | med/157 |
| MeSH | D017379 |
Le rétrécissement aortique (RA) ou sténose aortique est une valvulopathie consistant en la diminution de diamètre de l'orifice de sortie du ventricule gauche du cœur. Il provient le plus souvent d'une atteinte de la valve aortique, mais il peut parfois résulter d'une anomalie localisée au-dessus ou en dessous de cette valve qui sont d'origine congénitale.
Dans cet article, c'est le rétrécissement valvulaire aortique qui est plus particulièrement détaillé.
Ses causes principales sont représentées par la dégénérescence valvulaire chez le sujet âgé, la bicuspidie aortique congénitale chez le sujet jeune, et le rhumatisme articulaire aigu (RAA) ou maladie post-streptococcique qui est devenu rare dans les pays développés mais est toujours responsable d'un grand nombre de valvulopathies dans les pays en développement.
La maladie est longtemps asymptomatique et se révèle finalement par une symptomatologie d'effort dominée par la dyspnée, l'angor et les syncopes d'effort. Le diagnostic est orienté par l'auscultation, qui détecte un souffle éjectionnel systolique typique au foyer aortique. Il est confirmé par l'échographie Doppler qui précise le bilan des lésions.
Les RA asymptomatiques justifient d'une simple surveillance clinique et échographique tant qu'ils ne sont pas trop serrés, tandis que les RA serrés symptomatiques sont associés à un risque élevé de mort subite et doivent donc être traités. On peut proposer selon le contexte un remplacement valvulaire chirurgical qui constitue le traitement de référence, ou bien l'implantation percutanée d'une prothèse valvulaire aortique (TAVI) dans certains cas.
Épidémiologie
[modifier | modifier le code]Le rétrécissement aortique est l'atteinte valvulaire la plus fréquente de l'adulte dans les pays développés[1] et représente un peu moins de la moitié des cas de valvulopathie en Europe[2]. La maladie est fréquente chez les personnes âgées de plus de 65 ans avec une prévalence évaluée à 2 %[3]. Parvenu au stade symptomatique, le rétrécissement aortique est une maladie grave associée à une mortalité supérieure à 60 % à 5 ans[4] du début des symptômes, et de 90 % à 10 ans.
Aux États-Unis, le coût chirurgical (remplacement conventionnel ou par voie trans cutanée) dépasse 4 milliards de dollars en 2016[5].
Physiopathologie
[modifier | modifier le code]Dans le RA quelle qu'en soit la cause, la diminution de surface de l'orifice aortique représente un obstacle à l'éjection systolique du ventricule gauche, qui doit donc développer une pression plus importante lors de l'éjection (ce qu'on appelle une augmentation de la post-charge, comme dans le cas de l'HTA), pour maintenir le volume de sang éjecté à chaque contraction : le ventricule gauche doit pousser plus fort pour propulser le volume d'éjection systolique à travers un orifice aortique rétréci, on parle d'augmentation des pressions systoliques intraventriculaires gauche. Il en résulte que la pression dans le ventricule gauche devient supérieure à la pression dans l'aorte ascendante pendant la contraction, ou systole : c'est le gradient de pression systolique VG-aorte, qui est nul (ou minime, de l'ordre de 5 mmHg) à l'état physiologique et nettement augmenté (pouvant atteindre momentanément 100 mmHg), lors d'un rétrécissement aortique serré.
On parle donc de surcharge « de pression », « purement systolique », il n'y a pas de modification au départ de ce qui se passe en diastole, le volume du ventricule gauche n'est pas augmenté en fin de diastole (volume télédiastolique), contrairement à ce qui se passe par exemple dans l'insuffisance aortique.
L'existence de ce gradient de pression a pour conséquences :
- la prolongation de l'éjection ventriculaire gauche ;
- l'impossibilité pour le débit cardiaque de s'adapter à l'effort, en effet l'orifice aortique rétréci devient un facteur limitant du débit cardiaque ;
- surtout, une hypertrophie concentrique du ventricule gauche.
En effet la loi de Laplace indique que la relation entre contraintes pariétales T (ou tension s'exerçant sur la paroi du ventricule gauche), diamètre ventriculaire D, pression intraventriculaire P et épaisseur pariétale e est donnée par la relation : à diamètre ventriculaire constant, l'augmentation de la pression dans le ventricule gauche induit ainsi une augmentation de la tension de la paroi (contrainte pariétale), qui s'oppose au raccourcissement des fibres myocardiques et donc à la contraction du ventricule gauche et à l'éjection systolique. La loi de Laplace indique que seule une augmentation de l'épaisseur pariétale peut alors faire diminuer les contraintes pariétales : c'est pourquoi l'hypertrophie ventriculaire gauche concentrique ou systolique (c'est-à-dire obtenue par une augmentation de l'épaisseur et non pas du diamètre du ventricule gauche) représente le principal mécanisme adaptatif au cours du rétrécissement aortique.
À son tour, cette hypertrophie ventriculaire gauche entraîne :
- rapidement, une diminution de la compliance du ventricule gauche (la compliance est l'équivalent de la distensibilité, plus elle est basse plus il faut une pression élevée pour faire entrer dans le ventricule gauche un volume de sang donné pendant la diastole) ; de plus la relaxation du muscle se fait moins bien pendant la diastole (troubles de relaxation). L'ensemble est responsable d'une anomalie de la phase de remplissage du ventricule gauche avec augmentation des pressions en diastole (dysfonction diastolique) ; cette dysfonction diastolique est en partie compensée par l'existence d'une systole auriculaire efficace, qui « pousse » le sang vers le ventricule gauche en fin de diastole, expliquant la mauvaise tolérance de l'AC/FA lorsqu'elle s'associe au RA, puisqu'il n'y a plus alors de systole auriculaire efficace.
- initialement une conservation de la fonction systolique du ventricule gauche, expliquant que le RA demeure si longtemps asymptomatique ; après une longue évolution, la détérioration des cardiomyocytes soumis à des régimes de pression anormalement élevés est telle que leur capacité de se contracter (contractilité) finit par diminuer, avec alors (tardivement) une dilatation ventriculaire, une diminution du raccourcissement des fibres musculaires cardiaques en systole (dysfonction systolique) et une diminution de la fraction d'éjection du ventricule gauche (FEVG).
À cette physiopathologie classique, qui rend compte des principaux symptômes et complications du rétrécissement aortique, s'ajoutent des facteurs :
- génétiques avec la possible implication d'une mutation du gène NOTCH1[6] ou du gène LPA[7] ;
- métaboliques, l'hypercholestérolémie étant potentiellement impliquée (du moins dans des modèles animaux[8]) dans la genèse de la maladie, d'où les tentatives d'emploi de statines pour ralentir l'évolution du RA.
Causes
[modifier | modifier le code]Le RA dégénératif ou maladie de Mönckeberg[9] représente 82 % des cas[10]. C'est la première cause de RA chez le sujet âgé de plus de 65 ans. Il s'agit d'une sclérose avec calcification progressive intéressant aussi bien l'anneau aortique que les valvules. Outre l'âge, la présence d'une hypertension artérielle, d'un diabète sucré ou d'une dyslipidémie sont corrélés avec un risque de survenue d'un rétrécissement aortique[11]. Il n'est, pour l'instant, pas démontré que la prise en charge de ces éléments pourrait diminuer ce risque.
Le RA congénital (5 à 6 % des cas)[10] est la première cause de RA chez le sujet de moins de 65 ans. Il s'agit le plus souvent d'une bicuspidie aortique, la valve étant composée de deux valvules au lieu de trois. Une anomalie de l'aorte ascendante est fréquemment associée, le plus souvent à type d'ectasie voie d'anévrysme vrai, bien plus rarement à type de coarctation.
Le RA rhumatismal c'est-à-dire post-RAA (d'origine infectieuse) est devenu plus rare dans les pays développés (près de 11 % des cas[10]), avec l'amélioration des conditions de vie et d'accès aux soins. La lésion anatomopathologique est constituée par une fusion des commissures valvulaires avec rétraction des valvules. D'autres valvulopathies, notamment du cœur gauche, sont très souvent associées.
Dans les pays en développement, le RA rhumatismal demeure une cause prépondérante dans les pays en développement, où l'accès aux soins est beaucoup plus réduit (défaut de prise en charge des angines à streptococoque)[12]. Dans des pays d'endémie persistante de RAA, comme l'Inde ou le Pakistan, la prévalence des valvulopathies rhumatismales est de l'ordre de 5 cas pour mille personnes alors qu'elle est inférieure à 0,5 pour mille dans les pays occidentaux. Lorsque le dépistage est échocardiographique les chiffres peuvent atteindre 20 à 30 pour mille (Cambodge, Mozambique)[13].
Diagnostic
[modifier | modifier le code]Signes fonctionnels : symptômes
[modifier | modifier le code]Dans le rétrécissement aortique, l'apparition de symptômes marque un tournant évolutif indiquant un RA serré et signifiant que le pronostic vital est engagé à plus ou moins court terme. Les symptômes traduisent l'existence de complications et prédominent initialement à l'effort :
- l'essoufflement à l'effort (dyspnée d'effort) traduit une surcharge pulmonaire qui se produit lorsque le débit cardiaque doit augmenter pour répondre à l'accroissement des besoins de l'organisme lors de l'effort. L'essoufflement peut survenir pour des efforts de plus en plus minimes, voire au repos ;
- l'angor est multifactoriel : d'une part l'augmentation de la masse musculaire du ventricule gauche (hypertrophie ventriculaire gauche) entraîne une augmentation des besoins en oxygène du myocarde alors que les coronaires sont plutôt comprimées par cette hypertrophie musculaire, ce qui gêne l'augmentation de leur débit (inadaptation besoins/apports en O2), il s'agit alors d'un angor dit fonctionnel car les artères coronaires sont normales ; cependant des sténoses coronaires athéromateuses sont fréquemment associées ;
- les syncopes d'effort traduisent l'incapacité du débit cardiaque à augmenter en situation d'exercice physique. Dans ce cas les muscles en activité «volent» la plus grande partie du débit cardiaque et il n'est plus possible de maintenir un débit suffisant vers l'encéphale, surtout en position debout, avec pour conséquence une baisse du débit cérébral responsable de la perte de connaissance. Il existe également parfois des syncopes indépendantes de l'effort qui sont, elles, en rapport avec des troubles conductifs ou même des arythmies ventriculaires paroxystiques, qui peuvent cependant se produire dans de nombreuses pathologies autres que le rétrécissement aortique. Une aggravation iatrogène est possible en cas d'usage de traitements vasodilatateurs (tels les dérivés nitrés) qui majorent le gradient de pression VG-aorte.
Signes physiques : examen clinique
[modifier | modifier le code]L'auscultation cardiaque met en évidence un souffle de RA typique :
- maximal au foyer aortique c'est-à-dire au bord droit du sternum dans le 2e espace intercostal, et pouvant irradier vers les carotides ;
- de chronologie systolique, voire mésosystolique (en milieu de systole) avec un maximum dans la systole d'autant plus tardif que le RA est serré ; en cas d'arythmie associée, il peut être renforcé après les diastoles longues ;
- de timbre éjectionnel c'est-à-dire rude ou « râpeux » ;
- éventuellement associé à l'un ou plusieurs des signes suivants :
- une diminution du deuxième bruit du cœur B2 lorsque le RA est serré, sauf si sa cause est rhumatismale,
- un bruit surajouté de type B4 réalisant un galop présystolique, qui traduit l'effet de la systole auriculaire sur un ventricule gauche hypertrophié, sauf en cas de fibrillation auriculaire (la perte de la systole auriculaire entraîne alors une disparition du B4),
- un souffle d'insuffisance aortique (IA), l'association des deux valvulopathies aortiques réalisant le tableau de maladie aortique.
La palpation thoracique peut retrouver :
- un frémissement au foyer aortique, maximal en fin d'inspiration et en position d'antéflexion du thorax ;
- avec dans le RA évolué un élargissement du choc de pointe traduisant l'hypertrophie ventriculaire gauche.
Enfin, on décrit classiquement sous le nom de syndrome de Heyde l'association des signes de RA avec des saignements digestifs dont la physiopathologie demeure mal connue. Il est probable que ces saignements soient le fait d'une angiodysplasie colique elle-même induite par un excès de consommation du facteur von Willebrand[14],[15],[16],[17],[18] : dans la zone de sténose aortique, la turbulence du flux sanguin serait à l'origine d'une majoration locale des contraintes mécaniques qui favoriserait un changement de conformation du facteur von Willebrand, lequel serait alors plus facilement dégradé par la protéase ADAMTS13 (l'ensemble réalisant une sorte de maladie de Willebrand acquise).
Examens complémentaires
[modifier | modifier le code]ECG
[modifier | modifier le code]L'électrocardiogramme n'est modifié que dans les rétrécissements aortiques serrés, mettant en évidence des anomalies peu spécifiques :
- une hypertrophie ventriculaire gauche électrique de type « systolique «, c'est-à-dire : indice de Sokolow-Lyon augmenté (traduisant l'augmentation de la masse musculaire myocardique), ondes T négatives en dérivations précordiales gauches ;
- parfois, divers troubles conductifs et arythmies (cf. infra Complications).
Radiographie pulmonaire
[modifier | modifier le code]Elle aussi peu contributive, car souvent normale ou ne montrant que des signes peu spécifiques :
- élargissement du médiastin supérieur en cas de dilatation de l'aorte ascendante ;
- calcifications valvulaires radio-opaques, rendant la valve aortique artificiellement visible ;
- cardiomégalie tardive, reflet alors de la dilatation du ventricule gauche, avec possibles signes de surcharge pulmonaire (syndrome alvéolo-interstitiel bilatéral à prédominance péri-hilaire) dans les RA serrés.
Échographie-Doppler cardiaque
[modifier | modifier le code]L'échocardiographie est l'examen essentiel du diagnostic paraclinique. Elle est pratiquée à visée de confirmation diagnostique, d'orientation étiologique et surtout d'évaluation pronostique. L'échographie cardiaque transthoracique (ETT) est souvent suffisante mais certains patients peuvent bénéficier d'une échographie transœsophagienne (ETO) dans des indications particulières : mesure précise de la surface aortique avant TAVI, suspicion d'endocardite infectieuse etc.
Le diagnostic positif, qui est avant tout clinique, est confirmé par la visualisation des remaniements valvulaires et (dans les RA dégénératifs) des calcifications de la valve aortique. La mobilité des valvules et l'amplitude d'ouverture de la valve sont évaluées.
La sévérité du RA est très bien évaluée par l'échographie-Doppler cardiaque qui permet de quantifier :
- la vitesse maximale Vmax à la sortie de l'orifice aortique, le RA étant considéré comme serré si Vmax > 4 m/s (la vitesse à cet endroit est de l'ordre de 1 m/s chez un individu ayant une valve aortique normale) ;
- le gradient de pression moyen entre ventricule gauche et aorte au cours de la systole (la différence de pression de part et d'autre du rétrécissement est déduite de la vitesse par une application simplifiée du théorème de Bernoulli), le RA étant dit serré pour un gradient moyen > 40 mmHg ;
- la surface d'ouverture de la valve aortique (dite surface aortique), qui est calculée en divisant la surface de l'anneau aortique par le rapport de la vitesse enregistrée à l'endroit du rétrécissement maximal sur la vitesse dans l'aorte d'aval qui n'est pas rétrécie. Ainsi si la vitesse est 4 fois plus rapide à l'endroit du rétrécissement qu'en aval, avec un anneau aortique d'une surface de 3 cm2, la surface aortique est calculée à 0,75 cm2 :
- on parle de RA serré pour une Saortique < 1 cm2 (ou Saortique < 0,6 cm2/m2 de surface corporelle) ;
- on parle de RA critique pour une Saortique < 0,75 cm2 (ou Saortique < 0,4 cm2/m2 de surface corporelle).
Les deux premiers critères sont considérés comme moins fiables car contrairement à la surface de l'orifice aortique, ils varient en fonction de l'hémodynamique intracardiaque : la vitesse maximale est influencée par le débit sanguin et le gradient de pression VG-aorte dépend de la fonction systolique du ventricule gauche (lorsque l'insuffisance cardiaque systolique commence à décompenser, la diminution de la contractilité (perte d'inotropisme) abaisse le gradient de pression sans que cet abaissement traduise un agrandissement de l'orifice aortique dont la sténose ne fait au contraire que progresser).
Le retentissement du RA s'évalue sur :
- l'hypertrophie ventriculaire gauche, dont le caractère concentrique est bien mis en évidence par l'épaississement (plus ou moins) proportionnel du septum, de la paroi postérieure et de la paroi antérieure du ventricule gauche ;
- tardivement la dilatation du ventricule gauche, la diminution de la FEVG (< 50 %) voire l'HTAP (très tardive dans le RA).
Autres examens
[modifier | modifier le code]Le cathétérisme cardiaque gauche a été largement supplanté par les techniques échographiques car il est beaucoup plus invasif mais rarement plus informatif. Dans le RA, ses indications sont limitées aux cas de discordance clinico-échographique. Sous réserve que le rétrécissement ne soit pas trop serré pour autoriser le passage de la sonde, il fournit par des méthodes directes (mesure des pressions et thermodilution) les mêmes informations que l'ETT ou l'ETO.
La coronarographie est utile à la détection de sténoses coronaires athéromateuses associées au RA. Elle est indiquée en pré-opératoire :
- chez l'homme de plus de 40 ans et chez la femme ménopausée ;
- et/ou en présence de facteurs de risque cardio-vasculaire, notamment des antécédents personnels ou familiaux de coronaropathie ;
- et/ou devant un angor d'effort, des signes cliniques d'insuffisance cardiaque ou une FEVG < 50 %.
Le coroscanner a une place moins consensuelle, son utilisation en remplacement de la coronarographie pré-opératoire étant particulièrement discutée. Il est utilisé :
- pour la mesure précise de la surface aortique avant TAVI, afin de choisir une prothèse valvulaire de dimensions adaptées ;
- pour la mesure du diamètre de l'aorte ascendante lorsque l'échographie est peu contributive ;
- voire pour l'évaluation du degré de calcification de la valve aortique, en rapport avec la sévérité du rétrécissement[19].
Son usage est principalement limité par la nécessité d'une immobilité complète (apnée) pendant l'acquisition, et l'impossibilité de réaliser l'examen si le rythme cardiaque est irrégulier ou trop rapide (la tachycardie étant moins limitante avec les appareils multibarettes bitubes de nouvelle génération).
Parmi les autres examens paracliniques parfois indiqués dans le RA, citons :
- l'épreuve d'effort ou ECG d'effort : réalisée avec les précautions habituelles (en présence d'un médecin et d'un infirmier, avec le matériel de réanimation à disposition dans la salle), elle permet de d'évaluer le retentissement de RA serrés paraissant asymptomatiques, en recherchant l'apparition de symptômes ou d'une chute de la pression artérielle à l'effort ;
- l'échographie-Doppler d'effort ou sous dobutamine, indiquée dans les RA serrés asymptomatiques avec dysfonction ventriculaire gauche échographique : son intérêt est double puisqu'elle permet d'une part d'évaluer la réserve de contractilité myocardique, et d'autre part d'écarter les « faux » RA serrés dans lesquels la mauvaise ouverture valvulaire est en fait imputable à la dysfonction systolique du ventricule gauche sans que le RA soit véritablement serré ;
- le Holter ECG, qui peut permettre le dépistage de troubles conductifs ou rythmiques paroxystiques devant un tableau de syncopes et/ou palpitations spontanées (indépendantes de l'effort) ;
- le dosage du BNP ou du NT-proBNP plasmatique, dont la valeur pronostique est suspectée mais encore mal évaluée.
L'épreuve d'effort et l'échographie-Doppler d'effort ou sous dobutamine sont formellement contre-indiqués en cas RA serré symptomatique car ils exposent alors à un risque de mort subite.
Complications
[modifier | modifier le code]La mort subite est bien entendu la plus redoutable, elle est surtout la conséquence des RA serrés symptomatiques négligés mais peut rarement (environ 4 % des cas[20]) constituer un mode de révélation de la maladie.
Les autres complications incluent :
- l'insuffisance cardiaque d'abord gauche puis globale, parfois décompensée sous forme d'œdème aigu du poumon (OAP) cardiogénique : elle est tardive (la fonction systolique étant longtemps préservée) et de mauvais pronostic ;
- la fibrillation auriculaire, secondaire à la distension chronique de l'oreillette gauche (sur laquelle finit par se répercuter l'élévation des pressions intraventriculaires gauches), elle est souvent mal tolérée car la systole auriculaire représente un mécanisme compensateur de la dysfonction diastolique du ventricule gauche (cf. Physiopathologie) ;
- les arythmies ventriculaires qui résultent des altérations structurelles et électrophysiologiques des cardiomyocytes soumis à des pressions intraventriculaires gauches excessives : elles sont rares et surviennent sur le mode paroxystique en occasionnant des syncopes indépendantes de l'effort ;
- les troubles conductifs qui sont surtout observés dans les RA calcifiés car ils sont secondaires à l'invasion du faisceau de His par des calcifications de l'anneau mitral s'étendant en direction du septum interventriculaire : tous types de troubles peuvent se voir, mais il s'agit surtout de blocs auriculoventriculaires ;
- l'endocardite infectieuse plutôt rare dans le RA (plus fréquemment associée aux insuffisances qu'aux rétrécissements valvulaires) ;
- l'embolie calcaire (à point de départ valvulaire) qui est exceptionnelle : c'est une embolie systémique pouvant intéresser le système nerveux central (AVC), l'artère centrale de la rétine (OACR), les coronaires (SCA), les artères rénales (infarctus rénal) etc.
Facteurs pronostiques
[modifier | modifier le code]On considère généralement que le rétrécissement aortique est à faible risque tant qu'il reste asymptomatique. La vitesse d'évolution moyenne de la diminution de surface aortique est d'environ 0,1 cm2/an (un peu plus rapide dans les RA dégénératifs).
À l'inverse le pronostic vital est engagé en cas de RA symptomatique : la survie moyenne à compter du début des symptômes va de 4 à 5 ans en cas d'angor d'effort, 3 ans en cas de syncope, à 2 ans en cas d'insuffisance cardiaque symptomatique et 6 mois en cas d'OAP cardiogénique.
Prise en charge
[modifier | modifier le code]Moyens thérapeutiques
[modifier | modifier le code]Traitement médical
[modifier | modifier le code]S'il peut être adjuvant, il n'a pas d'efficacité prouvée sur la progression de la maladie lorsqu'il est utilisé seul. C'est un traitement au mieux symptomatique et conservateur. Les options thérapeutiques sont limitées :
- les diurétiques peuvent améliorer la qualité de vie en réduisant la dyspnée associée à l'insuffisance cardiaque ;
- les vasodilatateurs peuvent par contre avoir un effet délétère par le biais d'une majoration du gradient de pression VG-aorte et d'une diminution du remplissage ventriculaire gauche qui dégrade la fonction systolique (loi de Starling) du cœur ;
- les inotropes (« tonicardiaques ») sont contre-indiqués car ils aggravent l'élévation des pressions intraventriculaires gauches, et ne sont de toute façon pas indiqués tant que la fonction systolique est conservée.
L'intérêt des statines dans le traitement des RA dégénératifs reste à démontrer[21]. La prophylaxie antibiotique de l'endocardite infectieuse a été fortement remise en question dans les dernières recommandations européennes (2009) pour le rétrécissement aortique, entre autres valvulopathies[22].
Remplacement valvulaire chirurgical
[modifier | modifier le code]Le remplacement valvulaire aortique chirurgical sous CEC (circulation extra-corporelle) demeure la technique de référence, en particulier dans les RA serrés calcifiés. L'exérèse de la valve native est suivie de l'implantation d'une prothèse valvulaire qui peut être :
- soit mécanique, avec la garantie d'une très longue durée de vie mais impliquant obligatoirement la prise d'un traitement anticoagulant à vie avec les contraintes et risques qu'il suppose ;
- soit biologique c'est-à-dire confectionnée à partir de tissus animaux traités, ne nécessitant pas de traitement anticoagulant, mais dont la durée de vie limitée de 10 à 15 ans peut imposer un second remplacement valvulaire si elle est implantée chez un sujet trop jeune. Le développement du TAVI, et notamment du TAVI dans une valve biologique anciennement implantée, devrait faire réévaluer les indications.
Implantation percutanée d'une prothèse valvulaire aortique
[modifier | modifier le code]L'implantation percutanée d'une prothèse valvulaire aortique, ou TAVI (Transcatheter Aortic Valve Implantation), est une technique qui a été expérimentée pour la première fois en 2002 chez l'homme[23], désormais passée dans la pratique courante. Il s'agit de l'implantation in situ (sans exérèse de la valve native) d'une prothèse valvulaire biologique assujettie à une armature métallique, l'ensemble étant monté jusqu'au cœur par voie endovasculaire. Les résultats de ce type d'intervention semblent comparables à ceux de la chirurgie traditionnelle en termes de mortalité, avec cependant un léger sur-risque d'AVC[24].
Valvuloplastie percutanée par ballonnet
[modifier | modifier le code]Cette technique développée dans les années 1980[25] consiste à utiliser le gonflement d'un ballonnet monté par voie endovasculaire (via l'artère fémorale) pour redilater l'orifice aortique sténosé en faisant « craquer » les commissures valvulaires. Cette technique est depuis relativement délaissée en raison d'un taux élevé de complications et d'une récidive quasi constante du RA[26], mais conserve quelques indications spécifiques.
Indications
[modifier | modifier le code]Dans les RA asymptomatiques, la simple surveillance est suffisante tant que la sténose n'est pas trop serrée (surface valvulaire > 1 cm2 ou > 0,6 cm2/m2 de surface corporelle) et n'est pas associée à une insuffisance cardiaque ou à une diminution asymptomatique de la fraction d'éjection du ventricule gauche (FEVG normale).
Le remplacement valvulaire aortique chirurgical est généralement indiqué :
- dans tous les RA serrés symptomatiques ;
- ainsi que dans certains RA serrés asymptomatiques :
- s'il existe une dysfonction systolique du ventricule gauche avec FEVG < 50 %,
- si l'épreuve d'effort est positive (RA serré « démasqué ») : apparition d'une symptomatologie d'effort (dyspnée/angor/syncope), augmentation insuffisante (< 20 mmHg), voire diminution, de la pression artérielle systolique à l'effort,
- si le RA est très serré (Vmax > 5,5 m/s) et/ou rapidement évolutif.
Les modalités sont le plus souvent fonction de l'âge du patient : compte tenu de leurs durées de vie respectives, il est a priori plus logique de proposer une prothèse valvulaire mécanique à un patient jeune et une prothèse biologique à un patient âgé. Certains patients jeunes peuvent cependant se voir proposer une prothèse biologique en raison d'une contre-indication au traitement anticoagulant et sous réserve d'accepter le risque d'une ré-intervention 10 à 15 ans plus tard : c'est le cas notamment lorsque le patient pratique une activité sportive à risque traumatique, ou chez la femme jeune susceptible d'être enceinte.
Cependant le remplacement valvulaire aortique chirurgical est une intervention lourde dont le rapport bénéfice-risque doit être soigneusement pesé, tout particulièrement chez les patients souvent (très) âgés auxquels il est proposé. Cette évaluation du risque opératoire peut être aidée par des outils tels que l'EuroSCORE[27] (European System for Cardiax Operative Risk Evaluation) et le score STS[28] (Society of Thoracic Surgeons).
Les traitements non chirurgicaux trouvent leur place en cas de contre-indication à l'intervention :
- le TAVI est indiqué dans le RA serré symptomatique si la chirurgie est récusée (en raison d'un risque opératoire excessif et/ou de comorbidités trop sévères) et si l'espérance de vie du patient est jugée supérieure à 1 an. La Haute Autorité de santé (HAS) publie des recommandations précises sur les indications du TAVI, qui évoluent dans le temps ;
- la valvuloplastie au ballonnet apporte une amélioration hémodynamique transitoire qui, si elle est significative, peut être mise à profit pour réaliser secondairement un remplacement valvulaire aortique chirurgical ou une autre intervention lourde difficilement envisageable auparavant ;
- le traitement médical seul ne se conçoit que chez des patients très âgés, à l'état général profondément altéré et/ou atteints d'une pathologie engageant à court terme le pronostic vital.
Recommandations
[modifier | modifier le code]Les recommandations américaines relatives au diagnostic et la prise en charge des valvulopathies ont été mises à jour en 2020[29]. Un document spécifique au rétrécissement aortique a été édité en 2017 [30].
Les recommandations de la Société européenne de cardiologie (European Society of Cardiology, ESC) datent de 2007 ont été mises à jour en 2021[31].
Références
[modifier | modifier le code]- Manning WJ, « Asymptomatic aortic stenosis in the elderly: a clinical review », JAMA, vol. 310, no 14, , p. 1490–7 (PMID 24104373, DOI 10.1001/jama.2013.279194)
- Lung B, Baron G, Butchart EG, Delahaye F et al. A prospective survey of patients with valvular heart disease in Europe: the Euro heart survey on valvular heart disease, Eur Heart J, 2003;24:1231-43
- MJ Czarny et JR Resar, « Diagnosis and management of valvular aortic stenosis. », Clinical Medicine Insights. Cardiology, vol. 8, no Suppl 1, , p. 15–24 (PMID 25368539, DOI 10.4137/CMC.S15716)
- (en) E. Braunwald et J Jr. Ross, « Aortic stenosis » [« Rétrécissement aortique »], Circulation, vol. 38, no 1 Suppl, , p. 61-67 (PMID 4894151)
- Alkhouli M, Alqahtani F, Ziada KM, Aljohani S, Holmes DR, Mathew V, Contemporary trends in the management of aortic stenosis in the USA, Eur Heart J, 2020;41:921–928
- Garg V, Muth AN, Ransom JF et als. Mutations in NOTCH1 cause aortic valve disease, Nature, 2005;437:270-274
- Thanassoulis G, Campbell CY, Owens DS et al. Genetic associations with valvular calcification and aortic stenosis, N Engl J Med, 2013;368:503-512
- Weiss RM, Ohashi M, Miller JD, Young SG, Heistad DD. Calcific aortic valve stenosis in old hypercholesterolemic mice, Circulation, 2006;114:2065-2069
- Il s'agit de (en) « Johann Georg Mönckeberg (1877-1925) », sur Whonamedit.com
- Farzin Beygui, « Traitement percutané du rétrécissement aortique », La Revue du Praticien - médecine générale, vol. 23, no 826, , p. 520-521.
- Yan AT, Koh M, Chan KK et al. Association between cardiovascular risk factors and aortic stenosis: the CANHEART aortic stenosis study, J Am Coll Cardiol, 2017;69:1523–1532
- (en) Catherine M. Otto, « Aortic-Valve Stenosis », The New England Journal of Medicine, vol. 371, no 8, , p. 744-756 (p. 746).
- Bernard Lung, « Epidémiologie des valvulopathies cardiaques de l'adulte », La Revue du Praticien, vol. 59, no 2, , p. 173-177.
- H. M. Tsai, I. I. Sussman et R. L. Nagel, « Shear stress enhances the proteolysis of von Willebrand factor in normal plasma », Blood, vol. 83, no 8, , p. 2171–9 (ISSN 0006-4971, PMID 8161783, lire en ligne)
- Warkentin TE, Moore JC, Morgan DG, « Aortic stenosis and bleeding gastrointestinal angiodysplasia: is acquired von Willebrand's disease the link? », The Lancet, vol. 340, no 8810, , p. 35–7 (ISSN 0140-6736, PMID 1351610, DOI 10.1016/0140-6736(92)92434-H, lire en ligne)
- A. Veyradier, A. Balian, M. Wolf, .V Giraud, S. Montembault, B. Obert, I. Dagher, J. C. Chaput, D. Meyer et S. Naveau, « Abnormal von Willebrand factor in bleeding angiodysplasias of the digestive tract », Gastroenterology, vol. 120, no 2, , p. 346–53 (ISSN 0016-5085, PMID 11159874, DOI 10.1053/gast.2001.21204, lire en ligne)
- T. E. Warkentin, J. C. Moore, S. S. Anand, E. M. Lonn et D. G. Morgan, « Gastrointestinal bleeding, angiodysplasia, cardiovascular disease, and acquired von Willebrand syndrome », Transfusion Medicine Reviews, vol. 17, no 4, , p. 272–86 (ISSN 0887-7963, PMID 14571395, DOI 10.1016/S0887-7963(03)00037-3, lire en ligne)
- A. Vincentelli, S. Susen, T. Le Tourneau, I. Six, O. Fabre, F. Juthier, A. Bauters, C. Decoene, J. Goudemand, A. Prat et B. Jude, « Acquired von Willebrand syndrome in aortic stenosis », The New England Journal of Medicine, vol. 349, no 4, , p. 343–9 (ISSN 0028-4793, PMID 12878741, DOI 10.1056/NEJMoa022831, lire en ligne)
- Pawade T, Clavel M-A, Tribouilloy C, et al. Computed tomography aortic valve calcium scoring in patients with aortic stenosis, Circ Cardiovasc Imaging, 2018; 11:e007146
- Pellikka PA, Sarano ME, Nishimura RA et als. Outcome of 622 adults with asymptomatic, hemodynamically significant aortic stenosis during prolonged follow-up, Circulation, 2005;111:3290-5
- Parolari A, Tremoli E, Cavallotti L et Als. Do statins improve outcomes and delay the progression of non-rheumatic calcific aortic stenosis?, Heart, 2011;97:523-529
- (en) Société européenne de cardiologie, « Guidelines on the prevention, diagnosis, and treatment of infective endocarditis (new version 2009): The Task Force on the Prevention, Diagnosis, and Treatment of Infective Endocarditis of the European Society of Cardiology (ESC) », European Heart Journal, Volume 30, Issue 19, 1 October 2009, Pages 2369–2413, https://doi.org/10.1093/eurheartj/ehp285, vol. 30, no 19, , p. 2369–2413 (DOI 10.1093/eurheartj/ehp285, lire en ligne, consulté le ).
- Cribier A, Eltchaninoff H, Tron C et als. Treatment of calcific aortic stenosis with the percutaneous heart valve: mid-term follow-up from the initial feasibility studies: the French experience, J Am Coll Cardiol, 2006;47:1214–23
- Smith CR, Leon MB, Mack MJ et al. Transcatheter versus surgical aortic-valve replacement in high-risk patients, N Engl J Med, 2011;364:2187-2198
- Cribier A, Savin T, Saoudi N et als. Percutaneous transluminal valvuloplasty of acquired aortic stenosis in elderly patients: an alternative to valve replacement?, Lancet, 1986;1:63–7
- Vahanian A, Palacios IF, Percutaneous approaches to valvular disease, Circulation, 2004;109:1572–1579
- Roques F, Michel P, Goldstone AR et als. The logistic EuroSCORE, Eur Heart J, 2003;24:881–882
- Edwards FH, Grover FL, Shroyer AL et als. The Society of Thoracic Surgeons National Cardiac Surgery Database: current risk assessment, Ann Thorac Surg, 1997;63:903–908
- Otto CM, Nishimura RA, Bonow RO et al. 2020 ACC/AHA guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines, Circulation, 2021;143:e72–e227
- (en) Robert O. Bonow, Brown AS, Gillam LD et al., « ACC/AATS/AHA/ASE/EACTS/HVS/SCA/SCAI/SCCT/SCMR/STS2017 Appropriate Use Criteria for the Treatment of Patients WithSevere Aortic Stenosis » [« Critères à utiliser pour le traitement de patients ayant une sténose aortique sévère »], J Am Coll Cardiol, vol. 70, no 20, , p. 2566-2598 (DOI 10.1016/j.jacc.2017.09.018, lire en ligne, consulté le ).
- Vahanian A, Beyersdorf F, Prazet F al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease: Developed by the Task Force for the management of valvular heart disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS), Eur Heart J, 2022;43:561–632
- (en) Valvular Aortic Stenosis : Disease Severity and Timing of Intervention, C Otto, J Am Coll Cardiol 2006;47:2141–51