Isocitrate déshydrogénase
| IDH cytosolique | ||
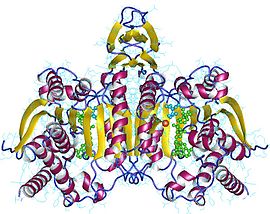 Dimère d'isocitrate déshydrogénase cytosolique humaine avec NADP en vert, isocitrate en cyan et Ca2+ en orange (PDB 1T0L[1]) | ||
| Caractéristiques générales | ||
|---|---|---|
| Symbole | IDH1 | |
| N° EC | 1.1.1.42 | |
| Homo sapiens | ||
| Locus | 2q34 | |
| Masse moléculaire | 46 659 Da[2] | |
| Nombre de résidus | 414 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
| IDH mitochondriale à NADP+ | ||
| Caractéristiques générales | ||
| Symbole | IDH2 | |
| N° EC | 1.1.1.42 | |
| Homo sapiens | ||
| Locus | 15q26.1 | |
| Masse moléculaire | 50 909 Da[2] | |
| Nombre de résidus | 452 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
| IDH mitochondriale à NAD+ | ||
| Caractéristiques générales | ||
| Symbole | IDH3 | |
| N° EC | 1.1.1.41 | |
| Gène IDH3A – Chaînes α | ||
| Homo sapiens | ||
| Locus | 15q25.1 | |
| Masse moléculaire | 39 592 Da[2] | |
| Nombre de résidus | 366 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
| Gène IDH3B – Chaîne β | ||
| Homo sapiens | ||
| Locus | 20p13 | |
| Masse moléculaire | 42 184 Da[2] | |
| Nombre de résidus | 385 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
| Gène IDH3G – Chaîne γ | ||
| Homo sapiens | ||
| Locus | Xq28 | |
| Masse moléculaire | 42 794 Da[2] | |
| Nombre de résidus | 393 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
L´isocitrate déshydrogénase (IDH) est une oxydoréductase qui catalyse la réaction :
- isocitrate + NADP+ / NAD+ α-cétoglutarate + CO2 + NADPH / NADH + H+.
Cette réaction globale se déroule en deux étapes :
- isocitrate + NADP+ / NAD+ oxalosuccinate + NADPH / NADH + H+ ;
- oxalosuccinate α-cétoglutarate + CO2.
Chez l'homme, cette enzyme existe en trois isoformes appelées IDH1, IDH2 et IDH3. L'isoenzyme IDH3 est présente dans les mitochondries où elle intervient aux 4e et 5e étapes du cycle de Krebs pour catalyser la décarboxylation de l'isocitrate en α-cétoglutarate[3] en réduisant le NAD+ en NADH ; les deux autres sont présentes dans le cytosol, les peroxysomes et les mitochondries, où elles catalysent la même réaction qu'IDH3, éventuellement indépendamment du cycle de Krebs, et réduisent le NADP+ en NADPH au lieu d'utiliser le NAD+ comme coenzyme
Ces trois isoformes humaines de l'isocitrate déshydrogénase ont les caractéristiques suivantes :
- IDH1 est fortement exprimée dans le foie et se présente comme un homodimère. Cette enzyme intervient dans le cycle de Krebs mais aussi dans la défense contre le stress oxydant dû aux dérivés réactifs de l'oxygène. Elle est NADP+-dépendante[3].
- IDH2 est fortement exprimée dans le cœur, les muscles et les lymphocytes activés, et se présente comme un homodimère. Elle est également NADP+-dépendante[3].
- IDH3 est une enzyme mitochondriale qui se présente comme un hétérotétramère α2βγ. Contrairement aux deux précédentes, elle est NAD+-dépendante[3].
| N° EC | EC |
|---|---|
| N° CAS | |
| Cofacteur(s) | Mn ou Mg |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
| N° EC | EC |
|---|---|
| N° CAS | |
| Cofacteur(s) | Mn ou Mg |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
Cible thérapeutique[modifier | modifier le code]
Des mutations des IDH ont été détectés dans les cancers, conduisant à des dysfonctions du métabolisme cellulaire pouvant participer à la croissance des cellules tumorales. Des inhibiteurs des IDH ont donc été développés :
- énasidénib : inhibiteur de l'IDH 2
- ivosidénib : inhibiteur de l'IDH 1
- vorasidénib : inhibiteur IDH1 et 2
Notes et références[modifier | modifier le code]
- (en) Xiang Xu, Jingyue Zhao, Zhen Xu, Baozhen Peng, Qiuhua Huang, Eddy Arnold et Jianping Ding, « Structures of Human Cytosolic NADP-dependent Isocitrate Dehydrogenase Reveal a Novel Self-regulatory Mechanism of Activity », Journal of Biological Chemistry, vol. 279, no 32, , p. 33946-33957 (PMID 15173171, DOI 10.1074/jbc.M404298200, lire en ligne)
- Les valeurs de la masse et du nombre de résidus indiquées ici sont celles du précurseur protéique issu de la traduction du gène, avant modifications post-traductionnelles, et peuvent différer significativement des valeurs correspondantes pour la protéine fonctionnelle.
- (en) Daniel Krell, Mawuelikem Assoku , Malcolm Galloway, Paul Mulholland, Ian Tomlinson et Chiara Bardella, « Screen for IDH1, IDH2, IDH3, D2HGDH and L2HGDH Mutations in Glioblastoma », PLoS One, vol. 6, no 5, , e19868 (PMID 21625441, PMCID 3100313, DOI 10.1371/journal.pone.0019868, Bibcode 2011PLoSO...619868K, lire en ligne)
- (en) Andrew D. Mesecar, Barry L. Stoddard et Daniel E. Koshland Jr., « Orbital Steering in the Catalytic Power of Enzymes: Small Structural Changes with Large Catalytic Consequences », Science, vol. 277, no 5323, , p. 202-206 (PMID 9211842, DOI 10.1126/science.277.5323.202, lire en ligne)



