Aldolase C
| Fructose-bisphosphate aldolase C | ||
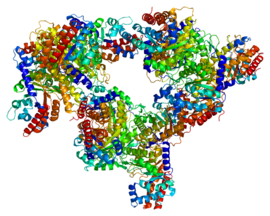 Structure d'une aldolase C de cerveau humain (PDB 1XFB[1]) | ||
| Caractéristiques générales | ||
|---|---|---|
| Symbole | ALDOC | |
| N° EC | 4.1.2.13 | |
| Homo sapiens | ||
| Locus | 17q11.2 | |
| Masse moléculaire | 39 456 Da[2] | |
| Nombre de résidus | 364 acides aminés[2] | |
| Entrez | 230 | |
| HUGO | 418 | |
| OMIM | 103870 | |
| UniProt | P09972 | |
| RefSeq (ARNm) | NM_005165.2 | |
| RefSeq (protéine) | NP_005156.1 | |
| Ensembl | ENSG00000109107 | |
| PDB | 1XFB | |
|
GENATLAS • GeneTests • GoPubmed • HCOP • H-InvDB • Treefam • Vega | ||
| Liens accessibles depuis GeneCards et HUGO. | ||
L’aldolase C est l'une des trois isoformes de l'aldolase, une lyase qui catalyse les réactions :
- D-fructose-1-phosphate D-glycéraldéhyde + dihydroxyacétone phosphate ;
- D-fructose-1,6-bisphosphate D-glycéraldéhyde-3-phosphate + dihydroxyacétone phosphate.
Cette enzyme cytosolique[3] intervient à la 4e étape de la glycolyse ainsi que dans la gluconéogenèse[1],[4]. Chez l'homme, elle est encodée par le gène ALDOC, situé sur le chromosome 17[5] et particulièrement exprimé dans l'hippocampe et les cellules de Purkinje du cerveau. Plus précisément, cette enzyme est exprimée dans la plupart des tissus mais est prépondérante dans le cerveau, le muscle lisse et les cellules du système nerveux[1],[3],[4],[6].
Dans la mesure où elle est exprimée dans le système nerveux central parallèlement à l'aldolase A, on pense qu'elle assure également des fonctions particulière au système nerveux central indépendantes de la glycolyse[4]. Sa présence dans d'autres types de cellules, tels que les thrombocytes (plaquettes sanguines) et les mastocytes pourrait permettre à celles-ci de disposer d'une voie de secours en cas de défaillance des autres aldolases[6].
D'une manière générale, elle assure certaines fonctions non catalytiques, à l'instar des autres aldolases, mais de manière semble-t-il moins marquée. Ainsi, elle se lie moins étroitement au cytosquelette que les autres aldolases, probablement en raison de son point isoélectrique plus acide[1]. Elle participe également à la réponse au stress des cellules épithéliales en hypoxie et des cellules de Purkinje dans le cervelet exposées à une situation d'excitotoxicité[6].
Notes et références[modifier | modifier le code]
- (en) Tracy L. Arakaki, John A. Pezza, Michelle A. Cronin, Chris E. Hopkins, Danna B. Zimmer, Dean R. Tolan et Karen N. Allen, « Structure of human brain fructose 1,6-(bis)phosphate aldolase: Linking isozyme structure with function », Protein Science, vol. 13, no 12, , p. 3077-3084 (PMID 15537755, PMCID 2287316, DOI 10.1110/ps.04915904, lire en ligne)
- Les valeurs de la masse et du nombre de résidus indiquées ici sont celles du précurseur protéique issu de la traduction du gène, avant modifications post-traductionnelles, et peuvent différer significativement des valeurs correspondantes pour la protéine fonctionnelle.
- (en) Piotr Mamczur, Andrzej Gamian, Jerzy Kolodziej, Piotr Dziegiel et Dariusz Rakus, « Nuclear localization of aldolase A correlates with cell proliferation », Biochimica et Biophysica Acta (BBA) - Molecular Cell Research, vol. 1833, no 12, , p. 2812-2822 (PMID 23886627, DOI 10.1016/j.bbamcr.2013.07.013, lire en ligne)
- (en) Simona Langellotti, Maurizio Romano, Corrado Guarnaccia, Vincenzo Granata, Stefania Orrù, Adriana Zagari, Francisco E. Baralle et Francesco Salvatore, « A novel anti-aldolase C antibody specifically interacts with residues 85–102 of the protein », mAbs, vol. 6, no 3, , p. 708-717 (PMID 24525694, DOI 10.4161/mabs.28191, lire en ligne)
- (en) Mariano Rocchi, Emilia Vitale, Istituto G. Gaslini, Angela Covone, Giovanni Romeo, Rita Santamaria, Pasqualina Buono, Giovanni Paolella et Francesco Salvatore, « Assignment of human aldolase C gene to chromosome 17, region cen→q21.1 », Human Genetics, vol. 82, no 3, , p. 279-282 (PMID 2731939, DOI 10.1007/BF00291170, lire en ligne)
- (en) Yokananth Sekar, Tae Chul Moon, Carolyn M. Slupsky et A. Dean Befus, « Protein Tyrosine Nitration of Aldolase in Mast Cells: A Plausible Pathway in Nitric Oxide-Mediated Regulation of Mast Cell Function », Journal of Immunology, vol. 85, no 1, , p. 578-587 (PMID 20511553, DOI 10.4049/jimmunol.0902720, lire en ligne)

