Bromochlorodifluorométhane
| Bromochlorodifluorométhane | ||
| ||
 | ||
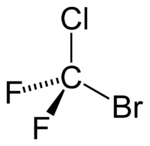
| représentations du Bromochlorodifluorométhane | ||
| Identification | ||
|---|---|---|
| Nom UICPA | Bromochlorodifluorométhane | |
| Synonymes |
fréon 12B1, |
|
| No CAS | ||
| No ECHA | 100.005.944 | |
| Apparence | gaz comprimé, liquéfié, d'odeur caractéristique[1]. | |
| Propriétés chimiques | ||
| Formule | CBrClF2 [Isomères] |
|
| Masse molaire[2] | 165,365 ± 0,004 g/mol C 7,26 %, Br 48,32 %, Cl 21,44 %, F 22,98 %, |
|
| Propriétés physiques | ||
| T° fusion | −160,5 °C[1] | |
| T° ébullition | −4 °C[1] | |
| Solubilité | dans l'eau : nulle[1] | |
| Masse volumique | 1,799 g·cm-3 | |
| Pression de vapeur saturante | 2,5 Bar (20 °C) | |
| Point critique | 42,5 bar, 153,75 °C [3] | |
| Thermochimie | ||
| Cp | ||
| Précautions | ||
| SIMDUT[5] | ||
 A, |
||
| Transport | ||
| Écotoxicologie | ||
| LogP | 2,1[1] | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Le bromochlorodifluorométhane aussi appelé R-12B1, fréon 12B1, Halocarbone R12 B1, halon 1211, ou R12B1, est un halon. C'est un gaz ininflammable. Il est principalement utilisé pour éteindre les incendies (extincteur), mais entre également dans la fabrication de mélanges réfrigérants.
Destruction de la couche d'ozone[modifier | modifier le code]
Selon la variété, il est de 3 (halon-1211) à 10 fois (halon-1301) plus nocif pour l'ozone que les CFC. Le halon serait responsable, à lui seul, actuellement, de 20 % de la destruction d'ozone. En vertu de l'Amendement de Copenhague (1992) au Protocole de Montréal relatif à des substances qui appauvrissent la couche d'ozone, les pays industrialisés devaient cesser la production dès 1994[6]. Mais les pays en voie de développement en 2010 seulement. La Chine augmente sa production de halon-1211 de 200 tonnes par année au lieu de la réduire. Ce pays est responsable de 90 % de la production mondiale de ce gaz[7].
Applications industrielles[modifier | modifier le code]
- Entre dans la composition de mélanges réfrigérants
- C'est un agent de lutte contre l'incendie
Propriétés[modifier | modifier le code]
- Gazeux dans les conditions atmosphériques (plus lourd que l'air)
- Incolore
- ininflammable
- Odeur : légèrement éthérée
- ODP (Ozone Depletion Potential) : 3
- GWP (Global Warming Potential) : 1300
Notes et références[modifier | modifier le code]
- BROMOCHLORODIFLUOROMETHANE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Inorganic Compounds and Elements, vol. 1, 2 et 3, Huston, Texas, Gulf Pub. Co., , 384 p. (ISBN 0-88415-857-8, 0-88415-858-6 et 0-88415-859-4)
- « Bromochlorodifluorométhane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Jean-Maurice Arbour, Sophie Lavallée, Jochen Sohnle et Hélène Trudeau (ill. Stefan Horik), Droit international de l'environnement, Montréal (Québec), Yvons Blais, 3e trimestre 2016, 3e édition éd., 1527 p. (ISBN 978-2-89730-224-5), p. 740
- Claire König, « CFC : Chlorofluocarbure », sur futura-sciences.com, (consulté le )




