Hexachlorobenzène
| Hexachlorobenzène | |
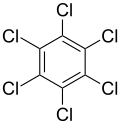  Structure de l'hexachlorobenzène |
|
| Identification | |
|---|---|
| Nom UICPA | hexachlorobenzène |
| Synonymes |
perchlorobenzène, HCB |
| No CAS | |
| No ECHA | 100.003.886 |
| No CE | 204-273-9 |
| PubChem | 8370 |
| ChEBI | 5692 |
| SMILES | |
| InChI | |
| Apparence | poudre cristalline |
| Propriétés chimiques | |
| Formule | C6Cl6 [Isomères] |
| Masse molaire[1] | 284,782 ± 0,017 g/mol C 25,31 %, Cl 74,69 %, |
| Propriétés physiques | |
| T° fusion | 229,5 °C[2] |
| T° ébullition | 322,2 °C[2] |
| Solubilité | 0,01 mg·l-1 à 20 °C[2] |
| Masse volumique | 2,049 g·cm-3 à 20 °C[2] |
| Point d’éclair | 242 °C[2] |
| Précautions | |
| SGH[2] | |
| H350, H372 et H410 |
|
| Transport[2] | |
| Classification du CIRC | |
| Cancérogène du groupe 2B du CIRC | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L’hexachlorobenzène (HCB) est un composé chimique de formule C6Cl6. Il s'agit d'un composé organique aromatique dérivant formellement du benzène C6H6 par substitution des six atomes d'hydrogène par six atomes de chlore.
Propriétés physico-chimiques[modifier | modifier le code]
Il se présente sous forme d'une poudre blanche de cristaux incolores dont la masse volumique apparente est voisine de 0,8 g·cm-3[2].
Il est très faiblement soluble dans l'eau, mais l'est bien davantage dans le benzène C6H6, l'éthanol C2H5OH, l'éther diéthylique C2H5–O–C2H5 et le chloroforme CHCl3.
Utilisation[modifier | modifier le code]
Il a été utilisé comme fongicide avant d'être interdit par la convention de Stockholm sur les polluants organiques persistants[3].
Il s'agit d'un cancérogène probable pour l'homme[4] dont les effets sont avérés chez les animaux ; il fait partie des cancérogènes du groupe 2B du CIRC.
L'hexachlorobenzène continue à être produit pour la réalisation des caoutchoucs synthétiques, comme plastifiant du PVC, et pour la production du pentachlorophénol.
La production mondiale a atteint 10 000 tonnes par an en 1981.
En 1996, 4 000 tonnes étaient encore produites en tant que sous produit du perchloroéthylène, avant d'être détruites par incinération[5].
Le , Ségolène Royal, la Ministre de l'Écologie, s'est opposée au projet d'incinération en Isère, à Salaise-sur-Sanne, par la Société Tredi (appartenant au Groupe Séché), de 9 000 tonnes de déchets chimiques, hautement toxiques, de type HCB, en provenance d'Australie. Elle a refusé la demande préalable à l'importation, présentée par la société australienne Orica, en indiquant que le transport de déchets dangereux en provenance des antipodes constitue une aberration écologique[6].
Réglementation[modifier | modifier le code]
L'usage de l'hexachlorobenzène est interdit dans la communauté européenne depuis 1981[7] et la convention de Stockholm depuis 2001.
Production et synthèse[modifier | modifier le code]
La synthèse d'hexachlorobenzène peut être réalisée principalement de trois façons différentes. Tout d'abord, la chloration directe du benzène liquide par du chlore Cl2 gazeux conduit au C6Cl6. Cette chloration peut également être réalisée, en présence de chlorure de cuivre(II) CuCl2 comme catalyseur, par action du chlorure d'hydrogène HCl et de l'oxygène O2 gazeux sur le benzène :
Enfin, il peut également être obtenu à partir d'hexachlorocyclohexanes, mélange de stéréoisomères de formule brute C6H6Cl6 dont le lindane fait partie, par pyrolyse à haute température (de 350 à 600 °C) en présence de chlore Cl2 :
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Hexachlorobenzene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 24 septembre 2011 (JavaScript nécessaire)
- (en) STOCKHOLM CONVENTION ON PERSISTENT ORGANIC POLLUTANTS (POPs) « The 12 POPs under the Stockholm Convention ».
- (en) The Carcinogenic Potency Database (CPDB) « Hexachlorobenzene (CAS 118-74-1) ».
- « Hexachlorobenzene », INTERNATIONAL LABOUR ORGANISATION, WORLD HEALTH ORGANIZATION
- Ségolène Royal se dresse contre l'importation de déchets toxiques australiens, sur le site actu-environnement.com, consulté le 19 juillet 2014
- Directive 78/117/CEE du 21/12/78
Voir aussi[modifier | modifier le code]
- Cancérogène chimique
- Chlorobenzène
- Perturbateur endocrinien
- Fongicide
- Cancérogène du groupe 2B du CIRC
- Hexachlorure
- Polluant organique persistant au titre de la convention de Stockholm
- Polluant atmosphérique dangereux
- Polluant organique persistant au titre de la convention sur la pollution atmosphérique transfrontière à longue distance
- Tératogène présumé
- Embryotoxique présumé
- Perchlorocarbure



