Complexe majeur d'histocompatibilité
Le complexe majeur d'histocompatibilité (CMH) est, en immunologie, un système de reconnaissance du soi présent chez la plupart des vertébrés. On distingue les complexes majeurs d'histocompatibilité de classe I et de classe II. Chez l'être humain, on parle d'antigène HLA. Les molécules du CMH sont à la surface de toutes les cellules nucléées pour le CMH de classe I et sur les cellules présentatrices de l'antigène pour le CMH de classe II qui assurent la présentation de l'antigène aux lymphocytes T afin de les activer.
Il fut découvert en 1958 par Jean Dausset, qui fait la première description de ces antigènes à la surface des globules blancs sanguins (leucocytes) à partir de l'analyse de réactions d'agglutination obtenues avec des sérums de sujets immunisés à l'occasion de transfusions sanguines.
Principe[modifier | modifier le code]
Génétiquement, c'est un ensemble complexe de gènes (englobant le système HLA) localisés sur le chromosome 6 (chez l'humain), qui ne peut être identique chez deux individus (sauf vrais jumeaux) étant donné le nombre d'allèles et de configurations possibles (polymorphisme élevé). En effet, chaque individu à la naissance reçoit un haplotype paternel et un haplotype maternel, soit 6 allèles de CMH II et 12 allèles de CMH I.
Au niveau moléculaire, cette information génétique est exprimée notamment en protéines de surface. Les molécules de CMH I sont présentes sur toutes les cellules nucléées des vertébrés à mâchoires, à l'exception de certains tissus comme la cornée ou les glandes salivaires. Quant au CMH II, il est essentiellement présent sur les cellules présentatrices de l'antigène (lymphocytes B, macrophages, cellules dendritiques et sur les cellules épithéliales thymiques). Il est démontré depuis 2010 que les neurones expriment également des molécules de CMH I. Elles présentent l'antigène aux lymphocytes T cytotoxiques (TCD8) et servent avec les molécules de classe I non classiques de marqueur du soi (cellules faisant partie de l'organisme) pour les lymphocytes NK. Le CMH II permet à certains globules blancs de présenter des parties des corps intrus pour déclencher une réponse immunitaire.
Ces complexes participent aux réponses immunitaires, c'est la clef de l'immunité cellulaire et de la communication entre les cellules qui travaillent à la protection de l'organisme contre des agressions d'organismes pathogènes. Dans de rares cas, les peptides du CMH peuvent devenir à leur tour responsables de maladies auto-immunes indépendamment de l'immunité cellulaire.
Technique[modifier | modifier le code]
Les cellules présentatrices d'antigènes (CPA) expriment à leurs surface des structures polypeptidiques, soit le CMH I (« CMH de classe I »), soit les CMH I et CMH II (CMH de classe I et de classe II). L'association des deux permet de présenter le code peptidique d'un antigène du non-soi, qui sera reconnu par la suite par les lymphocytes et ou des macrophages (ce qui aura pour fonction de les activer en lançant la réaction immunitaire). Toutes les cellules nucléées possèdent le CMH I, quelques-unes (comme les cellules dendritiques) possèdent aussi le CMH II. Le facteur de transcription CIITA permet aux molécules du CMH II d'être synthétisées par certaines cellules comme les thymocytes, les cellules dendritiques, les monocytes et macrophages, les lymphocytes B et les granulocytes éosinophiles et basophiles[réf. nécessaire]. Dans des conditions particulières, certaines cellules épithéliales peuvent aussi exprimer le CMH II : exemple des cellules stromales ganglionnaires.
Association entre peptide antigénique et CMH[modifier | modifier le code]
Quelle que soit la classe de CMH, ces molécules ne sont stables que si elles sont associées au peptide logé dans sa poche. Des interactions faibles de type liaisons hydrogène et ioniques sont établies entre les résidus d’acide aminés de la cavité, appelés résidus d’ancrage, et ceux du peptide antigénique. Donc pour chaque poche à peptide, seul le peptide antigénique ayant les résidus d’ancrage capables d’établir de telles liaisons pourra s’y loger. Mais seuls quelques résidus d’acides aminés interviennent dans l’ancrage, donc plusieurs types de peptides peuvent se loger dans une molécule de CMH donnée. La liaison du CMH au peptide est dite dégénérée. Cette dégénérescence et l’expression de plusieurs types de molécules du CMH permettent aux cellules de présenter de nombreux peptides augmentant les chances de présenter un peptide antigénique aux lymphocytes T. Les antigènes peuvent se lier aux CMH II grâce aux agrétopes.
CMH de classe I[modifier | modifier le code]
Ce complexe permet de venir en aide à toute cellule défaillante touchée notamment par des agents pathogènes. Il est exprimé de manière ubiquitaire par toutes les cellules, à l'exception des érythrocytes. Le CMH de classe I est reconnu par les lymphocytes T CD8+.
CMH de classe II[modifier | modifier le code]
Ce complexe permet de contrer les cellules exogènes. Il est uniquement exprimé par des cellules présentatrices de l'antigène (CPA), telles que les cellules dendritiques, les macrophages, ou les lymphocytes B.
Structure[modifier | modifier le code]
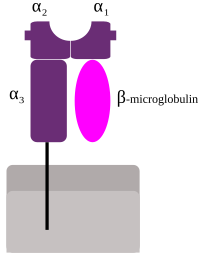
CMH de classe I : deux chaînes polypeptidiques α et β qui présentent toutes deux des domaines « immunoglobuline-like » et qui sont associées de manière non covalente
- la chaîne α est polymorphe ;
- la chaîne β est non polymorphe et elle est codée par un gène non présent dans le CMH.
Les molécules du CMH I sont constituées de quatre parties caractéristiques :
- une région de liaison au peptide antigénique ;
- une région immunoglobuline-like est formée par les domaines β2m et α3 et est la région qui fixe le CD8 ;
- une région transmembranaire qui est unique, la chaîne β2m ne présentant pas de segment transmembranaire ;
- une région intra-cytoplasmique qui est également unique pour les mêmes raisons que pour la région transmembranaire.
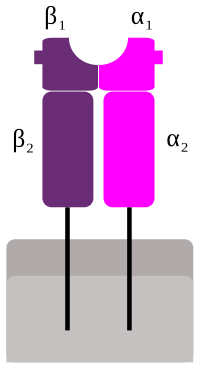
CMH de classe II : idem CMH de classe I
- la chaîne α est polymorphe ;
- la chaîne β est non polymorphe et codée par un gène présent dans le CMH (contrairement à la chaine β du CMH de classe I).
Les molécules du CMH II sont constituées de quatre parties caractéristiques :
- une région de liaison au peptide antigénique est formée par les domaines α1 et β1 qui forment une cavité dans laquelle ira se loger le peptide antigénique ;
- une région immunoglobuline like est formée par les domaines α2 et β2 est la région qui fixe le CD4 ;
- une région transmembranaire constituée de deux segments, un provenant de la chaîne α et l’autre de la chaîne β ;
- une région intra-cytoplasmique est également constituée de deux segments pour les mêmes raisons que la région transmembranaire.
