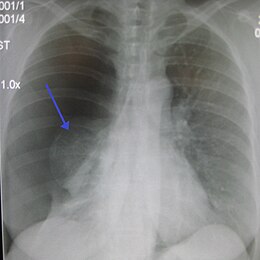
Pneumothorax
| Symptômes | Douleur thoracique, dyspnée et toux sèche (d) |
|---|
| Traitement | Drainage pleural, traitement conservateur (en) et Pleurodèse |
|---|---|
| Médicament | Talc |
| Spécialité | Médecine d'urgence, pneumologie et chirurgie thoracique |
| CISP-2 | R99 |
|---|---|
| CIM-10 | J93, P25.1, S27.0 |
| CIM-9 | 512, 860 |
| OMIM | 173600 |
| DiseasesDB | 10195 |
| MedlinePlus | 000087 |
| eMedicine |
424547 article/424547 article/360796 article/808162 article/827551 article/1003552 |
| MeSH | D011030 |
| Patient UK | Pneumothorax-pro |
En médecine (pneumologie), un pneumothorax est une affection de la plèvre, mettant en communication l'espace pleural et l’atmosphère (accolement de la plèvre pariétale et viscérale ; on parle de séreuses, qui tapissent respectivement la cage thoracique et les poumons). Le poumon s’affaisse alors avec des conséquences respiratoires et hémodynamiques parfois graves (notamment en cas de pneumothorax bilatéral ou suffoquant) et urgentes pouvant aller jusqu'à la mort.
Causes[modifier | modifier le code]



Le pneumothorax est soit spontané soit traumatique. Lorsqu’il survient chez un patient sans maladie identifiable connue, il est dit « primaire » ; si le patient présente une maladie sous-jacente en rapport avec le pneumothorax, il est alors dit « secondaire ». Beaucoup de pneumothorax spontanés primaires sont, en fait, de petites lésions pulmonaires (emphysème local[1]) non diagnostiquées auparavant.
Pneumothorax spontanés[modifier | modifier le code]
Primaires[modifier | modifier le code]
L’incidence est de 8 à 18 cas sur 100 000 chez les hommes et de 2 à 6 cas sur 100 000 chez les femmes.
Dans la plupart des cas, ce type de maladie est idiopathique. Il survient principalement chez les personnes jeunes (entre 15 et 40 ans), fumeuses[2] et le plus souvent de sexe masculin, et d'aspect longiligne.
Dans la structure du poumon, des alvéoles peuvent se rompre et laisser de l’air se collecter sous la plèvre viscérale formant ce que l’on appelle un « bleb » ou « bulle sous-pleurale emphysémateuse ». Quand, pour une raison connue ou non, un ou plusieurs de ces blebs se rompent, il se crée un pneumothorax. Ces blebs sont souvent localisés au niveau de l'apex du poumon, en quantité plus ou moins importante et parfois sur les deux (forme bilatérale).
Un pneumothorax survient généralement chez les sujets jeunes de grande taille. Il n'est pas favorisé par un effort à glotte fermée conformément à une croyance communément admise (selon le collège des enseignants de pneumologie).
D'autres facteurs de risque existent comme les variations brutales de la pression atmosphérique, les conditions climatiques, les expositions à des sons soutenus, répétés et à basse fréquence ; des formes familiales existent et sont liées à des mutations génétiques connues.
Secondaires[modifier | modifier le code]
Broncho-pneumopathie chronique obstructive (BPCO)[modifier | modifier le code]
Un pneumothorax peut arriver chez des personnes souffrant d'insuffisance respiratoire chronique, et de maladies broncho-pulmonaires obstructives. À la suite des quintes de toux répétitives, l'élasticité de la plèvre perd de son efficacité. Ces atteintes entraînent, sur le long terme, des lésions de la membrane pulmonaire.
Ces états pathologiques ou maladies sont responsables de plus de la moitié des pneumothorax spontanés secondaires[3] et augmentent le risque de récidives[4].
Les maladies infectieuses[modifier | modifier le code]
- Syndrome d’immunodéficience acquise : ils sont habituellement dus à des pneumopathies à Pneumocystis carinii. Mais des infections à cytomégalo-virus et à mycobactéries sont aussi retrouvées ainsi que des syndromes de Kaposi
- Tuberculose
- Toutes les infections bactériennes, mycosiques et parasitaires
Tumeurs[modifier | modifier le code]
Toute rupture d’une lésion maligne située dans le poumon peut occasionner un pneumothorax.
Cataménial[modifier | modifier le code]
Ce sont des pneumothorax qui surviennent avec les règles. La plupart sont situés à droite. Ils récidivent parfois pendant plusieurs années avant d’être diagnostiqués. Ils sont liés à la localisation ectopique (ailleurs qu'à l'endroit habituel) d'endomètre (tissu utérin) dans le poumon (endométriose). Cette cause peut être retrouvée jusque chez près d'un tiers des patientes faisant un pneumothorax, avec une atteinte diaphragmatique très fréquente[5].
Divers[modifier | modifier le code]
Il peut être d'origine génétique : mucoviscidose, maladie de Marfan, Syndrome d'Ehlers-Danlos.
D'autres maladies peuvent se compliquer d'un pneumothorax : sarcoïdose, asthme, histiocytose X, lymphangioleiomyomatose et autres maladies de système ou auto-immunes…
Pneumothorax traumatiques[modifier | modifier le code]
L'air passe alors par effraction du poumon vers l'espace pleural (entre les 2 feuillets qui constituent la plèvre), le feuillet viscéral (recouvrant le poumon) pouvant être lésée par plaie directe ou par une fracture de côtes.
Iatrogènes[modifier | modifier le code]
Il résulte d'une complication d'un acte médical, lors de l'effraction de la plèvre et du poumon par une aiguille lors de la pose d'une voie veineuse centrale par cathétérisme des veines sous-clavières, lors d'une biopsie trans-thoracique ou plus rarement au cours d'une ventilation assistée mal réglée ou sous de fortes pressions[6].
Le pneumothorax iatrogénique est reconnu dans la littérature scientifique comme la plus fréquente des complications sévères de l’acupuncture[7],[8], mais il reste un événement très rare.
Non iatrogènes[modifier | modifier le code]
Traumas thoraciques fermés (fractures des côtes)[6] ou avec plaie pénétrante (couteau, arme à feu).
Pneumothorax thérapeutique[modifier | modifier le code]
Le pneumothorax thérapeutique consiste à provoquer volontairement un pneumothorax dans le but de guérir une maladie. C'était le cas de la tuberculose, que l'on traitait de cette manière jusqu'aux années 1950. La technique appelée collapsothérapie fut inventée par Forlanini en 1888. Elle permettait de faire cicatriser la plèvre lésée par les mouvements de la respiration et la création de cavernes tuberculeuses[9].
Symptômes[modifier | modifier le code]
Suivant l'importance, il peut se manifester par une simple douleur thoracique isolée, avec ou sans essoufflement (dyspnée) ou se traduire par un tableau de détresse respiratoire aiguë. Un pneumothorax peut aussi se manifester, s'il est situé sur la partie supérieure du poumon, par une douleur s'apparentant à une douleur intercostale, située de part et d'autre de l’omoplate. Si la douleur vient à s'accentuer, il est aussi possible qu'elle se ressente comme une pression violente sur le poumon, provoquant l'essoufflement et une perte de connaissance temporaire.
À l'examen[modifier | modifier le code]
À l'inspection, on peut noter une baisse de l’ampliation (voire une immobilité) du thorax du côté atteint.
Le murmure vésiculaire est classiquement diminué ou aboli du côté atteint.
La transmission des vibrations vocales est abolie sur l'hémithorax atteint.
La percussion du côté du thorax atteint montre un tympanisme (bruit creux).
Examens complémentaires[modifier | modifier le code]
La radiographie du thorax de face permet de faire, en règle générale, le diagnostic, sous forme d'une clarté d'un sommet (ou péri hilaire dans les cas plus important) avec visualisation d'un fin liseré convexe vers le haut, correspondant au poumon rétracté. Dans les cas difficiles, on peut s'aider d'une radiographie prise en expiration. La présence simultanée d'un épanchement liquidien donne l'aspect de niveau hydro-aérique rectiligne horizontal caractéristique.
L'échographie permet également de détecter un pneumothorax (méthode dite eFAST, extended focused assessment with sonography for trauma).
Physiopathologie[modifier | modifier le code]
En temps normal, le poumon adhère à la paroi thoracique par l'existence d'une pression négative entre les deux feuillets de la plèvre. À la suite de l'irruption d'air dans l'espace pleural, le poumon se trouve décollé de la paroi et rétracté dans le thorax en région hilaire (au niveau du hile du poumon). La conséquence est que la ventilation du côté est diminuée voire nulle.
Les symptômes dépendent du degré d’affaissement du poumon et de la fonction respiratoire du patient. Le poumon en s’affaissant affecte la capacité du patient à respirer, il peut donc avoir de la difficulté à respirer (dyspnée) à l’effort ou au repos. La plèvre est richement innervée, le patient peut donc avoir mal et tousser.
Premiers soins[modifier | modifier le code]
Il nécessite une prise en charge en urgence pour juger de son importance et de la conduite de son traitement.
La mise sous oxygène peut être utile s'il est mal toléré, éventuellement guidé par la mesure de la saturation sanguine en oxygène (SaO2).
Les formes graves peuvent nécessiter une surveillance des constantes vitales.
Bien que la radiologie ne détecte pas toujours les pneumothorax, la première ligne de soin exige une radio de face en respiration normale puis, si le cliché est non contributif en inspiration forcée, une tomodensitométrie (scanner) si poumon pathologique.
Traitement[modifier | modifier le code]
La prise en charge des pneumothorax spontanés a fait l'objet de la publication de recommandations par l'« American College of Chest Physicians » en 2001[10], celles, anglaises, de 2010[11].
Le traitement est adapté à la symptomatologie, à l’étendue du pneumothorax et à l’état du poumon sous-jacent.
Le traitement peut en être parfois médical, mais son règlement définitif ne sera souvent que chirurgical. Le traitement envisagé dépendra de la sévérité des symptômes et de la maladie sous-jacente.
Le pneumothorax spontané de faible abondance guérit spontanément en 2 ou 3 semaines. Des antalgiques et du repos sont prescrits.
Dans tous les cas l'arrêt du tabagisme est fortement conseillé, avec une réduction du risque de récidive[12].
Le traitement conservateur[modifier | modifier le code]
C'est la surveillance simple du patient et de son pneumothorax.
Elle est fondée sur la constatation que la cavité pleurale réabsorbe spontanément l’air au rythme de 2,2 % du volume de l’hémithorax par jour[13]. La mise sous oxygène accélère cette résorption[14]. Elle nécessite souvent une hospitalisation initiale de 24 h, puis le patient peut retourner à son domicile en étant suivi régulièrement.
Elle est réservée aux pneumothorax de faible volume chez des patients asymptomatiques. Le risque est la survenue d’une complication (pneumothorax compressif). La nécessité d’une surveillance rapprochée prolongée est aussi un désavantage.
L’exsufflation à l’aiguille[modifier | modifier le code]
Il s’agit d’évacuer l’air avec un petit cathéter relié à une aspiration d’air. La méthode est plus simple que le drainage, avec une durée d'hospitalisation moindre[15], certaines procédures pouvant même être faites aux urgences, sans nécessité d'une hospitalisation dans la foulée[16]. Le lieu de la ponction est le deuxième espace intercostal sur la ligne médio-claviculaire[17]. Le succès de la procédure est contrôlé par une première radiographie du thorax montrant la disparition du pneumothorax et un second cliché quelques heures après afin de vérifier l'absence de récidive précoce[17]. Le risque d'infection existe, cette intervention doit être réalisée en milieu médicalisé dans des règles d'asepsie rigoureuses. L'indication type est le pneumothorax spontané non récidivant[17], avec des résultats à court et moyen termes équivalents à ceux d'un drainage[18].
Le drainage thoracique[modifier | modifier le code]
C’est la technique la plus utilisée et la plus efficace de première intention. Elle consiste à placer un drain thoracique en aspiration dans la cavité pleurale. Elle assure la réexpansion du poumon et favorise la cicatrisation.
Une fuite d’air prolongée (plus de 4-7 jours) nécessitera une chirurgie. Si le patient présente un haut risque anesthésique, un drainage prolongé peut être envisagé, éventuellement accompagné d’une pleurodèse.
Une solution intermédiaire consiste à connecter le drain à une valve anti-retour, permettant la sortie immédiate du patient ainsi. Les résultats sont équivalents à ceux d'un drainage[19] mais avec un risque supérieur d'accidents[20].
La pleurodèse[modifier | modifier le code]
Il s’agit de « coller » les deux plèvres (pariétale et viscérale) l’une contre l’autre en créant une forte réaction inflammatoire. Cette réaction est créée le plus souvent en injectant dans la cavité pleurale une substance irritante comme du talc, des tétracyclines ou du sang autologue.
Les taux de récidive après tentative de pleurodèse par tétracycline sont de 13 % et de 8 % en cas d'usage du talc[21].
L'usage de talc comme agent dans cet acte médical n'augmenterait pas l'incidence de cancer de poumon ou de la plèvre dans la population générale d'après des recherches, d'autant que ces préparations sont réglementées par les différentes agences du médicaments et sont dépourvues d'amiante et d'autres impuretés[22].
La chirurgie[modifier | modifier le code]
Son but principal est d’éviter les récidives. Pour éviter les récidives à court terme les lésions pulmonaires (blebs, bulles) sont réséquées chirurgicalement en utilisant des agrafeuses mécaniques. La coagulation des blebs et bulles, par laser ou bistouri électrique, si elle permet de contrôler les fuites d’air et les saignements, est néanmoins entachée d’un taux de récidive allant jusqu’à 25 %.
Les récidives à moyen terme sont prévenues en réalisant l’oblitération de la cavité pleurale avec un principe analogue à la pleurodèse. Les moyens utilisés sont principalement la pleurectomie (ablation de la plèvre pariétale) et l’abrasion pleurale mécanique (la plèvre est frottée avec un tampon). Des substances irritantes sont utilisées par certains de manière complémentaire comme le talc, l’alcool iodé, ou les tétracyclines.
Le choix de la voie d’abord se fait habituellement entre la thoracoscopie vidéo-assistée et une petite thoracotomie, les deux techniques étant équivalentes au point de vue résultats[23].
Le taux de récidive est faible, après chirurgie il est en général inférieur à 2 %.
Les indications[modifier | modifier le code]
La chirurgie est proposée à tout pneumothorax récidivant dès la première récidive.
Le premier épisode de pneumothorax peut bénéficier d’une chirurgie dans les indications suivantes :
- l’absence de ré expansion du poumon malgré un drainage bien conduit ;
- la fuite d’air prolongée,
- le pneumothorax compressif : Il faut éviter que le patient récidive en faisant un nouveau pneumothorax compressif qui mettrait sa vie en danger s'il était loin de toute structure sanitaire,
- le pneumothorax bilatéral : Il faut éviter que le patient récidive en faisant un nouveau pneumothorax bilatéral qui lui aussi mettrait sa vie en danger s'il était loin de toute structure sanitaire,
- l’hémothorax non résolu par le drainage thoracique : L’intervention est nécessaire pour faire cesser le saignement,
- grosse bulle unique : La bulle comprime le poumon adjacent qui n’est donc pas utilisé à sa capacité normale, elle doit donc être enlevée,
- certaines professions comme pilote de chasse, plongeur sous-marin professionnel, sportif de haut niveau : La récidive du pneumothorax pendant l’exercice de leur profession représente un risque vital pour ces patients.
Avant l’intervention[modifier | modifier le code]
La consultation et l’avis de l’anesthésiste est obligatoire et indispensable.
La fibroscopie bronchique est intéressante pour exclure une lésion endobronchique, cancéreuse chez des patients tabagiques, ou pouvant empêcher la ré-expansion du poumon.
Le scanner thoracique permet de faire le bilan des blebs et des bulles des 2 poumons, de dépister une éventuelle tumeur pulmonaire et de connaître l’état du poumon sous-jacent.
Les complications[modifier | modifier le code]
Elles peuvent être de survenue immédiate, de résistance au traitement ou survenir après le traitement.
Survenue immédiate[modifier | modifier le code]
Le pneumothorax compressif[modifier | modifier le code]
C’est une complication grave, non traitée elle peut être rapidement mortelle. Il survient dans 2 à 3 % des cas. L’air qui rentre dans la cavité pleurale à l’inspiration ne peut plus en sortir à l’expiration habituellement sur un mécanisme de valve anti-retour. La pression augmente dans la plèvre comprimant le poumon (détresse respiratoire) et le cœur (détresse cardio-vasculaire). Le traitement consiste en une décompression urgente par insertion d'une aiguille ou d'un drain dans la cavité pleurale.
Le pneumothorax bilatéral[modifier | modifier le code]
Il survient de manière simultanée chez 1 % des pneumothorax et nécessite un traitement d’urgence par un drainage thoracique en aspiration des deux cavités pleurales.
L’hémothorax[modifier | modifier le code]
Parfois des adhérences (« brides ») se sont développées entre la plèvre pleurale et pariétale. Lors du pneumothorax si l’une d’entre elles se déchire, elle peut saigner dans la cavité pleurale, c’est l’hémothorax.
Le pneumo-médiastin[modifier | modifier le code]
L’air du pneumothorax va aller disséquer les tissus du médiastin.
Résistance au traitement[modifier | modifier le code]
Lorsqu’elles sont drainées la plupart des fuites d’air se tarissent en 2 jours. Malgré un drainage adéquat le poumon peut ne pas se ré-expandre ou la fuite peut persister plus de 7 jours.
Survenue après traitement[modifier | modifier le code]
Même si elle est classée parmi les complications, la récidive, alors qu'il n'y a pas eu de traitement chirurgical, n’est pas à proprement parler une complication mais plutôt un des aspects de l’évolution « normale » ou habituelle de l’histoire naturelle du pneumothorax.
Le risque de récidive du pneumothorax spontané homolatéral (du même côté) est de 20 à 50 % à deux ans après un premier épisode et de plus de 50 % après le deuxième épisode et augmente encore après le troisième épisode.
Le risque de pneumothorax spontané controlatéral est de 12 %.
Historique[modifier | modifier le code]
Jean Itard, un étudiant de René Laennec, a pour la première fois identifié un pneumothorax en 1803, et Laennec lui-même en décrivit l'image clinique complète en 1819.
Références[modifier | modifier le code]
- Bense L, Lewander R, Eklund G, Hedenstierna G, Wiman LG, Nonsmoking, non-alpha 1-antitrypsin deficiency-induced emphysema in nonsmokers with healed spontaneous pneumothorax, identified by computed tomography of the lungs, Chest, 1993;103:433-8
- Bense L, Eklund G, Wiman LG, Smoking and the increased risk of contracting spontaneous pneumothorax, Chest, 1987;92:1009-12
- Bintcliffe O, Maskell N, Spontaneous pneumothorax, BMJ, 2014;348:g2928
- Lippert HL, Lund O, Blegvad S, Larsen HV, Independent risk factors for cumulative recurrence rate after first spontaneous pneumothorax, Eur Respir J, 1991;4:324-31
- Alifano M, Roth T, Broet SC, Schussler O, Magdeleinat P, Regnard JF, Catamenial pneumothorax: a prospective study, Chest, 2003;124:1004-8.
- Leigh McCutcheon et Michael Yelland, « Iatrogenic pneumothorax: Safety concerns when using acupuncture or dry needling in the thoracic region », Physical Therapy Reviews, vol. 16, , p. 126–132 (DOI 10.1179/1743288X11Y.0000000012, lire en ligne, consulté le ).
- Marc Gozlan, « Quand l’acupuncture fait pschitt, littéralement », Réalités Biomédicales, (lire en ligne, consulté le ).
- Xiaoming Ying, Peng Wang, Peng Xu et Bo Zhu, « Pneumothorax associated with acupuncture: A systematic review and analysis », Acupuncture and Related Therapies, vol. 4, no 4, , p. 17–25 (DOI 10.1016/j.arthe.2016.11.002, lire en ligne, consulté le ).
- Association des Amis du Patrimoine Médical de Marseille – Pneumothorax artificiel pour tuberculose pulmonaire.
- Baumann MH, Strange C, Heffner JE et al. Management of spontaneous pneumothorax: an American College of Chest Physicians Delphi consensus statement, Chest, 2001;119:590-602
- MacDuff A, Arnold A, Harvey J, Management of spontaneous pneumothorax: British Thoracic Society Pleural Disease Guideline 2010, Thorax, 2010;65:ii18-ii31
- Sadikot RT, Greene T, Meadows K, Arnold AG, Recurrence of primary spontaneous pneumothorax, Thorax, 1997;52:805-9
- (en) Kelly AM, Loy J, Tsang AY, Graham CA, « Estimating the rate of re-expansion of spontaneous pneumothorax by a formula derived from computed tomography volumetry studies », Emerg Med J. 2006;23:780-2.
- (en) Northfield TC, « Oxygen therapy for spontaneous pneumothorax », BMJ 1971;4:86-8.
- Zehtabchi S, Rios CL, Management of emergency department patients with primary spontaneous pneumothorax: needle aspiration or tube thoracostomy?, Ann Emerg Med, 2008;51:91-100
- Ho KK, Ong ME, Koh MS, Wong E, Raghuram J, A randomized controlled trial comparing minichest tube and needle aspiration in outpatient management of primary spontaneous pneumothorax, Am J Emerg Med, 2011;29:1152-1157
- Pasquier M, Hugli O, Carron PN, Needle aspiration of primary spontaneous pneumothorax, N Engl J Med, 2013;368:e24
- Wakai A, O'Sullivan RG, McCabe G, Simple aspiration versus intercostal tube drainage for primary spontaneous pneumothorax in adults, Cochrane Database Syst Rev, 2007;1:CD004479-CD004479
- Brims FJ, Maskell NA, Ambulatory treatment in the management of pneumothorax: a systematic review of the literature, Thorax, 2013;68:664-669
- Hallifax RJ, McKeown E, Sivakumar P et al. Ambulatory management of primary spontaneous pneumothorax: an open-label, randomised controlled trial, Lancet, 2020;396:39-49
- Almind M, Lange P, Viskum K, Spontaneous pneumothorax: comparison of simple drainage, talc pleurodesis, and tetracycline pleurodesis, Thorax, 1989;44:627-30
- (en) S. Gyorik, S. Erni, U. Studler et R. Hodek-Wuerz, « Long-term follow-up of thoracoscopic talc pleurodesis for primary spontaneous pneumothorax », European Respiratory Journal, vol. 29, no 4, , p. 757–760 (ISSN 0903-1936 et 1399-3003, DOI 10.1183/09031936.00122106, lire en ligne, consulté le )
- Foroulis CN, Anastasiadis K, Charokopos N et al. A modified two-port thoracoscopic technique versus axillary minithoracotomy for the treatment of recurrent spontaneous pneumothorax: a prospective randomized study, Surg Endosc, 2012;26:607-14