Tétrafluoroborate d'argent
| Tétrafluoroborate d'argent | |||
| |||
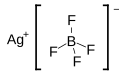
| Structure du tétrafluoroborate d'argent | |||
| Identification | |||
|---|---|---|---|
| No CAS | |||
| No ECHA | 100.034.491 | ||
| No CE | 237-956-5 | ||
| No RTECS | ED2875000 | ||
| PubChem | 159722 | ||
| SMILES | |||
| InChI | |||
| Apparence | solide blanc cristallisé soluble dans l'eau faiblement odorant[1] | ||
| Propriétés chimiques | |||
| Formule | AgBF4 |
||
| Masse molaire[2] | 194,673 ± 0,007 g/mol Ag 55,41 %, B 5,55 %, F 39,04 %, |
||
| Propriétés physiques | |||
| T° fusion | 70 à 73 °C[1] | ||
| Solubilité | très soluble dans l'eau[1] | ||
| Précautions | |||
| SGH[1] | |||
| H314, P280, P301+P330+P331, P305+P351+P338 et P309+P310 |
|||
| Transport[3] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Le tétrafluoroborate d'argent est un composé chimique de formule AgBF4. C'est un sel d'argent et d'acide tétrafluoroborique HBF4. Il se présente sous la forme d'un solide blanc hygroscopique, soluble dans l'eau, sensible à la lumière et quasiment dépourvu d'odeur.
Le tétrafluoroborate d'argent peut être obtenu en faisant réagir du trifluorure de bore BF3 avec de l'oxyde d'argent(I) Ag2O dans le benzène, ce qui donne également du métaborate d'argent[4] AgBO2 :
Le tétrafluoroborate d'argent est utilisé comme catalyseur pour des réactions de nitration, d'acylation et de sulfonation. Sa propension à former des complexes avec les alcènes et les hydrocarbures aromatiques est mise à profit dans les processus de séparation de ces composés. Dans le dichlorométhane CH2Cl2, c'est un oxydant modéré[5]. Comme l'hexafluorophosphate d'argent, il est couramment employé pour remplacer des anions halogénure ou des ligands par des anions tétrafluoroborate BF4− faiblement coordinants ; l'élimination de l'halogénure est favorisée par la formation du précipité de l'halogénure d'argent correspondant.
Notes et références[modifier | modifier le code]
- Entrée « Silver tetrafluoroborate » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 18 juin 2018 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé Silver tetrafluoroborate ≥99.99% trace metals basis, consultée le 18 juin 2018.
- (de) Andreas J. Wagner et Philipp von den Hoff, Darstellung von Silber(I)tetrafluoroborat(III) Ag(BF4), 26 juillet 2004, [PDF] 202 Ko.
- (en) Neil G. Connelly et William E. Geiger, « Chemical Redox Agents for Organometallic Chemistry », Chemical Reviews, vol. 96, no 2, , p. 877-910 (PMID 11848774, DOI 10.1021/cr940053x, lire en ligne)


