Bilharziose
| Causes | Schistosoma |
|---|---|
| Symptômes | Hématurie, diarrhée, nausée et frissonnement (en) |
| Spécialité | Infectiologie |
|---|
| CISP-2 | D96 |
|---|---|
| CIM-10 | B65{{{2}}} |
| CIM-9 | 120 |
| DiseasesDB | 11875 |
| MedlinePlus | 001321 |
| eMedicine | 228392 |
| MeSH | D012552 |
| Patient UK | Schistosomiasis-pro |
La bilharziose ou schistosomiase est une maladie parasitaire due à un ver hématophage, le schistosome. Elle est présente dans les zones tropicales et subtropicales : en Afrique, en Amérique du Sud, en Asie et dans le Bassin méditerranéen.
La maladie se propage par contact avec de l'eau douce contaminée par les schistosomes. Ces parasites sont souvent libérés par des excréments d'escargots d'eau douce infectés. La maladie est particulièrement fréquente chez les enfants des pays en développement, car ils sont plus susceptibles de jouer dans de l'eau contaminée. Les autres groupes à haut risque comprennent les agriculteurs, les pêcheurs et les personnes utilisant de l'eau insalubre au quotidien. La maladie appartient au groupe des infections helminthiques. Le diagnostic consiste à trouver des œufs du parasite dans l'urine ou les selles d'une personne. Il peut également être confirmé en trouvant des anticorps contre la maladie dans le sang.
Les méthodes de prévention de la maladie comprennent l'amélioration de l'accès à l'eau potable et la réduction du nombre d'escargots. Dans les régions où la maladie est courante, le médicament praziquantel (nom commercial : Biltricide) peut être administré une fois par an à l'ensemble du groupe. Ceci est fait pour diminuer le nombre de personnes infectées et, par conséquent, la propagation de la maladie. Le praziquantel est également le traitement recommandé par l'Organisation mondiale pour la santé pour les personnes infectées.
La bilharziose est la deuxième endémie parasitaire mondiale après le paludisme avec une prévalence de 180 millions d’individus affectés, pour environ 280 000 décès chaque année. La morbidité observée chez les populations humaines infectées est essentiellement liée à l’étonnante fécondité du parasite femelle dont les œufs, pondus par centaines chaque jour, sont piégés dans de nombreuses muqueuses et tissus formant des granulomes.
Le ver responsable de la bilharziose a été découvert au Caire en 1852, par le pathologiste allemand Theodor Bilharz[1].
Taxonomie[modifier | modifier le code]

Les bilharzioses humaines décrites en Égypte par Theodor Bilharz[2],[3], sont dues à un ver hématophage, le schistosome, appartenant à l’embranchement des Plathelminthes (vers plats non segmentés), à la classe des Trématodes (appareil digestif avec cæcum), à l’ordre des Strigeatida (ventouses ventrale et buccale), à la famille des Schistosomatidés (cercaires libres) et enfin au genre Schistosoma, car l’hôte définitif est un mammifère.
Le genre Schistosoma comporte 18 espèces dont cinq sont pathogènes pour l’Homme :
- Schistosoma mansoni : bilharziose intestinale aux Antilles et en Amérique centrale ;
- Schistosoma haematobium : bilharziose urogénitale en Afrique, Inde et Péninsule Arabique ;
- Schistosoma intercalatum : bilharziose rectale et génitale en Afrique centrale ;
- Schistosoma japonicum : bilharziose intestinale avec complications artério-veineuses en Chine, Japon et Thaïlande ;
- Schistosoma mekongi : bilharziose intestinale avec complications artério-veineuses en Chine, Japon, Cambodge[4] et Thaïlande.
Cycle de vie du schistosome[modifier | modifier le code]
Le schistosome se développe au cours d’un cycle dixène gonochorique où l’hôte intermédiaire est un mollusque d’eau douce, spécifique de chaque espèce de schistosome (Biomphalaria glabrata dans le cas de S. mansoni), et l’hôte définitif un mammifère (homme, rat, bœuf).
Épidémiologie[modifier | modifier le code]
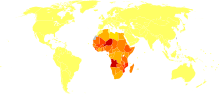
- données inconnues
- <50
- 50-75
- 75-100
- 100-150
- 150-200
- 200-250
- 250-300
- 300-350
- 350-400
- 400-450
- 450-500
- >500
De l'Antiquité au début du XXe siècle, le symptôme de la schistosomiase, à savoir la présence de sang dans l'urine, était si fréquent qu'il était considéré comme une version masculine de la menstruation en Égypte et était donc considéré comme un rite de passage pour les garçons[5],[6],[7].
C'est la seconde endémie parasitaire mondiale après le paludisme avec une prévalence de 180 millions d’individus affectés, pour environ 280 000 décès chaque année[8]. En Europe, une enquête épidémiologique a constaté la présence d'un hybride de Schistosoma haematobium et Schistosoma bovis dans une rivière du sud de la Corse, le Cavu, depuis 2011[9],[10]. Le réservoir naturel n'est à ce jour pas identifié, mais pourrait être un rat[10].
Pathologie[modifier | modifier le code]
Les manifestations pathologiques observées au cours de l’infection par S. mansoni sont essentiellement liées à la formation de granulomes autour des œufs piégés dans les tissus. Le granulome est la conséquence d’une réaction inflammatoire de type hypersensibilité retardée, provoquée par le dépôt des œufs dans le tissu hépatique[11], se traduisant par un afflux de cellules inflammatoires telles que les éosinophiles, les macrophages et les lymphocytes. Ces cellules sont progressivement remplacées par des fibroblastes producteurs de protéines matricielles (collagène) dont l’accumulation va constituer un nodule fibreux. L’évolution en fibrose cicatricielle provoque une hypertension portale responsable de l’hépatomégalie. Une circulation collatérale peut se développer, avec formation de varices œsophagiennes, dont la rupture peut provoquer des hémorragies mortelles.
Réponse immunitaire au cours de l’infection[modifier | modifier le code]
Des études ont révélé l’existence d’une dichotomie de la réponse immunitaire, essentiellement fondée sur la production de cytokines par les lymphocytes T (CD4+ et CD8+). Des travaux initiaux, réalisés chez la souris ont mis en évidence une réponse de type 1 (Th1/Tc1), caractérisée par la production d’IL-2 et d’IFN-γ, et de type 2 (Th2/Tc2), caractérisée par la production d’IL-4, -5, -10 et -13[12]. La réponse immune apparaît alors comme une balance dont l’équilibre peut être rompu par la sécrétion de cytokines immunorégulatrices (IL-12 et IFN-γ pour un profil de type 1, IL-4 et IL-10 pour un profil de type 2).
Dans le modèle de la schistosomiase murine, il a été montré qu’une réponse de type Th1 se développe, dirigée contre les formes larvaire et adulte du parasite, et caractérisée par la production d’IFN-γ et d’IL-2 par les lymphocytes T CD4+. La réponse humorale est également polarisée vers un profil Th1 puisque sont détectées majoritairement des immunoglobulines d'isotypes IgG2a et IgG2b. Cependant, cette réponse immune reste faible. Ce phénomène pourrait être lié au fait que les stades cutanés interfèrent avec les fonctions immunostimulantes des DCs. À titre d’exemple, une étude a montré que le schistosomule était capable d’inhiber la migration des cellules de Langerhans vers les ganglions lymphatiques par la production d’une prostaglandine, la PGD2[13],[14]. Par la suite, le dépôt des œufs dans les tissus par les vers femelles induit une réorientation de la réponse immune, spécifique et non spécifique vers une forte réponse Th2. Cette réponse est caractérisée par la production d’IL-4, IL-5, IL-10 et IL-13. Des immunoglobulines d'isotypes IgG1 et IgE, marqueurs d’un profil Th2, sont également détectées. Les mécanismes précoces responsables de l’induction de la réponse Th2 par les œufs du schistosome sont cependant encore mal connus. Il est possible que des cellules dendritiques régulatrices (CD11c low) puissent avoir un rôle important.
Symptômes[modifier | modifier le code]

La bilharziose est une maladie chronique. De nombreuses infections sont symptomatiques subcliniques, avec une légère anémie et de la malnutrition étant commun dans les zones endémiques. Une schistosomiase aiguë (fièvre de Katayama) pourrait survenir des semaines après l'infection initiale, en particulier par S. mansoni et S. japonicum. Les manifestations comprennent :
- douleurs abdominales ;
- toux ;
- diarrhée ;
- éosinophilie — population de granulocytes éosinophiles extrêmement élevée (globules blancs) ;
- fièvre ;
- fatigue ;
- hépatosplénomégalie — l'élargissement du volume du foie et de la rate. La schistosomiase hépatique est la deuxième cause la plus fréquente de varices œsophagiennes à travers le monde ;
- lésions génitales — lésions qui augmentent la vulnérabilité à l'infection par le VIH. Les lésions causées par la schistosomiase peuvent continuer à être un problème après le contrôle de la schistosomiase elle-même. Un traitement précoce, en particulier des enfants, ce qui est relativement peu coûteux, empêche la formation des plaies ;
- symptômes cutanés : au début de l'infection, une légère démangeaison et une dermatite papuleuse des pieds et d'autres parties après la baignade dans les rivières polluées contenant des cercaires.
- hématurie (sang dans les urines) est le signe classique de la schistosomiase urogénitale[15].
Parfois, des lésions du système nerveux central peuvent se produire : la maladie granulomateuse cérébrale peut être causée par des œufs ectopiques de S. japonicum dans le cerveau et des lésions granulomateuses autour des œufs extra-utérins dans la moelle épinière. Les infections à S. haematobium et S. mansoni peuvent entraîner une myélite transverse avec paraplégie flasque.
L'infection peut provoquer des réactions granulomateuses et la fibrose dans les organes touchés, ce qui peut entraîner des manifestations qui incluent :
- polypose colique avec diarrhée sanglante (S. mansoni la plupart du temps) ;
- hypertension portale avec hématémèse et une splénomégalie (S. mansoni, S. japonicum) ;
- Cystite et urétérite (S. haematobium) avec hématurie, qui peut évoluer en cancer de la vessie (carcinome épidermoïde) ;
- hypertension artérielle pulmonaire (S. mansoni, S. japonicum, plus rarement S. haematobium) ;
- glomérulonéphrite ;
- et lésions du système nerveux central.
Le cancer de la vessie et la mortalité sont généralement élevés dans les régions touchées.
Diagnostic[modifier | modifier le code]
Le parasite peut être mis en évidence avec un examen parasitologique des selles ou des urines. La sérologie[16] est une méthode de diagnostic indirect.
La sensibilité limitée[17] de la détection des œufs et des tests immunologiques est pertinente en particulier dans les régions à faible prévalence et à faible intensité d'infection, mais peut être surmontée par de nouveaux tests[18] reposant sur des diagnostics moléculaires comme la PCR et la LAMP. Malheureusement, le prix de ces techniques empêche généralement leur utilisation dans des environnements pauvres et il existe donc un besoin urgent de nouveaux tests, sensibles, spécifiques et peu coûteux qui répondent aux caractéristiques ASSURED de l'OMS[19] pour le diagnostic des maladies de la pauvreté.
Traitement[modifier | modifier le code]
L’antimoine a été utilisé dans le passé pour traiter cette maladie. À faible dose, il se fixe aux atomes de soufre des enzymes du parasite et le tue sans affecter l’hôte. Depuis quelques années, les sujets atteints de la bilharziose sont traités par une prise annuelle d’une dose de praziquantel[20],[21]. L’accès au praziquantel constitue néanmoins une limitation majeure. Selon les données disponibles en janvier 2012, moins de 14 % des personnes ayant besoin du traitement en bénéficient[22].
Comme c’est le cas pour la majorité des maladies parasitaires, la communauté scientifique s’attelle au développement d’un vaccin qui bloquerait le parasite dans son cycle de développement chez l’homme.
A la fin des années 80, le professeur André Capron et son équipe de l'Institut Pasteur de Lille ont mené des travaux fondamentaux sur la génétique moléculaire des schistosomes, qui ont conduit à l'identification et au clonage moléculaire d'une protéine vaccinante dans la schistosomiase[23]. Ce vaccin, entré en phase d'essais cliniques depuis 1998, est le résultat de progrès considérables dans la définition d'un vaccin potentiel contre la bilharziose.
En 2009, après plus de 20 ans de recherches internationales, un vaccin contre la bilharziose est entré dans la phase III de son développement. Ce vaccin a été mis au point par les chercheurs de l’Inserm et de l’Institut Pasteur de Lille et est produit par Eurogentec[24],[25].
En début d'année 2012, le site communautaire World Community Grid a intégré le projet Say No To Schistosoma. Fondé sur l'utilisation du temps de calcul inutilisé des ordinateurs participants au projet, il a pour but d'effectuer des simulations des interactions entre différents procédés chimiques et les protéines cibles de la maladie ce qui pourrait conduire à la création de traitements plus efficaces[26].
Notes et références[modifier | modifier le code]
- (en) Stefano Di Bella, Niccolò Riccardi, Daniele Roberto Giacobbe et Roberto Luzzati, « History of schistosomiasis (bilharziasis) in humans: from Egyptian medical papyri to molecular biology on mummies », Pathogens and Global Health, vol. 112, no 5, , p. 268–273 (ISSN 2047-7724 et 2047-7732, PMID 30016215, PMCID PMC6225400, DOI 10.1080/20477724.2018.1495357, lire en ligne, consulté le )
- John Farley, Bilharzia: A History of Imperial Tropical Medicine, Cambridge University Press, (lire en ligne), p. 5.
- François Pebret, Maladies infectieuses : toutes les pathologies des programmes officiels des études médicales ou paramédicales, Heures de France, , 592 p. (ISBN 978-2-85385-247-0, présentation en ligne)
- (en) A. H. R. Stich, S. Biays, P. Odermatt, Chan Men, Cheam Saem, Kiev Sokha, Chuong Seng Ly, P. Legros, M. Philips, J.-D. Lormand, M. Tanner, « Foci of Schistosomiasis mekongi, Northern Cambodia: II. Distribution of infection and morbidity », Tropical Medicine & International Health, vol. 4, no 10, , p. 674–85. (ISSN 1365-3156, PMID 10583901, DOI 10.1046/j.1365-3156.1999.00474.x, lire en ligne [PDF], consulté le )
- Helmut Kloos et Rosalie David, « The Paleoepidemiology of Schistosomiasis in Ancient Egypt », Human Ecology Review, vol. 9, no 1, , p. 14–25 (lire en ligne [archive du ]) :
« By the early twentieth century, the Egyptian population was well aware of the widespread occurrence of haematuria to the point where the passing of blood by boys was considered as a normal and even necessary part of growing up, a form of male menstruation linked with male fertility (Girges 1934, 103). »
- Patricia Rutherford, « The Diagnosis of Schistosomiasis in Modern and Ancient Tissues by Means of Immunocytochemistry », Chungara, Revista de Antropología Chilena, vol. 32, no 1, (ISSN 0717-7356, DOI 10.4067/s0717-73562000000100021) :
« The ancient Egyptians also wrote of boys becoming men when blood was seen in their urine, as this was likened to the young female's first menstruation (Despommier et al. 1995). Also, archaeological evidence such as wall reliefs, hieroglyphs, and papyri all confirm that their lifestyle encompassed activities such as bathing, fishing and playing in the Nile, and this combined with bad sanitation habits, would make almost everyone susceptible to this infection. »
- Jean-Philippe Chippaux, La lutte contre les schistosomoses en Afrique de l'Ouest, IRD Editions, (ISBN 978-2-7099-1460-4, lire en ligne), p. 9
- (en) « Partnership for Parasite Control, Second Meeting Rome »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) (consulté le ), avril 2002
- Institut de Veille Sanitaire, « Transmission autochtone de bilharziose en Corse du Sud 2011-2013 », sur invs.santepubliquefrance.fr, .
- « Bilharziose, Corse », sur www.gtvcorse.fr (consulté le ).
- (en) Warren, K. S., E. O. Domingo, and R. B. Cowan. 1967 « Granuloma formation around schistosome eggs as a manifestation of delayed hypersensitivity » Am J Pathol. 51:735.
- (en) Mosmann TR, Cherwinski H, Bond MW, Giedlin MA. et Coffman RL, « Two types of murine helper T cell clone. I. Definition according to profiles of lymphokine activities and secreted proteins » J Immunol. 1986;136:2348.
- (en) Angeli V, Faveeuw C, Roye O, Fontaine J, Teissier E, Capron A, Wolowczuk I, Capron M. et Trottein F, « Role of the parasite-derived prostaglandin D2 in the inhibition of epidermal Langerhans cell migration during schistosomiasis infection » J Exp Med. 2001;193:1135.
- (en) Herve, M., V. Angeli, E. Pinzar, R. Wintjens, C. Faveeuw, S. Narumiya, A. Capron, Y. Urade, M. Capron, G. Riveau et F. Trottein. « Pivotal roles of the parasite PGD2 synthase and of the host D prostanoid receptor 1 in schistosome immune evasion » Eur J Immunol. 2003;33:2764.
- « Schistosomiase (bilharziose) », sur www.who.int (consulté le ).
- (en) G. J. van Dam, J. H. Wichers, T. M. F. Ferreira et D. Ghati, « Diagnosis of Schistosomiasis by Reagent Strip Test for Detection of Circulating Cathodic Antigen », Journal of Clinical Microbiology, vol. 42, no 12, , p. 5458–5461 (ISSN 0095-1137, PMID 15583265, PMCID PMC535219, DOI 10.1128/JCM.42.12.5458-5461.2004, lire en ligne, consulté le )
- (en) J. Utzinger, S.L. Becker, L. van Lieshout et G.J. van Dam, « New diagnostic tools in schistosomiasis », Clinical Microbiology and Infection, vol. 21, no 6, , p. 529–542 (DOI 10.1016/j.cmi.2015.03.014, lire en ligne, consulté le )
- (en) Patrick Hunziker, Maurice Mutro Nigo, Georgette B. Salieb-Beugelaar et Peter Odermatt, « Schistosomiasis: from established diagnostic assays to emerging micro/nanotechnology-based rapid field testing for clinical management and epidemiology », Precision Nanomedicine, , p. 439–458 (DOI 10.33218/prnano3(1).191205.1, lire en ligne, consulté le )
- « WHO | Low-cost tools for diagnosing and monitoring HIV infection in low-resource settings »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur www.who.int (consulté le ).
- (en) « Schistosomiasis Control Program ».
- (en) « 20 April 2009 - Bilhvax - A Vaccine Against Bilharziose, A world first! ».
- Données OMS
- J. M. Grzych, M. Capron, P. H. Lambert et C. Dissous, « An anti-idiotype vaccine against experimental schistosomiasis », Nature, vol. 316, no 6023, , p. 74–76 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/316074a0, lire en ligne, consulté le )
- « 20 avril 2009 - 300.000 morts évitées grâce au vaccin liégeois ! ».
- « 22 avril 2009 - Eurogentec, la société de biotechnologie située au Sart Tilman, produit et produira le vaccin contre la bilharziose. ».
- (en) « World Community Grid - Say No To Schistosoma ».


