Menthol
| Menthol | |
  |
|
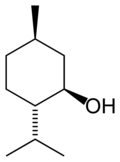
| Structure du menthol | |
| Identification | |
|---|---|
| Nom UICPA | (1R,2S,5R)-5-méthyl-2-(propan-2-yl)cyclohexanol |
| Synonymes |
5-méthyl-2-(1-méthyléthyl)-cyclohexan-1-ol |
| No CAS | , racémique , (−)-isomère (+)-isomère |
| No ECHA | 100.016.992 |
| No CE | 201-939-0, racémique 218-690-9 L |
| PubChem | |
| FEMA | 2665 |
| SMILES | |
| InChI | |
| Apparence | solide cristallin blanc ou incolore |
| Propriétés chimiques | |
| Formule | C10H20O [Isomères] |
| Masse molaire[1] | 156,265 2 ± 0,009 7 g/mol C 76,86 %, H 12,9 %, O 10,24 %, |
| Propriétés physiques | |
| T° fusion | 36 à 38 °C, racémique 42 à 45 °C, (−)-forme (α) 35-33-31 °C, (−)-isomère |
| T° ébullition | 212 °C |
| Solubilité | légèrement soluble dans l'eau |
| Masse volumique | 0,903 g·cm-3 (L, 15 °C)[2] |
| Point d’éclair | 93 °C |
| Point critique | 694,0 K[3] |
| Précautions | |
| SIMDUT[4] | |
 D2B, |
|
| Directive 67/548/EEC | |
| Composés apparentés | |
| Isomère(s) | Citronellol, Dihydrolinalol |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le menthol est un composé organique covalent obtenu soit par synthèse, soit par extraction à partir de l'huile essentielle de menthe poivrée ou d'autres huiles essentielles de menthe. Le stéréoisomère le plus courant du menthol est le (–)-menthol, de configuration (1R,2S,5R). Il appartient à la famille des monoterpénols. À température ambiante (20 à 25 °C), il se trouve sous forme de cristaux, d'une couleur blanc cireux. Il fond si l'on augmente légèrement la température. Le menthol a des propriétés anti-inflammatoires et antivirales. Il est d'ailleurs utilisé pour soulager les irritations mineures de la gorge. C'est également un anesthésique local.
Histoire
Le menthol est connu au Japon depuis plus de 2000 ans[5] mais il n'a été isolé pour la première fois qu'en 1771 par Gaubius. Le (–)-menthol (aussi appelé L-menthol ou (1R,2S,5R)-menthol) se trouve naturellement dans l'huile essentielle de menthe poivrée (Mentha ×piperita). Le menthol japonais contient également un léger pourcentage de (+)-néomenthol.
Structure
Le menthol existe à l'état natif sous la forme d'un seul énantiomère : (1R,2S,5R), en bas à gauche du schéma.
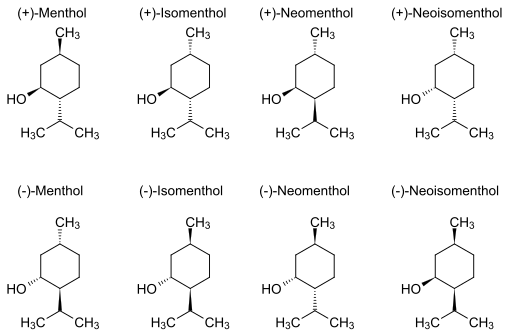
Dans les composés naturels, le groupe isopropyle est orienté trans par rapport aux deux groupes, méthyle et alcool, en position cis. Ainsi il peut être dessiné de l'une ou l'autre des façons ci-dessous :
Dans l'état fondamental, chacun des trois substituants est en position équatoriale, faisant du (–)-menthol et de son énantiomère (1S,2R,5S) les isomères les plus stables. Il existe deux formes cristallines pour le menthol racémique. L'une a des points de fusion de 28 °C et l'autre de 38 °C. Pur, le menthol a quatre formes solides, dont la plus stable est la forme α.
Applications


Le menthol est inclus dans nombre de produits différents pour plusieurs raisons comme :
- soulagement à court terme de la gorge endolorie et de l'irritation mineure de la bouche ou de la gorge (bains de bouche par exemple) ;
- antipruritique, pour réduire les démangeaisons ;
- anesthésique local pour soulager des maux et douleurs mineures telles que des crampes musculaires, entorses, migraines. Il peut être utilisé seul ou combiné à du piment ou du camphre. En Europe, il est plutôt utilisé en gel ou en crème ;
- décongestionnant pour les voies respiratoires et les sinus ;
- pesticide contre les acariens (acaricide) ;
- dans certains médicaments traitant les brûlures mineures, il produit une sensation de froid (souvent utilisés en application locale, en association avec l'aloès) ;
- additif dans certaines cigarettes, comme saveur ou pour réduire les irritations de la gorge ou des sinus provoqués par le tabagisme ;
- additif dans certaines saveurs de liquides pour cigarettes électroniques ;
- comme désinfectant pour l'hygiène orale, ou remède contre la mauvaise haleine, comme collutoire, dans les pâtes dentifrices, et plus généralement comme agent de saveur pour les chewing-gums et les sucreries ;
- dans les sodas, aussi bien mélangé avec de l'eau pour obtenir une boisson à très faible teneur en alcool, comme dans le Ricqlès (on fait ici référence à la boisson, et non à l'alcool de menthe de la même marque) ;
- en versant quelques gouttes d'alcool de menthe sur un morceau de sucre pour soulager la nausée ;
- pour préparer des esters menthylés afin d'agrémenter des notes florales en parfumerie ;
- en patchs pour faire tomber la fièvre ou obtenir une sensation de froid (très développé au Japon) ;
- additif à certains produits de beauté (produits coiffants par exemple).
Les défenseurs de l'homéopathie pensent que le menthol interfère avec les produits homéopathiques. Son utilisation est fortement déconseillée en association avec ceux-ci, au point de proscrire les dentifrices à base de menthol.
Le menthol peut être utilisé en aromathérapie sous forme d'huile essentielle de menthe poivrée (médecine naturelle), l'indigestion, la nausée, les maux de gorge, la diarrhée, les maux de tête et les refroidissements (médecine orientale).
Le menthol a une toxicité relativement basse : DL50 de 3 300 mg·kg-1 pour le rat, oral ; DL50 de 15 800 mg·kg-1 pour le lapin, peau.
En chimie organique, le menthol est utilisé comme auxiliaire chiral dans la synthèse de centres asymétriques.
Synthèse
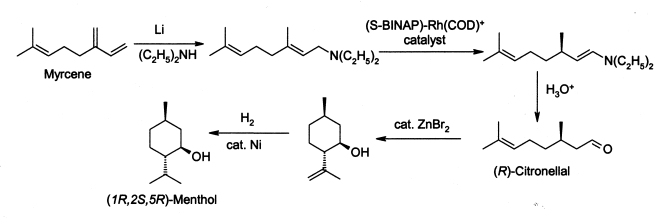
Comme beaucoup de produits naturels employés couramment, la demande de menthol excède considérablement l'approvisionnement des sources naturelles. Le menthol est fabriqué comme énantiomère simple par Takasago International Cie sur une échelle de 400 tonnes par an. Le processus implique une synthèse énantiosélective développée par une équipe menée par Ryōji Noyori, prix Nobel de chimie en 2001 :
Le processus commence en formant une amine allylique du myrcène, qui subit l'isomérisation asymétrique en présence d'un complexe de rhodium de BINAP pour donner (après hydrolyse) le R-citronellal énantiomériquement pur. Le résultat est traité au bromure de zinc pour obtenir l'isopulégol qui est alors hydrogéné pour donner du (1R, 2S, 5R)-menthol pur. Le menthol racémique peut être préparé simplement par l'hydrogénation du thymol, et le menthol est également constitué par l'hydrogénation de la pulégone.
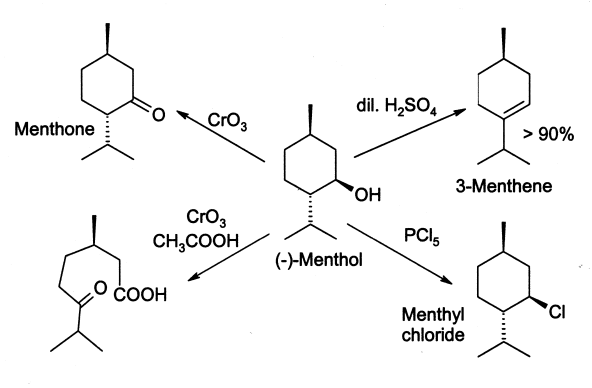
Propriétés chimiques
Le menthol réagit souvent de la même façon qu'un alcool secondaire normal. Il est oxydé en menthone en réduisant des agents tels que l'acide chromique, bien que dans certaines conditions l'oxydation puisse aller plus loin et casser le cycle. Le menthol est facilement déshydraté pour donner principalement le 3-menthène, par l'action de 2 % d'acide sulfurique. Le traitement au pentachlorure de phosphore (PCl5) donne du chlorure de menthyle.
Propriétés biologiques
La capacité du menthol de déclencher chimiquement les récepteurs sensibles au froid dans la peau est responsable de la sensation de refroidissement bien connue qu'elle provoque une fois absorbée. Dans ce sens, elle est semblable à la capsaïcine, l'espèce chimique responsable de la sensation épicée des piments.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) J. G. Speight et Norbert Adolph Lange, Lange's handbook of chemistry, New York, McGraw-Hill, , 16e éd., 1623 p. (ISBN 978-0-07-143220-7, LCCN 84643191), p. 2.289
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- « Menthol » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Martina Krčmár, Dans la pharmacie de mamie du charbon de Belloc au vinaigre des 4 voleurs, Larousse, (ISBN 9782035879615, lire en ligne)
Voir aussi
Articles connexes
Liens externes
- (en) Colacot T. J., Platinum Metals Review, 2002, 46(2), 82-83.
- (en) Ryoji Noyori Nobel lecture, 2001.
- (en) Menthol Information.
- (en) Cooler than Menthol.
Bibliographie
- E. E. Turner, M. M. Harris, Organic Chemistry, Longmans, Green & Co., Londres, 1952.
- Handbook of Chemistry and Physics, 71e éd., CRC Press, Ann Arbor, Michigan, 1990.
- (en) Maryadele J. O'Neil, Patricia E. Heckelman, Cherie B. Koch et al., The Merck index: an encyclopedia of chemicals, drugs, and biologicals, Whitehouse Station, N.J., Merck Research Laboratories, , 14e éd., 10973 p. (ISBN 978-0-911-91000-1, OCLC 708295355).