Nitrure de carbone graphitique

Le nitrure de carbone graphitique, ou g-C3N4, est un polymorphe de nitrure de carbone, de formule chimique approchée C3N4 omettant une certaine quantité d'hydrogène. Il s'agit d'un ensemble de polymères dont la géométrie moléculaire est bidimensionnelle comprenant des sous-structures de type heptazine et poly(triazine imide) dont le degré de condensation varie en fonction des conditions de formation. Ces matériaux ont des propriétés semiconductrices et catalytiques particulières qui les rendent intéressants par exemple pour l'activation du benzène, les réactions de trimérisation, ou encore l'activation du dioxyde de carbone dans les réactions de photosynthèse artificielle[1].
-
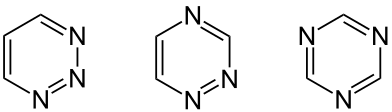
Structure des différentes triazines.
La caractérisation du nitrure de carbone graphitique cristallisé peut être réalisée en identifiant les cycles de triazine du matériau par spectrométrie photoélectronique X (XPS), spectre de photoluminescence et spectroscopie infrarouge à transformée de Fourier (FTIR) (pics à 800 cm−1, 1 310 cm−1 et 1 610 cm−1)[2].
On peut obtenir du nitrure de carbone graphitique par polymérisation de cyanamide N≡C–NH2, de dicyandiamide (2-cyanoguanidine) N≡C–N=C(NH2)2 ou de mélamine C3H6N6. La première structure C3N4 polymérique formée est un polymère très ordonné, avec des groupes amine libres. Si l'on poursuit la réaction, il se forme un composé plus condensé à base d'heptazine C6N7[1]. On peut également préparer le g-C3N4 par cataphorèse d'une solution saturée de mélamine et de chlorure cyanurique (ratio 1:1,5) sur un substrat Si(100) à température ambiante[3]. On a obtenu des nanocristallites de nitrure de carbone graphitique bien cristallisés en faisant réagir du chlorure cyanurique et de l'amidure de sodium NaNH2 de 180 à 220 °C pendant 8 à 12 heures[2]. Une autre méthode consiste à chauffer de 400 à 600 °C un mélange de mélamine C3H6N6 et d'acide urique C5H4O3N4 en présence d'alumine Al2O3 : l'alumine agit en favorisant la formation de nitrure de carbone graphitique sur les surfaces exposées selon une réaction apparentée au dépôt chimique en phase vapeur (CVD) in situ[4].
Applications[modifier | modifier le code]
Le nitrure de carbone graphitique est disponible sur le marché sous plusieurs formes, par exemple comme poudre à grains micrométriques ou sous forme de nanofeuillets. Il peut être utilisé pour réaliser des revêtements tribologiques, biocompatibles ou chimiquement inertes, des isolants, voire des matériaux pour stockage de l'énergie. Ce serait en particulier un matériau de choix pour le stockage de l'hydrogène[5],[6]. Compte tenu de la surface offerte par la structure du matériau, il peut servir de support pour nanoparticules catalytiques en catalyse hétérogène[7]. En particulier, la résilience particulière du matériau, combinée avec la réactivité en surface et à l'intérieur des couches qui le constituent, permet de concevoir des catalyseurs tirant profit de leurs protons labiles et de leur nature de base de Lewis. Des altérations comme le dopage, la protonation et la fonctionnalisation moléculaire peuvent permettre d'améliorer la sélectivité et les performances de la catalyse[1]. Des nanoparticules de catalyseur supportées par du nitrure de carbone graphitique sont étudiées dans le cadre de piles à combustible à membrane d'échange de protons et de cellules d'électrolyse de l'eau[8].
Les propriétés du g-C3N4 présentent quelques limitations lorsqu'elles ne sont pas corrigées pour rendre le matériau encore plus propice aux applications photocatalytiques. Sa largeur de bande interdite de 2,7 eV, sa bonne absorption de la lumière visible, sa flexibilité mécanique sont intéressantes, mais il présente un taux élevé de recombinaison des porteurs générés par photodissociation, une faible conductivité électrique et une surface spécifique somme toute limitée (moins de 10 m2·g-1)[9]. Il est cependant possible de pallier ces limitations par exemple en dopant le matériau avec des nanotubes de carbone, qui apportent une surface spécifique important susceptible de favoriser la séparation des porteurs de charge, réduire leur taux de recombinaison et améliorer l'activité de la réaction de réduction[10]. Les nanotubes de carbone présentent également une conductivité électrique élevée susceptible d'améliorer les propriétés électroniques du nitrure de carbone graphitique[11]. Enfin, les nanotubes de carbone peuvent être vus comme des semiconducteurs à bande interdite étroite, ce qui permet d'élargir le spectre d'absorption du matériau et donc d'augmenter ses performances photocatalytiques[12].
Les principaux domaines de recherche autour du g-C3N4 concernent ainsi la photocatalyse, notamment la décomposition de l'eau H2O en hydrogène H2 et oxygène O2[13] et la dégradation des polluants, les semiconducteurs à large bande interdite[8], et le stockage de l'énergie, avec notamment la possibilité d'héberger de grandes quantités de lithium par intercalation dans la structure du matériau[14].
Notes et références[modifier | modifier le code]
- (en) Arne Thomas, Anna Fischer, Frederic Goettmann, Markus Antonietti, Jens-Oliver Müller, Robert Schlögl et Johan M. Carlsson, « Graphitic carbon nitride materials: variation of structure and morphology and their use as metal-free catalysts », Journal of Materials Chemistry, vol. 18, no 41, , p. 4893-4908 (DOI 10.1039/B800274F, lire en ligne)
- (en) Qixun Guo, Yi Xie, Xinjun Wang, Shichang Lv, Tao Hou et Xianming Liu, « Characterization of well-crystallized graphitic carbon nitride nanocrystallites via a benzene-thermal route at low temperatures », Chemical Physics Letters, vol. 380, nos 1-2, , p. 84-87 (DOI 10.1016/j.cplett.2003.09.009, Bibcode 2003CPL...380...84G, lire en ligne)
- (en) Li Chao, Cao Chuanbao et Zhu Hesun, « Preparation of graphitic carbon nitride by electrodeposition », Chinese Science Bulletin, vol. 48, no 16, , p. 1737-1740 (DOI 10.1360/03wb0011, Bibcode 2003ChSBu..48.1737L, lire en ligne)
- (en) Roberto C. Dante, Pablo Martín-Ramos, Adriana Correa-Guimaraes et Jesús Martín-Gil, « Synthesis of graphitic carbon nitride by reaction of melamine and uric acid », Materials Chemistry and Physics, vol. 130, no 3, , p. 1094-1102 (DOI 10.1016/j.matchemphys.2011.08.041, lire en ligne)
- (en) Asalatha A.S.Nair, Ramaprabhu Sundara et N.Anitha, « Hydrogen storage performance of palladium nanoparticles decorated graphitic carbon nitride », International Journal of Hydrogen Energy, vol. 40, no 8, , p. 3259-3267 (DOI 10.1016/j.ijhydene.2014.12.065, lire en ligne)
- (en) Asalatha A. S. Nair et Ramaprabhu Sundara, « Palladium Cobalt Alloy Catalyst Nanoparticles Facilitated Enhanced Hydrogen Storage Performance of Graphitic Carbon Nitride », The Journal of Physical Chemistry, vol. 120, no 18, , p. 9612-9618 (DOI 10.1021/acs.jpcc.6b01850, lire en ligne)
- (en) Xiufang Chen, Ligang Zhang, Bo Zhang, Xingcui Guo et Xindong Mu, « Highly selective hydrogenation of furfural to furfuryl alcohol over Pt nanoparticles supported on g-C3N4 nanosheets catalysts in water », Scientific Reports, vol. 6, , article no 28558 (PMID 27328834, PMCID 4916514, DOI 10.1038/srep28558, Bibcode 2016NatSR...628558C, lire en ligne)
- (en) Noramalina Mansor, Thomas S. Miller, Ishanka Dedigama, Ana Belen Jorge, Jingjing Jia, Veronika Brázdová, Cecilia Mattevi, Chris Gibbs, David Hodgson, Paul R. Shearing, Christopher A. Howard, Furio Corà, Milo Shaffer, Daniel J.L. Brett et Paul F. McMillan, « Graphitic Carbon Nitride as a Catalyst Support in Fuel Cells and Electrolyzers », Electrochimica Acta, vol. 222, , p. 44-57 (DOI 10.1016/j.electacta.2016.11.008, lire en ligne)
- (en) Ping Niu, Lili Zhang, Gang Liu et Hui‐Ming Cheng, « Graphene‐Like Carbon Nitride Nanosheets for Improved Photocatalytic Activities », Advanced Functional Materials, vol. 22, no 22, , p. 4763-4770 (DOI 10.1002/adfm.201200922, lire en ligne)
- (en) Liqiang Zhang, Xing He, Xiuwen Xu, Chao Liu, Yongli Duan, Liqiang Hou, Qidong Zhou, Chi Ma, Xiaopeng Yang, Rui Liu, Fan Yang, Lishan Cui, Chunming Xu et Yongfeng Li, « Highly active TiO2/g-C3N4/G photocatalyst with extended spectral response towards selective reduction of nitrobenzene », Applied Catalysis B: Environmental, vol. 203, , p. 1-8 (DOI 10.1016/j.apcatb.2016.10.003, lire en ligne)
- (en) Fan Dong, Yuhan Li, Zhenyu Wang et Wing-Kei Ho, « Enhanced visible light photocatalytic activity and oxidation ability of porous graphene-like g-C3N4 nanosheets via thermal exfoliation », Applied Surface Science, vol. 357, no A, , p. 393-403 (DOI 10.1016/j.apsusc.2015.04.034, Bibcode 2015ApSS..358..393D, lire en ligne)
- (en) G. Mamba et A. K. Mishra, « Graphitic carbon nitride (g-C3N4) nanocomposites: A new and exciting generation of visible light driven photocatalysts for environmental pollution remediation », Applied Catalysis B: Environmental, vol. 198, , p. 347-377 (DOI 10.1016/j.apcatb.2016.05.052, lire en ligne)
- (en) Xinchen Wang, Kazuhiko Maeda, Arne Thomas, Kazuhiro Takanabe, Gang Xin, Johan M. Carlsson, Kazunari Domen et Markus Antonietti, « A metal-free polymeric photocatalyst for hydrogen production from water under visible light », Nature Materials, vol. 8, no 1, , p. 76-80 (PMID 18997776, DOI 10.1038/nmat2317, Bibcode 2009NatMa...8...76W, lire en ligne)
- (en) Menghao Wu, Qian Wang, Qiang Sun et Puru Jena, « Functionalized Graphitic Carbon Nitride for Efficient Energy Storage », The Journal of Physical Chemistry, vol. 117, no 12, , p. 6055-6059 (DOI 10.1021/jp311972f, lire en ligne)
Voir aussi[modifier | modifier le code]
- Nitrure de carbone β (β-C3N4)