Grossesse extra-utérine
| Symptômes | Douleur abdominale |
|---|
| Médicament | Mifépristone et méthotrexate |
|---|---|
| Spécialité | Maïeutique et gynécologie |
| CISP-2 | W80 |
|---|---|
| CIM-10 | O00m |
| CIM-9 | 633 |
| DiseasesDB | 4089 |
| MedlinePlus | 000895 |
| eMedicine |
2041923 emerg/478radio/231 |
| MeSH | D011271 |
| Patient UK | Ectopic-pregnancy-pro |
La grossesse extra-utérine (GEU), ou grossesse ectopique, est une grossesse se développant hors de l'utérus. La très grande majorité des grossesses extra-utérines sont des grossesses dans la trompe de Fallope ou grossesses tubaires. La grossesse extra-utérine justifie une urgence chirurgicale dans sa forme rompue. Son diagnostic est de plus en plus précoce permettant d'éviter sa rupture et la mise en jeu du pronostic vital et permettant un traitement non chirurgical sous certaines conditions strictes.
C'est un cas d'urgence chirurgicale pouvant compromettre le pronostic vital de la mère ou sa fertilité ultérieure.
Chez les femmes sans contraception, les deux principaux facteurs de risque sont d’une part les antécédents d'infection génitale ou de chirurgie tubaire et d’autre part le tabac.
Les dosages hormonaux, l’échographie et la cœlioscopie ont modifié la prise en charge de la pathologie.
Épidémiologie et facteurs de risque[modifier | modifier le code]
Il s'agit de la première cause de mortalité du premier trimestre de la grossesse aux États-Unis. Son incidence a été multipliée par 6 entre 1970 et 1989 mais tend à se stabiliser par la suite[1]. Sa prévalence est comprise entre 1 et 2 % des grossesses[2].
Les facteurs de risque principaux sont un antécédent de grossesse extra-utérine, de maladie des trompes, de chirurgie des trompes et l'exposition au diéthylstilbestrol (Distilbène)[3]. Les antécédents de césariennes augmentent aussi le risque de grossesse extra-utérine et de placenta praevia[4]. Le tabagisme est responsable de 35 % des GEU d'après certaines études[5], et l'antécédent d'infection des trompes de près d'un tiers[5] (bactérie Chlamydia trachomatis) ; ils sont également des facteurs de risque important[6]. S'y ajoute un dernier facteur, l'âge de la mère (0,4 % de risque de faire une GEU à 20 ans, pour 2 % entre 30 et 40)[5].
Physiopathologie[modifier | modifier le code]
Neuf dixièmes des grossesses extra-utérines ont lieu au niveau d'une trompe de Fallope[2], reliant l'ovaire à l'utérus. On parle alors de grossesse tubaire. Les rares cas de grossesses extra-tubaires sont de diagnostic plus difficile, entraînant un taux de complications plus important.
Grossesse extra-utérine organique[modifier | modifier le code]
S'il existe une lésion de la paroi tubaire sans obstruction de la trompe, la progression de l’œuf est ralentie par la perturbation du péristaltisme (contraction) tubaire.
Les causes peuvent être infectieuses (séquelles de salpingites à germes plus ou moins spécifiques), chirurgicales (brides post-opératoires de chirurgie sous-mésocolique, en cas d'appendicectomie par exemple, ou chirurgie pour stérilité tubaire).
La présence d'un dispositif intra-utérin (DIU) peut entraîner une déciliation et inflammation. De manière plus pratique, le DIU empêche toute implantation utérine mais pas une implantation extra-utérine.
Grossesse extra-utérine fonctionnelle[modifier | modifier le code]
Elle est causée par une perturbation du péristaltisme tubaire (contraction).
Les causes sont multiples, la principale étant le tabagisme. Par ailleurs, les césariennes font aussi partie des causes[4].
La présence d'une phase lutéale courte, d'une prise de progestatifs micro-dosés, de pilule du lendemain ou d'inducteurs de l’ovulation augmenterait le risque de grossesse extra-utérine.
Autres[modifier | modifier le code]
- Malformations utérines
- Migration prolongée de l'œuf
- Endométriose tubaire
- Lithopédion, fœtus calcifié dans l'abdomen.
Diagnostic positif[modifier | modifier le code]
Clinique[modifier | modifier le code]
Le tableau typique est celui d'un hématocèle non compliqué : douleurs à type de coliques, latéralisées, accompagnées de malaises, métrorragies (saignement génital) noirâtres ou sépia après une période d'aménorrhée.
L’interrogatoire complète l’examen et recherche des antécédents gynéco-obstétriques, chirurgicaux et médicaux.
L'examen montre l'absence de choc ou de tachycardie. Il existe une douleur provoquée à la palpation du ventre, avec parfois une défense (sous forme de contracture à la palpation) sous-ombilicale.
Les touchers pelviens notent un utérus moins gros que ne le voudrait l’âge gestationnel et peut percevoir une masse latéro-utérine douloureuse avec une douleur dans le cul-de-sac de Douglas (entre rectum et vagin). En règle, le toucher vaginal n'apporte que peu au diagnostic[7].
Biologie[modifier | modifier le code]
La NFS peut montrer une anémie, une augmentation du taux des leucocytes, non spécifique.
L'élévation du taux des β-HCG plasmatiques permet d'affirmer la grossesse, quelle que soit sa localisation, s'il est supérieur à 10 UI/l. Il peut être plus bas que ne le voudrait l’âge supposé de la grossesse.
Le bilan est complété par un ionogramme sanguin, une hémostase, la détermination du groupe sanguin, à visée pré-opératoire.
Imagerie[modifier | modifier le code]
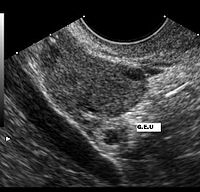
L'échographie par sonde abdominale permet de visualiser une masse hétérogène latéro-utérine, constitué par le sac gestationnel en dehors de la cavité utérine. L'utérus est vide mais ses parois épaissies. Un épanchement au niveau du cul-de sac de Douglas peut être mis en évidence. Cet examen a une très bonne sensibilité pour le diagnostic mais une spécificité moins importante[8].
Des β-HCG supérieurs à 4000 UI/l sans visualisation du sac ovulaire intra-utérin signent pratiquement la grossesse extra-utérine.
L'examen échographique peut être complété par l'utilisation d'une sonde endovaginale, permettant de mieux visualiser trompes, ovaires et contenu utérin et d'avoir une précision diagnostique plus importante[9].
La cœlioscopie permet de faire le diagnostic de certitude. Elle ne doit pas être faite trop précocement car on risque alors de méconnaître la grossesse extra-utérine[10]. Elle visualise une dilatation olivaire bleutée de la trompe, correspondant à un hématosalpinx (saignement dans la trompe) et permet de mettre en évidence l’hémopéritoine. Elle précise le siège de la grossesse.
Diagnostic différentiel[modifier | modifier le code]
L'examen clinique permet de retrouver une cause cervicale (col de l'utérus). L'échographie par voie endovaginale, en cas de grossesse intra-utérine, élimine les autres causes de métrorragies au premier trimestre.
Formes cliniques[modifier | modifier le code]
Formes symptomatiques[modifier | modifier le code]
La grossesse extra-utérine peut se présenter sous la forme d'une rupture cataclysmique, avec un tableau de choc hémorragique par hémopéritoine. Le diagnostic peut être aidé par une culdocentèse (ponction du cul de sac de Douglas) ramenant du sang. Il s'agit d'une urgence chirurgicale majeure.
Formes topographiques[modifier | modifier le code]
Les formes non tubaires sont rares. La localisation ampullaire est la plus fréquente. Elle est parfois de révélation tardive, pouvant réaliser un avortement tubo-abdominal.
La localisation peut être ovarienne, isthmique (de révélation précoce), interstitielle (avec rupture au niveau de la corne utérine), abdominale (avec implantation sur n’importe quel organe) ou rétro-utérin.
Traitement[modifier | modifier le code]
En 1863, Eugène Koeberlé fut le premier à opérer une grossesse extra-utérine avec enfant vivant[réf. nécessaire].
Le premier but est de sauver la vie de la patiente, car il s'agit d'une urgence vitale. Le second but est de préserver les chances d'une grossesse ultérieure en s'efforçant d’être le plus conservateur possible.
L'hospitalisation avec mise en condition (surveillance clinique et biologique) est indispensable. L’abstention thérapeutique peut être discutée en cas de grossesse extra-utérine à β-HCG très bas[11].
Dans tous les cas, il ne faut pas oublier la prévention de l’iso-immunisation rhésus aux patientes Rh-, ainsi qu'une éventuelle prise en charge psychologique.
Traitement médical[modifier | modifier le code]
Le traitement médical est l'utilisation du méthotrexate par voie générale (injection intra musculaire). Dans des situations particulières (grossesse cornuale, sur cicatrice de césarienne), elle peut être réalisée également in situ par ponction du sac gestationnel échoguidée puis injection du médicament. L'administration de doses répétées pourrait augmenter l'efficacité du traitement[12], ce qui laisse la possibilité d'une deuxième injection intramusculaire si la première était inefficace.
La surveillance est stricte et nécessite une observance de la part de la patiente par prélèvement sanguin régulier jusqu'à négativation totale du taux de grossesse β-HCG jusqu’à 2 UI/l.
Le traitement médicamenteux est au moins aussi efficace que la chirurgie dans les formes non compliquées:
- surtout si le taux de β-HCG est peu élevé[13]. de l'ordre de <5000 UI/ml
- patiente non ou peu douloureuse
- abdomen souple, hémodynamique normale de la patiente
- masse annexielle inférieure à 5 cm de diamètre.
Toute grossesse ultérieure est déconseillée jusqu'à trois mois après le traitement[2] par méthotrexate du fait d'une tératogénécité.
Traitement chirurgical[modifier | modifier le code]
La chirurgie peut être :
- radicale : salpingectomie totale avec résection de la portion isthmique et annexectomie en cas de lésion ovarienne ;
- conservatrice avec césarienne tubaire et ablation (par expression) du sac gestationnel après salpingotomie ;
- cœlioscopique avec salpingectomie ou salpingotomie et aspiration du trophoblaste.
L'intervention est réalisée généralement par cœlioscopie qui permet des suites plus simples (durées d'hospitalisation et de convalescence réduite)[14], mais dans toute chirurgie, le risque de laparoconversion doit être expliqué à la patiente.
Indications[modifier | modifier le code]
Elles dépendent de l'état hémodynamique, des antécédents de la patiente, de son désir de grossesse, de l'état de la trompe controlatérale.
Le traitement sera plus facilement chirurgical si :
- la patiente est instable hémodynamiquement
- la patiente est très douloureuse
- l'échographie montre une masse annexielle de plus de 5 cm, un épanchement intra péritonéal important
- antécédent de grossesse extra utérine homolatérale
- en cas de contre indications au traitement par le méthotrexate.
Schématiquement :
- 1re grossesse extra-utérine : Conservateur si désir de grossesse ultérieure, radical sinon ;
- 2e grossesse extra-utérine : Si la récidive est du même côté, on procède à un traitement radical, sinon un traitement conservateur ou médical est proposé.
- 3e grossesse extra-utérine : traitement radical, avec éventuellement prise en charge dans un programme de fécondation in vitro
Complications[modifier | modifier le code]
Précoces, elles sont communes à toutes chirurgie : hémorragie, thrombo-embolies, infectieuses...
Le risque tardif est celui d'une infertilité.
Voir aussi[modifier | modifier le code]
Références[modifier | modifier le code]
- Ectopic pregnancy -- United States, 1990-1992, MMWR Morb Mortal Wkly Rep, 1995 ; 44:46-48.
- Jurkovic D, Wilkinson H, Diagnosis and management of ectopic pregnancy, BMJ, 2011 ; 342 : doi:10.1136/bmj.d3397.
- Ankum WM, Mol BW, Van der Veen F, Bossuyt PM, Risk factors for ectopic pregnancy: a meta-analysis, Fertil Steril, 1996 ; 65:1093-9.
- (en) Sir Sabaratnam Arulkumaran, Best Practice in Labour and Delivery 2nd edition - -, Cambridge, Cambridge University Press, , 413 p. (ISBN 978-1-107-47234-1, lire en ligne), Chapitre 2
- Isabelle Hallot, « Grossesses extra-utérine - On peut limiter les risques. », Parents, (ISSN 0553-2159).
- Bouyer J, Coste J, Shojaei T et al. Risk factors for ectopic pregnancy: a comprehensive analysis based on a large case-control, population-based study in France, Am J Epidemiol, 2003 ; 157:185-94.
- Mol BW, Hajenuis P, Engelsbel S et al. Should patients who are suspected of having an ectopic pregnancy undergo a physical examination?, Fertil Steril, 1999;71:155-7
- Stein JC, Wang R, Adler N et al. Emergency physician ultrasonography for evaluating patients at risk for ectopic pregnancy: a meta-analysis, Ann Emerg Med, 2010;56:674-83
- Cacciatore B, Stenman UH, Ylostalo P, Comparison of abdominal and vaginal sonography in suspected ectopic pregnancy, Obstet Gynecol, 1989;73:770
- Li TC, Tristram A, Hill AS, Cooke ID, A review of 254 ectopic pregnancies in a teaching hospital in the Trent Region, 1977-1990, Hum Reprod, 1991;6:1002-7.
- Elson J, Tailor A, Banerjee S, Salim R, Hillaby K, Jurkovic D, Expectant management of tubal ectopic pregnancy: prediction of successful outcome using decision tree analysis, Ultrasound Obstet Gynecol, 2004;23:552-6
- Barnhart KT, Gosman G, Ashby R, Sammel M, The medical management of ectopic pregnancy: a meta-analysis comparing "single dose" and "multidose" regimens, Obstet Gynecol, 2003;101:778-784
- Mol F, Mol BW, Ankum WM, van der Veen F, Hajenius PJ. Current evidence on surgery, systemic methotrexate and expectant management in the treatment of tubal ectopic pregnancy: a systematic review and meta-analysis. Hum Reprod Update 2008;14:309-319
- Lundorff P, Thorburn J, Hahlin M, Kallfelt B, Lindblom B, Laparoscopic surgery in ectopic pregnancy. A randomised trial versus laparotomy, Acta Obstet Gynecol Scand, 1991;70:343-48.

