Poly(oxyde de phénylène)
| Poly(oxyde de 2,6-diméthyl-1,4-phénylène) | |
| |
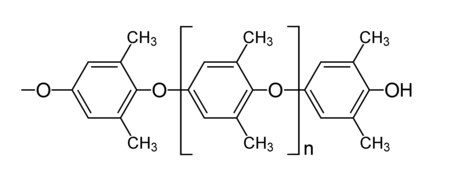
| Structure du poly(oxyde de 2,6-diméthyl-1,4-phénylène) | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.110.020 |
| No CE | 607-561-6 |
| PubChem | 11335 |
| ChEBI | 180557 |
| SMILES | |
| InChI | |
| Apparence | poudre[1] |
| Propriétés chimiques | |
| Formule | [C6H2(CH3)2O]n |
| Propriétés physiques | |
| Masse volumique | 1,6 g/mL[1] à 25 °C |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
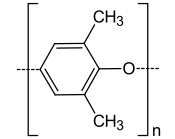
Un poly(oxyde de p-phénylène) (PPO) ou poly(éther de p-phénylène) (PPE), souvent simplifié en oxyde de polyphénylène, est un polymère organique thermoplastique adapté aux températures élevées. Le principal d'entre eux, le poly(oxyde de 2,6-diméthyl-1,4-phénylène), est constitué de monomères 2,6-xylénol.
-
Poly(oxyde de 1,4-phénylène) non substitué.
-
Poly(oxyde de 2,6-diméthyl-1,4-phénylène).
Le PPO est un plastique amorphe à hautes performances (en). Sa température de transition vitreuse est de 215 °C[2] mais peut être modulée en mélangeant le polymère avec du polystyrène. Ses propriétés générales peuvent être ajustées très largement en modifiant les molécules et incorporant des charges telles que des fibres de verre. Il a été produit pour la première fois en 1959 par Allan Hay (en)[3] et commercialisé dès 1960 par General Electric.
Production[modifier | modifier le code]
La réaction de 2,6-xylénol avec du chlorure de cuivre(I) CuCl ou du chlorure de cuivre(II) CuCl2 dans la pyridine en présence d'oxygène atmosphérique permet d'obtenir du PPO[4]. Le chlorure de cuivre(I) est d'abord oxydé par l'oxygène de l'air pour former du chlorure de cuivre(II), lequel reçoit un électron du 2,6-xylénol pour redonner du CuCl par réduction. Ce mécanisme se répète avec une autre molécule de 2,6-xylénol afin de former deux radicaux 2,6-xylénol susceptibles de dimériser, le dimère de 2,6-xylénol lui-même pouvant former un radical en cédant un électron au CuCl2 : cette réaction peut se répéter n fois et est appelée couplage oxydant ; comme cette réaction libère de l'eau comme produit de condensation, les PPO sont des polymères de condensation.
Certains PPO peuvent être obtenus par voie enzymatique à partir de phénols naturels (en). Ainsi, l'acide syringique peut être polymérisé par une laccase et une peroxydase pour donner un poly(oxyde de 1,4-phénylène) portant un groupe carboxyle à une extrémité et un hydroxyle phénolique de l'autre[5].
Applications[modifier | modifier le code]
On utilise rarement le PPO sous forme pure en raison des difficultés à le traiter, de sorte qu'on l'utilise plutôt en mélange avec du polystyrène, du copolymère styrène-butadiène choc, ou du polyamide. La SABIC distribue diverses résines de PPO sous la marque déposée Noryl[6], mais d'autres groupes tels que Asahi Kasei, BASF, Degussa, Mitsubishi Chemical ou encore Sumitomo Chemical ont également ce polymère en catalogue.
Les mélanges de PPO sont utilisés pour réaliser des pièces de structure, en électronique, dans l'électroménager, et dans les équipements automobiles dès lors qu'on a besoin de stabilité thermique à haute température, de stabilité dimensionnelle (conservation des longueurs et des formes) et de précision géométrique. On les utilise également en médecine pour les instruments devant être stérilisés[7]. Ils se caractérisent par une résistance élevée à l'eau chaude, une faible absorption d'eau, une résistance élevée aux chocs (résilience) et au feu (sans agent ignifuge bromé) et avec une faible masse volumique.
Ces polymères sont mise en forme par moulage par injection ou par extrusion. La température de traitement varie de 260 à 300 °C selon le type de matériau. Leur surface peut être imprimée, estampée à chaud (en), peinte ou métallisée. Ils peuvent être soudés au moyen d'un élément chauffant, d'un soudage par friction ou par ultrasons (en) ; ils peuvent être collés avec des solvants halogénés ou divers adhésifs.
On utilise également des PPO dans les systèmes de séparation des gaz par membrane (en) pour la production d'azote. Le polymère est filé dans une membrane à fibres creuses avec une couche de support poreuse et un revêtement extérieur très fin. La perméation de l'oxygène a lieu de l'intérieur vers l'extérieur à travers le revêtement externe avec un flux élevé. Les fibres sont très résistantes et très stables en raison de leur processus de fabrication. Contrairement aux membranes à fibres creuses en polysulfone, les fibres vieillissent rapidement de sorte que les performances de séparation des gaz de l'air demeurent stables tout au long de la durée de vie de la membrane. Les PPO permettent d'adapter les performances de séparation des gaz de l'air aux températures de l'ordre de 2 à 21 °C tandis que les membranes en polysulfone ont besoin d'air chauffé pour accroître la perméation.
Notes et références[modifier | modifier le code]
- Fiche Sigma-Aldrich du composé Poly(2,6-dimethyl-1,4-phenylene oxide) analytical standard, Mw 30,000 (Typical), Mn 20,000 (Typical), consultée le 1 octobre 2022..
Fiche de données de sécurité : (en) « Poly(2,6-dimethyl-1,4-phenylene oxide) » [PDF], sur sigmaaldrich.com, Sigma-Aldrich, (consulté le ). - (en) E. Kaisersberger, S. Knappe et H. Möhler, « TA for Polymer Engineering-DSC, TG, DMA: DSC, TG and DMA Results of Investigations of Thermoplastics, Thermosets, Paints, Elastomers, Rubber and Additives », Netzsch Annual for Science and Industry, vol. 2, , p. 83.
- (en) A. S. Hay, H. S. Blanchard, G. F. Endres et J. W. Eustance, « Polymerization by Oxidative Coupling », Journal of the American Chemical Society, vol. 81, no 23, , p. 6335-6336 (DOI 10.1021/ja01532a062, lire en ligne).
- (de) Martin Bartmann et Udo Kowalczik, « Zum Mechanismus der oxidativen Kupplung von Phenolen », Die Makromolekulare Chemie, vol. 189, no 10, , p. 2285-2292 (DOI 10.1002/macp.1988.021891008, lire en ligne).
- (en) Hiroshi Uyama, Ryohei Ikeda, Shigeru Yaguchi et Shiro Kobayashi, « Enzymatic Polymerization of Natural Phenol Derivatives and Enzymatic Synthesis of Polyesters from Vinyl Esters », Polymers from Renewable Resources, vol. 764, , p. 113-127 (DOI 10.1021/bk-2000-0764.ch009, lire en ligne).
- (de) D. Alberti, « Modifizierte aromatische Polyether », Kunststoffe, vol. 77, no 10, , p. 1001-1003.
- (de) Arnold Hohmann et Werner Hielscher, Lexikon der Zahntechnik, Neuer Merkur, (ISBN 978-3-929360-28-8).