« Récepteur Fc » : différence entre les versions
Créé en traduisant la page « Fc receptor » Balises : Nowiki dans un article Traduction de contenu |
(Aucune différence)
|
Version du 21 mars 2018 à 16:21
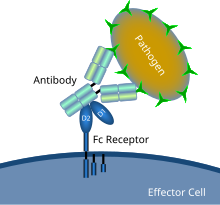
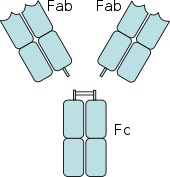
Un récepteur Fc est une protéine présente à la surface de certaines cellules -, dont les lymphocytes B, les cellules dendritiques folliculaires, les lymphocytes, les macrophages, les neutrophiles, les éosinophiles, les basophiles, les thrombocytes et les mastocytes – qui contribuent aux fonctions protectrices du système immunitaire. Son nom est dérivé de sa spécificité de liaison pour une partie d'un anticorps connue sous le nom de région Fc (Fragment cristallisable). Les récepteurs Fc se lient aux anticorps qui sont attachés aux cellules infectées ou aux pathogènes les envahissant. Leur activité stimule la destruction des microbes par des cellules phagocytes ou cytotoxiques, ou des cellules infectées par phagocytose ou cytotoxicité à médiation cellulaire dépendante des anticorps. Certains virus tels que les flavivirus utilisent les récepteurs Fc pour infecter les cellules, par un mécanisme connu sous le nom de facilitation facilitation dépendante des anticorps.[1]
Classes
Il existe plusieurs types de récepteurs Fc (en abrégé FcR), qui sont classés en fonction du type d'anticorps qu'ils reconnaissent. La lettre latine utilisée pour identifier un type d'anticorps est remplacée par la lettre grecque correspondante, après " Fc " pour former le nom du récepteur. Par exemple, ceux qui se lient le plus communément à la classe des anticorps IgG, sont appelés récepteurs Fc-gamma récepteurs (FcyR) ; ceux qui se lient à IgA sont appelés récepteurs Fc-alpha (FcaR) et ceux qui se lient à IgE sont appelés récepteurs Fc-epsilon (FceR). On distingue aussi les classes de FcR en fonction des cellules qui les expriment (macrophages, granulocytes, lymphocytes NK, cellules tueuses naturelles, les cellules T et B) et des propriétés de signalisation de chaque récepteur.[2]
Fc-gamma récepteurs
L'ensemble des récepteurs Fcy récepteurs (FcyR) appartiennent à la superfamille des immunoglobulines et les plus importants sont les récepteurs Fc induisant la phagocytose de microbes opsonisés (marqués).[3] Cette famille comprend plusieurs membres, FcyRI (CD64), FcyRIIA (CD32), FcyRIIB (CD32), FcyRIIIA (CD16a), FcyRIIIB (CD16b), qui diffèrent dans leurs affinités anticorps en raison de leurs différentes structures moléculaires.[4] Par exemple, FcyRI se lie à IgG plus fortement que FcyRII ou FcyRIII. FcyRI a aussi une partie extracellulaire composé de trois domaines de type immunoglobuline (Ig), soit un de plus que FcyRII ou FcyRIII. Cette propriété permet à FcyRI de se lier à une molécule isolée d'IgG (ou monomère), mais tous les récepteurs Fcy doivent se lier à plusieurs molécules d'IgG au sein d'un complexe immunitaire pour être activés.[5]
Les récepteurs Fc-gamma se distinguent par leur affinité pour les IgG et de la même manière les différentes sous-classes d'IgG ont des affinités pour chacun des récepteurs Fc gamma. Ces interactions sont de plus contrôlées par le glycane (oligosaccharides) présent à la position CH2-84.4 des IgG. Par exemple, en créant un encombrement stérique, la fucose contenant CH2-84.4 glycanes réduit l'affinité des IgG affinité pour FcyRIIIA. En revanche, les glycanes G0, qui manquent de galactose et se terminent par des groupements GlcNAc, ont une affinité accrue pour FcyRIIIA.
Un autre FcR est exprimé sur plusieurs types de cellules et possède une structure similaire à celle du la classe I du CMH. Ce récepteur se lie également aux IgG et est impliqué dans la préservation de cet anticorps.[6] Toutefois, comme ce récepteur Fc est également impliqué dans le transfert des IgG de la mère via le placenta à son fœtus ou via le lait au nourisson qu'elle allaite, il est appelé récepteur Fc néonatal Fc (FcRn).[7][8] Récemment, la recherche a suggéré que ce récepteur joue un rôle dans l'homéostasie des niveaux d'IgG sériques.
Récepteurs Fc- alpha
Un seul récepteur Fc appartient au sous-groupe Fca , il s'agit de FcaRI (ou CD89)[9]. FcaRI se trouve sur la surface des neutrophiles, des éosinophiles, monocytes, de certains macrophages (y compris les cellules de Kupffer), et de quelques cellules dendritiques. Il est composé de deux domaines extracellulaire de type Ig, et fait partie à la fois de la superfamille des immunoglobulines et de la famille des récepteurs de reconnaissance immunitaire multi-chaîne (MIRR). Il signale en s'associant avec deux FcRy de signalisation des chaînes. Un autre récepteur peut également se lier aux IgA, même si il a une plus grande affinité pour un autre anticorps IgM.[10] Ce récepteur est appelé récepteur Fc-alpha/mu (Caf/µR) et est un type I de protéine transmembranaire. Avec un domaine de type Ig dans sa partie extracellulaire, ce récepteur Fc est également un membre de la superfamille des immunoglobulines.[11]
Récepteurs Fc-epsilon
Deux types de FceR sont connus :
- Le récepteur FceRI de forte affinité est un membre de la superfamille des immunoglobulines (il a deux domaines de type Ig). On trouve FceRI sur les cellules de Langerhans épidermiques, les éosinophiles, les mastocytes et les basophiles[12][13] En raison de sa distribution cellulaire, ce récepteur joue un rôle majeur dans le contrôle des réactions allergiques. FceRI est également exprimé sur les cellules présentatrices de l'antigène, et contrôle la production d'importants médiateurs immunitaires appelées cytokines qui favorisent l'inflammation.[14]
- le récepteur de faible affinité FceRII (CD23) est une lectine de type C. FceRII a de multiples fonctions qu'il soit liée à la membrane ou comme récepteur soluble ; il contrôle la la croissance et la différenciation des cellules B et bloque la liaison IgE des éosinophiles, monocytes et des basophiles[15].
Tableau récapitulatif
| Nom du récepteur | Principal ligand anticorps | Affinité pour le ligand | Cellules concernées distribution | Effect following binding to antibody |
| FcγRI (CD64) | IgG1 et IgG3 | Forte (Kd ~ 10−9 M) | Macrophages Neutrophiles |
Phagocytosis Cell activation |
| FcγRIIA (CD32) | IgG | Faible (Kd > 10−7 M) | Macrophages Neutrophils |
Phagocytosis Degranulation (eosinophils) |
| FcγRIIB1 (CD32) | IgG | Faible(Kd > 10−7 M) | B Cells |
No phagocytosis Inhibition of cell activity |
| FcγRIIB2 (CD32) | IgG | Faible (Kd > 10−7 M) | Macrophages Neutrophils |
Phagocytosis Inhibition of cell activity |
| FcγRIIIA (CD16a) | IgG | Faible (Kd > 10−6 M) | NK cells Macrophages (certain tissues) |
Induction of antibody-dependent cell-mediated cytotoxicity (ADCC) Induction of cytokine release by macrophages |
| FcγRIIIB (CD16b) | IgG | Low (Kd > 10−6 M) | Eosinophils Macrophages |
Induction of microbe killing |
| FcεRI | IgE | High (Kd ~ 10−10 M) | Mast cells Eosinophils |
Degranulation Phagocytosis |
| FcεRII (CD23) | IgE | Low (Kd > 10−7 M) | B cells Eosinophils |
Possible adhesion molecule IgE transport across human intestinal epithelium |
| FcαRI (CD89) | IgA | Low (Kd > 10−6 M) | Monocytes Macrophages |
Phagocytosis Induction of microbe killing |
| Fcα/μR | IgA and IgM | High for IgM, Mid for IgA | B cells Mesangial cells |
Endocytosis Induction of microbe killing |
| FcRn | IgG | Monocytes Macrophages |
Transfers IgG from a mother to fetus through the placenta Transfers IgG from a mother to infant in milk |
Fonctions
Les récepteurs Fc sont présents sur nombre de cellules du système immunitaire, dont les phagocytes tels que macrophages et monocytes, les granulocytes tels que les neutrophiles et les éosinophiles et les lymphocytes du système immunitaire inné (cellules tueuses naturelles) ou du système immunitaire adaptatif (par exemple, les cellules B)[16][17][18]. Ils permettent à ces cellules de se lier aux anticorps qui sont attachés à la surface des microbes ou aux microbes de cellules infectées, en aidant ces cellules à identifier et à éliminer les microbes pathogènes. Les récepteurs Fc lient les anticorps à leur région Fc, une interaction qui active la cellule possèdant le récepteur Fc.[19] L'activation des phagocytes est la fonction la plus communément attribuée aux récepteurs Fc. Par exemple, les macrophages commencent à ingérer et à tuer les agents pathogènes enveloppés d'IgG en les phagocytant quand ils se sont liés à leurs récepteurs Fcy[20]. Un autre processus impliquant les récepteurs Fc est appelé anticorps-dépendante de la cytotoxicité à médiation cellulaire (ADCC). Au cours de l'ADCC, les récepteurs FcyRIII présents sur la surface des lymphocytes NK, stimulent la libération de molécules cytotoxiques à partir de leurs granules par les cellules NK, pour tuer les anticorps couvertes de cellules cibles couvertes d'anticorps.[21] FceRI a une fonction différente. FceRI est le récepteur Fc des granulocytes, qui est impliqué dans les réactions allergiques et de défense contre les parasites infectieux. Lorsqu'un certain allergique de l'antigène ou du parasite est présent, la réticulation d'au moins deux des IgE des molécules et de leurs récepteurs Fc sur la surface des granulocytes va déclencher les cellules pour libérer rapidement les médiateurs préformés de ses granules.
Les mécanismes de signalisation - récepteurs Fc gamma
Activation
Les récepteurs Fc gamma générent des signaux à l'intérieur de leurs cellules à travers un important motif d'activation appelé Immunorécepteurs tyrosine-based activation motif (ITAM).[22] Un ITAM est une séquence spécifique d' acides aminés (YXXL) se produisant deux fois en succession à proximité de la concentration intracellulaire de la queue d'un récepteur. Lorsque des groupes phosphate sont ajoutés à des résidus de tyrosine (Y) de l'ITAM par des enzymes appelées tyrosine kinases, une cascade de signalisation est générée à l'intérieur de la cellule. Cette réaction de phosphorylation suit généralement l'interaction d'un récepteur Fc avec son ligand. Un ITAM est présent dans la queue intracellulaire de FcyRIIA, et sa phosphorylation induit la phagocytose des macrophages. FcyRI et FcyRIIIA n'ont pas d'ITAM mais peuvent transmettre une activation du signal à leurs phagocytes par l'intermédiaire d'une autre protéine. Cette protéine adaptatrice est appelée sous-unité Fcy et, comme FcyRIIA, contient les deux séquences YXXL séquences qui sont caractéristiques d'un ITAM.
Références
- « Manipulation of cell surface macromolecules by flaviviruses », Advances in Virus Research, vol. 159, , p. 229–74 (PMID 14696331, DOI 10.1016/S0065-3527(03)59007-8)
- (en) Judith Owen, Jenni Punt, Sharon Stranford et Patricia Jones, Immunology, New York, 7th, (ISBN 978-14641-3784-6), p. 423
- « Fc receptors and immunoglobulin binding factors », FASEB Journal, vol. 5, no 12, , p. 2684–90 (PMID 1916092)
- « The molecular dissection of Fc gamma receptor mediated phagocytosis », Blood, vol. 86, no 12, , p. 4389–99 (PMID 8541526)
- « Binding of monomeric immunoglobulin G triggers Fc gamma RI-mediated endocytosis », The Journal of Biological Chemistry, vol. 269, no 39, , p. 24396–402 (PMID 7929100)
- « MHC class I-related neonatal Fc receptor for IgG is functionally expressed in monocytes, intestinal macrophages, and dendritic cells », Journal of Immunology, vol. 166, no 5, , p. 3266–76 (PMID 11207281, PMCID 2827247, DOI 10.4049/jimmunol.166.5.3266)
- « The MHC class I-related receptor, FcRn, plays an essential role in the maternofetal transfer of gamma-globulin in humans », International Immunology, vol. 13, no 8, , p. 993–1002 (PMID 11470769, DOI 10.1093/intimm/13.8.993)
- « New functions of the MHC class I-related Fc receptor, FcRn », Biochemical Society Transactions, vol. 25, no 2, , p. 481–6 (PMID 9191140, DOI 10.1042/bst0250481)
- « The Fc receptor for IgA (FcalphaRI, CD89) », Immunology Letters, vol. 92, nos 1–2, , p. 23–31 (PMID 15081523, DOI 10.1016/j.imlet.2003.11.018)
- « Molecular and functional characteristics of the Fcalpha/muR, a novel Fc receptor for IgM and IgA », Springer Seminars in Immunopathology, vol. 28, no 4, , p. 377–82 (PMID 17061088, DOI 10.1007/s00281-006-0050-3)
- « Molecular characteristics of IgA and IgM Fc binding to the Fcalpha/muR », Biochemical and Biophysical Research Communications, vol. 345, no 1, , p. 474–8 (PMID 16681999, DOI 10.1016/j.bbrc.2006.04.084)
- « A review on Fc epsilon RI on human epidermal Langerhans cells », International Archives of Allergy and Immunology, vol. 104 Suppl 1, no 1, , p. 63–4 (PMID 8156009, DOI 10.1159/000236756)
- « 5. IgE, mast cells, basophils, and eosinophils », The Journal of Allergy and Clinical Immunology, vol. 117, no 2 Suppl Mini-Primer, , S450-6 (PMID 16455345, DOI 10.1016/j.jaci.2005.11.016)
- « The central role of FcepsilonRI in allergy », Clinical and Experimental Dermatology, vol. 28, no 2, , p. 184–7 (PMID 12653710, DOI 10.1046/j.1365-2230.2003.01209.x)
- « Structure and function of Fc epsilon receptor II (Fc epsilon RII/CD23): a point of contact between the effector phase of allergy and B cell differentiation », Ciba Foundation Symposium, vol. 147, , p. 23-31; discussion 31-5 (PMID 2695308)
- « Functional regulation of human neutrophil Fc gamma receptors », Immunologic Research, vol. 29, nos 1–3, , p. 219–30 (PMID 15181284, DOI 10.1385/IR:29:1-3:219)
- « Divergent signal transduction pathways and effects on natural killer cell functions induced by interaction of Fc receptors with physiologic ligands or antireceptor antibodies », Natural Immunity, vol. 14, no 3, , p. 123–33 (PMID 8832896)
- « Expression, regulation and function of human Fc epsilon RII (CD23) antigen », Immunologic Research, vol. 11, nos 3–4, , p. 260–72 (PMID 1287120, DOI 10.1007/BF02919132)
- « Fc receptors and their interactions with immunoglobulins », Annual Review of Cell and Developmental Biology, vol. 12, , p. 181–220 (PMID 8970726, DOI 10.1146/annurev.cellbio.12.1.181)
- « The coordination of signaling during Fc receptor-mediated phagocytosis », Journal of Leukocyte Biology, vol. 76, no 6, , p. 1093–103 (PMID 15466916, DOI 10.1189/jlb.0804439)
- « Structure and function of natural-killer-cell receptors », Immunologic Research, vol. 27, nos 2–3, , p. 539–48 (PMID 12857997, DOI 10.1385/IR:27:2-3:539)
- New nomenclature for the Reth motif (or ARH1/TAM/ARAM/YXXL) Cambier J.C. (1995) Immunology Today Feb;16(2):110 DOI: 10.1016/0167-5699(95)80105-7
Erreur de référence : La balise <ref> nommée « immune_glycan » définie dans <references> n’est pas utilisée dans le texte précédent.
