Santonine
| Santonine | |||
| |||
| Identification | |||
|---|---|---|---|
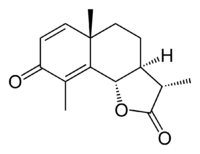
| Nom UICPA | (3S,3aS,5aS,9bS)-3,5a,9-triméthyl-3a,4,5,9b-tétrahydro-3H-benzo[g][1]benzofuran-2,8-dione | ||
| No CAS | |||
| No ECHA | 100.006.874 | ||
| No CE | 207-560-7 | ||
| No RTECS | LE3150000 | ||
| PubChem | 221071 | ||
| SMILES | |||
| InChI | |||
| Apparence | poudre cristalline beige[1] | ||
| Propriétés chimiques | |||
| Formule | C15H18O3 [Isomères] |
||
| Masse molaire[2] | 246,301 6 ± 0,014 2 g/mol C 73,15 %, H 7,37 %, O 19,49 %, |
||
| Propriétés physiques | |||
| T° fusion | 172-173 °C[1] 175 °C[3] |
||
| Solubilité | eau : 200 mg·l-1[3] | ||
| Cristallographie | |||
| Système cristallin | orthorhombique | ||
| Classe cristalline ou groupe d’espace | (no 19) [4] |
||
| Précautions | |||
| SGH[1] | |||
| H302, H310, H315, H319, H330, H335, P260, P280, P284, P310, P302+P350 et P305+P351+P338 |
|||
| Transport[1] | |||
|
|||
| Écotoxicologie | |||
| DL50 | 900 mg/kg (souris, oral)[1],[3] 180 mg/kg (souris, i.v.)[3] 130 mg/kg (souris, i.p.)[3] |
||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
La santonine ou plus exactement la (−)-α-santonine est un composé organique de la famille des naphtofuranes qui a été largement utilisé comme médicament anthelminthique c'est-à-dire que paralysant les vers, elle leur permet de quitter le corps. La santonine était autrefois répertoriée aux États-Unis et dans la pharmacopée britannique mais des ascaricides plus sûrs et mieux homologués médicalement existent dans la plupart des pays[5].
Structure
[modifier | modifier le code]La structure cristallographique de la santonine a été déterminée deux fois dans le groupe d'espace P212121 (no 19) avec comme paramètres de maille, α,β et γ égaux à 90° et :
| Paramètre | CCDC 794012[4] | CCDC 864314[6] |
|---|---|---|
| a | 699,62(5) pm | 689,00(3) pm |
| b | 1071,76(8) pm | 1050,97(4) pm |
| c | 3457,2(3) pm | 3447,63(13) pm |
Biosynthèse
[modifier | modifier le code]
La biosynthèse complète de l'α-santonine n'a pas été élucidée, mais l'α-santonine présente une grande similitude avec le parthénolide. La biosynthèse proposée commence par la cyclisation du farnésyl diphosphate (FPP) en (+)-germacrène A par une sesquiterpène synthase. La (+)-germacrene A hydroxylase hydroxyle alors la chaîne latérale d'isopropényle. L'oxydation du germacratrién-12-ol en acide germacratrién-12-oïque via l'intermédiaire germacratrién-12-al, est réalisée par une ou des déshydrogénases dépendantes du NADP. L'acide germacratrien-12-oïque est ensuite hydroxylé à C6 suivi ensuite par la lactonisation formant le (+)-costunolide[7].
Il a été proposé que le méthylène du (+)-costunolide soit réduit avant la deuxième fermeture du cycle. Le système cyclique de la décaline bicyclique est formé par le cation eudesmyle suivi d'une hydroxylation en C1. Une oxydation supplémentaire en C3 forme le β-cétohydroxyle qui, après élimination de H2O, complète la voie de biosynthèse proposée de l'α-santonine[8].
Réactions et propriétés
[modifier | modifier le code]La santonine peut être convertie en acide santonique (C15H20O4) via une hydrolyse à catalyse modérée suivie d'un processus de réarrangement en plusieurs étapes[9].
La santonine se dissout dans les alcalis avec formation de sels de cet acide carboxylique. La santonine, dans une solution d'acide acétique, exposée au soleil pendant environ un mois, est convertie en acide photosantonique (C15H22O5) qui est incolore et généralement considéré comme moins toxique. L'ester éthylique de ce dernier est obtenu lorsqu'une solution alcoolique de santonine est exposée au soleil (Sestini). La santonine est optiquement lévogyre.
La santonine est un produit chimique organique constitué de prismes plats incolores et inodores, devenant légèrement jaunes sous l'action de la lumière et soluble dans l'éthanol, le chloroforme, l'éther et l'eau bouillante. Ces prismes sont presque insipides lorsqu’ils sont mis en bouche pour la première fois, mais développent ensuite un goût amer[10].
Elle est dérivée de la santonica, les capitules non développés (pseudanthium) d’armoise maritime, Artemisia maritima var. Stechmanniana. Elle est aussi présente dans A. cina ou A. chamaemelifolia[11],[12].
Mode d'action
[modifier | modifier le code]La santonine a pour effet de paralyser l'extrémité antérieure (avant) du ver, tout en ayant un effet stimulant sur l'extrémité antérieure, en fonction de la concentration. De ce fait, le ver ne peut pas se coordonner et perd sa capacité à maintenir sa position dans l’hôte[13]. En utilisant un purgatif, le ver peut facilement être évacué. Des expériences menées dans les années 1880 ont montré que, même après 40 heures, la santonine n'avait pas d'effet mortel sur les vers ronds en utilisant une solution légèrement basique et saturée[14].
Usage pharmacologique historique
[modifier | modifier le code]Heckel et Schlagdenhauffen sont les premiers (1885) à signaler la présence d'une base organique de type alcaloïde dans les plantes à santonine[15], mais la vertu thérapeutique de ces plantes est connue depuis l'Antiquité.
La santonine, en grec Σαντóνιoς, est décrite par Dioscoride comme un vermifuge très apprécié à son époque. Elle tire son nom du peuple gaulois des Santons (capitale : Saintes[16]), dont elle aurait été originaire : il s'agissait vraisemblablement de l'Artemisia gallica[15], ou une sorte d'armoise.
La santonine est développée dans les années 1830 par les chimistes allemands en extrayant le produit chimique[réf. nécessaire] à partir d'Artemisia cina, une plante du Turkménistan[17]. À l’époque, les armoises était souvent utilisées comme antihelminthique et, en tant que plantes vivaces, elles étaient largement accessibles. Un remède commun dans le temps utilisait une infusion de 5-10 g de plante dans 500 ml d'eau. L'huile de ricin pourrait être utilisée pour faciliter le processus d'expulsion des vers. Il a été signalé qu'en 1843, des bonbons sous forme de pastilles et contenant de la santonine étaient disponibles en Allemagne.[réf. nécessaire]
La santonine a été utilisée du milieu du XIXe siècle aux années 1950 comme un anthelminthique, généralement administré avec un purgatif. La santonine a été utilisée dans le traitement de l'infestation par le ver Ascaris lumbricoides et chez les parasitoses à Ascaris en général et y compris la parasitose des Strongyloides stercoralis (anguillule). Cependant elle est inefficace dans le traitement de l'infection par des Eucestoda.[réf. nécessaire]
Un responsable de la société Eastern and Russian Trading a rapporté qu'en 1926, les fabricants japonais mélangeaient de la santonine dans presque toutes les pâtisseries, confiseries et toniques dans le cadre d'un effort gouvernemental visant à éradiquer les parasites intestinaux. Le Japon importait alors cinq tonnes de santonine de Russie chaque année et les États-Unis trois tonnes[18]. En 1885 Heckel et Schlagdenhauffen notent que la France est elle aussi tributaire sur ce point des importations de Russie et du Turkestan (où croissent abondamment l'Artemisia maritima et A. cina), et étudient l'Artemisia gallica pour la préparation de santonine[19].
L'Encyclopædia Britannica de 1911 note que la dose typique était de 2 à 5 grammes par jour[20]. Étant une dose totale, de nombreux traitements posent 3 doses par jour pendant 3 jours et la posologie « 3 cuillères à café 3 fois par jour pendant 3 jours » était habituelle vers la fin des années 1850 lorsque les doses de santonine commençaient à diminuer. La dose était plus proche de 20-30 milligrammes par dose adulte typique dans les années 1950, mais des doses « uniques » de santonine (en particulier par suppositoire) étaient courantes à la fin du XIXe siècle et au début du XXe siècle.[réf. nécessaire] Une préparation britannique enregistrée à partir de 1911 était le "trochiscus santonini" (pastille de santonine) et la préparation "sodii santoninas" (soude de santonine) était également autrefois une préparation officielle dans la pharmacopée américaine[20]. Des préparations commerciales contenant de la santonine (contenant également un laxatif purgatif) sont également apparues dans les listes de médicaments américaines jusque dans les années 1950. La Modern Drug Encyclopedia et Therapeutic Index de 1955 a répertorié un lombricide (produit par Massengill) et une préparation générique de santonine faite par Winthrop-Stearns (devenu depuis Winthrop-Sanofi).[réf. nécessaire]
La santonine a également été utilisée dans une moindre mesure dans le traitement de l’atonie de la vessie. Cet usage a largement diminué après le début du XXe siècle.[réf. nécessaire]
Les formes posologiques variaient pour la santonine. Initialement des pastilles et des suppositoires monodoses traitaient les infections à ascarides, tandis que dans les années 1950 les deux préparations de santonine disponibles aux États-Unis étaient des médicaments liquides.[réf. nécessaire]
Risques et difficultés d'utilisation
[modifier | modifier le code]La santonine est un médicament qui, comparé aux médicaments anthelminthiques plus modernes, est très compliqué à utiliser et comporte un risque assez grave pour le patient. Presque tous les médicaments à base de plantes contenant de la santonine indiquent le risque réel de vision en jaune et de réactions fatales. Même de petites doses de santonine provoquent des troubles de la vision, généralement une vision en jaune ou aussi en vert (xanthopsie ou chromathopsie). Même l'Encyclopædia Britannica (1911) a noté :
« … Ces effets passent généralement en quelques jours. De fortes doses, cependant, produisent des effets toxiques, une aphasie, des tremblements musculaires et des convulsions épileptiformes et les troubles de la vision peuvent aller jusqu'à la cécité totale »
— Encyclopædia Britannica (1911)[20].
Plus typique est l'avertissement concernant les effets secondaires de la santonine dans le King's American Dispensatory (en) :
« La santonine est un agent actif et, à des doses inappropriées, est capable de produire des symptômes graves et même la mort. Une dose aussi faible que 2 grains aurait tué un enfant de 5 ans, et 5 grains environ en une demi-heure chez un enfant du même âge ont le même effet, la mort. Parmi les effets toxiques, on peut citer les douleurs gastriques, la pâleur et la froideur de la peau, suivies de chaleur de la tête, de tremblements, de vertiges, de dilatation pupillaire, de secousses oculaires, de sueurs abondantes, d’hématurie, de convulsions, de crampes tétaniques, de la stupeur et de l'insensibilité. Parfois, des symptômes ressemblant au choléra morbus ont été produits et, dans tous les cas, l'urine présente une teinte caractéristique jaunâtre ou jaune verdâtre. Nous avons observé des convulsions causées par l'administration de «pastilles de ver». La mort par santonine est due à une paralysie respiratoire et l'examen post-mortem a révélé dans un cas un ventricule droit contracté et vide, et un peu de liquide, du sang noir dans le cœur gauche, un duodénum enflammé et des plaques enflammées dans l'estomac. »
— King's American Dispensatory (1905)[21]
La santonine produit souvent un effet singulier sur la vision, faisant apparaître les objets environnants décolorés, comme s'ils étaient jaunes ou verts et parfois bleus ou rouges; elle donne également une couleur jaune ou verte à l'urine et une couleur rouge-violet si ce liquide est alcalin. Le professeur Giovanni pense que la couleur jaune apparente des objets observés par l'œil, sous l'influence de la santonine, ne dépendait pas d'une action sélective sur les nerfs optiques, mais plutôt de la couleur jaune que le médicament lui-même prend quand il est exposé à l'air. L'air donne la couleur jaune à la santonine, à l'urine qui la contient et au sérum veineux. Selon Giovanni, c'est grâce à son action directe sur l'humeur aqueuse, où elle est portée par absorption, que les objets présentent cette couleur. L'idée maintenant acceptée, cependant, est celle d'Edmund Rose, que le sérum alcalin dissout la santonine, qui agit alors sur les centres de perspective du cerveau, produisant la chromathopsie ou la xanthopsie.
Même si la santonine est parmi les plus toxiques donc efficaces des anthelminthiques, le traitement vermifuge à la santonine est compliqué par rapport aux anthelminthiques plus modernes. En règle générale, la santonine doit être pris à jeun strictement (avant et après la prise du médicament) pour les posologies uniques ou sur un estomac plein, toutes les graisses et huiles étant écartées du régime pendant 2 à 3 jours avant le traitement et pendant traitement, et 2-3 jours après car la santonine est soluble dans les corps gras graisse et présente ainsi un risque accru d'effets secondaires. Après un traitement par la santonine, un purgatif doit être administré pour nettoyer le corps des vers morts.[réf. nécessaire]
En raison des effets secondaires graves (même lorsqu'elle est utilisée comme prescrit), du besoin d'un purgatif et du développement de nombreux médicaments vermifuges plus sûrs, l'utilisation de la santonine a complétement décru. Typiquement, le mébendazole ou le pamoate de pyrantel sont généralement utilisés dans la pharmacopée moderne. Même les guides de médecine holistique recommandent fortement d'éviter l'utilisation de la santonine[22]. La directive 65/65 du Conseil de l'Union européenne qui concerne les produits pharmaceutiques et les préparations naturopathiques, a officiellement déclaré que les préparations de santonine présentent un rapport bénéfice/risque « inacceptable » et que les préparations contenant de la santonine ne sont plus admissibles à l'enregistrement[23].
Santonine et absinthe
[modifier | modifier le code]Bien que l'absinthe soit certainement plus tristement célèbre pour sa teneur en thuyone[24], la liqueur contenait aussi de petites quantités de santonine[réf. nécessaire]. Il a été spéculé que l'art impressionniste, en particulier l'art de Van Gogh, pouvait être inspiré non pas par la thuyone et ses effets psychotropes présumés, mais par la vision en jaune ou xanthopsie, un effet secondaire connu de la santonine. Cela a toutefois été contesté, notamment par Arnold et Loftus en 1991, qui ont noté que la teneur en santonine aurait été insuffisante pour provoquer une xanthopsie.
Notes et références
[modifier | modifier le code]- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Santonin » (voir la liste des auteurs).
- Fiche Sigma-Aldrich du composé (−)-α-Santonin ≥99%, consultée le 15 août 2018. + (pdf) fiche SDS.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Santonine », sur ChemIDplus.
- CCDC 794012
- Modern Drug Encyclopedia and Therapeutic Index, 6e édition, Drug Publications Inc, 1955.
- CCDC 864314
- [Kraker et al. 2001] (en) Jan-Willem de Kraker, Maurice C. R. Franssen, Marcella C. F. Dalm, Aede de Groot et Harro J. Bouwmeester, « Biosynthesis of germacrene A carboxylic acid in chicory roots. Demonstration of a cytochrome P450 (+)-germacrene a hydroxylase and NADP+-dependent sesquiterpenoid dehydrogenase(s) involved in sesquiterpene lactone biosynthesis », Plant Physiol., vol. 125, no 4, , p. 1930-1940 (DOI 10.1104/pp.125.4.1930).
- [Barton, Moss & Whittle 1968] (en) D. H. R. Barton, G. P. Moss et J. A. Whittle, « Investigations on the Biosynthesis of Steroids and Terpenoids. Part I. A Preliminary Study of the Biosynthesis of Santonin », Journal of the Chemical Society, vol. 338, no 8, , p. 1813-1818 (résumé).
- (en) « Rearrangements Induced by Bases or Electron Rich Sites », paragraphe "Multistep Transformations", sur web.archive.org, Michigan State University (consulté en ).
- « Santoninum », The Pharmacopeia of the United States of America , 1916, p. 366.
- (en) « Santoninum (U.S.P.) », King's American Dispensatory (1898) (en), sur henriettes-herb.com (consulté en ).
- (en) « Wormseed, Levant », sur botanical.com (consulté en ).
- (en) Ernest Baldwin (en), « An in vitro method for the chemotherapeutic investigation of anthelminthic potency », Parasitology, vol. 35, no 3, , p. 89-111 (DOI 10.1017/S003118200002148X).
- Wilhelm von Schroeder, dans Archiv fur Experimentelle Pathologie und Pharmakologie, 1885, vol. 19, p. 290.
- [Heckel & Schlagdenhauffen 1885] Édouard Heckel et Frédéric Charles Schlagdenhauffen, « De l'Artemisia gallica Willd., comme plante à santonine, et de sa composition chimique », C.R. Hebd. Séances Acad. Sci., t. 100, , p. 804-806 (lire en ligne [sur gallica]).
- Le nom des Santons se retrouve aussi dans celui de la Saintonge.
- [Penati 2023] (en) Beatrice Penati, « Wormwood, nomads’ rights, and capitalism: the birth of a chemical industry in Russian Turkestan (1870s–1914) », Modern Asian Studies, vol. 57, no 4, , p. 1135-1197 (lire en ligne [sur cambridge.org], consulté en ).
- (en) « Santonin as a daily dose », Journal of the American Pharmaceutical Association, vol. 15, no 7, , p. 575 (DOI 10.1002/jps.3080150715, lire en ligne [sur archive.org]).
- [Keckel & Schlagdenhauffen 1885] « De l'Artemisia gallica Willd., comme plante à santonine, et de sa composition chimique », C.R. Hebd. Séances Acad. Sci., t. 100, , p. 804-806 (lire en ligne [sur gallica]).
- « Santonin », Encyclopædia Britannica, vol. 24, 1911, p. 195.
- Santoninum (U.S.P.), King's American Dispensatory (1905) (en), 1905, p. 1718.
- (en) « Worm infestations »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur indiangyan.com/books/healthbooks (consulté en ) (page accessible par Archive.is).
- « ??? »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?) [PDF], sur diahome.org (consulté en ).
- absinthe FAQ sur erowid.org, consulté le 15 août 2018.





