Rétrovirus endogène
Endorétrovirus
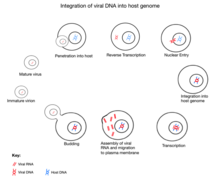
Un rétrovirus endogène (ERV, pour l'anglais endogenous retrovirus), ou endorétrovirus, est un endovirus (un élément viral endogène, EVE) issu d'un rétrovirus. Il s'agit ainsi d'une portion plus ou moins étendue du génome d'un rétrovirus (dont l'intégration au génome nucléaire de la cellule hôte est inhérente à leur cycle de réplication) qui, intégré à des cellules de la lignée germinale, a perdu sa capacité infectieuse et est devenue partie intégrante du génome de l'organisme où on l'a identifié.
Prévalence chez les espèces
[modifier | modifier le code]Des ERV ont été trouvés dans le génome de tous les eucaryotes étudiés[1], et sont généralement inactifs, et sans conséquence pathogène pour l'organisme. Ils sont en général présents en de multiples exemplaires dans le génome et constituent donc l'un des types de répétitions dispersées.
Origine
[modifier | modifier le code]L'origine des ERV est généralement attribuée à l'infection de cellules germinales (qui participent à la production des gamètes et assurant ainsi la transmission de leur patrimoine génétique aux générations suivantes) par un rétrovirus.
La plupart des rétrovirus infectent des cellules somatiques, mais ils peuvent aussi infecter des cellules germinales. Lorsqu'une telle infection a lieu et que les cellules survivent à l'infection (par exemple à cause d'une mutation du rétrovirus qui le rend défectif), le génome du rétrovirus peut être transmis à la génération suivante et persister dans la descendance au sein du génome de l'organisme sans avoir d'incidence notable sur son développement (ou les cas problématiques seraient éliminés par la sélection naturelle).
La plupart des rétrovirus endogènes connus ont envahi la lignée germinale de leur hôte depuis des millions d'années, si l'on en croit différentes horloges moléculaires. Le cas du rétrovirus KoRV (en) est particulier : impliqué dans le syndrome d'immunodéficience du Koala, il a commencé à envahir son génome germinal il y a seulement 50 000 ans. Il n'est pas présent chez tous les individus, ni toujours au même endroit du génome ; par ailleurs il se recombine avec un autre virus endogène et devient alors défectif. Il s'agit sans doute d'une transformation (d'un rétrovirus pathogène en un rétrovirus endogène et défectif) en train de s'accomplir[2],[3].
Contrôle par l'organisme
[modifier | modifier le code]On a montré en 2010 que l'expression de ces gènes dits « rétroéléments » est normalement inhibée par une protéine spécialisée dite « KAP1 (en) » responsable d'une méthylation des histones et ADN des rétroéléments, ce qui bloque (normalement définitivement) leur expression, et protège l'intégrité du reste du génome-hôte[4].
Plus précisément, la protéine KAP 1 joue un rôle de chef d'orchestre, en faisant appel à plusieurs protéines (histone-méthyltransférase ou SETDB1 (en), Hétérochromatine HP1 (en), complexe Histone-déacétylase NuRD (en) et de nombreuses autres protéines).
Ce processus complexe est activé dès le début de l'embryogenèse, qui, d'ailleurs, ne pourrait se poursuivre sans la protéine KAP 1, en raison de l'apparition de mutations délétères conduisant à la mort rapide de l'embryon[4].
On espère que mieux comprendre ce processus puisse aider à contrôler des rétrovirus comme le VIH ou celui de l'Herpès (HSV), qui ne sont que provisoirement « endormis »[4].
Des virus défectifs, mais pas nécessairement inactifs
[modifier | modifier le code]Bien que la séquence virale puisse être lue par la machinerie cellulaire de l'organisme, elle a subi au cours de l'évolution plusieurs mutations rendant généralement l'endovirus défectif, incapable de produire les protéines constituant les virions.
Bien qu'incapables d'assurer un cycle de réplication complet, les endorétrovirus ne sont pas toujours sans conséquences pour l'organisme hôte. Certains ont gardé leur pouvoir infectieux, notamment chez le porc et la souris voire l'homme[5]. Cette soudaine expression peut avoir diverses origines, comme les hormones, ou des facteurs externes à l'organisme comme des radiations ou l'exposition à des agents chimiques[1].
Certains gènes des endorétrovirus sont régulièrement exprimés, les protéines correspondantes ayant une utilité pour l'organisme. Les syncytines notamment, des protéines jouant un rôle important dans le développement du placenta (elles permettent le développement du syncytiotrophoblaste), sont codées par des gènes d'endorétrovirus, reliques de rétrovirus ayant infecté plusieurs fois les mammifères, de manière indépendante[6].
HERV
[modifier | modifier le code]
Les human endogenous retroviruses (HERV) n'ont été mis en évidence que depuis le séquençage du génome humain, et en représentent une partie importante (8 %, avec environ 98 000 éléments et fragments[5],[7], voire 450 000 si on compte tous les LTR[8]).
Les HERV sont classés en trois classes et plusieurs sous-groupes[5] :
- classe I : apparentée aux gammarétrovirus (en)
- classe II : apparentée aux bétarétrovirus (en)
- classe III : apparentée aux spumavirus (en)
Les rétrovirus des classes I et III sont plus anciens que ceux de la classe II, qui se seraient intégrés au génome du genre Homo il y a environ cinq millions d'années.
Bien que fortement soupçonnés, il n'y avait, en 2003, aucune preuve claire que les rétrovirus endogènes soient responsables, ou même constituent un cofacteur, de diverses maladies, comme les cancers, les maladies auto-immunes ou certaines affections neurologiques[5].
HERV-K
[modifier | modifier le code]HERV-K est une famille de rétrovirus endogènes qui a été intégrée au génome humain il y au moins 30 millions d'années. Cette famille est particulièrement étudiée, car il semblerait qu'elle ait encore été active il y a peu de temps, la rendant idéale pour distinguer les différents mécanismes de prolifération au sein du génome[7].
En 2006, une équipe de chercheurs de l'Institut Gustave-Roussy, à Villejuif, en France, a réussi, à partir d'une trentaine d'éléments copiés par ces rétrovirus au sein du génome humain, à reconstituer un rétrovirus, qu'ils ont appelé « Phœnix », et qui s'est révélé être capable d'assurer un cycle de réplication complet[9].
Dans la culture contemporaine
[modifier | modifier le code]Dans le roman L'Échelle de Darwin, Greg Bear, l'activation d'un HERV provoque des mutations et la transformation de l'espèce humaine en une autre.
Dans le roman « Gataca » Franck Thilliez, il est fait mention en page 546 d’un HERV qui provoque une flambée de violence chez les hommes entre 20 et 30 ans, afin de préserver la pureté génétique du genre Homo.
Notes et références
[modifier | modifier le code]- (en) Brian WJ Mahy, A Dictionary of Virology, Academic Press, (ISBN 0-12-465327-8), « Endogenous retrovirus », p. 122
- Aline Gerstner, « Invasion de rétrovirus en cours dans l'ADN des koalas », Pour la science, no 492, , p. 14.
- (en) Ulrike Löber, Matthew Hobbs, Anisha Dayaram, Kyriakos Tsangaras, Kiersten Jones et al., « Degradation and remobilization of endogenous retroviruses by recombination during the earliest stages of a germ-line invasion », PNAS, (DOI 10.1073/pnas.1807598115).
- (en) Helen M. Rowe, Johan Jakobsson, Daniel Mesnard, Jacques Rougemont, Séverine Reynard, Tugce Aktas, Pierre V. Maillard, Hillary Layard-Liesching, Sonia Verp, Julien Marquis, François Spitz, Daniel B. Constam et Didier Trono « KAP1 controls endogenous retroviruses in embryonic stem cells » Nature 2010;463:237-40. DOI 10.1038/nature08674
- Anne-Geneviève Marcelin et Vincent Calvez (Sous la direction de Jean-Marie Huraux), Traité de virologie médicale, Paris, Éditions Estem, , 699 p. (ISBN 2-84371-203-3, lire en ligne), « Rétrovirus humains émergents », p. 615
- Edward B. Chuong, « The placenta goes viral: Retroviruses control gene expression in pregnancy », PLOS Biology, vol. 16, no 10, , e3000028 (DOI 10.1371/journal.pbio.3000028, lire en ligne, consulté le ).
- (en) Robert Belshaw, Vini Pereira, Aris Katzourakis, Gillian Talbot, Jan Pačes, Austin Burt et Michael Tristem, « Long-term reinfection of the human genome by endogenous retroviruses », sur PubMed Central, Proceedings of the National Academy of Sciences of the United States of America, (consulté le )
- (en) International Human Genome Sequencing Consortium, « Initial sequencing and analysis of the human genome. », Nature, vol. 409, , p. 820-921 (PMID 11237011)
- (en) Marie Dewannieux, Francis Harper, Aurélien Richaud, Claire Letzelter, David Ribet, Gérard Pierron et Thierry Heidmann, « Identification of an infectious progenitor for the multiple-copy HERV-K human endogenous retroelements », Genome Research, (consulté le )
Voir aussi
[modifier | modifier le code]Bibliographie
[modifier | modifier le code]- Julie Medina, Benjamin Charvet, Pascal Leblanc, Raphaële Germi, Branka Horvat, Patrice N. Marche et Hervé Perron, « Des séquences rétrovirales endogènes dans le génome humain peuvent jouer un rôle physiologique ou pathologique [Endogenous retroviral sequences in the human genome can play a physiological or pathological role] », Med Sci (Paris), vol. 33, no 4, , p. 397-403. (DOI 10.1051/medsci/20173304009, lire en ligne [PDF])
- Pierre Ellul, Laurent Groc et Marion Leboyer, « Les rétrovirus endogènes humains, une implication dans la schizophrénie et le trouble bipolaire [Implication of human endogenous retroviruses in schizophrenia and bipolar disorder] », Med Sci (Paris), vol. 33, no 4, , p. 404-9. (DOI 10.1051/medsci/20173304010, lire en ligne [PDF])
