Photosynthèse artificielle
La photosynthèse artificielle est un procédé chimique qui imite la photosynthèse naturelle des plantes afin de transformer l'énergie solaire en énergie chimique.
La photosynthèse naturelle[modifier | modifier le code]
Définition[modifier | modifier le code]
La photosynthèse[1] existe chez les végétaux chlorophylliens et chez certaines bactéries (cyanophycées). Elle consiste en une suite de réactions biochimiques provoquées par la lumière, le type d'énergie faisant réagir des molécules minérales simples (CO2, H2O…). Ces réactions entraînent la production de molécules organiques glucidiques de masse molaire relativement faible. Certaines de ces molécules sont polymérisées en glucides de masse molaire élevée (amidon pour le stockage, saccharose pour le transport dans d'autres cellules), d’autres enfin s’unissent à des molécules azotées.
Le phénomène est caractérisé par une absorption de dioxyde de carbone et par un dégagement d’oxygène en présence de lumière (ou éventuellement de manière retardée dans le cas des cactées).
La photosynthèse est donc un terme dédié à la réaction s'opérant au sein des végétaux au contact de la lumière. On parlera cependant de photosynthèse artificielle lorsqu'il s'agit d'utiliser l'énergie lumineuse (notamment solaire) afin de réaliser des conversions énergétiques ne nécessitant pas la présence des cellules chlorophylliennes. Un domaine d'application de la photosynthèse artificielle est l'utilisation de panneaux photovoltaïques.
Rappels sur le rôle de la photosynthèse[modifier | modifier le code]
La photosynthèse permet aux organismes qui la pratiquent (végétaux, cyanobactéries, lichens) de stocker de l’énergie d'origine solaire, principalement sous forme de sucre (de l'amidon pour les plantes) pour répondre aux besoins présents et futurs de l'organisme[2]. Les organismes qui pratiquent la photosynthèse sont autotrophes[3]. Ils peuvent ainsi synthétiser des matières organiques (notamment des protéines) à partir de matières inorganiques et du rayonnement solaire.
Quelques animaux ont, au cours de l'évolution, appris à utiliser indirectement le mécanisme de la photosynthèse, via des endosymbioses. C'est spécifiquement le cas des coraux, de quelques vers plats, de l'éponge d'eau douce, Spongilla lacustris, de la Salamandre maculée (seul vertébré connu à ce jour (2011) qui ait pu établir une symbiose avec une algue, en l'occurrence Oophila amblystomatis) et de la limace de mer Elysia chlorotica (premier animal découvert capable d'utiliser la photosynthèse autrement que par symbiose avec une algue ; cette photosynthèse est effectuée par les chloroplastes de sa principale source de nourriture, l'algue Vaucheria litorea). À l'échelle planétaire, les algues et principalement le phytoplancton marin produisent le plus d’oxygène, suivis des forêts. Un domaine de recherche appliquée, la biomimétique, s'inspire de la nature pour développer des photosynthèses artificielles.
Le mécanisme de la photosynthèse[modifier | modifier le code]

La plante capte le dioxyde de carbone (CO2) présent dans l’air, et l’eau (H2O) dans le sol. L’énergie solaire est utilisée pour oxyder l’eau et réduire le gaz carbonique afin de synthétiser des substances organiques (glucides). Cette transformation se déroule dans les chloroplastes (organites cellulaires) qui contiennent la chlorophylle. Ce pigment assure l’absorption d’une partie de l’énergie des rayons solaires (bleus et rouges) qui rendent la photosynthèse possible. La photosynthèse a lieu au niveau des membranes thylakoïdes, une double membrane pigmentée qui se trouve à l’intérieur du chloroplaste chez les eucaryotes. C’est dans les thylakoïdes qu’a lieu la réaction lumineuse de la photosynthèse, là où se situent les photosystèmes 1 et 2 (Les photosystèmes interviennent dans les mécanismes de la photosynthèse en absorbant les photons de la lumière) et les cytochromes, protéines colorées qui transportent les électrons. Après plusieurs réactions chimiques entre l’énergie solaire, le CO₂ et l’H2O, du dioxygène (O2) et du sucre sont produits. L'O₂ est ensuite libéré dans l’atmosphère, et le sucre (généralement sous forme d'amidon) est stocké dans les fruits ou reste dans la feuille pour être transféré sous forme de saccharose dans la sève élaborée circulant dans les vaisseaux du phloème.
La phase claire[4] est un ensemble de réactions photochimiques dont le principe est de capter l’énergie lumineuse des photons et de la transmettre, via des électrons chargés de cette énergie, à une chaîne d’accepteur d’électrons (molécules ayant des potentiels d’oxydoréduction variables). Elles dépendent de la lumière, et durant leur déroulement, les électrons sont transportés à travers les deux photosystèmes (PSI et PSII), ce qui permet de produire de l’ATP, molécule riche en énergie et du NADPH,H+ (potentiel réducteur). L'ATP est synthétisé par la pompe ATP-synthase qui exploite le gradient protonique créé lors la réaction entre le lumen du thylakoïde et le stroma du chloroplaste. La phase claire permet donc directement la transformation de l’énergie lumineuse en énergie chimique, énergie qui sera forcément utilisée dans la phase sombre. La phase sombre correspond au cycle de Calvin, entièrement enzymatique et indépendant de la lumière, au cours duquel l’ATP et le NADPH,H+ produits sont utilisés pour la fixation du dioxyde de carbone en glucide. L’assimilation du CO2 se fait en quatre étapes principales, les trois premières se déroulant au sein du cycle de Calvin, la fixation du CO₂ (carboxylation) par la Rubisco puis sa réduction, la régénération de l’accepteur de CO₂ et la synthèse des sucres.
L'énergie captée chaque seconde par la photosynthèse — à l'échelle planétaire — est de l'ordre de 100 TJ, et c'est ce qui fournit toute l'énergie de la biosphère. C'est moins d'un millième de l'énergie solaire arrivant sur Terre (1,5 × 1018 kWh/an), mais c'est environ 10 fois plus que la consommation énergétique mondiale sur un an.
La photosynthèse artificielle[modifier | modifier le code]
Il existe plusieurs types de photosynthèses artificielles, tous à l’état de recherche ou de prototype. Une équipe du National Renewable Energy Laboratory rapporte en 1998 avoir créé un dispositif permettant de dissocier l'oxygène et l'hydrogène de l'eau à partir d'énergie solaire[5]. Mais, ce dispositif s’est révélé instable et trop cher[6],[7]. En 2007, une équipe de l’université de Kyoto annonce quant à elle avoir inventé un procédé capable de capter le CO2 atmosphérique 300 fois plus efficacement que les plantes. Néanmoins, la feuille artificielle (2011), le projet de Daniel Nocera[8], ancien chercheur au MIT (Massachusetts Institute of Technology) est le plus abouti technologiquement (il est le fruit de 25 années d’études et est en voie de commercialisation) et est représentatif du principe général qui est de dissocier l’eau pour produire de l’oxygène et du dihydrogène. Les projets concurrents utilisent différents matériaux pour provoquer cette réaction[9].
En 2010, des chercheurs du département de chimie de l'Université de Göteborg, en collaboration avec des équipes de l'École polytechnique Chalmers et d’autres universités européennes, ont observé grâce aux puissants rayons X de l'European Synchrotron Radiation Facility, les mouvements des atomes au sein de protéines engagées dans un processus de photosynthèse. L'expérience, qui a fourni des informations en trois dimensions sur des mouvements de l’ordre de 1,3 ångström de molécules, pourrait servir à créer des dispositifs faisant de la photosynthèse artificielle afin de produire l’énergie du futur à partir de la lumière du Soleil[10].
Une équipe franco-allemande de l'Institut Max Planck et une unité de recherche du CNRS ont construit en 2020, un chloroplaste artificiel qui convertit le CO₂ cent fois plus vite que les précédentes constructions semi-synthétiques[11].
Présentation de la feuille artificielle[modifier | modifier le code]
La feuille artificielle est composée d’un assemblage de fines couches de différents métaux[12] qui catalysent l’oxydation de l’eau une fois plongée dedans et exposée au soleil. Elle oxyde l’eau, comme dans la photosynthèse naturelle, et réassemble les atomes qui la composent de façon différente. Ces nouvelles molécules pourront être utilisées pour produire de l’énergie.

Le mécanisme de la feuille artificielle[modifier | modifier le code]
Équation chimique[modifier | modifier le code]
Comme dit précédemment, la feuille artificielle permet de reproduire l’oxydation de l’eau, puis d’utiliser les atomes et molécules obtenus pour en former de nouveaux. L’équation chimique de cette réaction est : 2 H2O ⇒ O2 + 4 H+ + 4 e−⇒ O2 + 2 H2
Les produits de la photosynthèse réalisée à partir de la feuille artificielle sont donc du dioxygène et du dihydrogène.
Les différents composants et leur utilisation[modifier | modifier le code]
La feuille artificielle est composée de différents métaux catalyseurs, le cobalt qui catalyse l'oxydation de l'eau, le silicium (utilisé dans les panneaux photovoltaïques) qui collecte les rayons lumineux et un alliage (nickel, molybdène, zinc) qui ressoude les électrons et les ions H+.
Le mécanisme[modifier | modifier le code]
Le silicium collecte l’énergie lumineuse, ce qui permet à l’eau de s’oxyder au contact du cobalt (l’oxydation est échange d’électrons) : 2 H2O ⇒ O2 + 4 H+ + 4 e−
Le dioxygène obtenu est sous forme de gaz (de bulles), il s’échappe donc du milieu. Le silicium recueille les électrons qui proviennent des atomes d’hydrogène et les envoie vers l’alliage tandis que les ions H+ se retrouvent dans l’eau. L’alliage permet ensuite d’assembler les ions H+ et les électrons : O2 + 4 H+ + 4 e−⇒ O2 + 2 H2
À la fin, nous obtenons ainsi du dioxygène et du dihydrogène, tous deux à l’état gazeux.
Avantages[modifier | modifier le code]
Ce type de production d'énergie se fait en consommant du CO₂, donc en luttant contre le réchauffement climatique[13].
Une feuille artificielle du type de celle de Daniel Nocera, contrairement aux autres technologies qui produisent de l’énergie à partir d’eau et d’électricité, ne nécessite pas un milieu très acide ni de l'eau très pure pour fonctionner. Elle fonctionne dans de l’eau à pH neutre, voire dans l’eau de mer. Et, les éléments du catalyseur s’autoassemblent si on leur fournit un peu d’énergie sous forme d’électricité. Et, si le bain dans lequel est plongée la feuille artificielle contient les éléments nécessaires, les catalyseurs se régénéreront seuls au fur et à mesure de leur consommation.
La dernière version de la feuille artificielle utilise des matériaux peu chers et communs (alors que les versions précédentes utilisaient du platine, de l’iridium ou du ruthénium rares et toxiques)[réf. nécessaire].
Productivité[modifier | modifier le code]
La feuille artificielle, tout comme la feuille naturelle, ne produit pas directement d’énergie, mais du dioxygène et du dihydrogène. Ces deux gaz peuvent ensuite être brûlés ou utilisés pour faire fonctionner une pile à combustible, et donc produire de l’électricité.
La feuille artificielle n’est pas encore compétitive : aujourd'hui, produire 1 kg d’hydrogène à partir d’une feuille artificielle coûte entre 5 et 6 €. Mais, produire la même quantité d’hydrogène à partir de méthane revient seulement à 2 € et à partir de panneaux solaires à moins de 2 € probablement aux environs de 2025[14],[15]. Et, la quantité d’électricité produite par rapport à la quantité d’énergie solaire reçue n’atteint que 2,5 % pour la feuille artificielle contre 15 à 20 % pour un panneau photovoltaïque. Les laboratoires de l’école polytechnique de Stockholm ont atteint un rendement de 300 molécules par seconde, comparable à celui des végétaux (100 à 400 molécules par seconde)[16].
Selon Daniel Nocera néanmoins, une première centrale électrique, de la taille d’un réfrigérateur, suffisante pour produire de l’énergie en quantité, aurait pu voir le jour dès 2013, avec un usage domestique plausible, mais en consommant de l'eau : une seule feuille immergée dans 4 litres d’eau suffirait à alimenter une maison en électricité pendant une journée. Il cherche à améliorer son système pour produire de l’hydrogène à 2,5 € le kilo, de manière à le rendre intéressant pour les pays pauvres ou en voie de développement.
Production d'énergie avec les produits de la photosynthèse artificielle[modifier | modifier le code]
La photosynthèse artificielle produit deux gaz, du dioxygène et du dihydrogène.
Propriétés des gaz[modifier | modifier le code]
Le dioxygène ou encore molécule d'oxygène est une molécule composée de deux atomes d'oxygène et de formule chimique O₂. Incolore, inodore et insipide, il participe à des réactions d'oxydo-réduction, essentiellement à la combustion et la corrosion. Il a été découvert en 1774 par Joseph Priestley, et baptisé oxygène par Lavoisier en 1778.
Le dihydrogène[17], aussi appelé molécule d’hydrogène existe à l'état gazeux aux conditions normales de pression et de température. Cette molécule est composée de deux atomes d'hydrogène et est de formule chimique H₂. Elle est présente sous forme de traces (0,5 ppmv) dans l’atmosphère. Elle brûle dans l'air en produisant de l'eau, d'où son nom composé étymologiquement par « hydro », du grec ὕδωρ (hudôr) signifiant « eau », et « gène », du grec γεννᾰν (gennen), « engendrer ». Le dihydrogène a un potentiel énergétique élevé (120 kJ/g contre 50 pour le gaz naturel[18]).
Production d'énergie[modifier | modifier le code]
L’hydrogène ayant été découvert il y a 300 ans[réf. souhaitée], de nombreux moyens d’en tirer de l’énergie ont été élaborés au cours des siècles tels que le voltamètre de Hofmann ou le moteur à hydrogène qui utilise le principe de la combustion du dihydrogène (H2) et du dioxygène (O2) pour laisser comme produit de l'eau (H2O) et de l'énergie[réf. souhaitée] (l'énergie dégagée par la combustion de 1 kilogramme d'hydrogène équivaut à celle de 3 kilogrammes d'essence[réf. souhaitée]). Il s'agit d'une réaction explosive qui actionne un piston de la même manière qu'avec l'essence ou le gazole. La réaction chimique est la suivante : 2 H2 + O2 → 2 H2O + Q (Q : quantité d'énergie libérée)[réf. souhaitée]
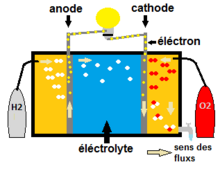
Le plus récent est la pile à combustible[19],[20],[21] c’est aussi le plus performant. Le principe de la pile à combustible est l’inverse de l’électrolyse. La pile à combustible est constituée d’une anode et d’une cathode séparées par un électrolyte, un matériau non-conducteur. L’anode est chargée en hydrogène ce qui signifie que projetée sur l’anode, le dihydrogène se sépare en deux molécules d’hydrogène en libérant un électron. Cet électron qui ne peut pas traverser l’électrolyte passe par l’anode conductrice, fournit de l’énergie au système branché sur la pile à combustible et passe par la cathode. La cathode est chargée en molécules de dioxygène. L’électron, l’atome d’hydrogène et l’atome oxygène se recomposent en formant de l’eau (H₂O, donc un atome d’oxygène et deux atomes d’hydrogène). On récupère donc de l’eau et de l’énergie sous forme de tension électrique d'environ 0,7 à 0,8 volt et de la chaleur (la température de fonctionnement varie de 60 à 200 °C selon les modèles)
Le rendement[modifier | modifier le code]
Le rendement de la pile à combustible est actuellement supérieur à 50 % (par comparaison, un moteur thermique d'automobile a un rendement qui varie entre 25 % et 30 %), ce qui signifie que l’énergie nécessaire à la production de l’hydrogène et l’oxygène (l’objectif étant que cette énergie soit fournie par le soleil) est récupérée à 50 %. Les 50 % restants sont dissipés en chaleur. Si l’on adjoint à la pile à combustible un système de récupération de chaleur (pour chauffer de l’eau par exemple), le rendement augmente jusqu’à 80 % voire 90 %.
Les dangers[modifier | modifier le code]
La pile à combustible ne présente pas de danger en elle-même, mais ses réactifs, en particulier l’hydrogène, ont une forte capacité à entrer en combustion. Ainsi, pour l'hydrogène, 20 microjoules sont suffisants, et sa concentration dans l'air peut la faire brûler ou exploser. Au-delà de 12 % de concentration dans l’air, la détonation génère 20 bars de pression et propage une flamme à 2 000 m/s. Malgré la dispersion rapide de l'hydrogène dans l'air, le risque d’explosion dans un milieu fermé est important, ce qui explique les recherches engagées pour trouver un moyen de stocker l'hydrogène sans risque. Les deux techniques de stockage actuelles sont le refroidissement à -273° (température du zéro absolu) et la compression (>200 bars) mais ne sont pas satisfaisantes en raison de leur consommation d'énergie et de leur sensibilité aux fuites. C’est pourquoi le stockage par solidification sous forme d’hydrures est privilégié (un hydrure est un composé chimique de l’hydrogène avec d’autres éléments, par exemple, le métal qui se présente comme une éponge). L’hydrogène ainsi stocké se présente sous forme de galette métallique solide ininflammable. Le processus est parfaitement réversible et les différents composés métalliques n’ont pas d’effet mémoire et peuvent resservir indéfiniment.
Avantages[modifier | modifier le code]
L’énergie dé-carbonée devient un enjeu majeur pour l'humanité confrontée au réchauffement climatique et aux pollutions dues aux hydrocarbures fossiles (véhicules, chauffages, centrale thermique...). Les panneaux photovoltaïques et les autres moyens renouvelables progressent mais sont encore trop limités ou coûteux par rapport aux besoins croissants des sociétés industrielles et/ou en expansion démographique. Le nucléaire est efficace mais pose des problèmes de déchets, de risques d'attaques terroristes et de prolifération nucléaire militaire.
Les moyens de recueillir l'énergie solaire autrement que via la biomasse sont encore peu performants. Les plantes utilisent l’énergie solaire via la photosynthèse pour produire du glucose et de la matière organique. La quantité d’énergie absorbée par les plantes est phénoménale mais ne représente qu’une toute petite partie de l’énergie solaire reçue par la terre (3 850 000 exajoules (EJ) par an en 2002). Les panneaux solaires sont une autre façon de récupérer cette énergie fournie en grande quantité par le soleil, l’énergie reçue en une heure correspondant à un an de consommation mondiale, et de la transformer en énergie électrique utilisable par l’homme, mais encore difficile à stocker massivement. Bien que le rendement moyen actuel de conversion des panneaux solaires soit passé d'environ 10 % à environ 20 % en quelques décennies, leur faible surface dans le monde ne leur permet de produire qu'une infime part des besoins mondiaux. Des scientifiques cherchent donc à imiter les plantes ou algues en tentant de catalyser une hydrolyse ou une oxydation de l’eau à la manière de la photosynthèse. Les produits de cette réaction sont l’oxygène et le dihydrogène, éléments qui peuvent être exploités comme combustibles ou utilisés dans une pile à combustible pour produire de l’électricité.
Notes et références[modifier | modifier le code]
- http://www.snv.jussieu.fr/bmedia/Photosynthese-cours/index.htm
- (en) « La photosynthèse », sur ikonet.com (consulté le ).
- « Pour en savoir plus : photosynthèse », sur univ-mrs.fr via Wikiwix (consulté le ).
- ORLUC Laurent, la source de la biodiversité, Science et vie no 1043
- « La photosynthèse artificielle : de l’énergie à partir de soleil et d’eau », sur Science étonnante, (consulté le ).
- « Accueil », sur Enerzine, (consulté le ).
- « Breakthrough in Artificial Photosynthesis Could Boost Solar Future / KTH », sur KTH (consulté le ).
- « American Chemical Society », sur American Chemical Society (consulté le ).
- science et vie junior numero 276 septembre
- futura-sciences.com du 12 mai 2010, A l'ESRF, on a photographié des atomes en pleine photosynthèse !
- Julie Kern, « Des chercheurs ont reproduit la photosynthèse artificiellement », sur futura-sciences.com,
- http://www.nature.com/nchem/journal/v4/n5/pdf/nchem.1301.pdf
- Aditya Prajapati & Meenesh R. Singh (2019). Assessment of Artificial Photosynthetic Systems for Integrated Carbon Capture and Conversion. ACS Sustainable Chemistry & Engineering, 2019; DOI: 10.1021/acssuschemeng.8b04969
- office parlementaire des choix technos, « L e s m o d e s d e p r o d u c t i o n d e l ’ h y d r o g è n e », Senat, , p6/10 (lire en ligne)
- « Le coût de l’hydrogène d’origine solaire pourrait atteindre entre 0,7 € et 1,8 €/kg d’ici 2030 », sur pv magazine France (consulté le )
- http://www.bulletins-electroniques.com/actualites/70071.htm
- CEA magazine sur l'hydrogène 2004
- ARTEROU, GUILLET, FRUCHART, FONTECAVE, L'hydrogène une énergie propre pour demain ?, Pour la Science no 405
- « cea.fr/UserFiles/File/Animatio… »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?).
- « Kiev - HF2CGroup », sur pile-a-combustible.com via Internet Archive (consulté le ).
- « Pile à combustible », sur Futura (consulté le ).
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Liens externes[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- Aditya Prajapati, Meenesh R. Singh. Assessment of Artificial Photosynthetic Systems for Integrated Carbon Capture and Conversion. ACS Sustainable Chemistry & Engineering, 2019; DOI: 10.1021/acssuschemeng.8b04969
Liens externes[modifier | modifier le code]
- Notice dans un dictionnaire ou une encyclopédie généraliste :

