Béribéri
| Médicament | Vitamine B1 |
|---|---|
| Spécialité | Endocrinologie |
| CIM-10 | E51.1 |
|---|---|
| CIM-9 | 265.0 |
| DiseasesDB | 14107 |
| MedlinePlus | 000339 |
| eMedicine |
984721 med/221 |
| MeSH | D001602 |
| Patient UK | Beriberi |
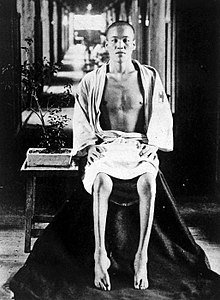





Le béribéri est une maladie causée par un déficit en vitamine B1 que l'on peut observer en cas de malnutrition chez des espèces ne synthétisant pas la vitamine B1 comme l'être humain, mais aussi par exemple la poule. Chez l'être humain elle provoque une insuffisance cardiaque et des troubles neurologiques. Son nom provient du singhalais — la langue de la population majoritaire du Sri Lanka — et signifie « je ne peux pas, je ne peux pas » ; en effet, une fatigue marquée est l'un des symptômes du béribéri.
Origine de la maladie[modifier | modifier le code]
L'organisme humain n'est pas capable de produire la vitamine B1 : il doit en trouver quotidiennement dans son alimentation. Les carences en vitamines B1 sont créées par un régime trop peu diversifié, composé principalement de glucides comme le riz blanc, la farine blanche ou le sucre blanc. À noter que la chair de certains poissons contient de la thiaminase, une enzyme qui détruit la vitamine B1. Cette enzyme est dénaturée lors de la cuisson des poissons, mais pas s’ils sont mangés crus, comme cela se fait au Japon, où des carences en vitamine B1 dues à ces modes d'alimentation ont été observées[1],[2],[3],[4].
Symptômes[modifier | modifier le code]
Chez l'être humain, la maladie se manifeste par une grande fatigue accompagnée d'une perte de poids, de problèmes neurologiques (troubles émotionnels, altération des perceptions), une faiblesse et une douleur dans les membres et un rythme cardiaque irrégulier. Un œdème (gonflement des tissus corporels) est fréquent. Les taux sanguins de lactate et de pyruvate peuvent augmenter. Dans les cas graves, une insuffisance cardiaque peut causer la mort.
Ces symptômes peuvent survenir simultanément à ceux de l'encéphalopathie de Wernicke, une affection neurologique principalement induite par une carence en thiamine.
Plusieurs formes de béribéri existent ; le béribéri est aujourd'hui divisé en quatre catégories (comme suit) ; les trois premières sont historiques et la quatrième (béribéri gastro-intestinal) est reconnue depuis 2004[5] :
- le béribéri sec affecte particulièrement le système nerveux périphérique ;
- le béribéri humide affecte particulièrement le système cardiovasculaire et d'autres systèmes corporels ;
- le béribéri infantile affecte les bébés nés de mères souffrant de malnutrition ;
- le béribéri gastro-intestinal affecte le système digestif et d'autres systèmes corporels.
Béribéri sec[modifier | modifier le code]
Il provoque un dépérissement, et une paralysie partielle (résultant d'une atteinte du système nerveux périphériques). Aussi appelé névrite endémique, il se caractérise par :
- une difficulté à marcher ;
- des picotements ou perte de sensation (engourdissement) dans les mains et les pieds ;
- une perte du réflexe tendineux[6] ;
- une dégradation de la fonction musculaire voire paralysie du bas des jambes ;
- une confusion mentale, avec des difficultés d'élocution ;
- des douleurs ;
- des mouvements oculaires involontaires (nystagmus) ;
- des vomissements ;
- une altération sélective des grandes fibres sensorielles proprioceptives sans altération motrice peut se produire et se présenter comme une ataxie sensorielle proéminente, qui est une perte d'équilibre et de coordination due à la perte des entrées proprioceptives de la périphérie et à une perte de sens de la position[7].
Maladie cérébrale : L'encéphalopathie de Wernicke (WE), le syndrome de Korsakoff (trouble amnésique de l'alcool), le syndrome de Wernicke – Korsakoff sont des formes de béribéri sec[8].
- L'encéphalopathie de Gayet-Wernicke est la manifestation la plus fréquemment rencontrée d'une carence en thiamine dans la société occidentale[9],[10], bien qu'elle puisse également survenir chez des patients souffrant de troubles nutritionnels dus à d'autres causes, telles que les maladies gastro-intestinales[9], ceux atteints du VIH/SIDA, et avec l'administration imprudente de glucose parentéral ou d'hyperalimentation sans supplémentation adéquate en vitamine B[11]. C'est un trouble neuropsychiatrique caractérisé par une paralysie des mouvements oculaires, une posture et une démarche anormales et une fonction mentale nettement perturbée[12] ;
- Le syndrome de Korsakoff est, en général, considéré comme se produisant avec une détérioration de la fonction cérébrale chez les patients initialement diagnostiqués avec WE[13]. C'est un syndrome amnésique-confabuleux caractérisé par une amnésie rétrograde et antérograde, une altération des fonctions conceptuelles et une diminution de la spontanéité et de l'initiative[14].
L'alcoolisme peut induire une carence en thiamine pour les raisons suivantes :
- apport nutritionnel insuffisant: les alcooliques ont tendance à consommer moins que la quantité recommandée de thiamine ;
- diminution de l'absorption de thiamine par le tractus gastro-intestinal: le transport actif de la thiamine dans les entérocytes est perturbé lors d'une exposition aiguë à l'alcool ;
- les réserves hépatiques de thiamine sont réduites en raison de la stéatose hépatique ou de la fibrose[15] ;
- utilisation altérée de la thiamine: le magnésium, qui est nécessaire pour la liaison de la thiamine aux enzymes utilisant la thiamine dans la cellule, est également déficient en raison de la consommation chronique d'alcool. L'utilisation inefficace de toute thiamine qui atteint les cellules aggravera encore la carence en thiamine ;
- l'éthanol des boissons alcoolisées inhibe le transport de la thiamine dans le système gastro-intestinal et bloque la phosphorylation de la thiamine en sa forme cofacteur (ThDP)[16].
Une nutrition améliorée et l'arrêt de la consommation d'alcool permettent à certaines déficiences liées à une carence en thiamine de l'inverser, en particulier une mauvaise fonctionnalité cérébrale, mais dans les cas plus graves, le syndrome de Wernicke – Korsakoff laisse des dommages permanents. (Voir aussi delirium tremens.)
Béribéri humide (shoshin béribéri)[modifier | modifier le code]
Il affecte le cœur et le système circulatoire, parfois mortellement, car provoquant une combinaison d'insuffisance cardiaque et d'affaiblissement des parois capillaires (ce qui se traduit notamment par des tissus périphériques devenant œdémateux). Le béribéri humide se caractérise par :
- un rythme cardiaque augmenté ;
- une vasodilatation entraînant une diminution de la résistance vasculaire systémique et une insuffisance cardiaque à haut débit[17] ;
- une pression veineuse jugulaire élevée[18] ;
- une dyspnée (essoufflement) à l'effort ; une dyspnée paroxystique nocturne ;
- un œdème périphérique (gonflement du bas des jambes)[18] ;
- une cardiomyopathie dilatée.
Béribéri gastro-intestinal[modifier | modifier le code]
Il se manifeste par des douleurs abdominales et est caractérisé par :
- des douleurs abdominales ;
- des nausées, des vomissements ;
- une acidose lactique[19],[20].
Le béribéri infantile (du nourrisson)[modifier | modifier le code]
Il survient généralement entre deux et six mois chez les enfants dont les mères ont un apport insuffisant en thiamine. Il peut se présenter sous forme de béribéri humide ou sec[21].
La forme aiguë, se traduit chez le bébé par une dyspnée et une cyanose conduisant à une mort rapide par insuffisance cardiaque.
Le béribéri infantile est caractérisé par :
- un enrouement, où l'enfant semble aphone : il fait des gestes pour gémir mais n'émet aucun son ou juste de légers gémissements[22] (en raison d'une paralysie nerveuse)[6] ;
- Perte de poids, amaigrissement puis marasme à mesure que la maladie progresse[22] ;
- vomissements[22] ;
- diarrhée[22] ;
- peau pâle[6] ;
- œdème[6],[22] ;
- colère, pleurs[6] ;
- altérations du système cardiovasculaire (tachycardie et rythme cardiaque rapide)[6] ;
- des convulsions sont parfois observées aux stades terminaux[22].
Histoire[modifier | modifier le code]
Bien que connu en Chine ancienne dès le IIIe millénaire av. J.-C., où son apparition avait été liée à la consommation de riz blanc[23],[5], il ne fut pas décrit par un médecin occidental avant 1630, à la suite des travaux du médecin néerlandais Jakob de Bondt à Java[24].
Le béribéri constituait un réel problème pour la marine japonaise de la fin du XIXe siècle ; en effet la ration journalière des marins était dominée par le riz blanc qui ne contient pas de vitamine B1. Le médecin naval japonais Takaki Kanehiro comprit en 1883-1884 que la maladie était liée à une carence nutritionnelle en observant que le béribéri était absent des marines occidentales, et il fit remplacer le riz par de l'orge tout en augmentant les rations de viande et de légumes, ce qui eut pour effet de faire chuter la mortalité due au béribéri dans la flotte japonaise[23]. Même après cela la population civile japonaise continua à souffrir du béribéri[25], sa mortalité au Japon culminant à 26 000 décès en 1923[5]. Le docteur Takaki Kanehiro ne chercha cependant pas si une molécule spécifique était à l'origine de la maladie, pensant qu'il ne s'agissait que d'une carence en protéines[23].
C'est un médecin néerlandais, Christiaan Eijkman (1858-1930), installé à Batavia (aujourd'hui Jakarta), dans les Indes néerlandaises, qui comprit par hasard la cause du béribéri en l'observant chez des poulets nourris au riz blanc plutôt qu'au riz complet. Il pensait initialement que la maladie était provoquée par une toxine présente dans le riz blanc et dont l'action était inhibée par une antitoxine présente dans le son. C'est le biochimiste Kazimierz Funk qui comprit le premier que la maladie provenait d'une carence nutritionnelle, corrigée par la consommation de riz complet dont le péricarpe contient naturellement la vitamine B1, et qui le premier isola la vitamine[23], la première découverte. Tous ces travaux valurent à Christiaan Eijkman le prix Nobel de physiologie ou médecine en 1929.
Épidémiologie[modifier | modifier le code]
Dans les pays occidentaux on observe aujourd'hui des cas de carence en vitamine B1 principalement dans des cas d'alcoolisme chronique[5].
Les populations du Tiers monde sont particulièrement touchées par cette carence à cause de la modification de leurs habitudes alimentaires. Des aliments contenant de la vitamine B1, tels le manioc, le poisson et le riz rouge, ont été remplacés pour des raisons strictement économiques et environnementales par le poulet et le riz blanc, modifiés industriellement. En effet la vitamine B1, naturellement présente dans le péricarpe du grain de riz, disparaît lors du polissage industriel des grains nécessaire à l'obtention du riz blanc.
En 2004, Mayotte a été touchée par une importante épidémie de béribéri infantile, qui a eu pour conséquence la mort d'une vingtaine de nouveau-nés, et dont la cause était le déficit de vitamine B1 dans le lait maternel, ainsi que les carences lors de la grossesse[26].
Notes et références[modifier | modifier le code]
- « Cornell University Department of Animal Science », sur poisonousplants.ansci.cornell.edu (consulté le )
- « Carence en thiamine - Troubles de la nutrition », sur Manuels MSD pour le grand public (consulté le )
- (en) « Office of Dietary Supplements - Thiamin », sur ods.od.nih.gov (consulté le )
- Kenneth Osiezagha, Shahid Ali, C. Freeman et Narviar C. Barker, « Thiamine Deficiency and Delirium », Innovations in Clinical Neuroscience, vol. 10, no 4, , p. 26–32 (ISSN 2158-8333, PMID 23696956, PMCID 3659035, lire en ligne, consulté le )
- « Les 100 ans d'une vieille dame : la vitamine B1 », sur edimark.fr, (consulté en )
- E. Katsura et T. Oiso, « Chapter 9. Beriberi », World Health Organization, Geneva, (lire en ligne [archive du ])
- Marco Spinazzi, Corrado Angelini et Cesare Patrini, « Subacute sensory ataxia and optic neuropathy with thiamine deficiency », Nature Reviews Neurology, vol. 6, no 5, , p. 288–93 (PMID 20308997, DOI 10.1038/nrneurol.2010.16)
- (en) « Nutrition and Growth Guidelines | Domestic Guidelines - Immigrant and Refugee Health » [archive du ], sur CDC, (consulté le ).
- (en) J. J. Kril, « Neuropathology of thiamine deficiency disorders », Metab Brain Dis, vol. 11, no 1, , p. 9–17 (PMID 8815394, DOI 10.1007/BF02080928).
- For an interesting discussion on thiamine fortification of foods, specifically targetting beer, see Leslie R. Drew et A. Stewart Truswell, « Wernicke's encephalopathy and thiamine fortification of food: time for a new direction? », Medical Journal of Australia, vol. 168, , p. 534-535 (lire en ligne [archive du ]).
- (en) R. F. Butterworth, C. Gaudreau et J Vincelette, « Thiamine deficiency and wernicke's encephalopathy in AIDS », Metab Brain Dis, vol. 6, no 4, , p. 207–12 (PMID 1812394, DOI 10.1007/BF00996920).
- (en) C. Harper, « Wernicke's encephalopathy, a more common disease than realised (a neuropathological study of 51 cases) », J Neurol Neurosurg Psychiatry, vol. 42, no 3, , p. 226–231 (PMID 438830, PMCID 490724, DOI 10.1136/jnnp.42.3.226)
- (en) E. V. McCollum, A History of Nutrition, Cambridge, Riverside Press, Houghton Mifflin, .
- (en) R. F. Butterworth, « Thiamin », dans M. E. Shils, M. Shike, A. C. Ross, B. Caballero, R. J. Cousins, Modern Nutrition in Health and Disease, Baltimore, Lippincott Williams & Wilkins, , 10e éd..
- Butterworth RF, « Pathophysiologic mechanisms responsible for the reversible (thiamine-responsive) and irreversible (thiamine non-responsive) neurological symptoms of Wernicke's encephalopathy », Drug Alcohol Rev, vol. 12, no 3, , p. 315–22 (PMID 16840290, DOI 10.1080/09595239300185371)
- Rindi G, Imarisio L, Patrini C, « Effects of acute and chronic ethanol administration on regional thiamin pyrophosphokinase activity of the rat brain », Biochem Pharmacol, vol. 35, no 22, , p. 3903–8 (PMID 3022743, DOI 10.1016/0006-2952(86)90002-X)
- I. S. Anand et V. G. Florea, « High Output Cardiac Failure », Current Treatment Options in Cardiovascular Medicine, vol. 3, no 2, , p. 151–159 (PMID 11242561, DOI 10.1007/s11936-001-0070-1)
- Neil McIntyre et Nigel N. Stanley, « Cardiac Beriberi: Two Modes of Presentation », BMJ, vol. 3, no 5774, , p. 567–9 (PMID 5571454, PMCID 1798841, DOI 10.1136/bmj.3.5774.567)
- Donnino M, « Gastrointestinal Beriberi: A Previously Unrecognized Syndrome », Ann Intern Med, vol. 141, no 11, , p. 898–899 (PMID 15583247, DOI 10.7326/0003-4819-141-11-200412070-00035)
- Duca, J., Lum, C., & Lo, A. (2015). Elevated Lactate Secondary to Gastrointestinal Beriberi. J GEN INTERN MED Journal of General Internal Medicine
- B Adamolekun et L Hiffler, « A diagnosis and treatment gap for thiamine deficiency disorders in sub-Saharan Africa? », Annals of the New York Academy of Sciences, vol. 1408, no 1, , p. 15–19 (PMID 29064578, DOI 10.1111/nyas.13509, Bibcode 2017NYASA1408...15A)
- Michael C. Latham, Human nutrition in the developing world (Food and Nutrition Series – No. 29), Rome, Food and Agriculture Organization of the United Nations (FAO), (ISSN 1014-3181), « Chapter 16. Beriberi and thiamine deficiency »
- Jean Guillaume, Ils ont domestiqué plantes et animaux : Prélude à la civilisation, Versailles, Éditions Quæ, , 456 p. (ISBN 978-2-7592-0892-0, lire en ligne), chap. 6 (« Quand la nutrition fait avancer les choses »).
- David W. McCandless, Thiamine Deficiency and Associated Clinical Disorders (2009), p. 31
- Le roman Le Bateau-Usine de Takiji Kobayashi paru en 1929 décrit par exemple de nombreux cas de béribéri parmi les marins et ouvriers d'un navire de pêche aux crabes.
- Isabelle Quatresous, Ayden Tajahmady, Daouda Sissoko. « Épidémie de béribéri infantile à Mayotte. Rapport d’investigation. 25 mai - 25 juin 2004 » Institut de veille sanitaire, novembre 2004, 69 p.
Voir aussi[modifier | modifier le code]
Liens externes[modifier | modifier le code]
- « Béribéri », sur le dictionnaire de l’Académie nationale de médecine
- « Béribéri », sur le dictionnaire de l’Académie nationale de médecine

